Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Practica No 3 PDF
Cargado por
Marvin RiveiroDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Practica No 3 PDF
Cargado por
Marvin RiveiroCopyright:
Formatos disponibles
Centro Universitario del Norte
Carrera de Técnico en Producción Agrícola
Curso: Suelos II
Docente: Ing. Armando Ruiz
Auxiliar: T.U. Mauricio Ismael Delgado Pacay
PRÁCTICA 3
Determinación del pH por diferentes métodos
Introducción
El pH es el análisis más común de los que son realizados en suelos. A la
vez es el parámetro químico más fácil de medir y el que mayor información provee
del suelo. El pH de un suelo es definido por el logaritmo negativo de la
concentración de hidrógeno.
Es de mucha importancia conocer el pH de un suelo, ya que no todas las
plantas se adecuan al mismo rango de acidez. Conociendo el valor de este
parámetro podemos tomar una decisión sobre las correcciones que debemos
hacer al suelo o sobre el tipo de cultivo que podemos implementar en el mismo.
La acidez incide directamente en la fertilidad de los suelos, ocasionando un mayor
o menor grado de solubilidad de los elementos nutrientes para las plantas y
afectando de este modo la producción agrícola. Además, la acidez incide en otros
fenómenos fisicoquímicos, como la capacidad de intercambio catiónico, la
adsorción de elementos y la presencia de aluminio en forma tóxica para las
plantas.
Valores extremos de pH del suelo, repercuten en deficiencias de
nutrimentos básicos especialmente calcio, magnesio y potasio para suelos muy
ácidos y de nutrimentos como hierro, zinc, manganeso para suelos muy alcalinos.
Además de deficiencias, algunas presentan en estos casos toxicidades de
elementos dañinos a las plantas, especialmente para el caso de suelos ácidos. El
pH es importante también para una buena absorción de los fertilizantes aplicados.
La mayoría de cultivos se desarrollan bien con pH entre 6 y 7.
El valor del pH varía también de acuerdo a la forma como fue determinado y
los reactivos usados. Siendo el método colorimétrico usado en el campo el menos
exacto y el método del potenciómetro con agua destilada o con sales a diferentes
relaciones el más adecuado.
En la Química del Suelo el pH es una variable maestra que controla
diferentes mecanismos y reacciones como el intercambio iónico, precipitación, los
fenómenos de adsorción, entre otros.
Centro Universitario del Norte
Carrera de Técnico en Producción Agrícola
Curso: Suelos II
Docente: Ing. Armando Ruiz
Auxiliar: T.U. Mauricio Ismael Delgado Pacay
Factores que afectan la medida del pH:
Entre los factores que afectan la medida del pH del suelo tenemos: la
relación suelo/solución, el contenido de sales o electrolitos en la solución, efecto
de suspensión y el contenido de bióxido de carbono del suelo.
Al aumentar la relación suelo seco / solución, tiende a aumentar el pH. Al
aumentar la concentración de sales neutrales como Na Cl2, Ca SO4, disminuye el
pH, difiere también de acuerdo a la normalidad del líquido de la solución. Al
aumentar la presión de CO2 disminuye el pH (se produce hidrógeno). En suelos
calcáreos el CO2 es alto. Otro factor que afecta es las variaciones estacionales y
anuales, así como las variaciones locales.
La medición de pH en agua ha sido muy criticada por varios factores que la
afectan (dilución y época de muestreo). Además, el agua no tiene la capacidad de
desplazar todos los cationes que se encuentran asociados con la partícula del
suelo y por lo tanto no toma en cuenta el efecto de los cationes de las sales en la
medición del pH.
Por la razón anterior es recomendable la medición potenciométrica del pH
usando soluciones 1 normal de KCl o CaCl2. El potasio y el calcio como son
cationes, desplazan a otros cationes (como H+, Ca++, Mg++, Al+++, etc.) que están
asociados con las partículas pequeñas del suelo (arcillas y materia orgánica) para
dejarlos en suspensión en la muestra donde se mide el pH. De esta manera se
toma en cuenta el efecto de los cationes de las sales en la medición.
Reactivos:
1. 1 N KCl pesar 74.5 gr de KCl y ponerlo en un frasco volumétrico de 1 litro.
Llegar al volumen final con agua destilada.
2. Buffers de pH conocido (4 y 7).
Procedimiento:
PH en agua:
1. Pesar 20 gr de suelo sin encalar y agregar 20 ml de agua destilada, en un
beaker de 100 ml (relación 1:1). Si al poner el agua se vuelve una pasta,
hacer la relación 1:1 por volumen (20 cc de suelo y 20 ml de agua).
2. Mezclar con un agitador de vidrio periódicamente por 30 minutos. Revolver
por lo menos 4 veces.
Centro Universitario del Norte
Carrera de Técnico en Producción Agrícola
Curso: Suelos II
Docente: Ing. Armando Ruiz
Auxiliar: T.U. Mauricio Ismael Delgado Pacay
3. Leer el pH de las muestras en el potenciómetro, previa estandarización.
4. Repetir el procedimiento con una muestra de suelo ya encalado.
pH en KCl:
1. Hacer el mismo procedimiento que el pH en agua, pero en lugar de agua
usar 20 ml de KCl 1 N.
Estandarización del potenciómetro:
1. Conectar el potenciómetro y dejarlo calentar por lo menos 30 minutos antes
de empezar a hacer las lecturas y la estandarización.
2. El electrodo del potenciómetro debe de estar en la posición de “stand by”
cuando no este sumergido en la solución.
3. Enjuagar los electrodos con agua destilada. Sumergir los electrodos.
4. en el buffer de pH más alto. Si la lectura no es la correcta, ajustar con los
botones de temperatura y estandarización.
5. Enjuagar los electrodos y sumergir en el buffer de pH más bajo. Ajustar la
lectura.
6. Repetir los dos pasos anteriores hasta que el potenciómetro lea
correctamente los pH de los buffers sin mover el botón de estandarización.
7. Si después de varios intentos, el potenciómetro no da la lectura correcta de
los buffers; entonces se procede a la corrección de lecturas de acuerdo al
siguiente procedimiento.
Corrección de lecturas del potenciómetro:
Primero determinar la precisión de las lecturas por medio de la siguiente fórmula.
Precisión de lecturas de pH =
pH leído del buffer más bajo – pH leído del buffer más alto
pH teórico del buffer más bajo – pH teórico del buffer más alto
Con el dato anterior se puede proceder a la corrección de lecturas de la siguiente
forma:
𝑝𝐻 𝑙𝑒í𝑑𝑜 𝑑𝑒 𝑙𝑎 𝑚𝑢𝑒𝑠𝑡𝑟𝑎 − 𝑝𝐻 𝑙𝑒í𝑑𝑜 𝑑𝑒𝑙 𝑏𝑢𝑓𝑓𝑒𝑟 𝑚á𝑠 𝑎𝑙𝑡𝑜 + 𝑝𝐻 𝑙𝑒𝑖𝑑𝑜 𝑑𝑒𝑙 𝑏𝑢𝑓𝑓𝑒𝑟 𝑚á𝑠 𝑎𝑙𝑡𝑜
precisión de lecturas de pH
También podría gustarte
- Simulacro - Examen Parcial - 2020-0Documento2 páginasSimulacro - Examen Parcial - 2020-0VanessaAún no hay calificaciones
- JU-001-06-41601-0000-08-02-0005 - 0 Proc. Soldadura Por ExtrusiónDocumento12 páginasJU-001-06-41601-0000-08-02-0005 - 0 Proc. Soldadura Por ExtrusiónjuanAún no hay calificaciones
- Cenizas Cascara-De ArrozDocumento23 páginasCenizas Cascara-De ArrozAlexander Montalvo Perez100% (1)
- Word ProyectoDocumento12 páginasWord ProyectoAngel Vilca poloAún no hay calificaciones
- La Capa Sub-Rasante, Subbase y BaseDocumento39 páginasLa Capa Sub-Rasante, Subbase y BaseLuis Enrique Valdez Mazariegos100% (1)
- GEOMALLASDocumento15 páginasGEOMALLASTania Canchumanya Calderon100% (1)
- PLAN de MINADO 2011 GoldPlata2 - Revision GoldPlata - 18.04.11Documento55 páginasPLAN de MINADO 2011 GoldPlata2 - Revision GoldPlata - 18.04.11ronaldAún no hay calificaciones
- Baño Galvanico NiquelDocumento15 páginasBaño Galvanico NiquelRosemary HuancaAún no hay calificaciones
- Gasolinera La Mortera AQDocumento6 páginasGasolinera La Mortera AQAngela QuinteroAún no hay calificaciones
- 10 Animales en Peligro de Extinción GuatemalaDocumento6 páginas10 Animales en Peligro de Extinción GuatemalaMarvin RiveiroAún no hay calificaciones
- Cotizacion 2Documento1 páginaCotizacion 2Marvin RiveiroAún no hay calificaciones
- Cuento Los 3 Cerditos Con 5 ImagenesDocumento3 páginasCuento Los 3 Cerditos Con 5 ImagenesMarvin RiveiroAún no hay calificaciones
- Concepto Caracteristicas EmprendedorDocumento1 páginaConcepto Caracteristicas EmprendedorMarvin RiveiroAún no hay calificaciones
- Civilizaciones Antiguas de AméricaDocumento23 páginasCivilizaciones Antiguas de AméricaMarvin RiveiroAún no hay calificaciones
- Costumbre, Tradiciones, Patrimonios y Sexualidad en AdolescenciaDocumento7 páginasCostumbre, Tradiciones, Patrimonios y Sexualidad en AdolescenciaMarvin RiveiroAún no hay calificaciones
- Poemas A Los Simbolos PatriosDocumento3 páginasPoemas A Los Simbolos PatriosMarvin RiveiroAún no hay calificaciones
- Acta Veteranos de GuerraDocumento2 páginasActa Veteranos de GuerraMarvin RiveiroAún no hay calificaciones
- La Democracia en GuatemalaDocumento6 páginasLa Democracia en GuatemalaMarvin RiveiroAún no hay calificaciones
- Las Capas de La Tierra, Grafias y Normas de CortesiaDocumento3 páginasLas Capas de La Tierra, Grafias y Normas de CortesiaMarvin RiveiroAún no hay calificaciones
- Cloroplasto, Vacuola y FotosintesisDocumento3 páginasCloroplasto, Vacuola y FotosintesisMarvin RiveiroAún no hay calificaciones
- Documentos Comerciales ConceptoDocumento3 páginasDocumentos Comerciales ConceptoMarvin RiveiroAún no hay calificaciones
- 15 Comidas Tipicas de GuatemalaDocumento5 páginas15 Comidas Tipicas de GuatemalaMarvin RiveiroAún no hay calificaciones
- Historia, Politologia, Arqueologia, EconomiaDocumento6 páginasHistoria, Politologia, Arqueologia, EconomiaMarvin RiveiroAún no hay calificaciones
- Danzas de GuatemalaDocumento5 páginasDanzas de GuatemalaMarvin RiveiroAún no hay calificaciones
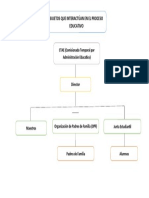
- Organigrama Sujetos Que Interactuan en El Proceso EducativoDocumento1 páginaOrganigrama Sujetos Que Interactuan en El Proceso EducativoMarvin RiveiroAún no hay calificaciones
- CienciasDocumento5 páginasCienciasMarvin RiveiroAún no hay calificaciones
- Ciencias NaturalesDocumento7 páginasCiencias NaturalesMarvin RiveiroAún no hay calificaciones
- Navegadores y BuscadoresDocumento3 páginasNavegadores y BuscadoresMarvin RiveiroAún no hay calificaciones
- DocumentoDocumento1 páginaDocumentoMarvin RiveiroAún no hay calificaciones
- Tipos de Cambios SemanticosDocumento5 páginasTipos de Cambios SemanticosMarvin RiveiroAún no hay calificaciones
- Resumen Libro AbismosDocumento1 páginaResumen Libro AbismosJavier MartinezAún no hay calificaciones
- Chance JeroniDocumento5 páginasChance JeroniMarvin RiveiroAún no hay calificaciones
- Infografía PrimeroBasicoDocumento2 páginasInfografía PrimeroBasicoMarvin RiveiroAún no hay calificaciones
- El Principito - Antoine de Saint-Exupéry (2 TECNOLOGÍA) (Vista Previa) Microsoft FormsDocumento6 páginasEl Principito - Antoine de Saint-Exupéry (2 TECNOLOGÍA) (Vista Previa) Microsoft FormsMarvin RiveiroAún no hay calificaciones
- Funciones de Excel 1Documento30 páginasFunciones de Excel 1Marvin RiveiroAún no hay calificaciones
- Fdocuments - Ec - Uso y Manejo Correcto Del TecladoDocumento13 páginasFdocuments - Ec - Uso y Manejo Correcto Del TecladoMarvin RiveiroAún no hay calificaciones
- Descarga y Manejo de ArchivosDocumento4 páginasDescarga y Manejo de ArchivosMarvin RiveiroAún no hay calificaciones
- Funciones de Excel 1Documento29 páginasFunciones de Excel 1Marvin RiveiroAún no hay calificaciones
- El Principito - Antoine de Saint-Exupéry (2 TECNOLOGÍA) (Vista Previa) Microsoft FormsDocumento6 páginasEl Principito - Antoine de Saint-Exupéry (2 TECNOLOGÍA) (Vista Previa) Microsoft FormsMarvin RiveiroAún no hay calificaciones
- Reacciones de DescomposiciónDocumento10 páginasReacciones de DescomposiciónEmily Gb0% (1)
- Examen Química Selectividad Madrid Junio 2013Documento3 páginasExamen Química Selectividad Madrid Junio 2013MundoEstudiante.comAún no hay calificaciones
- Diversion 165 y 180: Especs. RápidasDocumento4 páginasDiversion 165 y 180: Especs. Rápidasyasser awadallhAún no hay calificaciones
- Tabla Periódica 4Documento2 páginasTabla Periódica 4Michael Slater Ocaña PuiconAún no hay calificaciones
- Adriana Mendez - MATERIALES CERAMICOSDocumento5 páginasAdriana Mendez - MATERIALES CERAMICOSNajhely MagalhãensAún no hay calificaciones
- Exacavaciones y Zanjas PDFDocumento76 páginasExacavaciones y Zanjas PDFEDGAR GENARO PARI BENITESAún no hay calificaciones
- Presentacion Prevencion SilicosisDocumento29 páginasPresentacion Prevencion SilicosisRosa Escalona ValdiviaAún no hay calificaciones
- Solucionario Química IV Medio Guías 1 2 y 3Documento3 páginasSolucionario Química IV Medio Guías 1 2 y 3FernandaAún no hay calificaciones
- Rotulo DesinfectanteDocumento4 páginasRotulo DesinfectanteAndrew MyWorldAún no hay calificaciones
- 4.-Drilling Bits EngineeringDocumento56 páginas4.-Drilling Bits EngineeringRulo LinceAún no hay calificaciones
- Operaciones Unitarias Utilizadas en La Industria AlimenticiaDocumento3 páginasOperaciones Unitarias Utilizadas en La Industria AlimenticiaNancy Carbajal SolariAún no hay calificaciones
- TEORIA DE LA DOBLE CAPA ELECTRICA Teoria de HELMHOTZDocumento8 páginasTEORIA DE LA DOBLE CAPA ELECTRICA Teoria de HELMHOTZJohn W. CMAún no hay calificaciones
- Binder 1444Documento76 páginasBinder 1444Jorge MoscosoAún no hay calificaciones
- Fester CM201 MX 2020Documento3 páginasFester CM201 MX 2020Jesús Manuel Robledo AcostaAún no hay calificaciones
- Crs-ssoma-In-003 - Estandar de Orden y Limpieza en El Area de TrabajoDocumento2 páginasCrs-ssoma-In-003 - Estandar de Orden y Limpieza en El Area de TrabajoMario Andrée Martinez TrujilloAún no hay calificaciones
- NTG 36011 (Astm A615-A615 M-12) V.3Documento17 páginasNTG 36011 (Astm A615-A615 M-12) V.3CarlosNoriegaAún no hay calificaciones
- Tecnología de Procesos de Fundición de Aluminio Parte 2Documento90 páginasTecnología de Procesos de Fundición de Aluminio Parte 2Rodrigo MontalvoAún no hay calificaciones
- Tesis (Evaporador Multiple Efecto) PDFDocumento218 páginasTesis (Evaporador Multiple Efecto) PDFRuben Omar Quiroga67% (3)
- Catálogo de Productos Distribución (A-5) - v2 PDFDocumento28 páginasCatálogo de Productos Distribución (A-5) - v2 PDFAlb PerezAún no hay calificaciones