Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Guia de Ejercicios de Cinetica Química.1
Cargado por
andreaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Guia de Ejercicios de Cinetica Química.1
Cargado por
andreaCopyright:
Formatos disponibles
UNIVERSIDAD DE CARABOBO
FACULTAD DE INGENIERIA
ESCUELA DE QUMICA
DEPARTAMENTO DE INGENIERIA QUMICA
CINETICA Y DISEO DE REACTORES
GUA DE EJERCICIOS DE CINTICA QUMICA (1-2017)
1. Prepare una tabla estequiomtrica para cada una de las reacciones siguientes y exprese
la concentracin de cada especie en la reaccin como una funcin de la conversin,
evaluando todas las constantes ( p.ej., , )
a) La reaccin en fase lquida
(CH2)2O + H2O (CH2)2(OH)2
Las concentraciones iniciales de xido de etileno y agua son 1 lbmol/ft3 y 3.47
lbmol/ft3 respectivamente.
b) La pirolisis isotrmica, isobrica, en fase gaseosa
C2H6 C2H4 + H2
Entra etano puro en el reactor a 6 atm y 1100 K. Cmo cambiara su ecuacin para
la concentracin, s la reaccin se efectuara en un reactor por lotes de volumen
constante?
c) La oxidacin isotrmica, isobrica, cataltica, en fase gaseosa
2C2H4 + O2 2(CH2)2O
La alimentacin entra en un reactor continuo de lecho fijo (PBR) a 6 atm y 260 C
y es una mezcla estequiomtrica de oxgeno y etileno.
2. El anhdrido ftlico se puede producir por oxidacin parcial de naftaleno en un lecho
cataltico fijo o fluidizado:
2C10H8 + 9O2 2C8H4O3 + 4CO2 + 4H2O
Prepare una tabla estequiomtrica para esta reaccin si la mezcla inicial consiste de
3.5% naftaleno y 96.5% de aire (% en moles) y sela para plantear las relaciones que
se piden a continuacin. P0 = 10 atm y T0 = 500 K.
Para un reactor de flujo isotrmico en el que no hay cada de presin, determine lo
siguiente en funcin de la conversin de naftaleno (XN):
a) Las presiones parciales de O2 y CO2
b) Las concentraciones de O2 y naftaleno
c) la velocidad de flujo volumtrico ()
3. a) Tomando al H2 como base de clculo, construya una tabla estequiomtrica completa
para la reaccin:
N2 + 3H2 2NH3
que se efecta en un sistema de flujo isobrico e isotrmico con alimentaciones
equimolares de N2 y H2.
a) Si la presin total en la entrada es de 16.4 atm y la temperatura es de 1727 C, calcule
las concentraciones de amoniaco y de hidrgeno cuando la conversin de H2 es de
60%
b) Si tomara el N2 como base de clculo, podra alcanzarse una conversin de 60% del
N2?
4. El cido ntrico se prepara comercialmente a partir de xido ntrico, el cual se produce
por oxidacin del amoniaco en fase gaseosa:
4NH3 + 5O2 4NO + 6H2O
La alimentacin consiste en 15% en mol de amoniaco en aire a 8.2 atm y 227 C.
a) Calcule la concentacin total en la entrada.
b) Qu concentracin tiene el amoniaco en la entrada?
c) Prepare una tabla estequiomtrica usando al amoniaco como base de clculo y
luego
c.1) Exprese Pi y Ci para todas las especies en funcin de la conversin para un
reactor por lotes a presin constante que opera isotrmicamente.
c.2) Exprese Pi y Ci para todas las especies en funcin de la conversin para un
reactor volumen constante. Exprese PT en funcin de X.
5. a) Exprese la velocidad de formacin de bromuro de hidrgeno en trminos de las
constantes k1 y k2 y la conversin del bromo, X. Evale numricamente todas las
dems cantidades. La alimentacin consiste en 25% de hidrgeno, 25% de bromo y
50% de inertes a una presin de 10 atm y una temperatura de 400C.
b) Escriba la velocidad de descomposicin de cumeno, -rC, en trminos de la
conversin, la concentracin inicial del cumeno y las constantes de velocidad y de
equilibrio especficas. La mezcla inicial consiste de 75% de cumeno y 25% inertes.
6. Calcule la conversin y las concentraciones en el equilibrio para cada una de la
reacciones siguientes:
a) La reaccin en fase lquida: A + B C
con CA0 = CB0 = 2 mol/dm3 y KC = dm3/mol
b) La reaccin en fase gaseosa: A 3C
efectuada en un reactor de flujo sin cada de presin. Se alimenta A puro a una
temperatura de 400 K y 10 atm. A esta temperatura, KC = 0.25 dm3/mol2.
c) La reaccin en fase gaseosa de la parte (b) efectuada en un reactor por lotes de
volumen constante.
d) La reaccin en fase gaseosa de la parte (b) efectuada en un reactor por lotes de
presin constante.
7. Un lquido A se descompone de acuerdo con la cintica de primer orden, logrando una
conversin del 50 % de A en 5 minutos. Calcule el tiempo adicional necesario para que
la conversin sea del 75 %.
8. El reactivo acuoso A reacciona para dar R (A R) y en el primer minuto su
concentracin en un reactor intermitente disminuye desde CA0 = 2.03 mol/litro hasta
CAf = 1.97 mol/litro. Encontrar la ecuacin de velocidad si la cintica es de segundo
orden respecto al reactivo A.
9. En un reactor discontinuo un reactante (CAo = 1 mol/L) alcanza la conversin del 80 %
en 8 minutos y se necesitan 18 minutos para que la conversin sea del 90 %, dedzcase
una ecuacin cintica que represente esta reaccin.
10. Encontrar la constante de velocidad de primer orden para la desaparicin de A en la
reaccin en fase gaseosa A l.6R si el volumen de la mezcla de reaccin aumenta
50% en 4 minutos, cuando se empieza la reaccin con A puro. la presin total en el
sistema permanece constante a 1.2 atm y la temperatura es 25 C
11. Se efectu la reaccin irreversible en fase lquida
A B + C
en un reactor por lotes. Se obtuvieron los siguientes datos durante el curso de la
reaccin
t (min) 0.0 2.0 4.0 6.0
CA(mol/dm3) 2.00 1.31 0.95 0.73
Determine el orden de reaccin y la velocidad de reaccin especfica usando mtodos
para diferenciar sus datos:
a) Tcnica numrica: frmulas de diferenciacin.
b) Tcnica grfica: diferenciacin por reas iguales.
c) Diferenciacin de un polinomio
12. Evale la constante de velocidad para la reaccin irreversible:
(CH3)2O CH4 + H2 + CO
usando la siguiente data experimental. La data fue recolectada a 504 C en un
reactor de volumen constante. En el tiempo t = 0, el reactor es cargado con (CH3)2O
puro.
Tiempo (s) 390 777 1195 3155
PT (mmHg) 408 488 562 799 931
13. Para la reaccin A R y teniendo en cuenta los datos tabulados, Es razonable
representar la relacin velocidad concentracin por una expresin cintica de orden
n? En caso afirmativo hallar el orden de la reaccin.
CA(mol/L) 6,1 8,2 8,5 9,1 13,3
-rA (mol/L min) 110 200 220 250 530
14. Calcular el orden global de la reaccin irreversible:
2H2 +2NO N2 + 2H2O
a partir de los siguientes datos a volumen constante, empleando cantidades
equimolares de hidrgeno y xido ntrico
Presin total, mm Hg 200 240 280 320 360
Tiempo de vida media, s 265 186 115 104 67
15. Se obtuvieron los siguientes datos en un reactor intermitente de volumen constante a 0
C usando el gas A puro:
PA(mmHg) 760 600 475 390 320 275 240 215 150
t (min) 0 2 4 6 8 10 12 14
La estequiometria de la descomposicin es A 2.5R. Encontrar una ecuacin
cintica que represente satisfactoriamente esta descomposicin.
16. La Sacarosa se Hidroliza a la temperatura ambiente por la accin cataltica de la enzima
sacarasa: SACARASA
SACAROSA PRODUCTOS
En un reactor discontinuo se obtienen los siguientes datos cinticos partiendo de una
concentracin de sacarosa CAo = 1,0 mmol/L y una concentracin de enzima de
CE0 = 0,01 mmol/L.
CA(mmol/L) 0,840 0,680 0,530 0,380 0,270 0,160 0,090 0,040 0,018
t (h) 1 2 3 4 5 6 7 8 9
Compruebe si estos datos se pueden ajustarse por una ecuacin cintica del tipo de la
de MICHAELIS-MANTEN:
k3 C A C E 0
(rA )
C A CM
En caso afirmativo calclese los valores de k3 y CM, utilizando el mtodo integral y
diferencial.
17. Una pequea bomba de reaccin equipada con un dispositivo sensible para medir la
presin, se evacua y despus se llena de reactivo A puro a 1 atm de presin. La
operacin se efecta a 25 C, temperatura lo suficientemente baja para que la reaccin
no transcurra de forma apreciable.
Se eleva entonces la temperatura lo ms rpidamente posible hasta 100 C
sumergiendo la bomba en agua hirviendo, obtenindose los datos dados en la tabla. La
estequiometria de la reaccin es 2A R y despus de permanecer la bomba en el
bao durante un fin de semana se efecta un anlisis para determinar la cantidad de A,
encontrndose que ya no queda nada de ese componente. Encontrar una ecuacin
cintica que se ajuste a estos datos, expresando las unidades en moles, litros y min.
t (min) PT (atm) t (min) PT (atm)
1 1,140 7 0,850
2 1,040 8 0,832
3 0,982 9 0,815
4 0,940 10 0,800
5 0,905 15 0,754
6 0,870 20 0,728
18. Se introduce reactivo acuoso A con una concentracin inicial CA0 = l mol/1itro en un
reactor intermitente, donde reacciona para formar el producto R de acuerdo con la
estequiometria A R. La concentracin de A en el reactor es monitoreada en
distintos tiempos, obtenindose:
t(min) 0 100 200 300 400
CA(mol/m3) 1000 500 333 250 200
a) Encontrar la conversin del reactivo despus de 5 horas en el reactor para un
experimento con CA0 = 500 mol/m3
b) Encontrar la velocidad de reaccin.
19. En un reactor Discontinuo se efecta la reaccin reversible de primer orden en fase
lquida:
A B CAo = 0,5 mol/L , CBo = 0
Calclese la ecuacin cintica de esta reaccin, si en 8 min se alcanza una conversin
del 33,3 % y la conversin del equilibrio es de 66,7 %.
20. La pirolisis del etano tiene lugar con una Energa de Activacin de unas 75000
cal/mol. Calclese el aumento relativo de la velocidad de descomposicin a 650 C
con respecto a 500 C.
21. En un reactor intermitente se est planteando la conversin de A en R. La reaccin se
efecta en fase lquida con estequiometria: A R, y la velocidad de reaccin se
indica en la tabla. Calcular el tiempo (min) necesario para que la concentracin
disminuya desde CAo = 1,3 mol/L a CAf = 0,3 mol/L.
CA mol/L -rA mol/L min
0,1 0,1
0,2 0,3
0,3 0,5
0,4 0,6
0,5 0,5
0,6 0,25
0,7 0,10
0,8 0,06
1,0 0,05
1,3 0,045
2,0 0,042
22. La reaccin en fase acuosa A R + S , transcurre de acuerdo con los datos
siguientes:
t (min) 0 36 65 100 160
CA(mol/L) 0,1823 0,1453 0,1216 0,1025 0,0795 0,0494
CAo = 0,1823 mol/L
CRo = 0
CSo = 55 mol/L
Dedzcase la ecuacin cintica.
23. M. Bodcnstcin [Z. phy s. chem., 29, 295] encontr los siguientes datos:
T (C) 508 427 393 356 283
k(cm3/gmols) 0.1059 0.00310 0.000588 80.9 10-6 0.942 10-6
para la descomposicin trmica del ioduro de hidrgeno
2HI H2 + I2
Encontrar la ecuacin de velocidad completa para esta reaccin. Utilizar las
unidades de julios, gmol, cm3 y segundos.
También podría gustarte
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Reactores Con RecirculacionDocumento34 páginasReactores Con RecirculacionBorisJeanUsuriaga100% (1)
- II Examen de Diseño de ReactoresDocumento10 páginasII Examen de Diseño de ReactoresJosep LopezAún no hay calificaciones
- Problemas de Diseño de ReactoresDocumento6 páginasProblemas de Diseño de ReactoresJAIME MARTINEZ HERNANDEZ100% (1)
- Manual de Laboratorio de Quimica CarDocumento113 páginasManual de Laboratorio de Quimica CarRomeliaAlbertinaGamboaSolis100% (1)
- Cinetica Química EjerciciosDocumento8 páginasCinetica Química EjerciciosJose LozanoAún no hay calificaciones
- Problemas Reacciones CataliticasDocumento34 páginasProblemas Reacciones CataliticasDanitza Yessenia Rojas QuintanaAún no hay calificaciones
- Guía 2 - 2018Documento13 páginasGuía 2 - 2018DarioTejerinaAún no hay calificaciones
- Guia de Ejercicios de Cinetica Química (Ceing 2021)Documento8 páginasGuia de Ejercicios de Cinetica Química (Ceing 2021)jose jimenezAún no hay calificaciones
- Repartido1 2009Documento3 páginasRepartido1 2009Roberto FigueroaAún no hay calificaciones
- Problemas Cinetica QuimicaDocumento2 páginasProblemas Cinetica QuimicaDaniel Andres PaezAún no hay calificaciones
- PB9697Documento23 páginasPB9697ZeolitaAún no hay calificaciones
- Problemas Cinética QuimicaDocumento3 páginasProblemas Cinética QuimicaNatalia Estupiñán0% (1)
- U3 ProblemasDocumento9 páginasU3 ProblemasmarianzavaAún no hay calificaciones
- Discusion 2Documento8 páginasDiscusion 2Luis Enrique100% (1)
- Guía #2 - Investigacion Cinética en Un Reactor BatchDocumento16 páginasGuía #2 - Investigacion Cinética en Un Reactor BatchNicole Retamal YevenesAún no hay calificaciones
- Problemario de CQ y Reactores (Parte 2)Documento5 páginasProblemario de CQ y Reactores (Parte 2)Paty ParedsAún no hay calificaciones
- Ejercicios de Diseño de Reactores IsotérmicosDocumento11 páginasEjercicios de Diseño de Reactores IsotérmicosJulián Scortechini0% (1)
- Problemas ReversiblesDocumento4 páginasProblemas ReversiblesAlberto ArteagaAún no hay calificaciones
- Practico Idea Les 2010Documento14 páginasPractico Idea Les 2010Bartolome Garcia ReyAún no hay calificaciones
- Guia de Ejercicios Tema 1Documento5 páginasGuia de Ejercicios Tema 1jose carranza leonAún no hay calificaciones
- Discusion 2Documento8 páginasDiscusion 2Dee-Deecita ItiAún no hay calificaciones
- Hoja de Practica Ingenieria de Las ReaccionesDocumento5 páginasHoja de Practica Ingenieria de Las Reaccioneso0jhony0oAún no hay calificaciones
- Problemas de Diseno de Reactores IdealesDocumento5 páginasProblemas de Diseno de Reactores IdealesJose Demons Peña CarvajalAún no hay calificaciones
- EXAMENSustit2020 1Documento1 páginaEXAMENSustit2020 1Reaven :3Aún no hay calificaciones
- Problemas Tema2Documento8 páginasProblemas Tema2Pelayo RodrigoAún no hay calificaciones
- U1 ProblemasDocumento9 páginasU1 Problemasn_a_n_i_t_aAún no hay calificaciones
- Boletin Tema 3-1920Documento3 páginasBoletin Tema 3-1920manu regueiroAún no hay calificaciones
- Relacion de Problemas 3defDocumento1 páginaRelacion de Problemas 3defmanzana nananaAún no hay calificaciones
- Diapositiva 03 EstqDocumento30 páginasDiapositiva 03 EstqDENIS LEYVAAún no hay calificaciones
- Guía de Ejercicios Unidad 2Documento2 páginasGuía de Ejercicios Unidad 2Ana Victoria Marquez ChaconAún no hay calificaciones
- Guía #3 - Reactores Continuos en Estado EstacionarioDocumento9 páginasGuía #3 - Reactores Continuos en Estado EstacionarioNicole Retamal YevenesAún no hay calificaciones
- Sistemas Con Reacciones QuimicasDocumento6 páginasSistemas Con Reacciones QuimicasNatali CondeñaAún no hay calificaciones
- Prob1 2008Documento2 páginasProb1 2008Rosa100% (1)
- GUIA ReactoresDocumento3 páginasGUIA ReactoresFidel Flores CaricariAún no hay calificaciones
- Boletin Tema 2-1920Documento1 páginaBoletin Tema 2-1920manu regueiroAún no hay calificaciones
- TALLER Ingeniería de Las Reacciones Químicas 1 PDFDocumento4 páginasTALLER Ingeniería de Las Reacciones Químicas 1 PDFAndres LlorenteAún no hay calificaciones
- Trabajo CineticaDocumento2 páginasTrabajo Cineticaenriquejo joAún no hay calificaciones
- Abril 2023 Ejercicios Tema 1Documento3 páginasAbril 2023 Ejercicios Tema 1Sonia LecunaAún no hay calificaciones
- Guia N 6 Efectos TermicosDocumento10 páginasGuia N 6 Efectos TermicosRicky Reyes CastilloAún no hay calificaciones
- 3 - Prob RFP 11-12 23-35Documento4 páginas3 - Prob RFP 11-12 23-35adonis aguero pajueloAún no hay calificaciones
- Deber Reacciones 2 Tarea 1Documento4 páginasDeber Reacciones 2 Tarea 1Daniel LoorAún no hay calificaciones
- TD Cinética y Diseño de ReactoresDocumento33 páginasTD Cinética y Diseño de ReactoresIsaac Rodriguez100% (1)
- Problemas de Cinética QuímicaDocumento5 páginasProblemas de Cinética QuímicaCharlotte BaskervilleAún no hay calificaciones
- Problemas de InternetDocumento10 páginasProblemas de InternetFranz Tucta Huillca0% (1)
- Asignación de Ingenieria de Las Reacciones QuimicasDocumento5 páginasAsignación de Ingenieria de Las Reacciones QuimicasAnonymous 6XVcvzAún no hay calificaciones
- Asignación de Ingenieria de Las Reacciones QuimicasDocumento5 páginasAsignación de Ingenieria de Las Reacciones QuimicasAnonymous 0JIsUMUkEAún no hay calificaciones
- Problemas Tema 3.Documento7 páginasProblemas Tema 3.Servicio ComunitarioAún no hay calificaciones
- Serie 01 - Cinetica en Sistemas Homogeneos 2017Documento6 páginasSerie 01 - Cinetica en Sistemas Homogeneos 2017Félix BaezAún no hay calificaciones
- Tarea 6Documento2 páginasTarea 6Paola VillalobosAún no hay calificaciones
- Respuestas Ejercicios REACTORESDocumento6 páginasRespuestas Ejercicios REACTORESAmbar FajardoAún no hay calificaciones
- H3-EFECTOS - TERMICOS - EN - REACTORES - IDEALES-2014-2015 CampusDocumento5 páginasH3-EFECTOS - TERMICOS - EN - REACTORES - IDEALES-2014-2015 CampusCenaida ColinaAún no hay calificaciones
- Problemes Reactors No-IsotermesDocumento5 páginasProblemes Reactors No-IsotermesAlbert VictoriAún no hay calificaciones
- Ejercicios Corte 2Documento2 páginasEjercicios Corte 2José EstebanAún no hay calificaciones
- U1 ProblemasDocumento7 páginasU1 ProblemasMaggi Condori GuarachiAún no hay calificaciones
- Tema 2.3Documento1 páginaTema 2.3morfe 878Aún no hay calificaciones
- Serie 04 - Reactores No IsotermicosDocumento4 páginasSerie 04 - Reactores No IsotermicosLuciana NeirotAún no hay calificaciones
- Practica Primer Parcial 2 - 2021Documento6 páginasPractica Primer Parcial 2 - 2021Agni SelmanAún no hay calificaciones
- Actividad de Aprendizaje # 6 Balanceo de EcuacionesDocumento2 páginasActividad de Aprendizaje # 6 Balanceo de Ecuacionesesteban anguloAún no hay calificaciones
- Lab1.sintesis de Bromuro de N-Butilo Por Mecanismo SN2Documento4 páginasLab1.sintesis de Bromuro de N-Butilo Por Mecanismo SN2Angely VergaraAún no hay calificaciones
- Cinetica IDocumento1 páginaCinetica IRodrigo Mozo PizarroAún no hay calificaciones
- Taller R-XDocumento2 páginasTaller R-XCamilo PérezAún no hay calificaciones
- Actividad 8Documento3 páginasActividad 8Alberto Rosas SilvaAún no hay calificaciones
- Unidad Educativa "Santo Domingo de Guzmán": Ambato - EcuadorDocumento9 páginasUnidad Educativa "Santo Domingo de Guzmán": Ambato - EcuadorNel VelaAún no hay calificaciones
- El Postulado de HammondDocumento23 páginasEl Postulado de HammondMariana TiscareñoAún no hay calificaciones
- Soluciones Ejercicios de Síntesis PDFDocumento24 páginasSoluciones Ejercicios de Síntesis PDFAnaAún no hay calificaciones
- E1P5L1013Documento14 páginasE1P5L1013Monserrat HernandezAún no hay calificaciones
- 635 7%2Bclase%2Bcapitulo%2B14%2BCin%25C3%25A9tica%2BQu%25C3%25ADmicaDocumento76 páginas635 7%2Bclase%2Bcapitulo%2B14%2BCin%25C3%25A9tica%2BQu%25C3%25ADmicahipiAún no hay calificaciones
- Guia - Oxido - Reduccion 2020Documento3 páginasGuia - Oxido - Reduccion 2020Pablo Lobatón HildaAún no hay calificaciones
- Clase 6-1Documento15 páginasClase 6-1Daniel GarciaAún no hay calificaciones
- Equilibrio Químico 03Documento43 páginasEquilibrio Químico 03Mario Edgar Cordero SánchezAún no hay calificaciones
- Cp10-Descomposición Catalítica Del Peróxido de HidrógenoDocumento4 páginasCp10-Descomposición Catalítica Del Peróxido de HidrógenoPaulina SegoviaAún no hay calificaciones
- Serie 2 LDocumento2 páginasSerie 2 LDiego BarreraAún no hay calificaciones
- U1 ProblemasDocumento7 páginasU1 ProblemasMaggi Condori GuarachiAún no hay calificaciones
- Practica de Laboratorio de La CatalasaDocumento4 páginasPractica de Laboratorio de La CatalasaFrank Antonio Quispe TorresAún no hay calificaciones
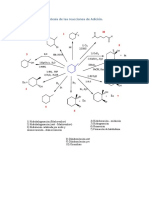
- Síntesis de Las Reacciones de AdiciónDocumento1 páginaSíntesis de Las Reacciones de AdiciónMiri AldreteAún no hay calificaciones
- 1.2 Velocidad de Las Reacciones Quimicas-Cinética Química-JgalDocumento57 páginas1.2 Velocidad de Las Reacciones Quimicas-Cinética Química-JgalEudaldo Cime FigueroaAún no hay calificaciones
- Informe Estequiometria1Documento12 páginasInforme Estequiometria1JAIME ANDRES POVEDA MURILLOAún no hay calificaciones
- 1° Medio - Guía N°3 - Balance de Ecuaciones - Método Del Tanteo y Método Algebraico - Lunes 26 de AbrilDocumento3 páginas1° Medio - Guía N°3 - Balance de Ecuaciones - Método Del Tanteo y Método Algebraico - Lunes 26 de AbrilDenisse Alejandra Pinto CaroAún no hay calificaciones
- Síntesis Del Ácido CinámicoDocumento7 páginasSíntesis Del Ácido CinámicoISABELA RENTERIA RUIZAún no hay calificaciones
- Estequiometria ResumidaDocumento32 páginasEstequiometria ResumidaLUZ KARIME TORRES LOZADAAún no hay calificaciones
- Anexo 1 - Tablas para El Desarrollo de Los EjerciciosDocumento17 páginasAnexo 1 - Tablas para El Desarrollo de Los EjerciciosyarlenAún no hay calificaciones
- Informe IV - Nrc8671 - EstequiometriaDocumento11 páginasInforme IV - Nrc8671 - Estequiometriagianella calla100% (1)
- Taller Unidad Alquenos y Alquinos (2020) PDFDocumento8 páginasTaller Unidad Alquenos y Alquinos (2020) PDFMaria Isabella Trochez PumalpaAún no hay calificaciones
- Practica 3Documento25 páginasPractica 3Tannya OrellanaAún no hay calificaciones