Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Modelo de Bohr Unidad 1.2
Cargado por
Darío Félix0 calificaciones0% encontró este documento útil (0 votos)
24 vistas13 páginasDerechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
24 vistas13 páginasModelo de Bohr Unidad 1.2
Cargado por
Darío FélixCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 13
Espectros de Emisin
Desde el siglo XVII, poca en que Newton demostr que la
luz solar esta formada de diversos componentes de color
que al volver a combinarlos producen la luz blanca, los
fsicos y los qumicos ya haban estudiado las
caractersticas de los espectros de emisin, es decirlos
espectros continuos o lneas de radiacin emitida por las
sustancias.
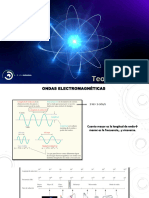
Se llama espectro visible a la regin
del espectro electromagntico que el
ojo humano es capaz de percibir. A la
radiacin electromagntica en este
rango de longitudes de onda se le
llama luz visible o simplemente luz. No
hay lmites exactos en el espectro
visible: un tpico ojo humano
responder a longitudes de onda de
400 a 700 nm, aunque algunas
personas pueden ser capaces de
percibir longitudes de onda desde 380
hasta 780 nm.
Los arcoris son un ejemplo de
refraccin del espectro visible.
Cada elemento tiene un espectro de emisin nico. Las
lneas caractersticas de un espectro atmico se emplean
en el anlisis qumico para identificar tomos
desconocidos, de la misma forma en que las huellas
digitales sirven para identificar a una persona. Cuando las
lneas del espectro de emisin de una muestra
desconocida, es posible establecer la identidad de esta
muestra.
Espectro de emisin del tomo de
hidrgeno.
En 1913, Niels Bohr dio a conocer una explicacin
terica del espectro de emisin del tomo de
hidrgeno. El tratamiento de Bohr es muy complejo
y no se considera correcto en todos sus detalles.
Cuando este abord por primera vez este problema,
los fsicos ya saban que los tomos estaban
formados de electrones y protones. Consideraban al
tomo como una unidad donde los electrones
giraban alrededor del ncleo en orbitas circulares a
gran velocidad.
Este modelo resultaba atractivo porque semejaba el
movimiento de los planetas alrededor del sol.
El modelo de Bohr tambin inclua la idea de
que los electrones se movan en orbitas
circulares pero impona restricciones rigurosas:
el nico electrn del tomo de hidrgeno poda
estar localizado slo en ciertas rbitas. Dado
que cada orbita tiene una energa particular ,
las energas asociadas al movimiento del
electrn en las rbitas permitidas debern
tener un valor fijo, es decir estar cuantizadas.
Bohr supuso que la emisin de radiacin por un
tomo de hidrgeno energizado se deba a la
cada del electrn desde una orbita de mayor
energa a una de menor energa y esto originaba
un cuanto de energa en forma de luz. Con
argumentos fundamentados en la interaccin
electrosttica y en la leyes de movimiento de
Newton , Bohr demostr que las energas que
tienen el electrn en el tomo de hidrgeno
estn dadas por:
1.- Los electrones se mueven alrededor
del ncleo en orbitas circulares estables.
De acuerdo a la fsica clsica, si los electrones se movieran en rbitas
circulares, se aceleraran irradiando constantemente energa (perderan
energa), describiendo una espiral hasta colapsar finalmente con el ncleo.
2.- Slo son permitidas aquellas rbitas en las cuales el
momento angular del electrn est cuantizado, siendo
un mltiplo entero de
2
m v r= n
Momento angular
E1 < E2
E1
E2
Esto implica que un electrn en una orbita o estado estacionario n,
posee un momento angular constante, y por lo tanto su energa en
dicha orbita se mantiene constante.
3.- Cuando un electrn pasa de una rbita a otra, dicha
transicin va acompaada de la absorcin o emisin de
una cantidad definida de energa.
Ef =
El fotn absorbido y el fotn emitido tienen la misma
longitud de onda y por lo tanto la misma energa.
La energa del fotn emitido o absorbido es igual a la
diferencia de energas entre las dos orbitas.
En = - RH
1
( 2
Donde RH =Constante de Rydberg tiene un valor de
2.18 x10-18 J
n= nmero cuntico principal, es un entero que
tiene valores de n= 1,2,3,..
El signo negativo es una convencin arbitraria para
indicar que la energa del electrn en el tomo es
menor que la energa del electrn libre, es decir,
un electrn situado a distancia infinita del ncleo
También podría gustarte
- Teoría electromagnética para estudiantes de ingeniería: Notas de claseDe EverandTeoría electromagnética para estudiantes de ingeniería: Notas de claseCalificación: 4.5 de 5 estrellas4.5/5 (7)
- 5 Ejercicios Luminarias Resueltos PDFDocumento10 páginas5 Ejercicios Luminarias Resueltos PDFRodolfo Rodriguez57% (7)
- Modelo Atomico de BohrDocumento33 páginasModelo Atomico de BohrLorena Herrera Hernandez0% (1)
- M R U V - Separata-Rptas PDFDocumento7 páginasM R U V - Separata-Rptas PDFDaciia Milagros Diaz FernandezAún no hay calificaciones
- La Luz CuestionarioDocumento4 páginasLa Luz CuestionarioJoseph HernndezAún no hay calificaciones
- 3er Informe de Lab. Fisica-Segunda Ley de NewtonDocumento20 páginas3er Informe de Lab. Fisica-Segunda Ley de Newtonjonathan100% (2)
- Modelo Mecano CuanticoDocumento46 páginasModelo Mecano CuanticoVíctor Cárcamo Echeverría100% (2)
- El Modelo Atomico de BohrDocumento3 páginasEl Modelo Atomico de BohrFrida LlerenaAún no hay calificaciones
- Base Experimental de La Teoría CuanticaDocumento5 páginasBase Experimental de La Teoría CuanticaBrenda Liz Ramos100% (1)
- Absorción y Emisión de Radiación ElectromagnéticaDocumento17 páginasAbsorción y Emisión de Radiación ElectromagnéticaGrecia De La CruzAún no hay calificaciones
- Estructura Electrónica de Los ÁtomosDocumento8 páginasEstructura Electrónica de Los ÁtomosPILAR SANCHEZAún no hay calificaciones
- Estructura Atómica TeoriaDocumento44 páginasEstructura Atómica TeoriaFran BrennanAún no hay calificaciones
- Apunte QuimicaDocumento62 páginasApunte QuimicacokemaxmaxAún no hay calificaciones
- Tema 4. Quimica I - 2018Documento28 páginasTema 4. Quimica I - 2018Alex TorresAún no hay calificaciones
- Teoría Cuántica y La Estructura Electrónica de Los ÁtomosDocumento14 páginasTeoría Cuántica y La Estructura Electrónica de Los ÁtomosNayrobi AcostaAún no hay calificaciones
- Modelo Nuclear Del Atomo.Documento44 páginasModelo Nuclear Del Atomo.Joselyn OrtegaAún no hay calificaciones
- Modelo Atómico ActualDocumento4 páginasModelo Atómico ActualLeo SAún no hay calificaciones
- Química General T7-14Documento49 páginasQuímica General T7-14Ilian GilAún no hay calificaciones
- Base Experimental de La Teoría CuanticaDocumento6 páginasBase Experimental de La Teoría CuanticaKarina OsorioAún no hay calificaciones
- Modelos AtómicosDocumento8 páginasModelos AtómicosLeilaAún no hay calificaciones
- Trabajo en Equipo QuimicaDocumento6 páginasTrabajo en Equipo QuimicaYAREMI ADALID LOPEZ LLANOSAún no hay calificaciones
- Modelo Atómico de BohrDocumento3 páginasModelo Atómico de Bohrdccg1112Aún no hay calificaciones
- Condensado de BoseDocumento10 páginasCondensado de BoseHiram LoyaAún no hay calificaciones
- Teoria Atomica de BohrDocumento10 páginasTeoria Atomica de BohrErick MartínezAún no hay calificaciones
- Modelos AtomicosDocumento28 páginasModelos AtomicosNATALY ALMANZA AVILAAún no hay calificaciones
- Balotario QuimicaDocumento142 páginasBalotario QuimicaSteven SosaAún no hay calificaciones
- SEMANA 02.1 Estructura AtomicaDocumento70 páginasSEMANA 02.1 Estructura AtomicaKevin Eduardo Medina DiazAún no hay calificaciones
- Niels Bohr Sabía Que Las Principales Objeciones Al Modelo Atómico de Rutherford Eran QueDocumento2 páginasNiels Bohr Sabía Que Las Principales Objeciones Al Modelo Atómico de Rutherford Eran QueEdgar Campusano SanchezAún no hay calificaciones
- 3-Teoría Cuántica-VfinalDocumento48 páginas3-Teoría Cuántica-VfinaljuanixgenoAún no hay calificaciones
- Documento No. 3 Modelo de Bohr y SommerfeldDocumento5 páginasDocumento No. 3 Modelo de Bohr y SommerfeldRocio HernándezAún no hay calificaciones
- Teoría de BohrDocumento3 páginasTeoría de BohrJuan Diego Guzmán GuerreroAún no hay calificaciones
- Teoría Atómica de BohrDocumento5 páginasTeoría Atómica de BohrCarlos Alamilla RamosAún no hay calificaciones
- Química Estructura de La MateriaDocumento19 páginasQuímica Estructura de La MateriaIvan Oliver SanchezAún no hay calificaciones
- Estructura AtómicaDocumento47 páginasEstructura AtómicaMARIEL BENITEZ DELGADOAún no hay calificaciones
- Teoría Cuántica y Estructura AtómicaDocumento34 páginasTeoría Cuántica y Estructura AtómicaLuis Angel Jose SanchzAún no hay calificaciones
- Modelo Atomico BohrDocumento4 páginasModelo Atomico BohrMarco SolísAún no hay calificaciones
- Modelo Atomico de BorhDocumento14 páginasModelo Atomico de BorhArtijopa JatpAún no hay calificaciones
- Espectros ÓpticosDocumento18 páginasEspectros Ópticosmau365100% (1)
- Unidad 1. Teoría Cuántica y Estructura AtómicaDocumento55 páginasUnidad 1. Teoría Cuántica y Estructura AtómicaElenaAún no hay calificaciones
- Tema 1Documento10 páginasTema 1maria reverteAún no hay calificaciones
- Sesion 2 (T)Documento44 páginasSesion 2 (T)Piero Aaron SolanoAún no hay calificaciones
- 18 de Septiembre 2019Documento15 páginas18 de Septiembre 2019Anonymous FEkJ6UAún no hay calificaciones
- Modelo Atómico ActualDocumento3 páginasModelo Atómico ActualCamila SocaAún no hay calificaciones
- Base Experimental de La Teoría CuánticaDocumento4 páginasBase Experimental de La Teoría CuánticaJ ABRICAAún no hay calificaciones
- Dualidad Onda-Partículas, U3.Documento17 páginasDualidad Onda-Partículas, U3.RAUL SEBASTIAN NEAVEZ DEL BOSQUEAún no hay calificaciones
- LECTURA 2.1 El Átomo, Historia y Estructura.Documento7 páginasLECTURA 2.1 El Átomo, Historia y Estructura.Esther GuanangaAún no hay calificaciones
- Formulario Fisica ModernaDocumento6 páginasFormulario Fisica ModernaDiego CandoAún no hay calificaciones
- Quimica Inorganica DIAPOSITIVASDocumento33 páginasQuimica Inorganica DIAPOSITIVASJuan Contreras BelAún no hay calificaciones
- Resolucion de La GuiaDocumento39 páginasResolucion de La GuiaAldo Ortega González0% (2)
- Apuntes UnidadiDocumento15 páginasApuntes UnidadigenericolaneroAún no hay calificaciones
- Documento Sin TítuloDocumento7 páginasDocumento Sin TítuloYeison David100% (1)
- Modelo Atómico de BohrDocumento22 páginasModelo Atómico de BohrValentina CarpioAún no hay calificaciones
- Ochoas 5 (1) .09Documento17 páginasOchoas 5 (1) .09zumbaclauAún no hay calificaciones
- Clase N°3 Estructura AtómicaDocumento49 páginasClase N°3 Estructura AtómicaMireya Herrera100% (1)
- Modelo Atomico de BohrDocumento15 páginasModelo Atomico de BohrAlexander MoranAún no hay calificaciones
- Modelo Atómico de BohrDocumento3 páginasModelo Atómico de BohrManuel PatAún no hay calificaciones
- 2.1 Modelos AtómicosDocumento42 páginas2.1 Modelos AtómicosVal MorasAún no hay calificaciones
- Bitácora DigitalDocumento6 páginasBitácora DigitalAdriana OsorioAún no hay calificaciones
- CUADERNILLO QUIMICA - Unit II Teoria CuanticaDocumento18 páginasCUADERNILLO QUIMICA - Unit II Teoria CuanticaAngie Gabriela Torres MorenoAún no hay calificaciones
- Estructura Del Atomo y ModelosDocumento11 páginasEstructura Del Atomo y ModelosGarciaHuichoAún no hay calificaciones
- FísicaDocumento6 páginasFísicaDanielAún no hay calificaciones
- Semana 7 VicenteDocumento5 páginasSemana 7 VicenteAbisael CortesAún no hay calificaciones
- Teoría CuánticaDocumento92 páginasTeoría CuánticaJuanMaNoriegaAún no hay calificaciones
- Tema 2 Modelo Nuclear Del AtomoDocumento16 páginasTema 2 Modelo Nuclear Del Atomokimi VolkovaAún no hay calificaciones
- Mineralogia TeoriaDocumento30 páginasMineralogia Teoriarichard_17dAún no hay calificaciones
- P5 Conservacion MateriaDocumento1 páginaP5 Conservacion MateriaDarío FélixAún no hay calificaciones
- Museo Regional Mixteco TlayuaDocumento1 páginaMuseo Regional Mixteco TlayuaDarío FélixAún no hay calificaciones
- P5 Conservacion MateriaDocumento7 páginasP5 Conservacion MateriaCristian J. ChavezAún no hay calificaciones
- Conic AsDocumento1 páginaConic AsDarío FélixAún no hay calificaciones
- Programación de EquiposDocumento1 páginaProgramación de EquiposDarío FélixAún no hay calificaciones
- Programación de EquiposDocumento1 páginaProgramación de EquiposDarío FélixAún no hay calificaciones
- Solucionario Del Examen Parcial de AntenasDocumento4 páginasSolucionario Del Examen Parcial de AntenasHuber MuñozAún no hay calificaciones
- Clase 2 - Sedimentación y CentrifugaciónDocumento47 páginasClase 2 - Sedimentación y CentrifugaciónAnthony Rodriguez ParedesAún no hay calificaciones
- Informe Lab Fis 100 - Caida LibreDocumento12 páginasInforme Lab Fis 100 - Caida LibreKim Arty SelAún no hay calificaciones
- Tipos de OndasDocumento10 páginasTipos de OndasIsidoraAún no hay calificaciones
- Movimiento OndulatorioDocumento27 páginasMovimiento OndulatorioJakov Bustamante100% (1)
- Informe Ley de Coulomb YaDocumento21 páginasInforme Ley de Coulomb YaJUAN DAVID BORRERO FIERROAún no hay calificaciones
- Práctica 8 Tipos de LentesDocumento3 páginasPráctica 8 Tipos de Lentesegmc7Aún no hay calificaciones
- ElestrostáticaDocumento14 páginasElestrostáticaEDUARDO MADERA RICOAún no hay calificaciones
- Sol Caf 1 Taller Previo EpDocumento8 páginasSol Caf 1 Taller Previo EpBrayan CamarenaAún no hay calificaciones
- Imágenes Formadas Por Una Lente ConvexaDocumento3 páginasImágenes Formadas Por Una Lente Convexaalberto cepilloAún no hay calificaciones
- Apéndice, Principios y Técnicas de Microscopía.Documento33 páginasApéndice, Principios y Técnicas de Microscopía.Sonia Araceli Gallegos GalvezAún no hay calificaciones
- Mapeo de Campo EléctricoDocumento3 páginasMapeo de Campo EléctricoSofi BoeroAún no hay calificaciones
- Propiedades de Los Circuitos Eléctricos Laboratorio #4Documento7 páginasPropiedades de Los Circuitos Eléctricos Laboratorio #4Rigo MejiaAún no hay calificaciones
- CuestionarioDocumento4 páginasCuestionarioLorena López50% (2)
- Complemento de Física III. Ondas, Héctor Alzate LópezDocumento73 páginasComplemento de Física III. Ondas, Héctor Alzate LópezDaniel LozanoAún no hay calificaciones
- U4 La Corriente y La Resistencia V.F.Documento32 páginasU4 La Corriente y La Resistencia V.F.Saúl UreñaAún no hay calificaciones
- Infome - El Microscopio CompuestoDocumento14 páginasInfome - El Microscopio CompuestoMARYMAR MEDINA GUERRAAún no hay calificaciones
- Electrostática DivertidaDocumento2 páginasElectrostática DivertidaDaniel Matute100% (1)
- WWW Asifunciona Com Electrotecnia Ke Factor Potencia Ke Factor Potencia 5 HTMDocumento4 páginasWWW Asifunciona Com Electrotecnia Ke Factor Potencia Ke Factor Potencia 5 HTMMario Gabriel MoralliAún no hay calificaciones
- Cámara de Gran FormatoDocumento9 páginasCámara de Gran FormatoOctavio ArgüelloAún no hay calificaciones
- TABLA DE FORMULAS Fisica PDFDocumento2 páginasTABLA DE FORMULAS Fisica PDFWilmar Lopez NeiraAún no hay calificaciones
- 03 Ejercicios Resueltos de DinámicaDocumento52 páginas03 Ejercicios Resueltos de Dinámicavanessa gonzalezAún no hay calificaciones
- Secuencia PrincipalDocumento5 páginasSecuencia PrincipalAugusto GloopAún no hay calificaciones
- Reflaxion de La Luz TrabajoDocumento1 páginaReflaxion de La Luz TrabajoKATHERINE DIAZAún no hay calificaciones
- Evaluación de Fisica Grado 11° Online No. 2Documento2 páginasEvaluación de Fisica Grado 11° Online No. 2Ricardo Cifuentes TriviñoAún no hay calificaciones
- Capitulo11 Motores de Induccion Delta EstrellaDocumento36 páginasCapitulo11 Motores de Induccion Delta EstrellaVladimir E. BalvinAún no hay calificaciones