Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Diagrama de Fases
Cargado por
Jaeger16Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Diagrama de Fases
Cargado por
Jaeger16Copyright:
Formatos disponibles
UNMSM
FACULTAD DE INGENIERA INDUSTRIAL
ESCUELA DE INGENIERA INDUSTRIAL
Laboratorio De F.Q.B
REGLA DE FASES
Profesor:
AGERICO, PANTOJA CADILLO
Alumnos:
FERNANDEZ PEREZ, MICHELL
Turno:
MARTES 8-10H
GASES
NDICE
I. INTRODUCCION...................................................................................................2
i.
Objetivo:............................................................................................................2
ii. Proceso Experimental......................................................................................2
Materiales.......................................................................................................2
iii.
Conclusion.....................................................................................................9
II.
OBJETIVO........................................................................................................10
III.
FUNDAMENTOS TEORICOS..........................................................................11
IV. CLCULOS Y RESULTADOS:...........................................................................13
V.
CONCLUSION..................................................................................................23
VI.
APENDICE.......................................................................................................24
VII.
CUESTIONARIO..............................................................................................25
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
I.
INTRODUCCION
El objetivo de la prctica de laboratorio es saber determinar experimentalmente el
diagrama de fases, la curva de enfriamiento y encontrar el punto Eutctico de una
mezcla binaria cuyos componentes no se mezclan qumicamente, es decir, que no
son miscibles en estado slido, pero son solubles en estado lquido.
Las condiciones de laboratorio en la que se realiz esta experiencia fueron
temperatura a 23C, presin 756 mmHg , HR% igual a 96% y los reactivos que
fueron utilizados fueron el naftaleno QP, p-diclorobenceno QP que fueron
depositados en ocho muestras preparadas en dos sets de tubos de ensayo
separados en grupos A y B.
Durante la experiencia con estos tubos se not que la temperatura de cristalizacin
vara ligeramente con referencia al valor aproximado considerado terico dispuesto
en tablas. En algunos casos la diferencia de temperatura es bastante notoria, lo cual
podra influir de forma significativa en el valor experimental, lo que lleva a un error
importante.
II.-PROCEDIMIENTO Y MATERIALES
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
2.1-MATERIALES:
a) Instrumentos
NAFTALENO
P-DICLOROBENCENO
8 TUBOS DE PRUEBA GRANDES
AGITADOR METLICO PEQUEO
AGITADOR METLICO GRANDE
VASOS DE 400ml Y 600 ml.
COCINILLA
FIGURA 2.1.1
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
b) Reactivos
FIGURA 2.1.2
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
1) Seleccionamos un tubo
que
contenga
un
componente, es decir, el 1 o
el 8(nuestro grupo se
encargo del tubo 8).
2) Colocamos el tubo en un
bao a una temperatura
inicial mayor entre 5 y 8C a
la cristalizacin de
dicho tubo.
3) Tomar la temperatura cada
5/10 segundos hasta que se
vuelva constante.
4) Hacemos mismo
procedimiento pero con un tubo
que contenga dos
componente(tubo 6), pero
tomamos la temperatura hasta
que descienda de forma continua.
2.2_PROCEDIMIENTO:
DETERMINACIN DE LAS CURVAS DE ENFRIAMIENTO
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
FIGURA 2.2.1
Concluimos
que
puras es mucho ms
mucho ms precisos,
muestras que son
llevan a errores, los
difciles de identificar
engendran.
trabajando con muestras
fcil obtener resultados
lo cual indica que las
mezclas
comnmente
cuales son bastante
las causas que los
Una
recomendacin
tratar de evitar que las
con impurezas que
temperaturas
de
solubilidad, por lo que
un ambiente bastante
muestras puras, se
ms cuidado.
es que es necesario
muestras se contaminen
puedan alterar tanto las
fusin, as como su
es necesario trabajar en
limpio, y si se trata de
debe de tener mucho
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
III.- OBJETIVOS
El objetivo de la prctica de laboratorio es saber determinar experimentalmente el
diagrama de fases, la curva de enfriamiento y encontrar el punto Eutctico de una
mezcla binaria cuyos componentes no se mezclan qumicamente, es decir, que no
son miscibles en estado slido, pero son solubles en estado lquido.
IV.-FUNDAMENTOS TEORICOS
REGLA DE FASES DE GIBBS:
Esta regla nos define los grados de libertad que posee el sistema dependiendo del
tipo de variables que consideremos. Establece la siguiente relacin:
F+ P=C+2
Donde:
F = nmero de grados de libertad
C = nmero de componentes.
P = nmero de fases presentes.
Y el 2 = es el nmero de variables de estado del sistema (temperatura y presin).
En los casos experimentales que nosotros trataremos, el efecto de la variacin de la
presin es
despreciable, as establecemos que: P = 1 atm = constante
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
durante todo el experimento. As pues, la regla de las fases queda establecida para
nuestros propsitos empricos como:
F+ P=C+1
Los trminos usados en la expresin anterior as como otros necesarios para
entender los diagramas de fase se definen a continuacin.
SISTEMA: Cualquier porcin del universo material que pueda aislarse completa y
arbitrariamente del resto, para considerar los cambios que puedan ocurrir en su
interior y bajo condiciones variantes.
FASE: Cualquier porcin del sistema fsicamente homognea y separada por una
superficie mecnicamente separable de otras porciones. Por ejemplo, un vaso de
agua con cubos de hielo constituye dos fases distintas de una misma sustancia
(agua). Los cubos de hielo son una fase slida y el agua lquida es una fase lquida.
COMPONENTES: el menor nmero de variables individuales independientes (vapor,
lquido o slido) por medio de los cuales la composicin del sistema puede
expresarse cuantitativamente. Normalmente un componente es un elemento,
compuesto o solucin del sistema. As por ejemplo, el vaso de agua con cubos de
hielo, es un sistema en el que hay dos fases pero una sola componente.FRACCIN
MOLAR
La fraccin molar es una unidad qumica para expresar la concentracin de soluto
en una disolucin. Nos expresa la proporcin en que se encuentran los moles de
soluto con respecto a los moles totales de disolucin, que se calculan sumando los
moles de soluto(s) y de disolvente. Para calcular la fraccin molar de una mezcla
homognea, se emplea la siguiente expresin:
X i=
ni
<1
nt
Donde ni es el nmero de moles del soluto, y nt el nmero total de moles en toda la
disolucin (tanto de solutos como de disolvente).
Como el volumen de una disolucin depende de la temperatura y de la presin;
cuando stas cambian, el volumen cambia con ellas. Gracias a que la fraccin molar
no est en funcin del volumen, es independiente de la temperatura y la presin.
Adems cabe notar que en los gases ideales la variacin del volumen ser
proporcional para cada uno de los solutos, y por lo tanto tambin para la solucin.
De esta manera hay una relacin directa entre las fracciones molares y los
volmenes parciales.
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
X i + X i ++ X i =1
1
Sumatoria de fracciones molares
DIAGRAMA DE FASE:
Un tpico diagrama de fase. La lnea con puntos muestra el comportamiento
anmalo del agua.
La lnea verde marca el punto de congelacin y la lnea azul, el punto de ebullicin.
Se muestra como ellos varan con la presin.
En termodinmica y ciencia de materiales se denomina diagrama de fase a la
representacin grfica de las fronteras entre diferentes estados de la materia de un
sistema, en funcin de variables elegidas para facilitar el estudio del mismo. Cuando
en una de estas representaciones todas las fases corresponden a estados de
agregacin diferentes se suele denominar diagrama de cambio de estado.
En ciencia de materiales se utilizan ampliamente los diagramas de fase binarios,
mientras que en termodinmica se emplean sobre todo los diagramas de fase de
una sustancia pura.
DIAGRAMA DE FASE DE UNA SUSTANCIA PURA:
Los diagramas de fase ms sencillos son los de presin - temperatura de una
sustancia pura, como puede ser el del agua. En el eje de ordenadas se coloca la
presin y en el de abscisas la temperatura. Generalmente, para una presin y
temperatura dadas, el cuerpo presenta una nica fase excepto en las siguientes
zonas:
Punto triple: En este punto del diagrama coexisten los estados slido, lquido y
gaseoso. Estos puntos tienen cierto inters, ya que representan un invariante y
FII UNMSM
LABORATORIO DE FISICOQUMICA
GASES
por lo tanto se pueden utilizar para calibrar termmetros. Los pares (presin,
temperatura)que corresponden a una transicin de fase entre:
Dos fases slidas: Cambio alotrpico.
Entre una fase slida y una fase lquida: fusin solidificacin.
Entre una fase slida y una fase vapor (gas): sublimacin - deposicin (o
sublimacin inversa).
Entre una fase lquida y una fase vapor: vaporizacin - condensacin (o
licuefaccin).
Es importante sealar que la curva que separa las fases vapor-lquido se detiene en
un punto llamado punto crtico. Ms all de este punto, la materia se presenta como
un fluido supercrtico que tiene propiedades tanto de los lquidos como de los gases.
Modificando la presin y temperatura en valores alrededor del punto crtico se
producen reacciones que pueden tener inters industrial, como por ejemplo las
utilizadas para obtener caf descafeinado.
Es preciso anotar que, en el diagrama P vs. V del agua, la lnea que separa los
estados lquido y slido tiene pendiente negativa, lo cual es algo bastante inusual.
Esto quiere decir que aumentando la presin el hielo se funde, y tambin que la fase
slida tiene menor densidad que la fase lquida.
DIAGRAMA DE FASE BINARIO:
Cuando aparecen varias sustancias, la representacin de los cambios de fase
puede ser ms compleja. Un caso particular, el ms sencillo, corresponde a los
diagramas de fase binarios. Ahora las variables a tener en cuenta son la
temperatura y la concentracin, normalmente en masa. En un diagrama binario
pueden aparecer las siguientes regiones:
FII UNMSM
LABORATORIO DE FISICOQUMICA
10
GASES
Slido puro o solucin slida .
Mezcla de soluciones slidas (eutctica, eutectoide, peritctica, peritectoide).
Mezcla slido - lquido.
nicamente lquido, ya sea mezcla de lquidos inmiscibles (emulsin), ya sea
un lquido completamente homogneo.
Mezcla lquido - gas.
Gas (lo consideraremos siempre homogneo, trabajando con pocas
variaciones da altitud).
Hay punto y lneas en estos diagramas importantes para su caracterizacin:
Lnea de lquidos, por encima de la cual solo existen fases lquidas.
Lnea de slidos, por debajo de la cual solo existen fases slidas.
Lnea eutctica y eutectoide. Son lneas horizontales (isotermas) en las que
tienen lugar transformaciones eutcticas y eutectoides, respectivamente.
Concentraciones definidas, en las que ocurren transformaciones a
temperatura constante:
NUMERO DE GRADOS DE LIBERTAD:
El nmero de grados de libertad es el nmero de factores variables
independientes, tomados de entre la temperatura, presin y composicin de las
fases. Es decir, es el nmero de estas variables que deben especificarse para que el
sistema quede completamente definido.
PUNTO EUTCTICO:
Punto eutctico, vocablo que deriva del griego y que quiere decir fcilmente fusible.
Es la mxima temperatura a la que puede producirse la mayor cristalizacin del
FII UNMSM
LABORATORIO DE FISICOQUMICA
11
GASES
solvente y soluto, o tambin se define como la temperatura ms baja a la cual puede
fundir una mezcla de slidos A y B con una composicin fija.
FII UNMSM
LABORATORIO DE FISICOQUMICA
12
GASES
V.-CALCULOS Y RESULTADOS
TABLAS, CALCULOS Y RESULTADOS
TABLAS
Tabla N1: Condiciones de laboratorio
P(mmHg)
T(C)
%HR
759
27
68
Tabla N2: Temperaturas tericas de cristalizacin
Tubo N
Temperatura de cristalizacin (C)
54
47
43
32
48
58
72
80
Tabla N3: Temperaturas experimentales de cristalizacin
Tubo N
Temperatura de cristalizacin (C)
53.2
46.6
42.6
31.7
47.8
FII UNMSM
LABORATORIO DE FISICOQUMICA
13
GASES
58.1
71.4
79.9
Tabla N4: Pesos moleculares
Sustancia
Peso molecular (g/mol)
p-C6H4Cl2
151
C10H8
128
Tabla N5: Temperaturas de enfriamiento
Sustancia pura:
C10 H 8 (Tubo N 8)
Tiempo(s)
Temperatura(C)
Tiempo(s)
Temperatura(C)
89.0
175
81.2
88.5
180
81.2
10
88.2
185
81.2
15
88.0
190
80.9
20
87.8
195
80.9
25
87.6
200
80.8
30
87.5
205
80.6
35
87.3
210
80.6
40
87.0
215
80.3
45
86.8
220
80.3
50
86.5
225
80.2
55
86.3
230
80.0
60
86.1
235
80.0
FII UNMSM
LABORATORIO DE FISICOQUMICA
14
GASES
65
85.8
240
80.0
70
85.5
245
79.8
75
85.1
250
79.8
80
84.8
255
79.8
85
84.5
260
79.7
90
84.1
265
79.7
95
83.8
270
79.7
100
83.6
275
79.5
105
83.2
280
79.5
110
83.0
285
79.5
115
83.0
290
79.3
120
82.8
295
79.2
125
82.7
300
79.0
130
82.5
305
79.0
135
82.3
310
79.0
140
82.0
315
78.8
145
81.8
320
78.8
150
81.8
325
78.8
160
81.6
330
78.8
165
81.4
335
78.8
170
81.4
340
78.8
Mezcla (Tubo N 6)
FII UNMSM
LABORATORIO DE FISICOQUMICA
15
GASES
Tiempo(s)
Temperatura(C
)
Tiempo(s)
Temperatura(C
)
65.0
135
61.6
64.8
140
61.4
10
64.8
145
61.3
15
64.6
150
61.1
20
64.5
160
60.9
25
64.2
165
60.6
30
64.2
170
60.4
35
64.0
175
60.1
40
63.9
180
59.8
45
63.7
185
59.7
50
63.5
190
59.6
55
63.2
195
59.3
60
63.0
200
59.1
65
63.0
205
58.8
70
63.0
210
58.6
75
62.9
215
58.4
80
62.8
220
58.3
85
62.8
225
58.1
90
62.5
230
57.9
95
62.5
235
57.9
100
62.4
240
57.6
105
62.2
245
57.6
110
62.2
250
57.6
115
62.0
255
57.6
120
62.0
260
57.6
125
61.8
265
57.6
130
61.8
270
57.6
FII UNMSM
LABORATORIO DE FISICOQUMICA
16
GASES
CALCULOS
a) Mediante la composicin de cada una de las muestras, calcule la fraccin
molar experimental de cada componente en cada muestra.
log X PDB=
log X NF =
2239.9
+ 47.343 logT 0.03302T 115.0924
T
932.03
13.241 log T + 0.0332T 2.3382 x 105 T 2 +27.5264
T
Tubo N1:( T cristalizacion=53.2 C=326.2 K )
log X PDB=
2239.9
+ 47.343 log326.20.03302(326.2)115.0924
326.2
X PDB = 0.9977
log X NF =
932.03
13.241 log 326.2+0.0332(326.2)2.3382 x 105 (326.2)2 +27.5264
326.2
X NF =0.5370
Tubo N2:( T cristalizacion=46.6 C=319.6 K )
log X PDB=
2239.9
+ 47.343 log319.60.03302(319.6)115.0924
319.6
X PDB=0.8679
FII UNMSM
LABORATORIO DE FISICOQUMICA
17
GASES
log X NF =
932.03
13.241 log 319.6+0.0332(319.6)2.3382 x 105( 319.6)2 +27.5264
319.6
X NF =0.4667
Tubo N3:( T cristalizacion=42.6 C=315.6 K )
log X PDB=
2239.9
+ 47.343 log315.60.03302(315.6)115.0924
315.6
X PDB=0.7951
log X NF =
932.03
5
2
13.241 log 315.6+0.0332(315.6)2.3382 x 10 ( 315.6) +27.5264
315.6
X NF =0.4277
Tubo N4:( T cristalizacion=31.7 C=304.7 K )
log X PDB=
2239.9
+ 47.343 log304.70.03302(304.7)115.0924
304.7
X PDB=0.6188
log X NF =
932.03
5
2
13.241 log 304.7+0.0332(304.7)2.3382 x 10 (304.7) +27.5264
304.7
X NF =0.3340
Tubo N5:( T cristalizacion=47.8 C=320.8 K )
log X PDB=
2239.9
+ 47.343 log320.80.03302(320.8)115.0924
320.8
FII UNMSM
LABORATORIO DE FISICOQUMICA
18
GASES
X PDB=0.8906
log X NF =
932.03
13.241 log 320.8+0.0332(320.8)2.3382 x 105 (320.8)2 +27.5264
320.8
X NF =0.4789
Tubo N6:( T cristalizacion=58.1 C=331.1 K )
log X PDB=
2239.9
+ 47.343 log331.10.03302(331.1)115.0924
331.1
X PDB=1.1019
log X NF =
932.03
13.241 log 331.1+0.0332(331.1)2.3382 x 105 (331.1)2 +27.5264
331.1
X NF =0.5941
Tubo N7:( T cristalizacion=71.4 C=344.4 K )
log X PDB=
2239.9
+ 47.343 log344.40.03302(344.4 )115.0924
344.4
X PDB=1.4173
log X NF =
932.03
13.241 log 344.4+ 0.0332( 344.4)2.3382 x 105 (344.4)2 +27.5264
344.4
X NF =0.7720
Tubo N8:( T cristalizacion=79.9 C=352.9 K )
log X PDB=
2239.9
+ 47.343 log352.90.03302(352.9)115.0924
352.9
FII UNMSM
LABORATORIO DE FISICOQUMICA
19
GASES
X PDB=1.6422
log X NF =
932.03
13.241 log 352.9+0.0332(352.9)2.3382 x 105 (352.9)2 +27.5264
352.9
X NF =0.9041
b) Con los datos de a) construya el diagrama de fases. Analcelo.
Diagrama de fases para el p-diclorobenceno (p-C 6H4Cl2)
Temperatura de cristalizacion vs fraccion molar
79.9
71.4
58.1
53.2
47.8
42.6
46.6
31.7
FIGURA 5.1
FII UNMSM
LABORATORIO DE FISICOQUMICA
20
GASES
Diagrama de fases para el naftaleno (C10H8)
Temperatura de cristalizacion vs Fraccion molar
79.9
71.4
58.1
53.2
46.6
47.8
42.6
31.7
FIGURA 5.2
FII UNMSM
LABORATORIO DE FISICOQUMICA
21
GASES
c) Construya las curvas de enfriamiento del componente puro y de la mezcla
elegida.
Curva de enfriamiento del tubo N 8 (Sustancia pura:
C10 H 8 )
FIGURA 5.3
Temperatura (T) vs tiempo (t)
FII UNMSM
LABORATORIO DE FISICOQUMICA
22
GASES
Temperatura (T) vs tiempo (t)
Curva de enfriamiento del tubo N 6 (Mezcla)
FIGURA 5.4
FII UNMSM
LABORATORIO DE FISICOQUMICA
23
GASES
d) Del diagrama de fases, determine el punto eutctico, igualmente determine
la temperatura y composicin de dicho punto.
FIGURA 5.5
FII UNMSM
LABORATORIO DE FISICOQUMICA
24
GASES
----------- p-diclorobenceno
----------- naftaleno
Temperatura de cristalizacion vs fraccion molar
FII UNMSM
LABORATORIO DE FISICOQUMICA
25
GASES
En el punto eutctico:
Temperatura: 31.7 C
Composicion: 0.639 p-diclorobenceno / 0.361 naftaleno
e) Calcule la solubilidad del naftaleno (fraccin molar terica en la mezcla),
para el rango de temperaturas observadas, entre el punto de cristalizacin del
naftaleno y el punto eutctico.
log X NF =
932.03
5 2
13.241 log T + 0.0332T 2.3382 x 10 T +27.5264
T
FII UNMSM
LABORATORIO DE FISICOQUMICA
26
GASES
Tubo N5:( T cristalizacion=47.8 C=320.8 K )
log X NF =
932.03
5
2
13.241 log 320.8+0.0332(320.8)2.3382 x 10 (320.8) +27.5264
320.8
X NF =0.4789
Tubo N6:( T cristalizacion=58.1 C=331.1 K )
log X NF =
932.03
13.241 log 331.1+0.0332(331.1)2.3382 x 105 (331.1)2 +27.5264
331.1
X NF =0.5941
Tubo N7:( T cristalizacion=71.4 C=344.4 K )
log X NF =
932.03
13.241 log 344.4+ 0.0332( 344.4)2.3382 x 105 (344.4)2 +27.5264
344.4
X NF =0.7720
Tubo N8:( T cristalizacion=79.9 C=352.9 K )
log X NF =
932.03
13.241 log 352.9+0.0332(352.9)2.3382 x 105 (352.9)2 +27.5264
352.9
X NF =0.9041
FII UNMSM
LABORATORIO DE FISICOQUMICA
27
GASES
f) Repita el clculo anterior para el p-diclorobenceno, en el rango de
temperaturas desde su punto de cristalizacin hasta su punto eutctico.
log X PDB=
2239.9
+ 47.343 logT 0.03302T 115.0924
T
Tubo N1:( T cristalizacion=53.2 C=326.2 K )
log X PDB=
2239.9
+ 47.343 log326.20.03302(326.2)115.0924
326.2
X PDB = 0.9977
Tubo N2:( T cristalizacion=46.6 C=319.6 K )
log X PDB=
2239.9
+ 47.343 log319.60.03302(319.6)115.0924
319.6
X PDB=0.8679
Tubo N3:( T cristalizacion=42.6 C=315.6 K )
log X PDB=
2239.9
+ 47.343 log315.60.03302(315.6)115.0924
315.6
X PDB=0.7951
FII UNMSM
LABORATORIO DE FISICOQUMICA
28
GASES
Tubo N4:( T cristalizacion=31.7 C=304.7 K )
log X PDB=
2239.9
+ 47.343 log304.70.03302(304.7)115.0924
304.7
X PDB=0.6188
g) Calcule el calor latente de fusin de los componentes puros en sus puntos
de fusin observados. Calcule tambin los valores tericos correspondientes.
pC 6 H 4 Cl 2: H B =10250+ 94.07 T 0.1511 T 2 cal/mol
C 10 H 8: H A=426526.31 T + 0.1525T 0.000214 T cal/mol
teorica
Tubo N1:( T cristalizacion=54 C=327 K )
pC 6 H 4 Cl 2: H B =10250+ 94.07(327)0.1511(327) cal/mol
H B =4353.9181 cal/mol
experimental
Tubo N1:( T cristalizacion=53.2 C=326.2 K )
pC 6 H 4 Cl 2: H B =10250+ 94.07(326.2)0.1511( 326.2)2 cal/mol
H B =4357.6209 cal /mol
teorica
Tubo N8:( T cristalizacion=80 C=353 K )
FII UNMSM
LABORATORIO DE FISICOQUMICA
29
GASES
C 10 H 8: H A=426526.31(353)+0.1525(353)20.000214(353)3 cal/mol
H A =4567.2294 cal/mol
experimental
Tubo N8:( T cristalizacion=79.9 C=352.9 K )
C 10 H 8: H A=426526.31( 352.9)+0.1525(352.9)20.000214(352.9)3 cal/mol
H A =4567.0931 cal/mol
h) Determine el nmero de grados de libertad en el punto eutctico.
F+ P=C+1
F=CP+1=21+1=1
El grado de libertad es 1.
j) Compare los valores tericos con los experimentales.
Determinacin del error
experimental
|Valor tericoValor
|100
Valor terico
%E=
Errores de las fracciones molares
Error de tubo N1.
FII UNMSM
LABORATORIO DE FISICOQUMICA
30
GASES
|11.002
| 100 =0.20
1
%E=
Error de tubo N2:
|0.8760.875
|100 =0.11
0.876
%E=
Error de tubo N3:
|0.8090.800
|100 =1.11
0.809
%E=
Error de tubo N4:
|0.6390.629
|100 =1.56
0.639
%E=
Error de tubo N5:
|0.5410.499
|100 =7.76
0.541
%E=
Error de tubo N6:
|0.6780.595
|100 =12.24
0.678
%E=
Error de tubo N7:
|0.8550.766
|100 =10.41
0.855
%E=
Error de tubo N8:
|10.906
|100 =9.40
1
%E=
FII UNMSM
LABORATORIO DE FISICOQUMICA
31
GASES
VI.- CONCLUSIONES
Nuestro porcentaje de error se debe a que nuestras temperaturas varan
debido a que dejamos de agitar un momento y eso causa un porcentaje de
error.
Se deduce la temperatura de cristalizacin cuando empiezan a aparecer
pequeos cristales en el tubo.
El punto eutctico, se calcul hallando el punto ms bajo de temperatura, la
cual es la interseccin de las fases, las cuales fueron tres.
Hemos graficado los valores de
xA
con respecto a la temperatura y
observamos un descenso y luego un ascenso de la curva el cual indica el
equilibrio que describe este en cada fase.
FII UNMSM
LABORATORIO DE FISICOQUMICA
32
GASES
La grfica de la curva que nos representa el diagrama de fases de este
sistema de dos componentes; hallamos que segn el grfico el punto
eutctico est a una temperatura de 43C.
VII.- CUESTIONARIO
1. Qu es un diagrama de fases? Cul es la importancia?
FIGURA 6.1
Es la representacin entre diferentes estados de
la materia, en funcin de variables elegidas para
facilitar el estudio del mismo. Cuando en una de
estas representaciones todas las fases
corresponden a estados de agregacin
diferentes se suele denominar diagrama de
cambio de estado.
La lnea en el diagrama de fases lo divide en
regiones definidas, como slido, lquido y lquido
ms slido.
Esencialmente, la importancia del diagrama de
fases est en realizarlo para encontrar el punto
de fusin o de ebullicin de una mezcla de sustancias donde por efecto del
soluto, se ven modificadas los puntos de ebullicin o fusin del disolvente y
de manera grfica se puede predecir en qu proporcin se pueden separar
esta mezcla y a que temperatura se lograr la separacin.
Los diagramas de fases se realizan mediante condiciones de equilibrio
(enfriamiento lento) y son utilizados para entender y predecir muchos
aspectos del comportamiento de los materiales.
Parte de la informacin que se puede obtener a partir de ellos es la siguiente:
Fases presentes a diferentes composiciones y temperaturas.
Solubilidad de un elemento o compuesto en otro.
Temperatura a la cual una aleacin que se deja enfriar empieza a
solidificar as como el rango de temperaturas en el que tiene lugar la
solidificacin.
Temperatura a la que se funden o empiezan a fundirse las distintas fases.
FII UNMSM
LABORATORIO DE FISICOQUMICA
33
GASES
2. Describa un sistema eutctico simple no metlico
Eutctico es una mezcla de dos componentes con punto de fusin o punto de
vaporizacin mnima, inferior al correspondiente a cada uno de los
compuestos en estado puro. Esto ocurre en mezclas que poseen alta
estabilidad en estado lquido, cuyos componentes son inmiscibles en estado
slido.
En mezclas que presentan solubilidad total en estado slido, la temperatura
de solidificacin de la mezcla estar comprendida entre las correspondientes
a cada uno de los componentes en estado puro. De manera que al aumentar
la concentracin del componente de temperatura de solidificacin ms baja,
disminuir la temperatura de solidificacin de la mezcla. Dados un disolvente
y un soluto insolubles en estado slido, existe para ellos una composicin
llamada mezcla eutctica en la que, a presin constante, la adicin de soluto
ya no logra disminuir ms el punto de fusin. Esto hace que la mezcla
alcance el punto de congelacin (en caso de lquidos, licuefaccin) ms baja
posible y ambos se solidifiquen a esa temperatura (temperatura eutctica).
En procesos a presin constante, el cambio de estado en el caso de un
eutctico, a diferencia de las mezclas, tiene lugar a temperatura constante,
como en el caso de componentes puros.
3. En un diagrama de punto eutctico simple, explique la aplicacin de la
regla de la palanca.
La regla de la palanca es el
mtodo comnmente utilizado en
la
determinacin
de
la
composicin qumica real de
una aleacin en equilibrio a
cualquier temperatura en una
regin bifsica, como en las
fases slida y lquida presentes
en una aleacin de una cierta
concentracin
cuando
se
encuentra a una determinada
temperatura.
El porcentaje en peso del elemento B en el lquido viene dado por wl y en el
slido por ws. El porcentaje de slido y lquido puede ser calculado usando
las siguientes ecuaciones, que constituyen la regla de la palanca:
% peso de la fase slida
% peso de la fase lquida
Donde wo es el porcentaje en peso del elemento B en el sistema.
FII UNMSM
LABORATORIO DE FISICOQUMICA
34
GASES
FII UNMSM
LABORATORIO DE FISICOQUMICA
35
GASES
FII UNMSM
LABORATORIO DE FISICOQUMICA
36
También podría gustarte
- Práctica - 2 Ciencia de Los Materiales IiDocumento5 páginasPráctica - 2 Ciencia de Los Materiales IiGuussttAún no hay calificaciones
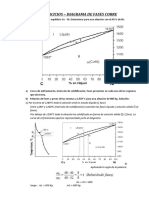
- Ejercicios Resueltos Diagrama de Fases COBREDocumento11 páginasEjercicios Resueltos Diagrama de Fases COBREDavid Zarate MansillaAún no hay calificaciones
- Tiempos Sublimacion - Tino SublimacionDocumento2 páginasTiempos Sublimacion - Tino SublimacionFrancis RiosAún no hay calificaciones
- Rodamientos PDFDocumento19 páginasRodamientos PDFRafael Chavez LopezAún no hay calificaciones
- Rodamientos PDFDocumento19 páginasRodamientos PDFRafael Chavez LopezAún no hay calificaciones
- Rodamientos PDFDocumento19 páginasRodamientos PDFRafael Chavez LopezAún no hay calificaciones
- Diagrama de Flijo Destilacion Simple QODocumento1 páginaDiagrama de Flijo Destilacion Simple QOMoOnse MoOnseAún no hay calificaciones
- Trabajo Final Labo EstDocumento26 páginasTrabajo Final Labo EstJaeger16Aún no hay calificaciones
- Investigacion OperativaDocumento153 páginasInvestigacion OperativaMarianoArguedasAún no hay calificaciones
- RODAMIENTOS Trabajo Monografico DescriptivaDocumento33 páginasRODAMIENTOS Trabajo Monografico DescriptivaJaeger16Aún no hay calificaciones
- 2 NormalizacionDocumento31 páginas2 NormalizacionJaeger16Aún no hay calificaciones
- Experiencia de Melde INFORME 2Documento16 páginasExperiencia de Melde INFORME 2Omar Garcia Flores100% (4)
- Lab Fiqi TermodinamicaDocumento32 páginasLab Fiqi TermodinamicaJaeger16Aún no hay calificaciones
- Electro Qui MicaDocumento28 páginasElectro Qui MicaJaeger16Aún no hay calificaciones
- Guia Rodamientos SKFDocumento23 páginasGuia Rodamientos SKFCirilo Hernandez Ayala100% (1)
- Diapos - 1Documento45 páginasDiapos - 1Jaeger16Aún no hay calificaciones
- Guia Rodamientos SKFDocumento23 páginasGuia Rodamientos SKFCirilo Hernandez Ayala100% (1)
- Informe de Fiscoquimica - Tema - Regla de FasesDocumento28 páginasInforme de Fiscoquimica - Tema - Regla de FasesJaeger16Aún no hay calificaciones
- Presión de VaporDocumento26 páginasPresión de VaporJaeger16Aún no hay calificaciones
- Informe de Fiscoquimica - Tema - Regla de FasesDocumento28 páginasInforme de Fiscoquimica - Tema - Regla de FasesJaeger16Aún no hay calificaciones
- Lab Fiqi TermodinamicaDocumento32 páginasLab Fiqi TermodinamicaJaeger16Aún no hay calificaciones
- Labo5 Tension SuperficialDocumento22 páginasLabo5 Tension SuperficialJaeger16Aún no hay calificaciones
- Fisica 2 ViscosidadDocumento14 páginasFisica 2 ViscosidadJaeger16Aún no hay calificaciones
- Diapo RodamientosDocumento12 páginasDiapo RodamientosJaeger16Aún no hay calificaciones
- Lab Fiqi TermodinamicaDocumento32 páginasLab Fiqi TermodinamicaJaeger16Aún no hay calificaciones
- SEMANA 4-Medidas de Variabilidad PDFDocumento65 páginasSEMANA 4-Medidas de Variabilidad PDFJaeger16Aún no hay calificaciones
- Lab 2 DensidadDocumento28 páginasLab 2 DensidadJaeger16Aún no hay calificaciones
- Regla de La Palanca TernarioDocumento10 páginasRegla de La Palanca TernarioEmanuelRomeroGAún no hay calificaciones
- Informe de Laboratorio 2Documento19 páginasInforme de Laboratorio 2Diego OxmanAún no hay calificaciones
- Examen 4 Unidad I Metodo Ponchon SavaritDocumento33 páginasExamen 4 Unidad I Metodo Ponchon SavaritKarel GerardoAún no hay calificaciones
- Qa Guia Tercer ParcialDocumento4 páginasQa Guia Tercer ParcialDiego SotresAún no hay calificaciones
- Resolución Parcial Quimica para Ingeniería UnlpDocumento6 páginasResolución Parcial Quimica para Ingeniería UnlpLiz BonaminoAún no hay calificaciones
- Tarea 2Documento19 páginasTarea 2Emily LeónAún no hay calificaciones
- Informe 3 Quimic LabDocumento4 páginasInforme 3 Quimic LabDenisse Hilda Yucra GuzmanAún no hay calificaciones
- PDF Cambios de Fase Del Agua - CompressDocumento22 páginasPDF Cambios de Fase Del Agua - CompressTania YankurAún no hay calificaciones
- Carburacion y Diagrama de FaseDocumento1 páginaCarburacion y Diagrama de FaseEysen PérezAún no hay calificaciones
- Tratamientos TérmicosDocumento2 páginasTratamientos TérmicosCamiloAún no hay calificaciones
- Caracterizacion 2-1Documento26 páginasCaracterizacion 2-1eduardoAún no hay calificaciones
- Practica 5Documento10 páginasPractica 5Christian Serna TerronesAún no hay calificaciones
- Taller Repaso DiagramasDocumento2 páginasTaller Repaso DiagramasDANIEL ISAIAS BAYONA PEãAAún no hay calificaciones
- Bloque 3Documento12 páginasBloque 3keniaAún no hay calificaciones
- Ejercicios de DestilacionDocumento12 páginasEjercicios de DestilacionClaudia Vanesa Gonzalez ReyesAún no hay calificaciones
- Destilacion EconomicaDocumento8 páginasDestilacion EconomicaDaniel MorenoAún no hay calificaciones
- Mezcla EutecticaDocumento10 páginasMezcla EutecticaEmanuel C QuisbertAún no hay calificaciones
- Clase N°3 Diagramas de FasesDocumento12 páginasClase N°3 Diagramas de FasesJordan G. TorresAún no hay calificaciones
- Temperatura de EbulliciónDocumento3 páginasTemperatura de Ebulliciónjuan carlosAún no hay calificaciones
- Reporte Azeotropo. Lab Equilibrio QuimicoDocumento10 páginasReporte Azeotropo. Lab Equilibrio QuimicoJose Emmanuel ChemaAún no hay calificaciones
- Azeótropo: A T (°C) B T (°C) T (°C) Azeótropo X (%) X (%) Tipo Máx/mín Agua (H O)Documento2 páginasAzeótropo: A T (°C) B T (°C) T (°C) Azeótropo X (%) X (%) Tipo Máx/mín Agua (H O)andreaAún no hay calificaciones
- Equilibrio de Fase PDFDocumento10 páginasEquilibrio de Fase PDFNevsaint MartinezAún no hay calificaciones
- Nicolas - EtanolDocumento12 páginasNicolas - EtanolAlejandro BallesterosAún no hay calificaciones
- Programa para Calculos de Columna de DestilaciónDocumento5 páginasPrograma para Calculos de Columna de DestilaciónAnonymous BYiAagMM2JAún no hay calificaciones
- COLUMNA ChemsepDocumento7 páginasCOLUMNA ChemsepLuluAún no hay calificaciones
- Ejercicio 8Documento3 páginasEjercicio 8jorge severinoAún no hay calificaciones