Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Rep Aspirina
Cargado por
Angel GazcaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Rep Aspirina
Cargado por
Angel GazcaCopyright:
Formatos disponibles
Universidad Nacional Autnoma de Mxico
Facultad de Estudios Superiores Cuautitln
Campo 1
Qumica
Laboratorio de qumica orgnica II
Georgina Franco Martnez
Luis Antonio Martnez Arellano
Reporte de la prctica
Acido Acetilsalicilico
Equipo 7
Gazca Villanueva ngel
Hernndez Capetillo Jorge Alberto
1/10/2014
Objetivos
La obtencin de un eter a partir de
un grupo fenlico y de anhdrido
actico, en un medio acido.
La sisntesis del Acido Acetil Salicilico
y las condiciones experimentales
para lograrlo.
La identificacin del Acido Acetil
Salicilico a partir de las propiedades
obtenidas experimentalmente.
Introduccin
Una esterificacin es el proceso por
el cual se sintetiza un ster, esto puede
ocurrir a partir de cidos carboxlicos,
alcoholes, cloruros de cido, anhdridos de
acido.
Los alcoholes reaccionan con los acidos
carboxlicos para formar alcoholes, se puede
realizar rpido si se utiiza un acido fuerte
como catalizador,aunque se mejora la
reactividad al convertir primero el acido
carboxlico en cloruro de acido carboxlico.
Los cloruros de acido reaccionan con
alcoholes para producir esteres, se realizan
en presencia de piridina o de NaOH que
reaccionan con el HCl formado.
Con frecuencia se ocupa el anhdrido actico
para la sntesis de esteres acetato a partir de
alcoholes. La aspirina se prepara por la
acetilacin del acido o-hidroxibenzoico con
anhdrido actico.
Hidrolisis
Ocurre cuando un ster se hidroliza por una
base o acido acuoso para producir un acido
carboxlico o un alcohol.
A la hidrolisis en disolucin bsica se le
conoce como saponificacin y ocurre de la
siguiente manera.
En cambio la que se realiza en disolucin
acida
El cido acetilsaliclico (cido
hidroxibenzoico) es un compuesto
bifuncional. Es un fenol (hidroxibenceno) y
un cido carboxlico. Por lo cual pueden
ocurrir dos reacciones diferentes de
esterificacin, actuando, el alcohol o la parte
cida en la reaccin. En presencia de
anhdrido actico, se forma cido
acetilsaliclico (aspirina); por el contrario, en
presencia de un exceso de metanol el
producto es salicilato de metilo. En este
experimento utilizaremos la primera
reaccin, para preparar aspirina. El cido
acetilsaliclico reacciona con el NaHCO3, para
formar una sal de sodio, soluble en agua,
mientras que el subproducto polimrico es
insoluble en NaHCO3. Esta diferencia de
solubilidades puede utilizarse en la
purificacin del producto final.
Mecanismo de Reaccin
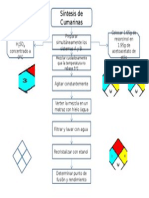
Diagrama de flujo
cido acetilsaliclico
En un matraz erlenmeyer colocar 1g de cido
acetilsaliclico, 2.5mL de anihdrido actico y 3 gotas
de acido sulfrico concentrado
Calentar en un bao maria durante 10 min y despues
enfriar para cristalizar.
Filtar al vaco y lave los cristales con agua helada.
Pesar para determinar rendimiento.
En tres tubo de ensaye colocar 5ml de agua y agregar
en el 1 fenol, en el tubo 2 acido acetilsalicilico, en el
tubo 3 el producto crudo por ultimo colocar una gota
de FeCl
3
.
Transferir el producto crrudo a un matraz y agregar
12.5 mL de una solucion daturada de de NaHCO
3.
Agitar hasta que no haya reaccion filtrar con 5 mL de
agua. Preparar una mezcla de 1.8mL de HCl
concentrado y 5mL de agua
Filtar lentamente y enfrie la mezcla para despues
filtar al vacio y lavar los crilstales con agua helada.
Pese los cristales y determine el punto de fusion y
calcule rendimiento (repetir prueba con FeCl
3
Disuelva el producto con el minimo de benceno
caliente, si hay solido filtar la solucion en caliente.
enfriar el filtrado hasta que precipite. Filtrar al vacio y
determinar rendimiento y punto de fusion (159C)
Resultados
Se obtuvieron 1.5 g de cristales blancos
brillantes, con un P.F de 135C ; sin purificar
el P.F fue de 125C
Pruebas
Anlisis de Resultados
Reactivo Cantidad moles
Acido
Saliclico
0.5g
3.62*10
-3
Anhdrido
Actico
2 ml
0.02115
Producto
Acido
Acetil
Saliclico
1.5g
8.31*10
-3
Al observar resultados se puede decir que el
rendimiento de la practica es muy bajo,
debido a 2 cosas, la primera que hubo un
pequeo derrame al momento de pasar los
cristales para su purificacin; la segunda es
que nuestro reactivo limitante es el acido
saliclico, el cual es el compuesto principal de
la reaccin puesto que ocupa la mayor parte
de la molcula del producto, con lo que no se
podra esperar un rendimiento alto.
En cuanto a la prueba de purificacin con
fenol y FeCl
3
-2
, se alcanzo a observar que la
que solo tena a l fenol y al FeCl
3
-2
presentaba un color morado, a la que se le
agrego el acido saliclico se torno de un color
gris concentrado, mientras la que contena el
producto crudo se torno de un color naranja
amarillezco, y as se podra decir que el
producto presentaba ciertas impurezas,
adems de que el primer PF era de 125C lo
que quedaba muy lejos del rango terico
reportado; al terminar la purificacin se
observo que el PF resultante fue de 135C
que al compararlo con el terico (138C) es
de una diferencia aceptable, sabiendo las
condiciones con las que trabajamos no son lo
suficientemente adecuadas, con lo que
podemos decir que se obtuvo el acido
acetilsalicilico aspirina.
Conclusiones
Se obtuvo un ester a partir de un grupo
fenolico (acido saliclico), comparando las
propiedades fsicas obtenidas con las
reportadas, en cuanto a las condiciones del
experimento, dadas las cantidades con las
que se trabajo el rendimiento fue muy bajo,
pero se puede concluir que el objetivo
principal de la practica el cual era la sntesis
de la aspirina se cumpli satisfactoriamente.
Referencias
McMurry, J., Qumica Orgnica, 5.
Edicin, Mxico, Ed. International
Thomson Editores, S.A. de C.V.,
2001.
Wade, L.G. Jr., Qumica Orgnica,
2. Edicin, Mxico.
También podría gustarte
- Dosis Pediatrica IPDocumento4 páginasDosis Pediatrica IPeliezer gomezAún no hay calificaciones
- Nomenclatura Organica OxigenadasDocumento2 páginasNomenclatura Organica OxigenadasDelincuente BuscadoAún no hay calificaciones
- ASTM D3230 - Método para Determinar Sal en CrudoDocumento19 páginasASTM D3230 - Método para Determinar Sal en CrudoJORGE ELIECER HERNÁNDEZ GARCÉS100% (1)
- Evolucion en El Pintado de PlásticosDocumento4 páginasEvolucion en El Pintado de PlásticosEmilio HipolaAún no hay calificaciones
- Planificación Unidad Hidrocarburos Cadena AbiertaDocumento3 páginasPlanificación Unidad Hidrocarburos Cadena Abiertavichosb67% (3)
- Azúcar blanco: características, propiedades y usos en pasteleríaDocumento3 páginasAzúcar blanco: características, propiedades y usos en pasteleríaVladimir Erick Mamani100% (1)
- Yodacion de AcetonaDocumento10 páginasYodacion de AcetonaAngel Gazca33% (3)
- HidantoinasDocumento2 páginasHidantoinasAngel GazcaAún no hay calificaciones
- CC de Nava Universidades Cultura de ResiduosDocumento36 páginasCC de Nava Universidades Cultura de ResiduosAngel GazcaAún no hay calificaciones
- Compromisos Internacionales de MéxicoDocumento28 páginasCompromisos Internacionales de MéxicoAngel GazcaAún no hay calificaciones
- Dioxinas y FuranosDocumento14 páginasDioxinas y FuranosAngel GazcaAún no hay calificaciones
- PiridinasDocumento18 páginasPiridinasAngel GazcaAún no hay calificaciones
- HidantoinasDocumento2 páginasHidantoinasAngel GazcaAún no hay calificaciones
- Modificación de La Síntesis de HäntzschDocumento8 páginasModificación de La Síntesis de HäntzschAngel GazcaAún no hay calificaciones
- Acido PicricoDocumento7 páginasAcido PicricoAngel GazcaAún no hay calificaciones
- AspirinaDocumento5 páginasAspirinaAngel GazcaAún no hay calificaciones
- Reporte Experimental 13. - CloretonaDocumento2 páginasReporte Experimental 13. - CloretonaJose Antonio Silva33% (3)
- Quimica IndutrialDocumento46 páginasQuimica IndutrialAngel GazcaAún no hay calificaciones
- OrganicaDocumento7 páginasOrganicaAngel GazcaAún no hay calificaciones
- Acido CinamicoDocumento8 páginasAcido CinamicoAngel GazcaAún no hay calificaciones
- Reporte Práctica 2 QO IIIDocumento3 páginasReporte Práctica 2 QO IIIAngel GazcaAún no hay calificaciones
- Diagrama de Sintesis de CumarinasDocumento1 páginaDiagrama de Sintesis de CumarinasAngel GazcaAún no hay calificaciones
- Organica 3Documento8 páginasOrganica 3Angel GazcaAún no hay calificaciones
- Previo Reaccion Diels AlderdDocumento9 páginasPrevio Reaccion Diels AlderdAngel GazcaAún no hay calificaciones
- Reducción selectiva de m-nitroanilinaDocumento5 páginasReducción selectiva de m-nitroanilinaAngel GazcaAún no hay calificaciones
- Como Se Defienden Las Plantas - Copia - PPT (Autoguardado)Documento36 páginasComo Se Defienden Las Plantas - Copia - PPT (Autoguardado)Rosany FacundoAún no hay calificaciones
- Actividad III3Documento3 páginasActividad III3Carlos Sequeda VelezAún no hay calificaciones
- Derivados OlefinasDocumento111 páginasDerivados Olefinasanthony p.Aún no hay calificaciones
- 04 Actividad Microbiana Sobre Sustratos EspecialesDocumento9 páginas04 Actividad Microbiana Sobre Sustratos EspecialesFabrizio Vasquez Cruzado0% (1)
- Copia de Vademecum SucedaneosDocumento11 páginasCopia de Vademecum SucedaneosVioletaLopezHernandez100% (1)
- Polietileno 1Documento31 páginasPolietileno 1jhonAún no hay calificaciones
- ALQUINOSDocumento18 páginasALQUINOSHalihins Jhonatan EspinozaAún no hay calificaciones
- Guia de Prácticas de Laboratorio AsignaturaDocumento5 páginasGuia de Prácticas de Laboratorio AsignaturaJuan Carlos Vargas VelásquezAún no hay calificaciones
- OHQ23NBTDocumento15 páginasOHQ23NBTAdrián GallardoAún no hay calificaciones
- Intensidad RespiratoriaDocumento234 páginasIntensidad Respiratoriaasuarez03100% (1)
- Celula-PSU GUIADocumento31 páginasCelula-PSU GUIAPorkSandwichAún no hay calificaciones
- Identificacion Materiales Plasticos AutomovilDocumento4 páginasIdentificacion Materiales Plasticos AutomovilMakarena Tapia RodriguezAún no hay calificaciones
- Taller Alquenos y AlquinosDocumento2 páginasTaller Alquenos y AlquinosThays Eliana BriceñoAún no hay calificaciones
- INDICADORES DE PH y CURVAS DE NEUTRALIZACIÓNDocumento9 páginasINDICADORES DE PH y CURVAS DE NEUTRALIZACIÓNjuanAún no hay calificaciones
- Proceso de Extraccion Del Aceite de Maiz.Documento3 páginasProceso de Extraccion Del Aceite de Maiz.santiago.velozpAún no hay calificaciones
- Efectos de La Contaminación Por Metales Pesados MercurioDocumento5 páginasEfectos de La Contaminación Por Metales Pesados MercurioMatias Vásquez0% (1)
- Diagrama de FlujoDocumento1 páginaDiagrama de FlujoKelly GCAún no hay calificaciones
- EBAU Biología Bloque 1: Componentes y estructura de la vidaDocumento2 páginasEBAU Biología Bloque 1: Componentes y estructura de la vidaRayz 2004 xAún no hay calificaciones
- Tarea6 Compuestos HeterociclicosDocumento8 páginasTarea6 Compuestos HeterociclicosHackson Rafael Vilcamango SanchezAún no hay calificaciones
- 38-Tesis Ip011 L52 PDFDocumento117 páginas38-Tesis Ip011 L52 PDFJose GomezAún no hay calificaciones
- Examen de Ubicacion Biologiasegundo BguDocumento5 páginasExamen de Ubicacion Biologiasegundo BguDarwin SanchezAún no hay calificaciones
- Taller de Exposiciones 5 Al 8Documento7 páginasTaller de Exposiciones 5 Al 8Jhoanna SernäAún no hay calificaciones
- AlcoholesDocumento8 páginasAlcoholesRonald Miguel E.Aún no hay calificaciones
- Quimica ActividadDocumento5 páginasQuimica Actividadflor benavides huamanAún no hay calificaciones