Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Equilibrio Químico
Cargado por
win104725Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Equilibrio Químico
Cargado por
win104725Copyright:
Formatos disponibles
1
UNIVERSIDAD DE SAN CARLOS DE GUATEMALA ESCUELA DE INGENIERA QUMICA
FACULTAD DE INGENIERA REA DE FISICOQUMICA
LABORATORIO DE FISICOQUMICA: 1 SECCIN: N
REPORTE
Practica No. 7
EQUILIBRIO DE REACCIN QUMICA
Jos Israel Reyes Cunech
Carn: 200815450
2
NDICE GENERAL
RESUMEN 3
OBJETIVOS. 5
RESULTADOS
1. Constante de equilibrio en funcin de agua 6
2. Constante de equilibrio en funcin volumen de acetato de etilo.. 7
3. Constante de equilibrio en funcin volumen de etanol.. 8
4. Constante de equilibrio en funcin volumen de acido actico.. 9
5. Constante de equilibrio en casos especiales 10
DISCUSIN DE RESULTADOS 11
CONCLUSIONES 14
RECOMENDACIONES.. 15
BIBLIOGRAFA 16
ANEXOS
a. Muestra de clculo 17
b. Datos calculados 21
c. Anlisis de error
i. Muestra de clculo.. 26
ii. Datos calculados.. 31
iii. Conclusiones.... 35
iv. Fuentes de error.. 36
3
RESUMEN
El presente documento contiene los datos empricos utilizados para calcular
la constante de equilibrio y el anlisis del equilibrio qumico de la reaccin del
etanol con cido actico en solucin acuosa variando los volmenes de los
reactivos y productos con el objeto de deducir relaciones grficas que ilustraran el
desarrollo del mismo.
Todos los procesos qumicos evolucionan desde los reactivos hasta la
formacin de productos a una determinada velocidad hasta que la reaccin se
completa. En ese momento, la velocidad de formacin de los productos es igual a
la velocidad de descomposicin de stos para formar nuevamente los reactivos de
los que proceden. Desde ese mismo momento las concentraciones de todas las
especies reaccionantes (reactivos y productos) permanecen constantes. Ese
estado se conoce con el nombre de equilibrio qumico. Es importante diferenciar
entre el equilibrio en trminos de velocidad, en el que ambas velocidades son
iguales, del equilibrio en trminos de concentraciones, donde stas pueden ser, y
normalmente son, distintas.
Se realiz una solucin de acetato de etilo, agua, cido actico y etanol,
variando el volumen de cado uno de los compuestos para cada solucin realizada.
Se agreg cido clorhdrico a cada una de las soluciones, el cual sirvi como
catalizador para luego titular la solucin con hidrxido de sodio.
4
Luego de realizar la titulacin y con los datos obtenidos se procedi a
calcular los moles iniciales de cada compuesto mediante estequiometria con el
volumen agregado a la solucin. Se calcul la concentracin al equilibrio del cido
actico y con ello se determin el grado de avance de la reaccin. Dado que el
grado de avance es igual para todos los compuestos, slo con saber los moles
iniciales se pudo determinar los moles al equilibrio y luego su concentracin.
Conociendo todas las concentraciones al equilibrio se pudo calcular la constante
de equilibrio y sus relaciones grficas.
Se obtuvieron 25 constantes de equilibrio con valores entre -0.01 y 10.5. A
partir de estos valores se obtuvieron relaciones graficas que muestran la constante
de equilibrio en funcin de la variacin de de volumen dentro de la solucin. En la
prctica se vari el volumen de agua, acetato de etilo, cido clorhdrico y etanol.
Al obtener las relaciones graficas de la constante de equilibrio en funcin de
la variacin de los mililitros de diferentes sustancias dentro de la solucin se
observo que la tendencia de los datos fue contraria al agregarle ms cantidad de
agua, cido actico y etanol. Sin embargo los valores de la constante de equilibrio
y la tendencia de la grafica al aumentar la cantidad de acetato de etilo fue
concuerda con las tendencias tericas. Y al tener nicamente productos en la
reaccin los valores de la constante tienen al infinito.
Los errores obtenidos por la incerteza de los instrumentos fueron por debajo
del 10% fijado como el lmite de aceptacin. Sin embargo los errores de precisin
obtenidos sobrepasaron el 10% de limite de aceptacin por lo cual se
consideraron los datos como insatisfactorios.
Se recomienda utilizar los instrumentos con la menor incerteza posible y
realizar tanto las titulaciones como las soluciones de manera atenta para lograr
obtener mejores resultados.
5
OBJETIVOS
General
Obtener datos empricos para calcular la constante de equilibrio de la
reaccin qumica del etanol con cido actico en disolucin acuosa, a partir
de estos datos deducir el tipo de relaciones grficas del equilibrio qumico y
determinar la validez de los resultados por medio del anlisis de error.
Especficos
1. Determinar las variables que permiten calcular la constante de equilibrio de
una reaccin qumica en fase lquida segn procedimientos establecidos.
2. Deducir el tipo de relaciones grficas necesarias para ilustrar el desarrollo
del equilibrio qumico en disolucin acuosa.
3. Analizar el efecto que los errores empricos tienen sobre los resultados y la
forma de manejarlos e interpretarlos.
6
RESULTADOS
Figura 1. Constante de equilibrio en funcin volumen de agua
Fuente: Tabla X, datos calculados.
Tabla I. Descripcin del modelo matemtico de la figura 1
Modelo R
2
Rango de
aceptacin(ml)
Incerteza
mxima
Keq = 4.43v
4
-22.7v
3
+
41.5v
2
-32.57v + 10.39
1.0000 0.0000 2.0000 0.09341
Fuente: Figura 1, resultados.
K
eq
0
2
4
6
8
10
12
0
2
4
6
8
10
12
Vol umen de H2O (ml )
-0.5 0 0.5 1 1.5 2 2.5
-0.5 0 0.5 1 1.5 2 2.5
7
Figura 2. Constante de equilibrio en funcin del volumen de acetato de
etilo
Fuente: Tabla X, datos calculados.
Tabla II. Descripcin del modelo matemtico de la figura 2
Modelo R
2
Rango de
aceptacin(ml)
Incerteza
mxima
Keq = 0.344v
2
-1.356v +
1.90
0.96912 0.000 2.000 0.00039
Fuente: Figura 2, resultados.
K
eq
0.4
0.6
0.8
1
1.2
1.4
1.6
1.8
2
0.4
0.6
0.8
1
1.2
1.4
1.6
1.8
2
vol umen de acetato de eti l o (ml )
-0.5 0 0.5 1 1.5 2 2.5
-0.5 0 0.5 1 1.5 2 2.5
8
Figura 3. Constante de equilibrio en funcin del volumen de etanol
Fuente: Tabla X, datos calculados.
Tabla III. Descripcin del modelo matemtico de la figura 3
Modelo R
2
Rango de
aceptacin(ml)
Incerteza
mxima
Keq = -34.2v
2
+1.27v -67.9 0.9771 0.000 2.000 0.59152
Fuente: Figura 3, resultados
K
eq
-0.8
-0.6
-0.4
-0.2
0
0.2
0.4
0.6
-0.8
-0.6
-0.4
-0.2
0
0.2
0.4
0.6
vol umen de etanol (ml )
-0.5 0 0.5 1 1.5 2 2.5
-0.5 0 0.5 1 1.5 2 2.5
9
Figura 4. Constante de equilibrio en funcin del volumen de cido
actico
Fuente: Tabla X, datos calculados.
Tabla IV. Descripcin del modelo matemtico de la figura 4
Modelo R
2
Rango de
aceptacin(ml)
Incerteza
mxima
Keq = -0.24v
2
+0.99v -0.526 0.9540 0.000 2.000 0.48177
Fuente: Figura 4, resultados
K
eq
-0.6
-0.4
-0.2
0
0.2
0.4
0.6
-0.6
-0.4
-0.2
0
0.2
0.4
0.6
vol umen de ci do acti co (ml )
-0.5 0 0.5 1 1.5 2 2.5
-0.5 0 0.5 1 1.5 2 2.5
10
Tabla V. Constantes de equilibrio de los casos especiales
Solucin Keq
21 2.47780
22 0.00007
23 0.45455
24 0.60791
Fuente: Tabla X, datos calculados.
Figura 5. Constante de equilibrio en funcin de las soluciones
Fuente: Tabla V, resultados.
K
eq
0
0.5
1
1.5
2
2.5
0
0.5
1
1.5
2
2.5
Sol uci n
20 21 22 23 24 25
20 21 22 23 24 25
11
DISCUSIN DE RESULTADOS
En la figura 1 se aprecia la constante K de equilibrio de reaccin al variar
los mililitros de agua dentro de la solucin titulada. Los valores de la constante K
se encuentran entre 0 y 12, al ser el agua un producto de la reaccin analizada la
grafica debera de tener una tendencia positiva, debido a que existe una mayor
cantidad de productos sin embargo en la figura obtenida la tendencia es contraria.
Los valores de K s concuerdan con los tericos, debido a que existen ms
productos y la mayora de los reactivos si reaccionaron las constantes de equilibrio
deben ser mayores que 1.
Para la figura 2 se muestra la constante de equilibrio al variar los mililitros
de acetato de etilo dentro de la solucin preparada, al ser el acetato de etilo un
reactivo de la reaccin se tienen valores de la constante de equilibrio debe ser
menor que 1 como se muestra en la grfica obtenida. Al aumentar los mililitros de
acetato de etilo se aumenta la concentracin de reactivos en la reaccin por lo que
los valores de la constante deben de disminuir, por lo que la tendencia de la
grafica si es correcta, segn las definiciones tericas.
En la figura 3 se presenta la constante de equilibrio variando los mililitros de
etanol, el etanol es un reactivo en la reaccin analizada, por lo que los valores de
la constante deben de ser valores menores que 1, sin embargo en la grfica se
presentan valores de la constante negativos y la constante no puede tener valores
negativos por lo que los resultados de esta grfica no son confiables ya que no
concuerdan con los valores esperados. Al igual que los valores de la constante la
tendencia de la grfica es contraria a la tendencia terica.
12
Para la figura 4 se muestra la constante de equilibrio en funcin de la
variacin de los mililitros de cido actico dentro de la solucin a analizar. Al ser el
cido actico un producto de la reaccin obtenida la tendencia de la grafica
deberia de ser negativa ya que al aumentar la cantidad de productos la constante
debe disminuir, siendo lo contrario de la grfica obtenida. Los valores de la
constante de equilibrio deben de ser menores que 1, sin embargo no pueden
existir valores negativos, como se muestran en la grfica obtenida, por lo que los
valores calculados no son confiables.
En la figura 5 se muestran los casos especiales analizados para esta
reaccin. En la solucin 21 existe la misma cantidad de productos como de
reactivos obteniendo una constante de equilibrio de 2.47 este valor se debe a que
al reaccionar el acetato de etilo con el etanol producen acido actico por lo que
existe nicamente productos en la reaccin. Para la solucin 22 existe al igual que
la solucin anterior la misma cantidad de productos y reactivos presentes
obteniendo una constante de equilibrio fue de 0.0007 esto pudo ser causado a que
existen nicamente productos en la reaccin. Al tener solo productos en una
reaccin qumica la constante de equilibrio tiende al infinito.
Para la solucin 23 se tiene una mayor cantidad de reactivos que de
productos, por lo que se obtuvo una constante de equilibrio de 0.45455, de
acuerdo con los datos tericos la constante debe ser menor que 1 por lo que el
valor obtenido si corresponde a esta teora. Para la solucin 24 se tienen ms
productos que reactivos por lo que la constante de equilibrio debe ser mayor que
uno, sin embargo el valor obtenido fue de 0.60791 por lo que el valor obtenido no
fue el esperado.
13
Los errores de incertidumbre provocados por los instrumentos utilizados
estuvieron por debajo del 10%, lo que indica que no influyen de manera
considerable en los resultados obtenidos. Los errores de precisin sobrepasan
valores de 50% por lo que se concluye que los resultados no son los esperados y
no se pueden considerar como confiables. El porcentaje de error obtenido fue
causado porque se utiliz el promedio del grado de avance, siendo estos valores
muy pequeos, por lo que los valores del error aumentaron considerablemente.
14
CONCLUSIONES
1. Conforme se iban agregando mayores volmenes de agua la constante iba
disminuyendo.
2. La tendencia de la figura de constante de equilibrio versus volumen de
acetato de etilo tuvo una tendencia negativa, lo que indica que a menos
volumen menor ser la constante de equilibrio.
3. La tendencia de la grfica de constante de equilibrio versus volumen de
etanol demuestra que a ms cantidad de etanol mayor ser la constante de
equilibrio.
4. La constante de equilibrio es directamente proporcional al volumen de cido
actico.
5. Los errores de incertidumbre estn por debajo del 10% por lo que no
influyen en los datos obtenidos. Sin embargo los errores de precisin
sobrepasaron valores del 50% por lo que los datos no son confiables.
15
RECOMENDACIONES
1. Estandarizar el hidrxido de sodio para poder conocer su concentracin real
antes de realizar la titulacin.
2. Realizar las correctamente las titulaciones para controlar bien el punto de
viraje.
3. Repetir las titulaciones donde el error sea mayor al establecido como
aceptable.
4. Hacer soluciones ms cantidad de las soluciones a titular para tener el mismo
volumen en todas las alcuotas.
16
REFERENCIAS BIBLIOGRFICAS
1. CHANG, Raymond. Equilibrio qumico Qumica. Dcima edicin. Mxico:
McGraw-Hill Interamericana, 2010. 1085 p. ISBN: 978-607-15-0307-7. pp. 18,
147-150, 616-644.
2. LEVINE, Ira. Equilibrio qumico en sistemas no ideales. Fisicoqumica. Cuarta
edicin. Volumen 1 Mxico: McGraw-Hill Interamericana, 1996. 427 p. ISBN:
84-481-0616-4. pp. 315-332
3. PERRY, Robert. Reaction Kinetics. PERRYS chemical engineers Handbook.
Green, Don (edit. Lit.). Octava edicin. E.E.U.U.: McGraw-Hill, 2008. 2735 p.
ISBN: 0-07-142294-3. pp. 7-7
4. WONNACOTT, Thomas H. Fundamentos de estadstica para administracin y
economa. Primera edicin. Mxico: Editorial Limusa, 1979. 623 p. ISBN-0-471-
95966-9, pp. 39, 231.
5. Laboratorio de fisicoqumica, Herramientas de ayuda para elaboracin de
reporte, annimo, Guatemala Centro Amrica 2010 [Ref. de 14 de agosto
2013], disponible en web: sites.google.com/site/labfisico/
17
ANEXOS
a. Muestra de clculo
Ecuacin de reaccin
CH
3
COOC
2
H
5
+ H
2
O CH
3
COOH + C
2
H
5
OH
Ec. No. 1
Ref. 1, pp. 620
Masa del compuesto en la solucin
m = V
Ec. No. 2
Ref. 1, pp. 18
Donde
m es la masa del compuesto en la solucin (g)
es la densidad del compuesto (g/ml)
V es el volumen del compuesto agregado a la solucin (ml)
Ejemplo
Para conocer la masa del acetato de etilo en la alcuota se tiene que el volumen
de acetato agregado fue de 2 mL y la densidad de este es 0.9 g/ml, por lo que se
obtiene:
m = (
0.9g
ml
) (2ml) = 1.8 g
Los resultados se reportan en la tabla VI.
18
Nmero de moles iniciales
n =
m
M
Ec. No. 3
Ref. 1, pp. 83
Donde
n es el nmero de moles iniciales en la solucin (mol)
m es la masa del compuesto en la solucin (g)
M es la masa molecular de la alcuota (g/mol)
Ejemplo:
Determinar el nmero de moles que se tienen de acetato de etilo si este posee
una masa de 1.8 g y la masa molecular de este es 88.1052 g/mol
n =
1.8 g
(88.1052
g
mol
)
= 0.02043 mol
Los resultados se reportan en la tabla VI.
Molaridad
M =
n
V
T
Ec. No. 4
Ref. 1, pp. 147
Donde
M es la molaridad del compuesto en la solucin (mol/L)
n es el nmero de moles en la solucin (mol)
V
T
es el volumen total de la solucin (L)
Ejemplo:
Para conocer la molaridad del acido actico en la solucin se sabe que hay
0.03497 mol en la solucin y que esta tiene un volumen 0.00700 L.
M =
(0.03497 mol)
0.00700 L
= 4.99570 mol/L
Los resultados se reportan en la tabla IX.
19
Concentracin al titular
2
=
1
2
Ec. No. 5
Ref 1, pp. 150
Donde
C2 es la concentracin del cido actico (mol/L)
C1 es la concentracin del hidrxido de sodio (mol/L)
V1 es el volumen de NaOH necesario para la titulacin (ml)
V2 es el volumen de cido actico que se titul (ml)
Ejemplo:
Determine la concentracin de cido actico si se sabe que se utilizaron 21 ml de
NaOH a 0.5 M para titular 2 ml de cido.
2
=
(0.5)(21)
(2)
= 5.25
Los resultados se reportan en la tabla VII.
Grado de avance de la reaccin
= n
eq
n
i
Ec. No. 6
Ref. 2, pp. 325
Donde
es el grado de avance de la reaccin (mol)
n
eq
es el nmero de moles al equilibrio del compuesto (mol)
n
i
es el nmero de moles iniciales del compuesto (mol)
20
Ejemplo:
Para conocer el grado de avance de la reaccin se tiene 0.02923 moles al
equilibrio y 0.03497 moles iniciales. Segn la ecuacin se obtiene:
= (0.02923mol) (0.03497mol) = 0.00574 mol
Los resultados se reportan en la tabla VIII.
Constante de equilibrio de reaccin
=
[
3
][
2
5
]
[
3
5
][
2
]
Ec. No. 7
Ref. 3, pp. 7-7
Donde:
K
eq
es la constante de equilibrio de una reaccin
[CH
3
COOH] es la concentracin al equilibrio del CH
3
COOH (mol/L)
[C
2
H
5
OH] es la concentracin al equilibrio del C
2
H
5
OH (mol/L)
[CH
3
COOC
2
H
5
] es la concentracin al equilibrio del CH
3
COOC
2
H
5
(mol/L)
[H
2
O] es la concentracin al equilibrio del H
2
O (mol/L)
Ejemplo:
Para calcular la constante de equilibrio se tiene 6,32647 M de concentracin al
equilibrio de CH3COOH, 6,35650 M de concentracin al equilibrio de C2H5OH,
4,08958 M de concentracin al equilibrio de CH3CHOOC2H5 y 0,94648 M de
concentracin al equilibiro de H2O, a partir de la ecuacin se obtiene:
=
(6,32647 M)(6,35650 M)
(0,94648 M)(4,08958 M)
= 10,38938
Los resultados se reportan en la tabla X.
21
b. Datos calculados
Tabla VI. Moles iniciales en la solucin
Solucin
Moles
H2O
Moles
CH3COOC2H5
Moles
C2H5OH
Moles
CH3COOH
Moles
HCl
1 0.0000 0.0204 0.0351 0.0349 0.0162
2 0.0277 0.0204 0.0351 0.0349 0.0162
3 0.0555 0.0204 0.0351 0.0349 0.0162
4 0.0832 0.0204 0.0351 0.0349 0.0162
5 0.1110 0.0204 0.0351 0.0349 0.0162
6 0.1110 0.0000 0.0351 0.0349 0.0162
7 0.1110 0.0051 0.0351 0.0349 0.0162
8 0.1110 0.0102 0.0351 0.0349 0.0162
9 0.1110 0.0153 0.0351 0.0349 0.0162
10 0.1110 0.0204 0.0351 0.0349 0.0162
11 0.1110 0.0204 0.0000 0.0349 0.0162
12 0.1110 0.0204 0.0087 0.0349 0.0162
13 0.1110 0.0204 0.0175 0.0349 0.0162
14 0.1110 0.0204 0.0263 0.0349 0.0162
15 0.1110 0.0204 0.0351 0.0349 0.0162
16 0.1110 0.0204 0.0351 0.0000 0.0162
17 0.1110 0.0204 0.0351 0.0087 0.0162
18 0.1110 0.0204 0.0351 0.0174 0.0162
19 0.1110 0.0204 0.0351 0.0262 0.0162
20 0.1110 0.0204 0.0351 0.0349 0.0162
21 0.0555 0.0102 0.0527 0.0524 0.0162
22 0.1665 0.0306 0.0175 0.0174 0.0162
23 0.0555 0.0306 0.0527 0.0174 0.0162
24 0.1665 0.0102 0.0175 0.0524 0.0162
25 0.4440 0.0000 0.0000 0.0000 0.0162
Fuente: Ecuacin 3, muestra de clculo; hoja de datos originales.
22
Tabla VII. Concentracin de cido actico al titular
Solucin
Volumen
1 (ml)
Volumen
2 (ml)
Volumen
3 (ml)
[CH3COOH]
muestra 1
[CH3COOH]
muestra 2
[CH3COOH]
muestra 3
1 21.0000 19.0000 8.4500 5.2500 4.7500 4.2250
2 16.7000 18.0000 16.2000 4.1750 4.5000 4.0500
3 16.6000 15.2000 16.5000 4.1500 3.8000 4.1250
4 16.8000 16.6500 15.1000 4.2000 4.1625 3.7750
5 17.1000 16.2000 16.3000 4.2750 4.0500 4.0750
6 15.5000 17.7000 16.5000 3.8750 4.4250 4.1250
7 16.2000 14.7000 17.3000 4.0500 3.6750 4.3250
8 16.9000 16.1000 14.8000 4.2250 4.0250 3.7000
9 17.5000 16.6000 16.4500 4.3750 4.1500 4.1125
10 17.1000 17.7000 16.9000 4.2750 4.4250 4.2250
11 29.9000 31.5000 16.4000 7.4750 7.8750 8.2000
12 25.5000 25.0000 25.5000 6.3750 6.2500 6.3750
13 23.6000 21.3500 21.2000 5.9000 5.3375 5.3000
14 18.0000 19.2000 19.3000 4.5000 4.8000 4.8250
15 16.2500 15.6000 17.3000 4.0625 3.9000 4.3250
16 9.4500 8.9000 9.0000 2.3625 2.2250 2.2500
17 10.5000 10.5000 10.2000 2.6250 2.6250 2.5500
18 13.2000 13.2000 12.9500 3.3000 3.3000 3.2375
19 13.7500 14.7000 15.1000 3.4375 3.6750 3.7750
20 15.7500 16.1500 16.7000 3.9375 4.0375 4.1750
21 17.1000 16.9000 16.6500 4.2750 4.2250 4.1625
22 16.1000 16.6000 16.2000 4.0250 4.1500 4.0500
23 10.6500 10.5000 11.0000 2.6625 2.6250 2.7500
24 25.7500 25.9000 26.5000 6.4375 6.4750 6.6250
25 3.10000 2.85000 2.75000 0.7750 0.7125 0.6875
Fuente: Ecuacin 5, Muestra de clculo; Hoja de datos originales.
23
Tabla VIII. Grado de avance de la reaccin
Solucin
Moles
CH3COOH
muestra 1
Moles
CH3COOH
muestra 2
Moles
CH3COOH
muestra 3
Grado de
avance 1
(mol)
Grado de
avance 2
(mol)
Grado de
avance 3
(mol)
1 0.0341 0.0309 0.0275 -0.0069 -0.0041 -0.0075
2 0.0292 0.0315 0.0284 -0.0057 -0.0035 -0.0066
3 0.0311 0.0285 0.0309 -0.0038 -0.0065 -0.0040
4 0.0336 0.0333 0.0302 -0.0014 -0.0017 -0.0015
5 0.0363 0.0344 0.0346 -0.0005 -0.0005 -0.0003
6 0.0252 0.0288 0.0268 -0.0098 -0.0062 -0.0082
7 0.0284 0.0257 0.0303 -0.0066 -0.0092 -0.0047
8 0.0317 0.0302 0.0278 -0.0033 -0.0048 -0.0072
9 0.0350 0.0332 0.0329 -0.0028 -0.0018 -0.0021
10 0.0363 0.0376 0.0359 0.0014 0.0026 0.0009
11 0.0486 0.0512 0.0533 0.0136 0.0162 0.0183
12 0.0446 0.0438 0.0446 0.0097 0.0088 0.0097
13 0.0443 0.0400 0.0398 0.0093 0.0051 0.0048
14 0.0360 0.0384 0.0386 0.0010 0.0034 0.0036
15 0.0345 0.0332 0.0368 -0.0004 -0.0018 -0.0018
16 0.0154 0.0145 0.0146 0.0154 0.0145 0.0146
17 0.0184 0.0184 0.0179 0.0096 0.0096 0.0091
18 0.0248 0.0248 0.0243 0.0073 0.0073 0.0068
19 0.0275 0.0294 0.0302 0.0013 0.0032 0.0040
20 0.0335 0.0343 0.0355 -0.0006 -0.0007 -0.0005
21 0.0363 0.0359 0.0354 -0.0161 -0.0165 -0.0171
22 0.0342 0.0353 0.0344 0.0167 0.0178 0.0169
23 0.0226 0.0223 0.0234 0.0051 0.0048 0.0059
24 0.0547 0.0550 0.0563 0.0023 0.0026 0.0039
25 0.0066 0.0061 0.0058 0.0066 0.0061 0.0058
Fuente: Ecuacin 3 y 6, muestra de clculo; tabla VII.
24
Tabla IX. Moles de los compuestos al equilibrio
Solucin
Moles
H2O
Moles
CH3COOC2H5
Moles
C2H5OH
Moles
CH3COOH
1 0.0062 0.0266 0.0413 0.0411
2 0.0330 0.0257 0.0404 0.0402
3 0.0603 0.0252 0.0399 0.0398
4 0.0848 0.0219 0.0367 0.0365
5 0.1115 0.0209 0.0356 0.0354
6 0.1191 0.0080 0.0432 0.0430
7 0.1179 0.0120 0.0420 0.0418
8 0.1161 0.0153 0.0403 0.0401
9 0.1132 0.0175 0.0374 0.0372
10 0.1094 0.0188 0.0335 0.0333
11 0.0950 0.0044 -0.0161 0.0189
12 0.1017 0.0111 -0.0006 0.0256
13 0.1046 0.0141 0.0112 0.0286
14 0.1083 0.0177 0.0237 0.0323
15 0.1124 0.0218 0.0365 0.0363
16 0.0962 0.0056 0.0204 -0.0148
17 0.1016 0.0110 0.0257 -0.0007
18 0.1039 0.0133 0.0281 0.0104
19 0.1082 0.0176 0.0324 0.0234
20 0.1116 0.0210 0.0357 0.0356
21 0.0721 0.0268 0.0693 0.0690
22 0.1494 0.0135 0.0004 0.0003
23 0.0502 0.0254 0.0475 0.0122
24 0.1636 0.0073 0.0147 0.0496
25 0.4379 -0.0062 -0.0062 -0.0062
Fuente: Ecuacin 6, muestra de clculo; Tabla VIII.
25
Tabla X. Constante de equilibrio
Solucin Keq
1 10.389
2 1.9168
3 1.0447
4 0.7193
5 0.5420
6 1.9397
7 1.2465
8 0.9074
9 0.7000
10 0.5437
11 -0.7309
12 -0.0130
13 0.2179
14 0.3978
15 0.5419
16 -0.5581
17 -0.0165
18 0.2103
19 0.3974
20 0.5420
21 2.4778
22 0.0001
23 0.4546
24 0.6079
25 -0.0141
Fuente: Ecuacin 4 y 7; muestra de clculo; Tabla IX.
26
C. Anlisis de error
I. Muestra de clculo
Incerteza de la masa del compuesto en la solucin
dm = dV
Ec. No. 8
Ref. 1, pp. 18
Donde
dm es la incerteza de la masa del compuesto en la solucin (g)
es la densidad de la solucin (g/mL)
dV es el diferencial de volumen (mL)
Ejemplo:
Para calcular la incerteza de la masa del acetato de etilo se tiene que su densidad
de 0.9 g/ml, peso molecular de 88.1052 g/mol y la incerteza de la pipeta es de
0,05ml, segn la ecuacin de incerteza se obtiene:
dm = (
0.9
g
ml
88.1052
g
mol
)(0.05 ml) = 0,00051g
Los resultados se reportan en la tabla XI.
Incerteza del nmero de moles iniciales
dn =
dV
M
Ec. No. 9
Ref. 1, pp. 83
Donde
dn es el diferencial del nmero de moles iniciales (mol)
es la densidad del compuesto (g/mL)
dV es el diferencial de volumen (mL)
M es la masa molecular de la alcuota (g/mol)
Ejemplo:
27
Para calcular el diferencial del nmero de moles iniciales se tiene una densidad de
acetato de etilo de0.9 g/ml, 0.05 ml de incerteza de la pipeta y 88.1052 g/mol de
masa molecular, utilizando la ecuacin anterior se obtiene:
dn =
(
0.9g
ml
) (0.05ml)
88.1052 g/mol
= 0,00051 mol
Los resultados se reportan en la tabla XII.
Incerteza de la molaridad de una alcuota
dM =
dn
V
T
Ec. No. 10
Ref. 1, pp. 147
Donde
dM es el diferencial de la molaridad (mol/L)
dn es el diferencial del nmero de moles (mol)
V
T
es el volumen total de la solucin (L)
Ejemplo:
Para conocer el diferencial de la molaridad se tiene un diferencial del nmero de
moles de 0,07858 mol y 0,00650 L de volumen total, de acuerdo a la ecuacin
anterior se obtiene:
=
0,00051
0.00650
= 0.7858 /
Los resultados se reportan en la tabla XIV.
Incerteza del grado de avance
d = dn
eq
dn
i
Ec. No. 11
Ref. 2, pp. 325
28
Donde
d es el diferencial del grado de avance de la reaccin (mol)
dn
eq
es el diferencial de los moles al equilibrio de un compuesto (mol)
dn
i
es el diferencial de los moles iniciales de un compuesto (mol)
Ejemplo:
Para conocer el diferencial del grado de avance de la reaccin se tiene un
diferencial de moles al equilibrio de 0,43327 mol y un diferencial de moles iniciales
de 0,00278 mol, segn la ecuacin anterior se obtiene:
d = (0.43327 mol) (0.00278 mol) = 0.4305 mol
Los resultados se reportan en la tabla XIII.
Incerteza de la constante de equilibrio de una reaccin
dK
eq
=
d[CH
3
COOH][C
2
H
5
OH]
[CH
3
COOC
2
H
5
][H
2
O]
[CH
3
COOH]d[C
2
H
5
OH]
[CH
3
COOC
2
H
5
][H
2
O]
+
[CH
3
COOH][C
2
H
5
OH]
[CH
3
COOC
2
H
5
]
2
[H
2
O]
+
[CH
3
COOH][C
2
H
5
OH]
[CH
3
COOC
2
H
5
][H
2
O]
2
Ec. No. 12
Ref. 3, pp. 7-7
Donde
dK
eq
es el diferencial de la constante de equilibrio
[CH
3
COOH] es la concentracin al equilibrio del CH
3
COOH (mol/L)
[C
2
H
5
OH] es la concentracin al equilibrio del C
2
H
5
OH (mol/L)
[CH
3
COOC
2
H
5
] es la concentracin al equilibrio del CH
3
COOC
2
H
5
(mol/L)
[H
2
O] es la concentracin al equilibrio del H
2
O (mol/L)
d[CH
3
COOH] es el diferencial de la concentracin del CH
3
COOH (mol/L
d[C
2
H
5
OH] es el diferencial de la concentracin del C
2
H
5
OH (mol/L)
29
Ejemplo:
Para encontrar el diferencial de la constante de equilibrio se tiene 0,13525 M de
diferencial de la concentracin al equilibrio del
2
5
, 0,13450 M de diferencial
de la concentracin al equilibrio de
3
, 6.32647 M de concentracin al
equilibrio del
3
, 6.35650 M de concentracin al equilibrio de
5
, 4.08958 M de concentracin al equilibrio de
3
5
y 0,94648M de
concentracin a equilibrio de H2O, utilizando la ecuacin anterior se obtiene:
dK
eq
=
(0,13450 M )(6.35650 M )
(4.08958 M)(0,94648M)
(6.32647 M)(0,13525 M)
(4.08958 M)(0,94648M)
+
(6.32647 M)(6.35650 M )
(4.08958 M)(0,94648M)
+
(6.32647 M)(6.35650 M )
(4.08958 M)(0,94648M)
2
dK
eq
= 0,09341
Los resultados se reportan en la tabla XV.
Media de los datos
Ec. No. 13
Ref. 5, pp. 2
Donde:
x
i
es el promedio de los datos (mol)
xi son los datos calculados (mol)
n es el nmero de datos
Ejemplo:
Para conocer el promedio de los datos se tienen los siguientes datos de grado de
avance -0.00685, -0.00409 y -0.00751
x
i
=
0.01845
3
= 0.00615mol
Los resultados se reportan en la tabla XI.
30
Desviacin estndar
=
(x
n
1
x
i
)
2
n-1
Ec. No. 14
Ref. 4, pp. 6
Donde:
es la desviacin estndar de los datos (mol)
x es la media de los datos (mol)
xi son los datos calculados
n es el nmero de dato
Ejemplo:
Para encontrar la desviacin estndar de los datos se tiene 0.00615 de media, 3
nmeros de datos y -0,00685, -0,00409, -0,00751 de datos calculados, segn la
ecuacin anterior se obtiene:
=
(0.00615 (0,00685))
2
+ (0.00615 (0,00409))
2
+ (0.00615 (0,00751))
2
2
= 0,00181
Los resultados se reportan en la tabla XI.
Coeficiente de variacin
C
v
=
x
*100
Ec. No. 15
Ref. 5, pp. 231
Donde:
Cv es el coeficiente de variacin (%)
es la desviacin estndar (mol)
es la media de los datos (mol)
31
Ejemplo:
Para conocer el coeficiente de variacin se tiene una desviacin estndar de
0,00181 y un promedio de -0,00615, utilizando la ecuacin se obtiene:
C
v
=
(0.00181)
(0,00615)
*100=-29,4417%
Los resultados se reportan en la tabla XI.
II. Datos calculados
Tabla XI. Error de precisin
Solucin
Promedio
del grado de
avance (mol)
Varianza
(mol)
Coeficiente
de variacin
(%)
1 -0.0062 0.0018 -29.4417
2 -0.0053 0.0016 -30.8061
3 -0.0048 0.0015 -30.6209
4 -0.0015 0.0002 -10.0978
5 -0.0004 0.0001 -24.0269
6 -0.0080 0.0018 -22.2380
7 -0.0069 0.0023 -33.3266
8 -0.0051 0.0020 -39.0048
9 -0.0022 0.0005 -23.1848
10 0.0017 0.0009 53.5892
11 0.0161 0.0024 14.7022
12 0.0094 0.0005 5.3953
13 0.0064 0.0025 39.5494
14 0.0027 0.0014 53.6513
15 -0.0014 0.0008 -58.4784
16 0.0148 0.0005 3.2136
17 0.0095 0.0003 3.2050
18 0.0071 0.0003 3.8070
19 0.0028 0.0014 49.4262
20 -0.0006 0.0001 -11.5161
21 -0.0166 0.0005 -2.8901
22 0.0172 0.0006 3.2778
23 0.0053 0.0005 10.3108
24 0.0029 0.0008 29.0668
25 0.0062 0.0004 6.2165
Fuente: Ecuacin 13, 14 y 15, muestra de clculo; Tabla VIII.
32
Tabla XII. Incerteza de los moles iniciales
Solucin
dMoles
H2O
dMoles
CH3COOC2H5
dMoles
C2H5OH
dMoles
CH3COOH
1 0.0028 0.0005 0.0009 0.0009
2 0.0028 0.0005 0.0009 0.0009
3 0.0028 0.0005 0.0009 0.0009
4 0.0028 0.0005 0.0009 0.0009
5 0.0028 0.0005 0.0009 0.0009
6 0.0028 0.0005 0.0009 0.0009
7 0.0028 0.0005 0.0009 0.0009
8 0.0028 0.0005 0.0009 0.0009
9 0.0028 0.0005 0.0009 0.0009
10 0.0028 0.0005 0.0009 0.0009
11 0.0028 0.0005 0.0009 0.0009
12 0.0028 0.0005 0.0009 0.0009
13 0.0028 0.0005 0.0009 0.0009
14 0.0028 0.0005 0.0009 0.0009
15 0.0028 0.0005 0.0009 0.0009
16 0.0028 0.0005 0.0009 0.0009
17 0.0028 0.0005 0.0009 0.0009
18 0.0028 0.0005 0.0009 0.0009
19 0.0028 0.0005 0.0009 0.0009
20 0.0028 0.0005 0.0009 0.0009
21 0.0028 0.0005 0.0009 0.0009
22 0.0028 0.0005 0.0009 0.0009
23 0.0028 0.0005 0.0009 0.0009
24 0.0028 0.0005 0.0009 0.0009
25 0.0028 0.0005 0.0009 0.0009
Fuente: Ecuacin 8 y 9, muestra de clculo; Tabla VI.
33
Tabla XIII. Incerteza de los moles al equilibrio
Solucin
dneq
H2O
(mol)
dneq
CH3COOC2H5
(mol)
dneq
C2H5OH
(mol)
dneq
CH3COOH
(mol)
1 0.4333 0.0847 0.1414 0.1407
2 0.4019 0.0782 0.1309 0.1302
3 0.3749 0.0729 0.1220 0.1214
4 0.3485 0.0653 0.1114 0.1108
5 0.3271 0.0605 0.1039 0.1033
6 0.4352 0.0866 0.1433 0.1426
7 0.4035 0.0798 0.1324 0.1317
8 0.3753 0.0732 0.1223 0.1217
9 0.3492 0.0660 0.1121 0.1115
10 0.3250 0.0584 0.1018 0.1012
11 0.4111 0.0625 0.1192 0.1184
12 0.3872 0.0636 0.1162 0.1155
13 0.3638 0.0617 0.1108 0.1102
14 0.3443 0.0611 0.1072 0.1066
15 0.3280 0.0614 0.1048 0.1042
16 0.4123 0.0638 0.1204 0.1197
17 0.3871 0.0635 0.1161 0.1154
18 0.3631 0.0610 0.1101 0.1095
19 0.3442 0.0610 0.1071 0.1065
20 0.3272 0.0607 0.1040 0.1034
21 0.3432 0.0767 0.1200 0.1194
22 0.3095 0.0429 0.0863 0.0857
23 0.3213 0.0548 0.0981 0.0976
24 0.3237 0.0572 0.1005 0.1000
25 0.3205 0.0539 0.0973 0.0967
Fuente: Ecuacin 11, muestra de clculo; tabla XII.
34
Tabla XIV. Incerteza de la molaridad
Solucin d[H2O] d[CH3COOC2H5] d[C2H5OH] d[CH3COOH]
1 0.4271 0.0786 0.1352 0.1345
2 0.3966 0.0730 0.1256 0.1249
3 0.3702 0.0681 0.1172 0.1166
4 0.3470 0.0638 0.1099 0.1093
5 0.3266 0.0601 0.1034 0.1029
6 0.4271 0.0786 0.1352 0.1345
7 0.3966 0.0730 0.1256 0.1249
8 0.3702 0.0681 0.1172 0.1166
9 0.3470 0.0638 0.1099 0.1093
10 0.3266 0.0601 0.1034 0.1029
11 0.4271 0.0786 0.1352 0.1345
12 0.3966 0.0730 0.1256 0.1249
13 0.3702 0.0681 0.1172 0.1166
14 0.3470 0.0638 0.1099 0.1093
15 0.3266 0.0601 0.1034 0.1029
16 0.4271 0.0786 0.1352 0.1345
17 0.3966 0.0730 0.1256 0.1249
18 0.3702 0.0681 0.1172 0.1166
19 0.3470 0.0638 0.1099 0.1093
20 0.3266 0.0601 0.1034 0.1029
21 0.3266 0.0601 0.1034 0.1029
22 0.3266 0.0601 0.1034 0.1029
23 0.3266 0.0601 0.1034 0.1029
24 0.3266 0.0601 0.1034 0.1029
25 0.3266 0.0601 0.1034 0.1029
Fuente: Ecuacin 10, muestra de clculo; Tabla XIII.
35
Tabla XV. Incerteza de la constante de equilibrio
Solucin dKeq
1 -0.0934
2 -0.1463
3 -0.0330
4 -0.0088
5 0.0011
6 -0.1360
7 -0.0543
8 -0.0252
9 -0.0103
10 0.0004
11 0.1126
12 -0.5915
13 0.0395
14 0.0131
15 0.0013
16 0.0208
17 -0.4818
18 0.0310
19 0.0092
20 0.0011
21 -0.1184
22 68.7599
23 0.0112
24 -0.0067
25 -0.1324
Fuente: Ecuacin 12, muestra de clculo; Tabla XIV.
III. Conclusiones
a. Los errores provocados por los instrumentos fueron menores al 10% lo
que demuestra que la incertidumbre de los instrumentos no influyen en
los resultados.
b. El coeficiente de variacin muestra que los resultados no fueron precisos.
c. Los errores de precisin sobrepasaron valores del 50% por lo que los
datos no son confiables.
36
IV. Fuentes de error
a. La solucin de hidrxido de sodio no se estandariz previo a la titulacin.
b. Mala apreciacin del punto de equivalencia a la hora de titular.
También podría gustarte
- Dispositivos Periféricos de Entrada y SalidaDocumento5 páginasDispositivos Periféricos de Entrada y Salidawin104725Aún no hay calificaciones
- Países y Capitales Las AntillasDocumento12 páginasPaíses y Capitales Las Antillaswin104725Aún no hay calificaciones
- Turismo Automatico - JavierDocumento5 páginasTurismo Automatico - Javierwin104725Aún no hay calificaciones
- 25 Personajes Importantes de GuatemalaDocumento26 páginas25 Personajes Importantes de Guatemalawin104725Aún no hay calificaciones
- Animales en Peligro de Extinción en GuatemalaDocumento4 páginasAnimales en Peligro de Extinción en Guatemalawin104725Aún no hay calificaciones
- 28 Tipos de Comunicación y Sus CaracterísticasDocumento5 páginas28 Tipos de Comunicación y Sus Característicaswin104725Aún no hay calificaciones
- Ciencias Auxiliares de La Historia Concepto e ImagenesDocumento2 páginasCiencias Auxiliares de La Historia Concepto e Imageneswin104725100% (2)
- Deportes DefiniciónDocumento6 páginasDeportes Definiciónwin104725Aún no hay calificaciones
- Escultores GuatemaltecosDocumento2 páginasEscultores Guatemaltecoswin104725100% (1)
- Anécdotas de Jorge UbicoDocumento2 páginasAnécdotas de Jorge Ubicowin10472550% (2)
- Reclamo de BeliceDocumento26 páginasReclamo de Belicewin104725Aún no hay calificaciones
- Los Pieles Rojas, Olmecas Tarascos Guaranies Patagones AraucanosDocumento7 páginasLos Pieles Rojas, Olmecas Tarascos Guaranies Patagones Araucanoswin104725Aún no hay calificaciones
- IMG - Cuentas de ContabilidadDocumento6 páginasIMG - Cuentas de Contabilidadwin104725Aún no hay calificaciones
- Ricardo Bressani y Miguel Angel AsturiasDocumento2 páginasRicardo Bressani y Miguel Angel Asturiaswin104725Aún no hay calificaciones
- Reino Fungí, Monera y ProtistaDocumento2 páginasReino Fungí, Monera y Protistawin104725Aún no hay calificaciones
- Monografias de Los 22 Departamentos de GuatemalaDocumento19 páginasMonografias de Los 22 Departamentos de Guatemalawin10472550% (4)
- Enfermedades Transmision SexualDocumento4 páginasEnfermedades Transmision Sexualwin104725Aún no hay calificaciones
- Cakchiquel DictionaryDocumento487 páginasCakchiquel DictionaryJosé Antonio Ortiz71% (7)
- Comidas Típicas Por Departamentos GuatemalaDocumento7 páginasComidas Típicas Por Departamentos Guatemalawin104725Aún no hay calificaciones
- Enfermedades Del Sistema DigestivoDocumento2 páginasEnfermedades Del Sistema Digestivowin104725100% (2)
- Tipos de Arreglos de CamasDocumento9 páginasTipos de Arreglos de Camaswin104725Aún no hay calificaciones
- Constitución Política de Guatemala Arituclos SaludDocumento8 páginasConstitución Política de Guatemala Arituclos Saludwin104725Aún no hay calificaciones
- Manual de Operacion de Motores Diesel New HollandDocumento72 páginasManual de Operacion de Motores Diesel New Hollandwin10472580% (5)
- Principales Causas de La DrogadicciónDocumento3 páginasPrincipales Causas de La Drogadicciónwin104725Aún no hay calificaciones
- Reporte 1 - Flujo de Fluidos A Través de Lechos PorososDocumento27 páginasReporte 1 - Flujo de Fluidos A Través de Lechos Porososwin104725Aún no hay calificaciones
- El Universo y Sus MaravillasDocumento2 páginasEl Universo y Sus Maravillaswin1047250% (1)
- Electrificación Ferroviaria Explicada 3er Riel + Catenaria PDFDocumento25 páginasElectrificación Ferroviaria Explicada 3er Riel + Catenaria PDFpabpplAún no hay calificaciones
- Problemas Capitulo 3 Leven Spiel CompletoDocumento54 páginasProblemas Capitulo 3 Leven Spiel Completonestor cosmeAún no hay calificaciones
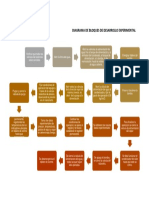
- Diagrama de Bloques de Desarrollo ExperimentalDocumento1 páginaDiagrama de Bloques de Desarrollo ExperimentalJesÜs ChIluAún no hay calificaciones
- FN-X Black DragónDocumento17 páginasFN-X Black DragónLemar GabrieleAún no hay calificaciones
- Practica 2 Q.O. IIDocumento5 páginasPractica 2 Q.O. IICarolina MezaAún no hay calificaciones
- Urea PRO IIDocumento13 páginasUrea PRO IIjulio925Aún no hay calificaciones
- Problemas Resueltos de Ley de Gauss y Potencial ElectricoDocumento9 páginasProblemas Resueltos de Ley de Gauss y Potencial ElectricoOscar Javier Pasten BravoAún no hay calificaciones
- Esp AP Physb Problemas de Ondas Sonora 2012-05-18Documento11 páginasEsp AP Physb Problemas de Ondas Sonora 2012-05-18Adriano Dvj RiveraAún no hay calificaciones
- CatenariaDocumento4 páginasCatenariaMauricio PozoAún no hay calificaciones
- Revista ElectroinstaladorDocumento32 páginasRevista ElectroinstaladorSEBASTIAN ARIELAún no hay calificaciones
- Examenfinal Estadistica y ProbDocumento4 páginasExamenfinal Estadistica y ProbEdson VasquezAún no hay calificaciones
- Resumen de PolimerosDocumento3 páginasResumen de PolimerosMaría Lucía IbañezAún no hay calificaciones
- Que Es Notación CientíficaDocumento21 páginasQue Es Notación CientíficaValentin CalderonAún no hay calificaciones
- Aplica GeoDocumento44 páginasAplica GeoJair De la VegaAún no hay calificaciones
- 5taunidad QuimicaDocumento7 páginas5taunidad QuimicaBeatriz MamaniAún no hay calificaciones
- Limite Superior y Inferior-2 PDFDocumento3 páginasLimite Superior y Inferior-2 PDFKevin PinedaAún no hay calificaciones
- Practica N° 6 TeodolitoDocumento8 páginasPractica N° 6 TeodolitoCleider Santos FloresAún no hay calificaciones
- Capitulo 1. Señales y SistemasDocumento36 páginasCapitulo 1. Señales y SistemasJuan DuarteAún no hay calificaciones
- Ficha Técnica Manguera de Succión PVCDocumento1 páginaFicha Técnica Manguera de Succión PVCAndres Bolivar67% (3)
- Desbalance de Tensiones en Sistemas TrifásicosDocumento4 páginasDesbalance de Tensiones en Sistemas TrifásicosJesús Yarleque RamosAún no hay calificaciones
- Columnas Excentricamente CargadasDocumento3 páginasColumnas Excentricamente CargadasMaikel Manuel RodríguezAún no hay calificaciones
- Aire Acondicionado OptraDocumento124 páginasAire Acondicionado OptrawilderAún no hay calificaciones
- Calculo Uniones Atornilladas, SoldadasDocumento88 páginasCalculo Uniones Atornilladas, Soldadasxevi00100% (7)
- 1 Cinematica de ParticulasDocumento47 páginas1 Cinematica de ParticulasphrasalverbsAún no hay calificaciones
- Lab 4Documento8 páginasLab 4sebastianAún no hay calificaciones
- Resolucion Del 2do Parcial CarreterasDocumento7 páginasResolucion Del 2do Parcial CarreterasMiguel Angel RieraAún no hay calificaciones
- 02-Cm 211-Silabo Dosificado Por ClasesDocumento4 páginas02-Cm 211-Silabo Dosificado Por ClasesLuis fiat luxAún no hay calificaciones
- Laboratorio 1 VectoresDocumento9 páginasLaboratorio 1 Vectorespanxoskatesk8Aún no hay calificaciones
- Ejercicios de ConicidadDocumento4 páginasEjercicios de ConicidadMecanizado SenaAún no hay calificaciones