Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Proceso de Deshidratación Del Gas Natural
Cargado por
Jesus Alberto Reyes MoyaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Proceso de Deshidratación Del Gas Natural
Cargado por
Jesus Alberto Reyes MoyaCopyright:
Formatos disponibles
1
Proceso de Deshidratacin del Gas Natural. La deshidratacin del gas natural se define como la extraccin del agua que esta asociada, con el gas natural en forma de vapor y en forma libre. La mayora de los gases naturales, contienen cantidades de agua a la presin y temperatura los cuales son extrados del yacimiento. En general, se puede sealar, que el contenido de agua o vapor de agua en el gas, as como el contenido de hidrocarburos condensables ante un aumento de presin o disminucin de temperatura, resultan inconvenientes para la conduccin del gas por tuberas ya que provocara obstrucciones de importancia Es por ello que el gas natural debe ser sometido a un proceso de deshidratacin y de extraccin de gasolina, las razones del porque se debe aplicar el proceso de deshidratacin son: Justificacin del Proceso de Deshidratacin: El proceso de deshidratacin del gas natural, esta justificado, debido fundamentalmente a: a.- Evitar la formacin de hidratos, en vista que estos componentes pueden detener y/o entorpecer el flujo de gas por tuberas La verdad es que hay que evitar la formacin de hidratos La formacin de hidratos ocurre siempre, que el gas natural contenga agua, y esta a su vez se condense dentro de la tubera y otros recipientes, que sirvan de transporte del gas Los hidratos son compuestos cristalinos blanquecinos, parecidos a la nieve, y que se forman por la reaccin entre los hidrocarburos livianos o gases cidos y el agua lquida. La composicin de los hidratos, por lo general es 10% de hidrocarburos y 90% de agua. La gravedad especfica de los hidratos anda por el orden de 0,98 y flotan en el agua pero se hunden en los hidrocarburos lquidos. La formacin de hidratos en el gas natural, ocurre siempre que haya agua libre y se enfre el gas por debajo de la temperatura de formacin de hidratos .Lo lgico sera establecer las normas para evitar la formacin de hidratos, en vista que si estos se llegan a formar los problemas operaciones se incrementan, ya que los hidratos taponan la tubera de transporte. Uno de los correctivos que se puede aplicar para evitar la formacin de hidratos es el metanol o monoetilenglicol, con los cuales se baja el punto de roco y se impide la formacin de hidratos. La formacin de hidratos se fundamenta en lo siguiente: a.- Condiciones Primarias 1.- El gas debe encontrarse a una temperatura igual o inferior al punto de roco del agua en el gas o en presencia de agua libre. 2.- Presencia de hidrocarburos livianos y/o gases cidos 3.- El proceso se encuentra a bajas temperaturas a las presiones de operacin, y 4.- Altas presiones a la temperatura de operacin. b.- Condiciones Secundarias:
1
1.- Altas velocidades de los fluidos 2.- Presiones pulsantes o inestables 3.- Fluidos sometidos a cualquier tipo de agitacin, y 4.- Introduccin del gas en un pequeo cristal de hidratos La Formacin de Hidratos en el Gas Natural, ocurre fundamentalmente, porque la humedad del gas al condensarse da origen, mediante su combinacin con los hidrocarburos a baja temperatura. Es as, entonces, que como consecuencia de la fuerte reduccin de presin, que puede ocurrir en las vlvulas reguladoras de presin de la Planta, se origina una importante disminucin de temperatura como consecuencia de la brusca expansin del gas, provocando la formacin de hidratos, los que se cristalizan formando hielo o una especie de nieve en la instalacin. Por dicho motivo, es necesario que en instalaciones en que se produzcan fuertes cadas de presin, adoptar medidas tendientes a evitar este problema, dado que dichos hidratos afectan el normal funcionamiento de la instalacin .Para ello se admite la utilizacin de dos mtodos Que son : Inyeccin de hidratantes y Calentamiento del Gas. Para evitar la formacin de hidratos se requiere una presin elevada y una temperatura baja. A cada valor de presin corresponde un valor de temperatura por debajo de la cual pueden formarse hidratos si existe humedad. A mayor presin es tambin mayor aquella temperatura. Por ello este inconveniente es ms comn a mayores presiones. Para evitarlo debe procederse a deshidratar el gas, es decir, bajar su punto de roco hasta temperaturas inferiores a 32F. Ello se efecta mediante procesos que emplean como absorbedores agentes slidos o lquidos Tambin se logra impedir la formacin de hidratos mediante la inyeccin en el gas de sustancias inhibidoras, tales como el metanol. En lo que respecta a los hidrocarburos condensables, ellos se extraen en forma de gasolina y gas licuado, en plantas especiales que pueden utilizar diversos procesos, tales como compresin y enfriamiento, absorcin con kerosn, etc. La formacin de hidratos en el gas natural ocurrir si existe agua libre y se enfra por debajo de la temperatura de formacin de hidratos. En la formacin de hidrato de hace presente una reaccin qumica, entre el agua, que se condensado, por aumentos en presin o disminuciones de la temperatura, con los hidrocarburos voltiles. Una vez formados los hidratos, no hay posibilidad de eliminarlos, y la nica forma de es sacarlos de la tubera. La temperatura y presin a las cuales puede ocurrir la formacin de hidratos puede predecirse en forma grfica, como tambin se puede determinar a travs de ecuaciones matemticas, que pueden indicar en forma aproximada la temperatura de formacin de hidratos, una de esas frmulas matemticas es:
TFH = 1,57206 P ( 0,8606 0, 0474 ln P ) (25) En donde: P es la presin del sistema En las situaciones donde los clculos predicen la formacin de hidratos, se puede evitar dicha formacin removiendo el agua del gas antes del enfriamiento de los hidrocarburos por debajo de la temperatura a la cual podran aparecer los problemas mediante el uso de inhibidores que se mezclan con el agua que se ha condensado. Para el problema planteado de deshidratacin, y como la presin tiene un valor de 2000 lpca, lo que significa que la temperatura de formacin de hidratos es:70,5 F
b.-Satisfacer los requerimientos, para transportar gas a los centros de consumo y distribucin Al gas que se transporta se le extrae el agua que contiene, hasta los niveles necesarios para que cumplan con la norma establecida, y que respondan al destino que, ha sido establecido para el gas. Por ejemplo, para poder transportar el gas, por un sistema de redes y tuberas de gas, debe tener un mximo de 5- 7 libras de agua por cada milln de pies cbicos normales de gas (5- 7 lb H20/ MM PCN. Aunque, el mximo contenido de agua del gas depende del tipo de clima, ya que en climas fros la cantidad aceptada es 1-2 lb de H20/ MM PCN. La cantidad 5-7 lb de H20 /MM PCN, es vlida para climas tropicales, con ello se garantiza que el punto de roco ocurra a 32F. Lo que significa que el fluido trabajara a temperatura por encima de 32 F sin que se produzca condensacin del agua. El punto de roco del agua es la temperatura a la cual se condensa el agua, a una presin previamente establecida c.- Evitar la congelacin del agua en los procesos criognicos. Cuando el gas ser utilizado en los procesos criognicos. La norma vlida para transportar gas por una tubera que es 7 lb H20/ MM PCN no es aplicable. En vista que los procesos criognicos deben de trabajar a una temperatura menor a la crtica, luego el agua en esas condiciones se congelara, y ser un impedimento, para la eficiencia del proceso. Luego en estos casos la cantidad de agua permisible en el gas debe de ser mucho menos. d.- Evitar la congelacin de agua durante el transporte del gas Cuando el gas natural contiene agua, que se condensa dentro de las tuberas se forman hidratos, que son causantes de taponamiento de los gasoductos e impiden que el gas pueda circular, por la tubera. Lo normal es que el ingeniero analice las condiciones de formacin de hidratos y aplique los correctivos a tiempo, para evitar la formacin de hidratos. Adems, si el gas transportado entra a una caldera y contiene baches de agua, de seguro habr una explosin, ya que el agua a evaporarse aumenta 1700 veces su volumen. La magnitud de la explosin depender de la cantidad de agua que llegue a la caldera y de la temperatura a la que se encuentren. Determinacin de la Cantidad de Agua en el gas Natural La cantidad de agua que los hidrocarburos gaseosos puedan transportar se puede determinar con Equipo denominados Medidores del Punto de Roco. Aunque este parmetro no
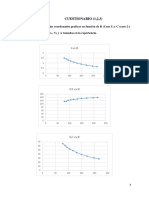
hace la diferencia entre hidrocarburos lquidos y agua propiamente tal. La presin y/o temperatura del gas natural incide en la cantidad de agua que pueda retener. Si, por ejemplo la presin es constante, a medida que se enfra un volumen dado del gas, su capacidad de retencin de agua disminuye, ya que no hay posibilidad de mantener el agua en forma de vapor. Para determinar la cantidad de agua que pueda estar en forma de vapor junto al gas se utiliza la figura 13 (Denominada Grfica de Mc Ketta- Webe), permite determinar la cantidad de agua que pueda retener el gas natural saturado a diversas condiciones de presin y temperatura Figura 13 Contenido de agua en los hidrocarburos, segn Mc Ketta- Webe
Para utilizar la figura 13 se necesita conocer las condiciones de presin y temperatura de operacin y, se busca la interseccin de ambas lneas, y despus se busca la cantidad de agua, que contiene el gas natural. El contenido de agua se expresa en libras de aguas por milln de pies cbicos normales de gas La
cantidad de agua que se cuantifica de esta forma corresponde al gas el gas dulce Por ejemplo, si se quiere determinar la cantidad de agua que tiene el gas dulce a una temperatura de 100F y presin de 1000 lpca. Simplemente se busca la lnea de la temperatura de 100F y se hace busca la interseccin con la lnea que representa el valor de la presin de 1000 lpca, y se encuentra que el gas contiene 80 libras de agua por cada milln de pies cbicos normales de gas. Lo que indica que el contenido de agua en este caso es 80 lb de agua/MMPCN, luego el gas tiene condiciones de gas hidratado, y por lo tanto para convertirlo en gas anhidro y que este dentro de la norma el gas debe de ser deshidratado, de tal forma que pueda ser comerciado, ya que el contenido de agua en el gas natural afecta sobre todo el contenido calorfico del gas, adems de otros procesos, donde el agua afecto las condiciones operacionales. Como el contenido de agua encontrado en estas condiciones corresponde al gas dulce. Si el gas natural que se esta analizando contiene gases cidos, es necesario determinar el contenido de agua que pueden contener estos componentes, y con ello determinar el contenido total de agua en el gas. El contenido de agua que contiene, el C02 se presenta en la figura 14, mientras que la figura 15 representa el Contenido de agua en el H2S. Figura 14 Contenido de agua en C02 saturado en Mezclas de Gas Natural
En ambas figuras se determina el contenido de agua, en los gases cidos, sin tener en cuenta la composicin molar de los gases cidos. Luego para determinar la cantidad total de agua en la mezcla de gas natural, se suman la cantidad de agua obtenida en la grfica del gas dulce (figura 13) y la cantidad de agua que se
obtiene en las figuras 14 del C02 y 15 del H2S., para la obtencin del contenido total de agua en el gas se utiliza la siguiente ecuacin: W(GA)= Y(HCS)(Wc(HCS)+Y(C02)(Wc(C02)+Y(H2S)(Wc(H2S) Figura 15 Contenido de Agua en el Sulfuro de Hidrgeno (26)
En donde: Wc(GA)= contenido de vapor de agua en la mezcla cida; Y(HCS)= Fraccin molar de los hidrocarburos en el gas dulce; (Wc(HCS)= Contenido de agua en el gas dulce; Y(C02)= Fraccin molar del ( C 0 2 ) en el gas Wc(C02) = Contenido de agua en ( C 0 2 ) Dixido de Carbono puro; Y(H2S)= Fraccin molar del sulfuro de hidrgeno en el gas natural y Wc(H 2S)= Contenido de agua en el Sulfuro de Hidrgeno puro. Esta frmula permite determinar la cantidad de agua que se encuentra en un gas natural, incluido la cantidad de impurezas, que puede tener tambin alguna en su composicin. La utilidad de la ecuacin (26) es de gran importancia para determinar el contenido total de agua en el gas, y con ello poder planificar todos los procesos a los que tiene que ser sometido el gas natural, antes de poder ser utilizado. Ejemplo Cul es el contenido de agua de una mezcla de gas que esta sometido a una presin de 2000 lpca y una temperatura de 120F, y que adems contiene 3,50 % de H2S y 8,25% de C02? Solucin La figura 13 Indica que el contenido de agua en el gas dulce es de 86 libras de agua por milln de pies cbicos normales de gas, mientras que la grfica 14 seala que el contenido de agua en el Dixido de Carbono es 90 libras de agua por milln de pies cbicos normales de gas, y por ltimo la grfica 15 indica que el
6
contenido de agua en el Sulfuro de Hidrgeno es 185 libras de agua por milln de pies cbicos normales de gas, luego aplicando la frmula (26), queda: W(GA)=0,8825x86+0,0825x90+0,035x185=89,80 lb de agua /MM PCN. El contenido de agua en el gas dulce se puede determinar, tambin por la correlacin de R Bukacek ,a partir de la presin del gas ,para ello se utiliza la siguiente ecuacin: W= A/ P(lpca) + B (lb/MM PCN) (27)
Las constantes A y B estn tabuladas en funcin de la temperatura, luego en el Cuadro 3. Para determinar el contenido de agua del problema anterior queda: W(H20)=80400/2000+23,7 =63,9 lb H20/ MM PCN Parmetros que participan en la Deshidratacin del Gas Natural Existen varios mtodos para deshidratar el gas natural .La seleccin de un proceso, depender fundamentalmente del grado de deshidratacin necesario y d la evaluacin econmica del proceso seleccionado. Los procesos ms conocidos son: a.- Enfriamiento Directo El contenido de agua saturada en un gas decrece con el aumento de la presin o con una disminucin de la temperatura. Por, lo tanto, gases calientes saturados con vapor de agua pueden ser parcialmente deshidratados por enfriamiento directo. Los gases sujetos a la compresin son normalmente enfriados antes de ir a la lnea de distribucin. Este proceso de enfriamiento puede remover agua del gas y es de naturaleza cclica, ya que el fluido recibe calor del sistema a enfriar El proceso de enfriamiento directo se lleva a cabo mediante el uso de refrigeracin mecnica con adicin de Inhibidores de Hidratos.Desde luego en este proceso de enfriamiento se puede remover agua del gas. En este caso el proceso ser de naturaleza cclica. Esto, es porque el fluido refrigerante recibir calor del sistema a enfriar. medio ambiente o se transmite a otro sistema, que acta como receptor de esa energa calorfica. Cuando la energa calorfica se disipa, el fluido refrigerante inicia de nuevo el ciclo. Los fluidos refrigerantes de mayor uso, en la industria del gas natural son el Propano y Metano. En este proceso hay que tener mucho cuidado con la cantidad de lquido que se acumula en los equipos. de enfriamiento del gas natural, se utiliza el Efecto de JouleThomson con adicin o sin adicin de inhibidores de hidratos El efecto de JouleThompson es el cambio en la temperatura del gas que se origina cuando el gas es expandido en condiciones isentlpicas En coeficiente de Joule y Thompson ( ) se define a travs de la siguiente ecuacin:
= ( T / P ) H
(28)
b.- Expansin del Gas a una Baja Presin. En este proceso para obtener el El descenso de la presin de una corriente de gas produce enfriamiento, excepto cuando se trata del Helio (He) y del Hidrgeno (H) :Luego se puede concluir que Cuadro 3 Constantes de R. BukaceK T(F) 60 66 72 78 84 90 96 102 108 114 120 126 132 138 144 150 156 162 168 174 180 186 192 198 204 210 216 222 228 234 242 248 254 260 320 380 440 A 12200 15000 18500 22500 27400 33200 39900 47900 57100 67900 80400 94700 111000 130000 152000 177000 205000 236000 272000 312000 357000 407000 463000 525000 594000 671000 755400 848000 950000 1060000 1230000 1370000 1520000 1680000 4260000 9300000 1810000 B 5,77 6,74 7,85 9,11 10,50 12,20 14,00 16,0 18,30 20,9 23,70 26,9 30,30 34,20 38,50 43,20 48,40 54,10 60,30 67,10 74,80 82,70 91,40 101,00 111,00 122,00 134,00 148,00 162,00 177,00 198,00 216,00 235,00 255,00 543,00 1090,0 T(F) 62 68 74 80 86 92 98 104 110 116 122 128 134 140 146 152 158 164 170 176 182 188 194 200 206 212 218 224 230 236 244 250 256 280 340 400 A 13100 16100 19700 24100 29200 35300 42400 50800 60500 71800 84900 100000 117000 137000 160000 186000 215000 248000 285000 326000 372000 425000 483000 547000 619000 690000 785000 881000 987000 1140000 1270000 1420000 1570000 2340000 5610000 1170000 0 2220000 B 6,08 7,10 8,25 9,57 11,10 12,70 14,80 16,70 19,10 21,8 24,70 28,0 31,6 35,60 40,00 44,90 50,20 56,10 62,50 69,50 77,20 85,80 94,80 104,00 115,00 126,00 139,00 152,00 166,00 187,00 204,00 222,00 242,00 333,00 692,00 1360,0 2550,0 T(F) 64 70 76 82 88 94 100 106 112 118 124 130 136 142 148 154 160 166 172 178 184 190 196 202 208 214 220 226 232 240 246 252 258 300 360 420 A 14000 17200 21100 25700 31100 37500 45100 53900 64100 76000 89700 106000 124000 144000 168000 195000 225000 259000 298000 341000 390000 443000 504000 570000 644000 725000 818000 915000 1020000 1190000 1320000 1470000 1630000 3180000 7270000 1470000 0 B 6,41 7,17 8,67 10,00 11,60 13,30 15,30 17,50 20,0 22,70 25,6 29,10 32,90 37,0 41,60 46,60 52,10 58,20 64,80 72,00 79,90 88,40 97,70 118,00 119,00 130,00 143,00 157,00 171,00 192,00 210,0 229,00 248,00 430,00 869,00 1700,0
2130,0 460
el Efecto de Joule- Thompson, es el cambio de temperatura que se produce en un gas que se expande a partir de una presin constante ms baja, sin transmisin de calor. Los procesos de transmisin de calor ocurren por medio de al Conduccin, Conversin y Radiacin La Expansin del gas a una baja presin, como forma de enfriamiento se puede realizar a travs de dos diferentes procesos: 1.- Expansin Isentlpica Este proceso se utiliza cuando se necesita aumentar la recuperacin de lquidos de un gas hmedo proveniente del pozo, por lo general con alta presin. En el proceso en flujo de gas hmedo es pasado a travs de una vlvula expansora, donde la temperatura del gas disminuye, con ello se logra que una fraccin de los componentes intermisos y pesados presentes en la mezcla de gas natural se condensen. Luego los lquidos condensados son retirados del flujo de gas usando, para ello un separador de baja presin. El gas fro y seco se utiliza para preenfriar la corriente de gas hmedo que alimenta el sistema. 2.- Expansin Isentrpica. Este proceso se produce cuando la corriente de gas hmedo pasa a travs de un turboexpansor. En este caso disminuye, ocurre una disminucin de la temperatura del gas y se obtiene una cierta cantidad de trabajo, el cual se utiliza para mover los equipos de bombeo. Tambin esta disminucin de la temperatura, que la mayora de los casos es un valor apreciable, se utiliza para recuperar lquidos del gas natural. Este es el principal principio de los procesos criognicos. Es necesario hacer resaltar que la expansin isentrpica es un proceso de mucho ms efectividad, pero los costos de instalacin de equipos, son mucho mayores. Transferencia de Calor: Este parmetro existe, siempre que hay una diferencia de temperatura en el universo, la energa se transfiere de la regin de mayor temperatura a la de menor temperatura. De acuerdo con los conceptos de la termodinmica, esta energa transmitida se denomina calor. Las leyes de la termodinmica tratan de la transferencia de energa, pero siempre se refieren a sistemas que estn en equilibrio, y solo pueden utilizarse para predecir la cantidad de energa requerida para cambiar un sistema de un estado de equilibrio a otro, por lo que no sirven para predecir la rapidez con que puedan producirse estos cambios. La ciencia llamada transmisin o transferencia de calor complementa los principios primero y segundo de la termodinmica clsica, proporcionando los mtodos de anlisis que pueden utilizarse para predecir la velocidad de la transmisin del calor, adems de los parmetros variables durante el proceso en funcin del tiempo Para un anlisis completo de la transferencia del calor es necesario considerar mecanismos fundamentales de transmisin: conduccin, conveccin y radiacin, adems del mecanismo de acumulacin. El anlisis de los sistemas y modelos de intercambio de calor requieren familiaridad con cada uno de estos mecanismos y sus fundamentos, as como de sus interacciones El calor puede transmitirse de tres maneras.
9
10
a.-Conduccin de Calor Puesto que el calor es la energa de la actividad molecular, una forma simple de transferencia, ser la comunicacin directa de la energa molecular a travs de una sustancia por medio de colisiones entre sus molculas, esta forma de transferir el calor se denomina conduccin Los metales son buenos conductores de electricidad, por tener electrones libres, y como estos electrones libres contribuyen poderosamente a la conduccin del calor, lo que hace que los metales sean excelentes conductores de electricidad b.- Conveccin de Calor. Esta es una forma de transmisin del calor de un lugar a otro por movimiento de la materia caliente La transferencia de calor por conveccin de un cuerpo comprende el movimiento de un fluido en relacin con el cuerpo. Si el movimiento es provocado por las diferencias de densidad debidas a la diferencia de temperatura en las diferentes localidades del fluido, se conoce como conveccin natural. Si el movimiento del fluido es provocado por un agente externo como un ventilador, se denomina conveccin forzada. La transferencia de calor por corrientes de conveccin en un lquido o en un gas, est asociada con cambios de presin, debidos comnmente a cambios locales de densidad. Un aumento de temperatura en un fluido va acompaado por un descenso de su densidad, lo que se puede utilizar para determinar el coeficiente de conveccin de calor. c.- La Combinacin de Radiacin y Absorcin Este es otro tipo de transferencia de calor. En la radiacin, la energa trmica se transforma en energa radiante, similar en su naturaleza a la luz. En realidad, una parte de esta radiacin es luminosa. En esta forma, la energa radiante puede atravesar distancias enormes antes de ser absorbida por un cuerpo y transformada de nuevo en calo. La radiacin es la transferencia de calor por radiacin no requiere ningn medio material intermedio en el proceso. La energa se traslada desde la superficie del sol hasta la tierra, donde es absorbida y convertida en energa calorfica. La radiacin es un proceso por el cual fluye calor desde un cuerpo de alta temperatura a un cuerpo de baja temperatura Reacciones Qumicas en el Proceso de Deshidratacin de Gas. El fundamento de este proceso es entre las reacciones qumicas, que ocurren entre el agua y ciertas sustancias qumicas. Lo que involucra, por lo general un proceso de alta efectividad, cuando se aplica a la deshidratacin del gas natural. Pero, el proceso de regeneracin de la sustancias puede convertirse en un proceso muy complejo. Y, desde luego le quita la posibilidad de utilizarlo a nivel industrial. Y convierte al proceso a condiciones de laboratorio, y se utiliza fundamentalmente para determinar el contenido de agua en el gas natural. d.- -Deshidratacin por Absorcin. Este es uno de los procesos de mayor utilidad, en la industria del gas natural. El proceso consiste en remover el vapor de agua de la corriente de gas natural, por medio de un contacto lquido. El lquido que sirve como superficie absorbente debe cumplir con una serie de condiciones, como por ejemplo:
10
11
1.- Alta afinidad pon el agua, y ser de bajo costo, 2.-Poseer estabilidad hacia los componentes del gas y bajo perfil corrosivo, 3.-Estabilidad para regeneracin 4.- Viscosidad baja, 5.- Baja presin de vapor a la temperatura de contacto, 6.- Baja solubilidad con las fracciones lquidas del gas natural 7.- Baja tendencia a la formacin de emulsiones y produccin de espumas. Los glicoles y el metano son los lquidos de mayor uso en la deshidratacin del gas natural El metanol, como agente deshidratantes es de alto costo, por lo que su uso tiene unas ciertas limitaciones, y se selecciona por lo general en los casos siguientes: Instalaciones temporales y es deseable aplazar las decisiones relativas en los equipos permanentes del manejo de gas. Las condiciones operacionales a las cuales puede ocurrir la formacin de hidratos son de alta inestabilidad. La temperatura de operacin es tan baja que las viscosidades de otras sustancias puedan ser muy altas, todo esto es muy necesario tener en cuenta para hacer una evaluacin de la efectividad del proceso de deshidratacin de una mezcla de gas natural. Deshidratacin del Gas Natural con Glicoles Estos componentes se encuentran en una gran cantidad, pero los que ms se utilizan en el proceso de deshidratacin del gas natural son: 1.- Etilnglicol (EG) cuya Frmula qumica es H0C2H40H, luego su peso molecular es 62,10 (lb/lbmol), tiene su punto de congelamiento en 8 F 2.-Dietilnglicol (DEG): Frmula qumica es 0H (C2H40)2H, su peso molecular es de 106,1 (lb/lbmol), mientras que el punto de congelacin es 17 F 3.- Trietilnglicol (TEG) :Frmula qumica es 0H(C 2H40)3H. El peso molecular alcanza un valor de 150,2 (lb/lbmol), y su punto de congelacin es 19 F 4.- Tetraetilnglico (TTEG) Frmula Qumica es 0H(C2H40)4H, su peso molecular es 194, 2 (lb/lbmol), y su punto de congelacin es 22 F. Los glicoles son usados corrientemente en torres de absorcin, ya que permiten obtener temperaturas inferiores al punto de roco, con lo las prdidas de vapor son menores que las obtenidas con otros compuestos. Pero el TEG no debe utilizarse a temperaturas inferiores a 50 F, ya que se incrementa mucho la viscosidad. El EG y DEG se utilizan con frecuencia inyectados en la corriente de gas, tanto en los
11
12
procesos de refrigeracin y expansin. Ninguno de los dos debe usarse a una temperatura menos a 20 F, todo provoca que el uso de los glicoles en el proceso de deshidratacin de gas natural, sea de mucha importancia, ya que es un proceso, que puede ser de alta eficiencia, siempre y cuando el proceso de maneje, dentro de los parmetros operacionales establecidos, ya que caso contrario no se puede producir un proceso eficiente. Los factores que influyen en la seleccin del glicol son: a.- Bajo costo: El costo de glicol no es muy alto, luego este factor provoca que sea de gran utilidad en el proceso de deshidratacin en cualquier industria. b.- Viscosidad, un valor de viscosidad por debajo de 100 - 150 CPS. Hace que los fluidos fluyan con dificultad. Luego se requiere conocer la concentracin del glicol y la temperatura del trabajo del equipo deshidratador. c.- Reduccin del Punto de Roco (RDR). En el momento en que el glicol absorbe agua, disminuye la temperatura de roco del gas natural. Este proceso el Descenso del Punto de Roco (DPR).La reduccin del (DPR) es influenciada por. La tasa de flujo del glicol; temperatura de contacto glicol /gas en el tope del absorbedor, eficiencia de contacto del glicol pobre. Cuando el proceso de deshidratacin del gas natural se realiza con (TEG) a 100 F y una concentracin de 95 %P/P, se puede reducir el punto de roco hasta 46 F. Mientras que el (DEG) a la misma concentracin, reduce el punto de roco en 54F. Pero, esta situacin cambia al aumenta la concentracin, si la concentracin del glicol en el agua es por ejemplo 99% P/P. En la (RDR), el agua pase antes a la fase lquida y el glicol simplemente la atrapa. EL (DPR) es en 90 F, mientras que si se utiliza (DEG) es 84F. Luego estas observaciones es conveniente tenerlas en cuenta, cuando se quiera seleccionar el tipo de glicol ms apropiado y eficiente para una operacin. Si el gas que se va a deshidratar no tiene contaminantes cidos, se puede obtener un (DPR) de hasta 65F, para ello se necesita subir la temperatura del horno. La reduccin del Punto de Roco se puede determinar por la Ecuacin de Hammerschmidth:
Tr = d = 2335 ,0 xW M (100 W )
(29)
Donde: (d)= descenso del punto de roco; (M)= peso molecular y (W)= concentracin del glicol en la fase lquida en la relacin %P/P. Este es un parmetro de gran importancia, ya que para que el proceso de deshidratacin sea efectivo la concentracin del glicol debe de ser alta. d.- Solubilidad del Glicol. Este compuesto es soluble en condensado. Adems se puede demostrar que el TEG es ms soluble que el DEG. La solubilidad del TEG es de quinientas partes por milln (500 ppm), a 90 F, mientras que la del DEG es 350 ppm. Cuando hay hidrocarburos aromticos, la solubilidad del glicol es todava ms alta.
12
13
e Presin de Vapor. Este parmetro es importante de conocerlo, en vista que permite determinar la cantidad de glicol que se sale de la planta por evaporacin. Tericamente se sabe, que las prdidas de glicol aumentan, cuando la presin de vapor se hace ms alta. Para determinar las prdidas por evaporizacin se utiliza la siguiente frmula: P M 492 14,7 6 Prdidas = V x x1x10 760 379 492 + T P (30)
Donde: (PV) = presin de vapor del glicol en mm de Hg; (M)= peso molecular del glicol ;(T)= temperatura de operacin en F y (P)= presin de operacin en lpcm. Factores de Deterioro del Glicol Los principales factores de deterioro son: a.- La acidez en el proceso de absorcin con glicol se produce por la presencia de los gases cidos, tambin por la descomposicin del glicol en presencia de oxgeno y excesivo calor en el horno. S el pH esta por debajo de 5,5 el glicol s autoxida, con la formacin de perxidos, aldehdos y cidos orgnicos. Luego para evitar la formacin de estos productos se recomienda mantener el pH entre un valor de 6 y 8,5, pero el valor ptimo es 7,3. Las sustancias, que ms se emplean para subir el valor del pH son las alcanolaminas. El uso de estas sustancias se fundamenta en que: b.- La solubilidad de las aminas en glicol no depende del contenido de agua, y en ella hay que tener en cuenta lo siguiente: 1.- Las aminas son fcilmente determinadas en condiciones de laboratorio 2.- La reaccin amina- gas es reversible, luego las aminas son retenidas en el horno y se puede reutilizar c.- Contaminacin con Sales, Hidrocarburos y Parafinas. En algunos casos el gas natural, que ser sometido al proceso de deshidratacin puede arrastrar sales de los pozos, luego al entrar el gas al deshidratador las sales se depositan en las paredes de los tubos del horno y puede provocar el rompimiento del tubo produciendo graves problemas operacionales. Ahora si el gas es del tipo parafnico, puede dejar depsitos de cera en los puntos fros del sistema, esto tambin produce problemas operaciones al proceso de deshidratacin. d.- Formacin de Espumas. Este factor es de alta incidencia en la eficiencia del proceso de deshidratacin. La formacin de espuma, puede ser de tipo mecnica, se considera que es mecnica, cuando la cada de presin a travs del absorbedor aumenta en 20 libras y el glicol removido del sistema no forma espuma. La formacin de espuma del tipo mecnico produce turbulencia. Es decir altas velocidades del gas a travs del absorbedor. El otro tipo de espuma es de
13
14
tipo qumico. El espumaje tipo qumico se puede detectar batiendo el glicol en una botella, si se produce altas prdidas de glicol, entonces la espuma es del tipo qumico. Esta espuma es contaminante, para algunos compuestos, como hidrocarburos. Los hidrocarburos pueden entrar al sistema de glicol si el separador de entrada esta daado, como tambin si se permite que la temperatura del glicol pobre este por debajo de la temperatura de entrada del gas al separador, con lo cual se condensan los hidrocarburos pesados en la unidad. En general la espuma, tanto mecnica, como qumica produce deshidratacin pobre y prdidas de glicol muy altas. Para evitar la formacin de espumas se puede utilizar antiespumante, pero esto debe ser temporal hasta que se encuentre la verdadera causa de la formacin de espumas. e.- Absorcin de Hidrocarburos. Si el punto de roco de los hidrocarburos es alto, el glicol tiende a absorberlos., esto todava es mayor cuando hay presencia de aromticos. f.- Punto de congelamiento de la solucin agua glicol. Esto permite conocer la formacin de los primeros cristales de hielo en la solucin de glicol- agua. Pasos de un Proceso de Deshidratacin con Glicol En Etilenoglicol y el Dietilenoglicol se utilizan con frecuencia inyectados en la corriente de gas en procesos de refrigeracin y expansin, pero hay que tener en cuenta que no pueden utilizarse a temperatura menores a 20F. El proceso de deshidratacin con glicol, no se puede realizar hasta el final, cuando el gas deshidratado debe de ir a los procesos criognicos, ya que aqu el contenido de agua debe de ser mucho menor, en cantidades no mayores a los 10 ppm. En la figura 16 se presenta una Tpica Planta de Deshidratacin con Glicol. Figura 16 Unidad de Deshidratacin con TEG
14
15
En la figura 16 se observa, que el gas hmedo, que ha sido previamente pasado por un depurador, entra por en fondo de la torre de absorcin. Luego el gas viaja hacia el tope de al torre en contracorriente al glicol que viaja del tope al fondo de la torre. El gas entra en contacto con el glicol en cada bandeja con copas, con lo cual hace posible que el glicol absorba el vapor de agua contenido en la corriente de gas. El gas seco, sale por el tope de la torre y pasa a travs de un separador, en donde se separan las gotas de glicol que pueda contener el gas. El glicol hmedo abandona la torre por el fondo. Es de hacer notar que el glicol hmedo no solo absorbe el vapor de agua de la corriente de gas, sino que tambin absorbe las fracciones de hidrocarburos. Posteriormente, el glicol pasa a travs de un tanque de vaporizacin a baja presin. Aqu la mayora de los hidrocarburos se evaporan y se envan al quemador del rehervidos. En general, se puede sealar que la eficiencia de un proceso de deshidratacin con glicol depende principalmente de las siguientes variables: a.- La Concentracin del Glicol La cantidad de glicol en la torre de absorcin es una de las variables que mayor influencia ejerce en el proceso de deshidratacin. La importancia de este parmetro, es que el punto de roco del agua en el glicol puede ser controlado mediante los ajustes de concentracin del glicol. La concentracin del glicol depende de la eficiencia de liberacin del agua en el regenerador. b.- La Tasa de Flujo del Glicol. Las plantas de glicol por lo general utilizan una tasa de circulacin de 2 a 4 galones de TEG / lb de agua extrada. c.- El Nmero de Platos. Este parmetro y la concentracin del glicol son variables que dependen entre si. Si se fija el nmero de platos y la tasa de
15
16
circulacin, entonces la eficiencia del proceso de deshidratacin solo depender de la concentracin del glicol. Principales Equipos de una Planta de Deshidratacin a.-Torre de Absorcin. Una torre de absorcin puede estar constituida por platos con copa (se usa cuando el flujo de lquido es bajo y el gas alto) o pueda estar empacada. El nmero de platos, con lo cual debe de estar conformado una torre de absorcin se determina a travs de equilibrios dinmicos. b.- Rehervidor. La fuente de energa de un equipo rehervidor puede ser de fuente directa o indirecta. c.- Filtros En el caso del glicol, los filtros de mayor uso son filtros tipo tamiz d.- Bombas. Las bombas de desplazamiento positivo son las que ms se usan e.- Acumulador de Glicol. Este acumulador debe de estar provisto de un nivel de lquido y de un aparato para determinar la temperatura del glicol pobre. En la zona de Orocual Repblica Bolivariana de Venezuela, existe una planta deshidratadora de gas. El gas llega a la estacin a una presin de 1300 (lpcm). La funcin de la planta deshidratadora es extraer el agua de la corriente de gas, que entra a la planta para dejarlo dentro de la Norma ( ( 7lbH 2 0 / MMPCND ) . El gas deshidratado es utilizar para recuperacin secundaria, as como su transferencia hacia la zona industrial de Maturn, donde es utilizado como fuente energtica. Parte del gas es enviado tambin al Centro de Acondicionamiento de gas, en el Complejo Jusepn, Estado Monagas. En la figura 17 se muestra un esquema de la Planta Deshidratadora de Gas de Orocual. Figura 17 Esquema de la Planta Deshidratadora Orocual
16
17
La figura 17 representa en esquema del proceso de deshidratacin de gas natural. con Trietilenglicol El Trietilenglicol tiene una concentracin mayor al 99% P/P. Lo que indica que su contenido de agua es menor al 1% de agua. La concentracin del componente deshidratador es de mucha importancia, para la eficiencia del proceso. La deshidratacin se inicia con la entrada del gas hmedo por la parte inferior de la torre contactora, donde ocurre la separacin del agua del gas. La corriente de gas hmedo, despus de incesar a la torre contactora fluye hacia los niveles superiores de la torre, donde entra en contacto con el glicol, el cual absorbe el agua. El gas una vez seco sale de la torre pasa por un intercambiador de calor gas/glicol y sale hacia el cabezal de segregacin y distribucin. Deshidratacin del Gas Natural por Adsorcin Este proceso describe cualquier proceso, donde las molculas de un fluido lquido o gaseoso puede ser retenidos en la superficie de una superficie slida o lquida, debido fundamentalmente a las fuerzas superficiales de la superficie. Los cuerpos slidos se mantienen juntos, debido a fuerzas cohesivas que generalmente no estn balanceadas en su superficie. Por esta razn, las molculas superficiales pueden atraer molculas de otros cuerpos. Lo que significa que un cuerpo slido, puede atraer otras molculas de una corriente de fluido de una manera similar a las fuerzas de atraccin magnticas. Con, lo que puede causar la adhesin de molculas del fluido a molculas de la superficie slida. Lo que en este caso concreto ocurre, ya que las molculas del agua son atradas, por las molculas de la superficie slida. Para que el proceso de adsorcin sea de alta eficiencia se requiere que el rea de adsorcin sea extremadamente grande. Luego para conseguir esta superficie se le comprime y se le coloca en envase pequeo, de tal forma que se expanda cuando tome contacto con la sustancia, que ser adsorbida El proceso de adsorcin puede ser fsico o qumico
17
18
a.- Adsorcin Qumica En este caso los principales adsorbentes se caracterizan por reacciones qumicas entre el fluido a tratar y el material adsorbente. Esta adsorcin tiene muy poca aplicabilidad en la deshidratacin del gas natural b.- Adsorcin Fsica Si es Fsico requiere del uso de un material adsorbente, y que debe de tener las siguientes caractersticas. Una gran rea para el tratamiento de altos caudales; una actividad alta para los componentes a ser removidos, una alta tasa de transferencia de masa, una regeneracin econmica y de baja complejidad. La adsorcin fsica requiere del uso de un material adsorbente, que debe de tener las siguientes caractersticas. La adsorcin fsica se considera que es un proceso reversible, mientras que la qumica es irreversible, esto es de gran utilidad, ya que aplicando calor a la adsorcin fsica se pueden recuperar los parmetros, proceso que se denomina Desercin Trmica. Una gran rea de superficie, una actividad con los elementos que sern removidos del fluido, una tasa de transferencia de masa relativamente grande, una regeneracin de fcil manejo, una resistencia mecnica alta, debe de ser econmico y no corrosivo, ni txico, y adems poseer una alta densidad de masa, tampoco debe de presentar cambios apreciables, en relacin con el volumen durante el proceso de adsorcin, mantener al resistencia mecnica. Materiales Utilizados en la Adsorcin de Agua en el Gas Natural Existen una gran cantidad de materiales que satisfacen algunas de los requerimientos, entre los ms utilizados son los tamices moleculares, almina activada, silica gel y carbn activado. a.- Tamices Moleculares. Estos son compuestos cristalinos, que por lo general son silicatos. Los cuales, son desecantes altamente especializados y manufacturados para un tamao de poros definidos, con lo cual permite que el desecante sea utilizado para la adsorcin selectiva de un componente dado. Por lo general el tamao de poros de los tamices moleculares anda por el orden de los 310 angstroms (3-10 A). Los tamices moleculares tienen una alta aplicabilidad, en el gas que servir como materia prima para los procesos criognicos. El proceso de deshidratacin del gas natural, con el uso de tamices moleculares no es ms que la fijacin del vapor de agua a la superficie del cuerpo slido, es decir remover el vapor de agua de la corriente de gas por medio del contacto con una superficie slida, las molculas de agua son atrapadas en la superficie debido a las fuerzas intermoleculares b.- Almina Activada. Este material esta compuesto fundamentalmente por Oxido de Aluminio ( Al 2 0 3 ) . El compuesto puede ser utilizado para deshidratar corrientes de gas y lquidos, y lo mismo adsorbe hidrocarburos pesados que puedan estar presentes en la corriente de gas, pero estos hidrocarburos son difciles de remover. El desecante es alcalino y puede reaccionar con cidos. Con este material se pueden condiciones muy favorables en los puntos de roco de hasta
18
19
menos cien grados (-100F). Este material tiene una gran utilidad, por ser altamente econmico y de alta densidad msica c.- Silica Gel. Este es uno de los desecantes slidos de gran utilidad, esta conformado principalmente por Oxido de Silicio ( Si 0 2 ) y se pueden obtener puntos de roco de hasta (-100F). El compuesto tambin puede adsorber hidrocarburos pesados, siendo ms fciles para remover en el proceso de regeneracin, lo que hace que el silica gel se recomiende para controlar los hidrocarburos con el punto de roco del agua en ciertas aplicaciones. El tamao promedio de los poros de la silica gel es de 20 A. El desecante es un material cido y puede reaccionar con componentes bsicos. d.- Carbn Activado El carbn activa es un producto tratado y activado qumicamente para que tenga la capacidad de adsorcin. Se utiliza, por lo general para adsorber hidrocarburos pesados y/o solventes aplicados en la corriente de gas natural, tiene poca aplicabilidad en el proceso de deshidratacin del gas natural, al utilizar este componentes hay que tener cierto cuidado, ya que al parecer tiene problemas ambientales, que hay que controlar. Ejemplo de un Proceso de Deshidratacin de Gas Natural Por Adsorcin. En este proceso el fluido al secarse es pasado a travs de una torre empacada. Tal como se muestra en la figura 18 La figura 18 representa un diagrama tpico de una planta de deshidratacin de gas natural por adsorcin En figura 18 se puede observar que mientras en una torre se deshidrata el gas, en la otra se regenera el material adsorbente. La mayor parte del gas es pasado por el tope de la torre de adsorcin En el fondo se obtiene gas seco. El gas que deja la torre de regeneracin se enfra y se le hace pasar por un separador, donde es despojado del agua e hidrocarburos Problemas Operaciones en el proceso de Deshidratacin del Gas Natural a Travs de la Adsorcin con Tamices Moleculares: Los tapones de agua daan en cierto grado los tamices moleculares, para evitar estos tapones se debe utilizar un separador a la entrada de la planta, antes del absorbedoer. Tambin hay que tener en cuenta que los cambios bruscos en la presin, la velocidad excesiva del gas y los movimientos de lecho debido al calentamiento y enfriamiento pueden causar compactacin del empaque desecante, estos problemas pueden evitarse con un buen diseo mecnico Figura 18 Unidad de Deshidratacin por Adsorcin
19
20
El problema ms comn para los lechos es la contaminacin del tamiz con hidrocarburos pesados, para evitarlo deben de utilizarse filtros o lechos de bauxita aguas arriba del absorberdor, de tal forma de poder mantener el proceso con una alta eficiencia, y que adems no se vean involucrados otros procesos. Componentes Utilizados en un Proceso de Deshidratacin del Gas Natural con TEG Para el diseo de una planta de deshidratacin, hay que tener en cuenta que la eficiencia de este proceso, esta muy relacionada con los clculos necesarios que se deben de utilizar: a.- Torre de Absorcin. Para el diseo se tienen los siguientes datos: Caudal del Gas a Tratar ( = 40 MMPCND ) Gravedad especfica del gas al aire ( G = 0,67 ) Presin de operacin de la torre ( Pop = 800 lpca ) Contenido de agua en el gas a tratar ( CWE = 81,46lbH 2 0 / MMPCN
El contenido de agua en el gas de alimentacin se puede determinar en forma grfica o a travs de la correlacin de BukaceK. En este caso se determina el contenido de agua en el gas dulce (WCAGD)
WCAGD = lbH 2 0 80400 + 23,7 = 77 ,3 MM PCN 1500
20
21
Los grficos 14 y 15 indicar que el C0 2 contiene 96 H2S contiene 220
lbH 2 0 MM PCN
lbdeH 2 0 MM PCN
, mientras que el
, luego el contenido de agua en el gas total es:
WCAGT=77,3x0,889+96x0,0935+220x0,0175= 81,46 (lb de H20/ MM PCN. Luego el porcentaje molar del agua en el gas de alimentacin es: %Molar de H20 en 81,46lbdeH 2 0 x379 ,63( PCN )(lbmol ) x100 = 0,1717 0,17 % 1x10 6 ( PCN ) x(lbmol ) x18,016 (lbdeH 2 0) el gas=
Contenido de agua requerida a la salida de la planta ( CWS = 7lbH 2 0 / MMPCN ) Concentracin del TEG que entra a la torre de absorcin es 99,5%P/P. La pureza de este material es algo que siempre hay que tratar de controlar, ya que eso depende en gran forma la eficiencia del proceso. b.- Temperatura de Operacin de la Torre se Absorcin. Este parmetro se determina en forma grfica para ello se utiliza la cantidad de agua a la entrada y la presin de operacin, con lo cual se obtiene la temperatura de saturacin del gas (TSG = 111,5F ) . Este valor es aproximadamente igual a la temperatura de operacin de la torre de absorcin. Se asume que el diseo de la torre, ser con platos, luego la correccin para la temperatura es de 0,991, lo que indica que la temperatura de operacin es
Top = TSG =111 ,5 x0,991 =110 ,5 F
c.-. Gravedad Especfica del Gas. Este parmetro se corrige, en tablas donde se obtiene que el factor de correccin para el valor de 0,67 es 1,024, luego el valor es:
G = 0,67 x1,024 = 0,6861
d.- Construccin de la lnea de Operacin. Para el diseo de este parmetro se necesita: definir los siguientes aspectos:
V2 =Flujo msico de Gas Hmedo que entra a la torre de absorcin en (lb/da) =
lb 4 x10 7 ( PCN ) x(lbmol ) x 0,6861 x 28 ,97 (lb ) = 2094283 ,07 da ) ( da ) x379 ,63 ( PCN ) x(lbmol )
flujo msico de gas saturado con agua que entra a la torre de absorcin menos el flujo de agua que viaja en la fase de vapor con el gas, este parmetro hay que tener bien en cuenta para los clculos, luego se tiene que:
V = Flujo Msico de gas seco (lb/da)= Este flujo msico de gas seco es igual al
21
22
(mH20
en
V2)= CWE x 40 MMPCN= 81,46
lbH 2 0 x 40 MMPCND MMPCN
3258,4
lbH 2 0 da
V = V2 (mH20 en V2)=2094283,07-3258,4= 2091024,67
lb da
(lb de agua /lb de gas seco)= m H20 en V2/ V = =
Y2 = Relacin de peso, del agua al gas seco, que entra a la torre de absorcin, en
lbH 2 0 3258 ,4(lbH 2 0)( da ) = 1,556 x10 3 lbgas sec o 2094024 ,67 (lbgas sec o)( da )
V1 =Flujo Msico de gas tratado que sale de la torre de absorcin, en (lb/da)=
V2-(m H20 absorbida)=2094283,07
lb lb lb -(3258,4-7x40) =2091304,67 da da da
Y1 =Relacin de peso del agua al gas seco que sale en el gas tratado, en
lbH20/lb de gas seco = (mH20 en V1)/(m de gas seco)=
lbH 2 0 7 x 40 (lbH 2 0) x ( da ) = 1,3371 x10 4 lbgas sec o ( da ) 2094024 ,67 (lbgas sec o)
L1 = Flujo msico de la solucin TEG regenerada que entra a la torre de
absorcin en (lb/da)
L2 = Flujo Msico de la solucin TEF que sale de al torre de absorcin, en (lb/da) X 1 = Relacin de peso del agua al TEG puro que entra a la torre de Absorcin en
( lb de agua/lb TEG).
X 2 = Relacin de peso del agua al TEG puro que sale de la torre de absorcin en
lb de agua/lb TEG
L = Flujo Msico del TEG puro (lb/da)
En forma grfica utilizando la cantidad de agua a la salida de la torre
lbH 2 0 CWS = 7 y la presin de operacin se obtiene la temperatura a la cual el MMPCN
gas natural y el agua estn en equilibrio, que en este caso es 28F. Con este valor y la temperatura de operacin de al torre de absorcin, se obtiene en forma grfica
22
23
la concentracin del TEG en % P/P del TEG a la salida de la torre, la cual en este caso es 98%P/P. El balance total de masa en la torre de absorcin es:
V2 + L1 = V1 + L2 L2 = (V2 V1 ) + L1
El balance de TEG puro en la torre de absorcin es: (%TEG en L1) x L1 = (%TEG en L2) xL 2 ( 0,995 ) L1 = ( 0,98) L2 = ( 0,98) [ (2978 ,4) + L1 ] .
lb lb L1 = 195688 ,8 ; L2 = 198667 ,2 da da
La cantidad de TEG puro que entra a la corriente de la solucin Agua- Glicol que entra a la torre de absorcin es:
L = (%TEG en L1)xL1=(0,995x195688,8=194710,36 da
La tasa de agua en la corriente de solucin Agua- Glicol que entra a la torre de absorcin es: (mH20 en L1)=[1-(%TEG en L1]L1= [1 (0,995 )]195688 ,8 = 978 ,44 Luego se obtiene que:
mH 2 0enL1 978,44 3 lb X1 = mTEGenL = 194710 ,36 = 5,025 x10 da 1
lb da
lb
La tasa agua la corriente de solucin Agua- Glicol que sale de la torre de absorcin es: (mH20 en L2)L2=[1-(%TEG en L2]L2= [1 (0,98 )] x198667 ,2 = 3973 ,34
mH 2 0enL 2 X2 = mTEGenL 2 3973,34 lbH 2 0 = = 2,041x10 2 lbTEG 194710 ,36
lb da
Despus de haber realizados todos los clculos necesarios para el diseo de la torre de absorcin, para el diseo se necesita determinar lo siguiente parmetros que juegan un importante papel, por lo tanto hay que tener bien claro, para utilizarlo en forma adecuada y correcta, y que no provoque problemas operacionales:
23
24
a.- Construccin de la Curva de Equilibrio Lquido (X)- Vapor (Y). La curva de equilibrio se obtiene de graficar la relacin de peso del agua al gas seco (Y), en funcin de la relacin del agua al TEG puro(X) b.- Clculo del Nmero de Platos Reales de la Torre de Absorcin. Este clculo se realiza en forma grfica c.- Determinacin del Dimetro de la Torre de Absorcin. En este caso es necesario calcular las reas de flujo correspondiente al lquido y gas, como tambin la velocidad del lquido, rea correspondiente al gas, tambin la velocidad de la fase gaseosa. d.- Clculo de los Orificios de entrada y salida del Gas en la Torre de Absorcin e.- Diseo del Regenerador. Para el diseo del Regenerador se necesita definir los siguientes parmetros: LER = Flujo msico de la solucin de TEG que viene de la torre de absorcin y entra a la torre de regeneracin en (lb/da). El valor de LER = al flujo msico del TEG que abandona la torre de absorcin, es decir
lb LER = L2 = 198667 ,2 da
LSR = Flujo msico de la solucin de TEG que sale de al torre de regeneracin en
lb/da
V ER = Flujo Msico de vapor de agua y gas de burbujeo que sale del rehervidor y
entra a la torre de regeneracin, en lb/da.
V SR =Flujo Msico de vapor de agua, gas de burbujeo y TEG(perdido), que sale
de la torre de regeneracin, en lb/da: Este flujo msico que sale de la torre de regeneracin es igual:
V SR =(mH20 en V SR )+(mTEg perdido)+(mgas de burbujeo). La concentracin de
la solucin del TEG a la salida de una unidad de regeneracin depende de la eficiencia de despojamiento del agua que se tenga en esa solucin, los datos indican que por lo general se utilizan 10 PCN/gal de TEG como gas de burbujeo
L1 = Flujo Msico de la solucin de TEG regenerada que sale del rehervidor y es
enviado a la torre de absorcin, en lb/da Q= Calor total cedido en el Rehervidos para evaporar el agua en exceso contenida en TEG , en (TBU/hora). Este parmetro se determina a partir de la frmula siguiente:
24
25
Q = Q( H 2 0) + Q(TEG ) , y desde luego se puede determinar el calor del agua y del
TEG, y con ello se determina el calor total. En vista que el calor cedido al agua es igual al calor sensible necesario para obtener agua saturada ms el calor latente necesario para evaporar el agua, hasta lograr vapor saturado Principales Equipos Utilizados en una Planta de Deshidratacin con Glicoles a.-Absorbedor de Glicol. Es una torre donde el gas cargado con agua, se pone en contacto en contracorriente con el glicol limpio o deshidratado, b.- Vlvulas de Expansin. En vista que, por lo general el glicol en el horno se encuentra a presin atmosfrica y en absorbedor existe alta presin, se debe de utilizar una vlvula para lograr controlar los siguientes aspectos, que son la cada de presin y el control del nivel de glicol en el absorbedor c.- Separador de Glicol e Hidrocarburos lquidos. Es equipo se encarga de la separacin del gas y el condensado que arrastra el glicol desde al absorbedor d.- Filtros. Estos equipos sirven para separar las impurezas e.- Intercambiadores. En este aparato el glicol rico a temperatura ambiente es utilizado para enfriar el glicol pobre que viene del horno. Para que este proceso ocurra se utilizan intercambiadores de tubo y carcasa. El glicol rico se puede calentar hasta una temperatura de 300F, mientras que el glicol pobre puede ser enfriado hasta 200 F. f.- Regenerador. La parte principal de este aparato se encuentra en el horno. El regenerador puede calentarse con vapores de agua, con aceite de calentamiento o fuego directo. El papel de los intercambiadores de calor ha adquirido una creciente importancia, en los procesos industriales, en vista que los usuarios han considerado la necesidad de ahorrar energa. Luego se desea obtener un equipo, que optimice el proceso, y por lo tanto pueda ahorrar energa, en la realizacin del proceso con una alta eficiencia. La optimizacin del proceso, no solo se debe realizar en funcin de un anlisis trmico y rendimiento econmico de lo invertido, sino tambin en funcin del aprovechamiento energtico del sistema. En trminos generales se puede sealar, que un intercambiador de calor consiste en un lmite slido, buen conductor, que separa dos fluidos que se intercambian energa por transmisin de calor. En la industria los intercambiadores de calor utilizados son los intercambiadores de carcasa y tubos, y su funcin consiste en evaluar el coeficiente global de calor entre las dos corrientes fluidas. Utilidad de los Diagramas de Fases en el Proceso de Deshidratacin del Gas Natural: Los diagramas de fases permiten comparar las condiciones extremas del gas que pudiera una planta de deshidratacin, esto debe de advertir al ingeniero
25
26
de proceso sobre los valores de presin y temperatura, con los cuales se debe de operar. El estudio de fases le permite al ingeniero saber la composicin y las cantidades de las fases en equilibrio a una presin y temperatura determinada, caracterizando de esa manera la muestra de gas que va a entrar a una planta de deshidratacin y con que cantidad de agua entra el gas. En el proceso de deshidratacin de gas natural, tiene una gran aplicabilidad los diagramas de fases binarios, como por ejemplo los diagramas de fases Glicol- Agua. En la figura 19 se presenta un diagrama de Fase para el TEG- Agua Figura 19 Diagrama de Fase TEG-Agua
En la figura 19 se observa la lnea envolvente del punto de roco, ms arriba de esa lnea solo debe de existir vapor. Entre la lnea envolvente del punto de roco y Punto de burbujeo se encuentra la regin de dos fases (lquido- Vapor), y ms debajo de la lnea del punto de burbujeo, solo debe de existir lquido. Estos diagramas se representan a la presin atmosfrica. Si se trabaja a la presin atmosfrica con una concentracin de 95 %P/P de TEG y la temperatura es de 200 F, luego segn el diagrama de fase la solucin debe de encontrarse en la fase lquida, ya que estara ms abajo del punto de burbujeo. Ahora si la condicin de concentracin es la misma y el valor de presin se mantiene constante, mientras que la temperatura es 250F, luego en este caso se debe de encontrar en la regin bifsica, y de la misma forma se aumenta la temperatura hasta 550F, ahora el proceso se encontrara en estado de vapor. Los diagramas de fases se sustentan en la ecuacin de la Regla de las fases..
26
27
Problema de Deshidratacin. Una mezcla de gas natural de 85 MMPCND, y tiene una temperatura y presin de operacin de 120 F y 1250 lpca, respectivamente y esta conformado por los siguientes componentes: Componente C1 C2 C3 C4 C5 C02 H2S N2 Total %molar sin agua PM)lb/lbmol) 82,15 16,043 1,52 30,070 0,96 44,097 0,71 58,123 0,55 72,150 9,56 44,010 0,80 34,084 3,75 28,013 100 PM sin Agua)=20,4027
= 0,7043
%( H 2 0) =
450(lbH 2 0) x379,6( PCN )(lbmol ) x100 = 0,9482% 1x10 6 ( PCN )(lbmol ) x18,016(lbH 2 0)
%molar Con agua PM con agua=20,2453 81,3784 = 0,6988 1,5057 0,9510 0,7033 0,5448 9,5547 0,7925 3,7148 0,9482 100
Componente C1 C2 C3 C4 C5 C02 H2S N2 H20 Total
Agua que debe de ser removida de la corriente de gas ( W )
( W ) = 450-7 = 443 lb de H20/MMPCN. Esto significa que para el caudal total en
lbmol/hora es:
443(lbH 2 0) x8 x10 7 ( PCN )(lbmol ) lbmol W ( H 2 0) = = 1967 ,14 6 1x10 ( PCN ) x 24 (hora ) x18,016 (lbH 2 0) hora
El caudal de flujo molar (n) es:
8 x10 7 ( PCN )( lbmol )( da ) lbmol lbmol n = 8781 ,1732 = hora ( da ) x379 ,6( PCN ) x 24 (hora ) hora
Para deshidratar el gas tiene que quedar un mximo de 7 lb de H 20/MMPCN, luego:
27
28
%( H 2 0) =
7(lbH 2 0) x379,6( PCN ) x(lbmol )100 = 0,0147% 1x10 6 ( PCN )(lbmol ) x18,016(lbH 2 0)
28
También podría gustarte
- Proceso de DeshidrataciónDocumento52 páginasProceso de DeshidrataciónEly RodvasAún no hay calificaciones
- Contenido de Agua y Predicción de Condiciones de Formación de HidratosDocumento28 páginasContenido de Agua y Predicción de Condiciones de Formación de HidratosJairo Puentes100% (5)
- Gas Natural - Punto de RocioDocumento162 páginasGas Natural - Punto de RocioPablo Edher Beteta Castillo100% (2)
- Proceso de Turbo Expander Pag 31Documento106 páginasProceso de Turbo Expander Pag 31Zeugirdor YddurAún no hay calificaciones
- Optimizando el tratamiento de gas natural a través de la tecnología de deshidratación por punto de rocíoDocumento9 páginasOptimizando el tratamiento de gas natural a través de la tecnología de deshidratación por punto de rocíoVanessa GuerraAún no hay calificaciones
- Tema 1 Aplicacion Practica de Adsor y Absor PresentacionDocumento231 páginasTema 1 Aplicacion Practica de Adsor y Absor PresentacionJorge Blanco ChoqueAún no hay calificaciones
- Procesos de Deshidratación Del Gas NaturalDocumento25 páginasProcesos de Deshidratación Del Gas NaturalGonzalo Olivera Arancibia100% (1)
- Procesos de endulzamiento del gas naturalDocumento36 páginasProcesos de endulzamiento del gas naturalM G C100% (1)
- Bloque San Antonio - Planta de procesamiento de gas SábaloDocumento16 páginasBloque San Antonio - Planta de procesamiento de gas Sábaloangelarosalia100% (1)
- Pg-Recuperacion de Licuables en Rio Grande (Jan12)Documento260 páginasPg-Recuperacion de Licuables en Rio Grande (Jan12)dennis_ugarte100% (1)
- Tarea 4 Modulo 2Documento5 páginasTarea 4 Modulo 2Luis Ballesteros ChoqueAún no hay calificaciones
- Recuperación de Hidrocarburos Líquido Grupo 4Documento72 páginasRecuperación de Hidrocarburos Líquido Grupo 4Linda Greace Zuzunaga VargasAún no hay calificaciones
- Limpieza Del Gas NaturalDocumento25 páginasLimpieza Del Gas NaturalOscar BetancurAún no hay calificaciones
- Diseño Conceptual de Una Planta de Gas To Liquids (GTL) para La Producción de Diesel Oil en CarraDocumento244 páginasDiseño Conceptual de Una Planta de Gas To Liquids (GTL) para La Producción de Diesel Oil en CarraRONALD MANCERA MARQUINA67% (3)
- Figura 1-23 Contenido de Agua de Dulce, en Natural Gas: Ejemplo de Mcketta-WeheDocumento14 páginasFigura 1-23 Contenido de Agua de Dulce, en Natural Gas: Ejemplo de Mcketta-WehepabelAún no hay calificaciones
- Planta de ColpaDocumento6 páginasPlanta de ColpaEliezerlunaAún no hay calificaciones
- Proceso de extracción de líquidos por turbo-expansiónDocumento10 páginasProceso de extracción de líquidos por turbo-expansiónroyer100% (1)
- Ajuste Del Punto de RocioDocumento32 páginasAjuste Del Punto de RocioGustavo Alexis Leon PerezAún no hay calificaciones
- Separador Trifásico VerticalDocumento11 páginasSeparador Trifásico VerticalYuriko Moy CaporaliAún no hay calificaciones
- Tema 2 Deshidratacion Del Gas Natural Pet 216 2 EjercicioDocumento23 páginasTema 2 Deshidratacion Del Gas Natural Pet 216 2 EjercicioSheilita Siv100% (1)
- Cap III Proceso de Separacion Del Gas NaturalDocumento31 páginasCap III Proceso de Separacion Del Gas NaturalEiner Leonel CaucotaAún no hay calificaciones
- Proceso de Endulzamiento Del Gas Natural Con Amina en La Planta TacoboDocumento41 páginasProceso de Endulzamiento Del Gas Natural Con Amina en La Planta Tacoboluis alfredoAún no hay calificaciones
- TurboDocumento8 páginasTurboAlex RivasAún no hay calificaciones
- Deshidratacion Con TrietilenglicolDocumento41 páginasDeshidratacion Con TrietilenglicolkevinAún no hay calificaciones
- Evaluación Del Sistema de Deshidratación Con Glicol DelDocumento144 páginasEvaluación Del Sistema de Deshidratación Con Glicol DelWilfredo Suarez TorresAún no hay calificaciones
- PET219 PetroquimicaDocumento79 páginasPET219 PetroquimicaCharly D White100% (1)
- Fundamentos del fraccionamientoDocumento38 páginasFundamentos del fraccionamientoFabiolaVincentiAún no hay calificaciones
- Extracción de Líquidos Del Gas NaturalDocumento55 páginasExtracción de Líquidos Del Gas NaturalRodrigoAún no hay calificaciones
- Sistema de refrigeración de una etapa con propano de 35 MM BTUH a -35°FDocumento91 páginasSistema de refrigeración de una etapa con propano de 35 MM BTUH a -35°FJose BurguillosAún no hay calificaciones
- Deshidratación Del Gas NaturalDocumento7 páginasDeshidratación Del Gas NaturalCristian González Burzichelli50% (2)
- Deshidratacion Del Gas NaturalDocumento18 páginasDeshidratacion Del Gas Naturaltaller de gradoAún no hay calificaciones
- Procesos de Extraccion de Liquidos Del Gas Natural, Disertacion de Gas II, Grupo 6Documento69 páginasProcesos de Extraccion de Liquidos Del Gas Natural, Disertacion de Gas II, Grupo 6jhonn1067% (3)
- Riqueza Del Gas Natural 2010Documento13 páginasRiqueza Del Gas Natural 2010ruben torricoAún no hay calificaciones
- Procesos Del GasDocumento70 páginasProcesos Del GasCeleste LugoAún no hay calificaciones
- Acondicionamiento de GAS NATURALDocumento24 páginasAcondicionamiento de GAS NATURALJuan Pablo Chavez Ixtepan93% (14)
- Separador Supersónico TwisterDocumento4 páginasSeparador Supersónico TwisterCristhian Soliz100% (1)
- Plantas de Extraccion de LicuablesDocumento6 páginasPlantas de Extraccion de LicuablesJHUCEAún no hay calificaciones
- Planta Proceso MargaritaDocumento4 páginasPlanta Proceso MargaritaAnonymous ejX5fcaNZPAún no hay calificaciones
- Extracción de Liquidos Del Gas Natural FinalDocumento15 páginasExtracción de Liquidos Del Gas Natural FinalAndreaTorloneAún no hay calificaciones
- Simulación de Procesos Con ASPEN HYSYS INEGAS8Documento215 páginasSimulación de Procesos Con ASPEN HYSYS INEGAS8Luis Alberto Flores Carballo100% (2)
- Control gas natural proceso tratamientoDocumento50 páginasControl gas natural proceso tratamientoSharon BotinyAún no hay calificaciones
- Problemas y Soluciones de Carga de Líquidos en Pozos de Gas Del Activo IntegralDocumento130 páginasProblemas y Soluciones de Carga de Líquidos en Pozos de Gas Del Activo IntegralJose MendozaAún no hay calificaciones
- Gas Virtual PDFDocumento16 páginasGas Virtual PDFWilsa Angelica Arias ArroyoAún no hay calificaciones
- Parámetros Que Intervienen en El Dimensionamiento de SeparadoresDocumento9 páginasParámetros Que Intervienen en El Dimensionamiento de SeparadoresArmando Matus GutierrezAún no hay calificaciones
- Proyecto de Red Primaria de GasDocumento143 páginasProyecto de Red Primaria de GasGary Lino CortezAún no hay calificaciones
- Turbo ExpanderDocumento5 páginasTurbo ExpanderbrionyleslyAún no hay calificaciones
- Inyeccion Alterna de Agua y GasDocumento26 páginasInyeccion Alterna de Agua y Gasivan paulAún no hay calificaciones
- Ajuste de Punto de RosioDocumento7 páginasAjuste de Punto de RosioAnonymous T5jCOqoAún no hay calificaciones
- Proceso de Deshidratación del Gas NaturalDocumento35 páginasProceso de Deshidratación del Gas Naturalsarah jerusalen veron bernalAún no hay calificaciones
- Planta de Deshidratacion de GasDocumento11 páginasPlanta de Deshidratacion de GasJhonattan RochaAún no hay calificaciones
- Deshidratacion Del Gas NaturalDocumento23 páginasDeshidratacion Del Gas Naturalmaria figueraAún no hay calificaciones
- Trabajo de Deshidratacion Del Gas NaturalDocumento39 páginasTrabajo de Deshidratacion Del Gas Naturaljesus hernandezAún no hay calificaciones
- Deshidratacion InformeDocumento18 páginasDeshidratacion InformeMichael Paz100% (1)
- Deshidratación Del Gas Natural PDFDocumento54 páginasDeshidratación Del Gas Natural PDFcarupano7Aún no hay calificaciones
- DESHIDROGENACIONDocumento28 páginasDESHIDROGENACIONDiego RojasAún no hay calificaciones
- Exposicion de TegDocumento28 páginasExposicion de TegYhoselyn LinnaAún no hay calificaciones
- Deshidratación Del Gas NaturalDocumento21 páginasDeshidratación Del Gas NaturalKATHERINE ARUPONAún no hay calificaciones
- Procesos de deshidratación del gas naturalDocumento54 páginasProcesos de deshidratación del gas naturalAndrea GarciaAún no hay calificaciones
- Exposición Final de Hidratos de Gas.Documento48 páginasExposición Final de Hidratos de Gas.Henry Gustavo Chaves Gutiérrez100% (1)
- Unidad 3 GasDocumento11 páginasUnidad 3 Gasalfred100% (1)
- Fracción: Representación Matemática de Una Porción de Un TodoDocumento59 páginasFracción: Representación Matemática de Una Porción de Un TodoErvin Geovany Estuardo Macz cuAún no hay calificaciones
- FloryanonuevoDocumento3 páginasFloryanonuevoJESUSAún no hay calificaciones
- DISEÑODocumento23 páginasDISEÑOJesus Alberto Reyes MoyaAún no hay calificaciones
- 51 Historias InfantilesDocumento104 páginas51 Historias InfantilesEdu BecerraAún no hay calificaciones
- Informe de Pasantia ModeloDocumento34 páginasInforme de Pasantia ModeloJesus Alberto Reyes MoyaAún no hay calificaciones
- HCTG de Desconectador 220kv Con Pat MarconaDocumento6 páginasHCTG de Desconectador 220kv Con Pat Marconamiguel nuñezAún no hay calificaciones
- Supervision de Inst. Residenciales y Comerciales de Gas Natural-VENTILACIONDocumento27 páginasSupervision de Inst. Residenciales y Comerciales de Gas Natural-VENTILACIONEdinson HerreraAún no hay calificaciones
- Alquiler de NanaDocumento2 páginasAlquiler de NanaClaribel Peguero BenitezAún no hay calificaciones
- Determinación evapotranspiración métodos balance cacaoDocumento5 páginasDeterminación evapotranspiración métodos balance cacaoAndrea PascuasAún no hay calificaciones
- Difraccion de Electrones y NeutronesDocumento14 páginasDifraccion de Electrones y NeutronesFelipe Vásquez ArribasplataAún no hay calificaciones
- Repelente ultrasonico mosquitos 10 componentesDocumento6 páginasRepelente ultrasonico mosquitos 10 componentesLeonel Corazon de LeonAún no hay calificaciones
- Ptar CarhuazDocumento105 páginasPtar CarhuazKevin Chavez LopezAún no hay calificaciones
- TALLER 2 Circuito SerieDocumento6 páginasTALLER 2 Circuito SerieMauro TeraAún no hay calificaciones
- Practica 1 Banco de MotoresDocumento4 páginasPractica 1 Banco de MotoresJuanAún no hay calificaciones
- Informe Laboratorio Calibrador de ManometrosDocumento10 páginasInforme Laboratorio Calibrador de ManometrosJeancarlos QuispeAún no hay calificaciones
- MecanismosDocumento6 páginasMecanismosSary CastilloAún no hay calificaciones
- Coleccion Problemas 1er ParcialDocumento25 páginasColeccion Problemas 1er ParcialBernat Lafuente FedericoAún no hay calificaciones
- Seguridad TBMDocumento36 páginasSeguridad TBMEsteban BravoAún no hay calificaciones
- Manual IQ2 SpaDocumento178 páginasManual IQ2 SpaMiguel Sayago Gonzalez100% (1)
- Catalogo vtt10 MP EsDocumento4 páginasCatalogo vtt10 MP EsWILSON KANKI GUEVARAAún no hay calificaciones
- Instalación de Aire Comprimido, SAMDocumento16 páginasInstalación de Aire Comprimido, SAMWinston Curo QuispeAún no hay calificaciones
- A6 Civ-238 JTP CoriaDocumento6 páginasA6 Civ-238 JTP CoriaFany XoriaAún no hay calificaciones
- Reporte EsterilizacionDocumento2 páginasReporte EsterilizacionPEDRO MANUEL CANDELARIO LOPEZAún no hay calificaciones
- 5 Reglas de OroDocumento6 páginas5 Reglas de Orolmarron25Aún no hay calificaciones
- Problemas Optimizacion EspañolDocumento2 páginasProblemas Optimizacion EspañolJanet Paulina Ramirez Morales0% (1)
- Jardineria 2011Documento34 páginasJardineria 2011Comercial y Ferreteria Diaz SAAún no hay calificaciones
- Geotecnia Colectores - CVCDocumento217 páginasGeotecnia Colectores - CVCEdson Orlando Hoyos CeronAún no hay calificaciones
- 00 SILLABU CE90 Fisica 2 202101Documento8 páginas00 SILLABU CE90 Fisica 2 202101Cristhian RuizAún no hay calificaciones
- lmh20186zkbb0 Manualservicio Lavadora AquaspeiraDocumento76 páginaslmh20186zkbb0 Manualservicio Lavadora Aquaspeiranibble1974100% (2)
- Guia 4 Ciencias Naturales 7° Segundo PeriodDocumento16 páginasGuia 4 Ciencias Naturales 7° Segundo PeriodCamila UrquizaAún no hay calificaciones
- Guía de bloqueo de energía paso a pasoDocumento8 páginasGuía de bloqueo de energía paso a pasoBeto VelázquezAún no hay calificaciones
- Cuestionario (4-5) y Recomendaciones Inf. 6Documento9 páginasCuestionario (4-5) y Recomendaciones Inf. 6Anonymous TFLtpxuWZAún no hay calificaciones
- Anexo 02. Informe SESGA, Inspección de Grupos Electrógenos - HospitalesDocumento7 páginasAnexo 02. Informe SESGA, Inspección de Grupos Electrógenos - HospitalesLuis LacheAún no hay calificaciones
- TelemediciónDocumento84 páginasTelemediciónatc_958195759Aún no hay calificaciones
- Tipos de TerminacionesDocumento24 páginasTipos de TerminacionesBonifacio Hernandez LopezAún no hay calificaciones