Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Oxidación-Reducción: Química Básica
Cargado por
Salma Irene Ríos MotaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Oxidación-Reducción: Química Básica
Cargado por
Salma Irene Ríos MotaCopyright:
Formatos disponibles
OXIDACIÓN-REDUCCIÓN
QUÍMICA BÁSICA
PROFA. ANA KAREN ACERO GUTIÉRREZ 1
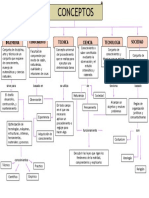
Conceptos
ión
Elemento o compuesto con carga
(debido a la perdida o ganancia de electrones)
Ión con carga positiva (+) Ión con carga negativa (-)
El elemento o compuesto pierde e- El elemento o compuesto gana e-
CATIÓN ANIÓN
11 protones 11 protones 17 protones 17 protones
Na Pierde 1 e- y se
hace catión Na+ Cl 17 electrones
Gana 1 e- y se
hace anión Cl- 18 electrones
11 electrones 10 electrones
PROFA. ANA KAREN ACERO GUTIÉRREZ 2
Reglas para determinar números de
oxidación
a) La carga total para compuestos y elementos f) El flúor (F) siempre tiene número de
libres (estado elemental) = 0 oxidación = -1
b) La carga total para aniones = (-) g) El hidrógeno (H) tiene número de
oxidación = +1
c) La carga total para cationes = (+)
h) El hidrógeno (H) sólo en hidruros tiene
(se adjunta al material tabla de iones) número de oxidación = -1
d) Los elementos del grupo 1A de la tabla i) El oxígeno (O) tiene número de
periódica (ejemplo: Na, Li, K) siempre tienen oxidación = -2
número de oxidación = +1
j) El oxígeno (O) sólo en peróxidos tiene
e) Los elementos del grupo 2A de la tabla número de oxidación = -1
periódica (ejemplo: Ca, Mg, Ba) siempre
tienen número de oxidación = +2
PROFA. ANA KAREN ACERO GUTIÉRREZ 3
Ejemplos NOTA: Para cargas de aniones y cationes se
puede apoyar de tabla de iones.
Se descompone en
sulfato férrico Fe2(SO4)3 catión + anión Fe3+ + (SO4)2-
Elemento # de átomos Número de oxidación Carga (2)
Números de oxidación de cada elemento
Fe 2 +3 +6 presente en el compuesto
S 3 +6 (5) +18 (4)
O 12 -2 (3) -24 +3 +6 -2
CARGA TOTAL (1) 0 Fe2(SO4)3
(1) Es un compuesto y por lo tanto cumple con la regla del inciso (a). Carga total = 0
(2) Se obtiene de multiplicar el #de átomos por el número de oxidación
(3) De la regla inciso (i)
(4) Como la carga total debe ser cero, se ajusta este valor para que con los otros valores de carga la sumatoria sea igual a 0
(5) Se obtiene de dividir la carga entre el # de átomos
PROFA. ANA KAREN ACERO GUTIÉRREZ 4
Ejemplos NOTA: Para cargas de aniones y cationes se
puede apoyar de tabla de iones.
(Cr2O7) -2
Ión dicromato Números de oxidación de cada elemento
presente en el compuesto
Elemento # de átomos Número de oxidación Carga (2)
Cr 2 +6 (5) +12 (4)
+6 -2
O 7 -2 (3) -14
CARGA TOTAL (1) -2
(Cr2O7)-2
(1) Es un anión y por lo tanto cumple con la regla del inciso (b). Carga total = -2 que corresponde a la carga de todo el anión
(2) Se obtiene de multiplicar el #de átomos por el número de oxidación
(3) De la regla inciso (i)
(4) Como la carga total debe ser -2, se ajusta este valor para que con los otros valores de carga la sumatoria sea igual a -2
(5) Se obtiene de dividir la carga entre el # de átomos
PROFA. ANA KAREN ACERO GUTIÉRREZ 5
Ejemplos NOTA: Para cargas de aniones y cationes se
puede apoyar de tabla de iones
(NH4) +1
Ión amonio Números de oxidación de cada elemento
presente en el compuesto
Elemento # de átomos Número de oxidación Carga (2)
N 1 -3 (5) -3 (4)
-3 +1
H 4 +1 (3) +4
CARGA TOTAL (1) +1
(NH4)+1
(1) Es un catión y por lo tanto cumple con la regla del inciso (c). Carga total = +1 que corresponde a la carga de todo el catión
(2) Se obtiene de multiplicar el #de átomos por el número de oxidación
(3) De la regla inciso (g)
(4) Como la carga total debe ser +1, se ajusta este valor para que con los otros valores de carga la sumatoria sea igual a +1
(5) Se obtiene de dividir la carga entre el # de átomos
PROFA. ANA KAREN ACERO GUTIÉRREZ 6
Ejercicios (actividad en clase 3)
PROFA. ANA KAREN ACERO GUTIÉRREZ 7
También podría gustarte
- Nomenclatura BinariaDocumento54 páginasNomenclatura Binariarayos100Aún no hay calificaciones
- Folleto NomenclaturaDocumento21 páginasFolleto NomenclaturaVasquez JulisaAún no hay calificaciones
- Manual-De-Nomenclatura-De-Compuestos QuimicaDocumento21 páginasManual-De-Nomenclatura-De-Compuestos QuimicaCatherine RodríguezAún no hay calificaciones
- Daniel Lillo Control3Documento6 páginasDaniel Lillo Control3danielAún no hay calificaciones
- Asm - Nomenclatura Inorganica - 2023Documento102 páginasAsm - Nomenclatura Inorganica - 2023Gabriela InocenteAún no hay calificaciones
- Clase Numero de OxidacíonDocumento15 páginasClase Numero de OxidacíonFatima Paola MoreiraAún no hay calificaciones
- Teoría Nomenclatura Compuestos InorgánicosDocumento9 páginasTeoría Nomenclatura Compuestos InorgánicosFLOR NAYELI ALEJOS PUMARICRAAún no hay calificaciones
- Nomenclatura Inorgánica Parte 1Documento22 páginasNomenclatura Inorgánica Parte 1Bryan Cieza RojasAún no hay calificaciones
- Manual de Nomenclatura PDFDocumento21 páginasManual de Nomenclatura PDFGatica17Aún no hay calificaciones
- MANUAL DE NOMENCLATURA DE COMPUESTOS 2024 RevDocumento27 páginasMANUAL DE NOMENCLATURA DE COMPUESTOS 2024 RevFebe Abigail Rosales VasquezAún no hay calificaciones
- Manual de Nomenclatura de CompuestosDocumento21 páginasManual de Nomenclatura de CompuestosBrandon CabreraAún no hay calificaciones
- CapXI ELECTROQUIMICADocumento37 páginasCapXI ELECTROQUIMICAMoira MirandaAún no hay calificaciones
- CAPITULO 5. NOMENCLATURA INORGANICA 2022 (Autoguardado)Documento33 páginasCAPITULO 5. NOMENCLATURA INORGANICA 2022 (Autoguardado)luis angel ruiz osorioAún no hay calificaciones
- Unidad 2 Nomenclatura InorganicaDocumento26 páginasUnidad 2 Nomenclatura InorganicaFernandoEstebanAún no hay calificaciones
- 1 Quimica Material Apoyo 11Documento10 páginas1 Quimica Material Apoyo 11Alvaro Gustavo Fernández AngaritaAún no hay calificaciones
- Taller - Estado de OxidaciónDocumento3 páginasTaller - Estado de OxidaciónIvan Villarreal100% (1)
- Capitulo - 7 - Nomenclatura InorgánicaDocumento26 páginasCapitulo - 7 - Nomenclatura InorgánicaNELLY LEON MAYTAAún no hay calificaciones
- S-8 Nomenclatura Química Inorgánica-ActivaDocumento100 páginasS-8 Nomenclatura Química Inorgánica-ActivaJMC YTAún no hay calificaciones
- Reacciones RedoxDocumento39 páginasReacciones RedoxALBIERI YAMEL GACIA FLORESAún no hay calificaciones
- Química Sem 14Documento16 páginasQuímica Sem 14Abeville SilexAún no hay calificaciones
- Clase Numero de OxidacíonDocumento15 páginasClase Numero de OxidacíonAdriana de Jesús Alas RivasAún no hay calificaciones
- Balanceo RedoxDocumento17 páginasBalanceo RedoxSantiago MacettoAún no hay calificaciones
- Tema 5. Nomenclatura Inorgánica-1Documento36 páginasTema 5. Nomenclatura Inorgánica-1michael mamaniAún no hay calificaciones
- Actividad Significativa Quinta Semana Primero de SecundariaDocumento9 páginasActividad Significativa Quinta Semana Primero de SecundariaKris KairaAún no hay calificaciones
- Formulación Inorgánica 4º ESODocumento11 páginasFormulación Inorgánica 4º ESOJorge RamonAún no hay calificaciones
- Cuaderno de Trabajo - Celdas GalvánicasDocumento30 páginasCuaderno de Trabajo - Celdas GalvánicasRenato Huaman QuispeAún no hay calificaciones
- CQ 3Documento17 páginasCQ 3nazarethAún no hay calificaciones
- Formulación 1 BachDocumento12 páginasFormulación 1 BachRAQUEL GONZALEZ CARRILLOAún no hay calificaciones
- Compuestos QuimicosDocumento36 páginasCompuestos QuimicosGabriel GuerreroAún no hay calificaciones
- Estado de OxDocumento2 páginasEstado de OxKennedy FloresAún no hay calificaciones
- 3 1 ApuntesDocumento13 páginas3 1 ApuntesMargarita RojasAún no hay calificaciones
- SEMANA 5 NOMENCLATURA INORGANICA 5TO PDF - 1Documento47 páginasSEMANA 5 NOMENCLATURA INORGANICA 5TO PDF - 1Anita BM100% (1)
- Guion de Clase Complementario Nomenclatura QuimicaDocumento44 páginasGuion de Clase Complementario Nomenclatura QuimicaBurgos LópezAún no hay calificaciones
- Manuel Cordero Control S3Documento5 páginasManuel Cordero Control S3Manuel Cordero HernandezAún no hay calificaciones
- Formulacion Inorganica Teoria2Documento8 páginasFormulacion Inorganica Teoria2Lisa María CatriniciAún no hay calificaciones
- Filemd9961-2023-09-09 13-42-02Documento31 páginasFilemd9961-2023-09-09 13-42-02erickelderestradaarenasAún no hay calificaciones
- NomenclaturaDocumento25 páginasNomenclaturaFriki StrskisAún no hay calificaciones
- Clase 12 Electroquimica PDFDocumento23 páginasClase 12 Electroquimica PDFAlvaro Guerra PeñaAún no hay calificaciones
- QuimcaDocumento28 páginasQuimcaAnonymous gSWfC8a50% (1)
- (211 - 214) Redox 1 - BiotecDocumento5 páginas(211 - 214) Redox 1 - Bioteccristian.rodriguez.f.a96Aún no hay calificaciones
- Nomenclatura QuímicaDocumento4 páginasNomenclatura QuímicaProfesor Luis pslAún no hay calificaciones
- Nomenclatura de Compuestos InorgánicosDocumento13 páginasNomenclatura de Compuestos InorgánicosMauricio AcostaAún no hay calificaciones
- Apuntes 2021Documento25 páginasApuntes 2021Jorge Manuel Fernández Arroyo PadillaAún no hay calificaciones
- Nomenclatura InorgánicaDocumento27 páginasNomenclatura Inorgánicajude100% (1)
- Quimica-Nomenclatura y Formulacion de Compuestos InorganicosDocumento21 páginasQuimica-Nomenclatura y Formulacion de Compuestos InorganicoszrimacmAún no hay calificaciones
- Nomenclatura y Formulación de Química Inorgánica - Iupac2005Documento63 páginasNomenclatura y Formulación de Química Inorgánica - Iupac2005D. AguiarAún no hay calificaciones
- 0 Nomenclatura InorganicaDocumento44 páginas0 Nomenclatura InorganicajhonthedummyAún no hay calificaciones
- Conceptos Previos de La Nomenclatura Inorganica para Quinto de SecundariaDocumento4 páginasConceptos Previos de La Nomenclatura Inorganica para Quinto de SecundariaJose luis Huaman gasparAún no hay calificaciones
- RedoxDocumento4 páginasRedoxCARLOS ANDRES CLAUSEN ALIAún no hay calificaciones
- Número de Oxidación. Reglas.Documento2 páginasNúmero de Oxidación. Reglas.veronica tapiaAún no hay calificaciones
- Tarea - Nomenclatura Química InorgánicaDocumento26 páginasTarea - Nomenclatura Química InorgánicaEULER ROSSEL CAMPOS SALDA�AAún no hay calificaciones
- Nomenclatura Inorganicos 1ROS MEDIO SEKDocumento48 páginasNomenclatura Inorganicos 1ROS MEDIO SEKignacia friasAún no hay calificaciones
- Guia 7 Quimica de NovenoDocumento4 páginasGuia 7 Quimica de NovenoArley TrianaAún no hay calificaciones
- Unidad 4 Formulación Química y NomenclaturaDocumento37 páginasUnidad 4 Formulación Química y NomenclaturaJUAN CAMILO POPAYAN ORTEGAAún no hay calificaciones
- Balanceo de Ecuaciones RedoxDocumento12 páginasBalanceo de Ecuaciones RedoxAngélica Tommaso AcevedoAún no hay calificaciones
- Introducción A Los Compuestos Químicos y Numero de OxidaciónDocumento4 páginasIntroducción A Los Compuestos Químicos y Numero de OxidaciónLuciana DomeAún no hay calificaciones
- Nomenclatura de Compuestos InorganicosDocumento21 páginasNomenclatura de Compuestos InorganicosMiguel André Salinas RevillaAún no hay calificaciones
- Nomenclatura InorganicaDocumento26 páginasNomenclatura InorganicaWilly Aranda CanalesAún no hay calificaciones
- Nomenclatura Inorgánica IDocumento16 páginasNomenclatura Inorgánica IAbueno tmecuidasAún no hay calificaciones
- En 1932 Surgió La Idea de Integrar y Estructurar Un Sistema de Enseñanza TécnicaDocumento3 páginasEn 1932 Surgió La Idea de Integrar y Estructurar Un Sistema de Enseñanza TécnicaSalma Irene Ríos Mota100% (1)
- Proyecto Algebra 1cm8Documento2 páginasProyecto Algebra 1cm8Salma Irene Ríos MotaAún no hay calificaciones
- Cal CuloDocumento17 páginasCal CuloSalma Irene Ríos MotaAún no hay calificaciones
- Tarea 3 - Equipo 5 - Calculo VectorialDocumento8 páginasTarea 3 - Equipo 5 - Calculo VectorialSalma Irene Ríos MotaAún no hay calificaciones
- Documento 1Documento4 páginasDocumento 1Salma Irene Ríos MotaAún no hay calificaciones
- Historia Del IpnDocumento3 páginasHistoria Del IpnSalma Irene Ríos MotaAún no hay calificaciones
- Ondas MecanicasDocumento18 páginasOndas MecanicasSalma Irene Ríos MotaAún no hay calificaciones
- En 1932 Surgió La Idea de Integrar y Estructurar Un Sistema de Enseñanza TécnicaDocumento3 páginasEn 1932 Surgió La Idea de Integrar y Estructurar Un Sistema de Enseñanza TécnicaSalma Irene Ríos MotaAún no hay calificaciones
- Acontecimientos IPN 1979Documento2 páginasAcontecimientos IPN 1979Salma Irene Ríos MotaAún no hay calificaciones
- Historia de La PlanchaDocumento5 páginasHistoria de La PlanchaSalma Irene Ríos MotaAún no hay calificaciones
- PUNTOSDocumento10 páginasPUNTOSSalma Irene Ríos MotaAún no hay calificaciones
- Mapa ConceptualDocumento1 páginaMapa ConceptualSalma Irene Ríos MotaAún no hay calificaciones
- Precursores de Las Ecuaciones DiferencialesDocumento1 páginaPrecursores de Las Ecuaciones DiferencialesSalma Irene Ríos Mota100% (1)
- Valores Capacitores Poliester Ceramicos 00270bcb7cDocumento3 páginasValores Capacitores Poliester Ceramicos 00270bcb7cSalma Irene Ríos MotaAún no hay calificaciones
- Cuestionario Equipo 01Documento2 páginasCuestionario Equipo 01Salma Irene Ríos MotaAún no hay calificaciones
- Lista 2 OMDocumento7 páginasLista 2 OMSalma Irene Ríos MotaAún no hay calificaciones