Documentos de Académico
Documentos de Profesional
Documentos de Cultura
S14.s2 - EJERCICIOS DE PRIMERA LEY DE TERMODINAMICA
Cargado por
Andre Huayta RivasTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
S14.s2 - EJERCICIOS DE PRIMERA LEY DE TERMODINAMICA
Cargado por
Andre Huayta RivasCopyright:
Formatos disponibles
EJERCICIOS DE PRIMERA LEY DE TERMODINAMICA
1.-Si se adicionan 400 kcal a un gas que se expande y realiza 800 kJ de trabajo, ¿Cuál es la
variación de la energía interna del gas?
2.- Una bala de plomo inicialmente a 30°C se funde al golpear un blanco. Suponiendo que toda la
energía cinética inicial de la bala se convierte en energía interna de la misma para elevar su
temperatura y fundirla, calcular su velocidad en el momento del impacto.
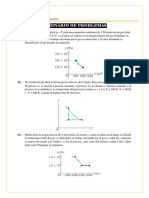
3.- Una cantidad de aire se lleva del estado a al b siguiendo una
trayectoria recta en una gráfica pV. Si Va = 0,0700 m3, Vb = 0,1100 m3,
pa = 1,00 x l05 Pa y pb = 1,40 x l05 Pa, ¿cuánto trabajo efectúa el gas en
este proceso. Suponga que el gas tiene comportamiento ideal.
4.- Un gas ideal inicialmente a Pi, Vi y Ti se lleva a través de un ciclo,
como se muestra en la figura
a) Encuentre el trabajo neto consumido en el gas por cada ciclo.
b) ¿Cuál es la energía neta agregada por calor al sistema por cada ciclo?
c) Obtenga un valor numérico para el trabajo neto consumido por cada ciclo
por 1 mol de gas inicialmente a 0°C.
5.- A un sistema formado por un gas encerrado en un cilindro con émbolo, se le suministran 200
calorías y realiza u trabajo de 300J. ¿Cuál es la variación de la energía interna del sistema expresado
en J?
6.-Determine el cambio de energia interna de un sistema que:
a) absorbe 500 cal de energía térmica mientras efectúa 800J de trabajo externo.
b) absorbe 500 cal de energía térmica mientras 500 J de trabajo externo se efectúan sobre el sistema.
c) se mantiene a un volumen constante mientras se extraen 1 000 cal del sistema.
7.-Un mol de gas ideal realiza 3000J de trabajo sobre su entorno cuando expande a temperatura
constante. Presión final 1 atmosfera y volumen final 25 litros. Determine Q, V o y T.
8.-Un mol de gas ideal se mantiene a 0º C durante una expansión desde 2 hasta 8 litros. ¿Cuánto
trabajo es realizado sobre el gas?
También podría gustarte
- Ejercicios Primera Ley de La TermodinámicaDocumento3 páginasEjercicios Primera Ley de La Termodinámicaemmanuel gonzalezAún no hay calificaciones
- TALLERDocumento2 páginasTALLERYohan Sebastian Medina RamirezAún no hay calificaciones
- B TermodinamicaDocumento2 páginasB TermodinamicaOscar OcsaAún no hay calificaciones
- Taller de Termodinámica 2Documento9 páginasTaller de Termodinámica 2LiyibethAún no hay calificaciones
- 21 EcuascionesDocumento4 páginas21 EcuascionesCarlos Herrera Delgado0% (1)
- Seminario 1 Ley TermodinámicaDocumento2 páginasSeminario 1 Ley TermodinámicaDiego MillaAún no hay calificaciones
- Taller 1. Primera Ley de La TermodinámicaDocumento3 páginasTaller 1. Primera Ley de La TermodinámicaDiego Armando Villamil ToscanoAún no hay calificaciones
- Practica 5. TermodinamicaDocumento3 páginasPractica 5. TermodinamicaMichael Morales AriasAún no hay calificaciones
- Trabajo de Fisica TermodinamicaDocumento3 páginasTrabajo de Fisica TermodinamicaLuis Alberto Acosta SanchezAún no hay calificaciones
- Ilide - Info Problemas Semana 14 Sesion 1 Primera Ley de Termodinamica PRDocumento2 páginasIlide - Info Problemas Semana 14 Sesion 1 Primera Ley de Termodinamica PRAkkiAún no hay calificaciones
- Práctica 06Documento3 páginasPráctica 06TadeoAún no hay calificaciones
- Problemas Semana 14 Sesión 1 (Primera Ley de Termodinámica)Documento2 páginasProblemas Semana 14 Sesión 1 (Primera Ley de Termodinámica)madabi100% (2)
- EJERCICIOSDocumento13 páginasEJERCICIOSAbrahamAún no hay calificaciones
- Ejercicios Recomendados-Termodinamica 1leyDocumento3 páginasEjercicios Recomendados-Termodinamica 1leyLily Margareth ArrietaAún no hay calificaciones
- Actividad de Aprendizaje - N°07Documento4 páginasActividad de Aprendizaje - N°07JadeAún no hay calificaciones
- T - Sem 10 - Ses 10 - MicroTaller 05 - 1era Ley TDDocumento1 páginaT - Sem 10 - Ses 10 - MicroTaller 05 - 1era Ley TDsantiagoAún no hay calificaciones
- Ahoduar - Ejercicio Primera Ley - para CombinarDocumento2 páginasAhoduar - Ejercicio Primera Ley - para CombinarFrancy Valentina Porras GalvisAún no hay calificaciones
- S Sem14 Ses2 PPRIMERA LEYDocumento2 páginasS Sem14 Ses2 PPRIMERA LEYBrandon TamaraAún no hay calificaciones
- Taller Numero 3Documento4 páginasTaller Numero 3Daniel DBAún no hay calificaciones
- EJERCICIOS 9 (Termodinamica)Documento3 páginasEJERCICIOS 9 (Termodinamica)Jenny UlloaAún no hay calificaciones
- S15-FG - Chinchay Garcia Eduin Omar.Documento8 páginasS15-FG - Chinchay Garcia Eduin Omar.Ch G Omąr100% (1)
- Taller Primera LeyDocumento4 páginasTaller Primera LeyScribdLibros11Aún no hay calificaciones
- 6 F 72386 D 1606 FD 529 Eb 2Documento2 páginas6 F 72386 D 1606 FD 529 Eb 2api-241491651Aún no hay calificaciones
- A15 FG - Ejercicios Procesos TermodinámicosDocumento3 páginasA15 FG - Ejercicios Procesos TermodinámicosPIERO MIGUEL VILLARAN PABLOAún no hay calificaciones
- Taller Primera LeyDocumento2 páginasTaller Primera LeyFernando Pazos MoralesAún no hay calificaciones
- Practica Dirigida Nº16 Termodinamica-Aplicaciones-uniDocumento4 páginasPractica Dirigida Nº16 Termodinamica-Aplicaciones-uniROGER SALVADOR LOAYZA SEGURAAún no hay calificaciones
- Ejercitario 4.4Documento3 páginasEjercitario 4.4Jorge TrinidadAún no hay calificaciones
- Hoja de Problemas #04Documento4 páginasHoja de Problemas #04Paul Quiroz AliagaAún no hay calificaciones
- Tarea #5Documento4 páginasTarea #5Joel Vidal Caldas OsorioAún no hay calificaciones
- Tarea - Practica Primera Ley TermodinamicaDocumento4 páginasTarea - Practica Primera Ley TermodinamicaLUIS DELGADO FLORESAún no hay calificaciones
- SEP 6-7 - 1 y 2 LT 12559Documento13 páginasSEP 6-7 - 1 y 2 LT 12559Roberto RicraAún no hay calificaciones
- Problemas Propuestos Primera LeyDocumento3 páginasProblemas Propuestos Primera LeyJunior PeñaAún no hay calificaciones
- Bol P3Documento5 páginasBol P3miguel miguez cotoAún no hay calificaciones
- Problemas Propuestos IIDocumento3 páginasProblemas Propuestos IILucas RojasAún no hay calificaciones
- Primera Ley de TermodinamicaDocumento3 páginasPrimera Ley de TermodinamicaCristian Andres Vargas GuerreroAún no hay calificaciones
- Serie de Problemas #1 Termodinamica IIDocumento4 páginasSerie de Problemas #1 Termodinamica IIFrank C. Flores100% (1)
- T Sem 09 Ses 10 MicroTaller 05Documento1 páginaT Sem 09 Ses 10 MicroTaller 05juancitoAún no hay calificaciones
- Guía5 Ejerc Termodinamica 4os DifDocumento4 páginasGuía5 Ejerc Termodinamica 4os DifalxcalixAún no hay calificaciones
- Ley TermodinamicaDocumento6 páginasLey TermodinamicaEdgard RodríguezAún no hay calificaciones
- Guia 19Documento4 páginasGuia 19Jikai ZenAún no hay calificaciones
- Ejercicios de TermodinamicaDocumento1 páginaEjercicios de TermodinamicaSamuel LaraAún no hay calificaciones
- Incremento de CalorDocumento6 páginasIncremento de CalorEmily TumamaentangasAún no hay calificaciones
- Problemas de Ciclos Termodinamicos - 1 - 1 - 2 - PDFDocumento2 páginasProblemas de Ciclos Termodinamicos - 1 - 1 - 2 - PDFRosario Gutierrez CelisAún no hay calificaciones
- ICI PI S2 Prueba v2Documento1 páginaICI PI S2 Prueba v2katherine Melo100% (1)
- Taller 5 Termodinámica - 2022Documento3 páginasTaller 5 Termodinámica - 2022William QuinchiaAún no hay calificaciones
- Tarea TermodinamicaDocumento4 páginasTarea TermodinamicaMichelle CervantesAún no hay calificaciones
- Guia 4Documento3 páginasGuia 4Diego Mamani0% (3)
- Fisica PracticaDocumento1 páginaFisica PracticaFiorella YarlequeAún no hay calificaciones
- Taller 5 Termodinámica - 2021Documento3 páginasTaller 5 Termodinámica - 2021Vanessa PortillaAún no hay calificaciones
- Capitulo 01-TermodinámicaDocumento7 páginasCapitulo 01-TermodinámicaTomas DamenoAún no hay calificaciones
- 1practica 06 FísicaDocumento1 página1practica 06 FísicaHUBERT SAUL ATO RENTERIAAún no hay calificaciones
- Guia 19 PDFDocumento4 páginasGuia 19 PDFCaroll IsabelAún no hay calificaciones
- Segunda Serie de TermodinámicaDocumento3 páginasSegunda Serie de TermodinámicaMiguel ReyesAún no hay calificaciones
- Preguntas 1 48Documento1 páginaPreguntas 1 48ShimonakiAún no hay calificaciones
- 1T Primera Ley de La TermodinamicaDocumento2 páginas1T Primera Ley de La TermodinamicaFernando MayorgaAún no hay calificaciones
- Taller 5Documento9 páginasTaller 5William Quinchia100% (1)
- Deber 6Documento4 páginasDeber 6jhonAún no hay calificaciones
- Pregunta 1 G.HDocumento1 páginaPregunta 1 G.HAndre Huayta RivasAún no hay calificaciones
- Caso de Estudio Hard Rock CafeDocumento4 páginasCaso de Estudio Hard Rock CafeAndre Huayta RivasAún no hay calificaciones
- Pregunta 3 G.HDocumento1 páginaPregunta 3 G.HAndre Huayta RivasAún no hay calificaciones
- S14.s1 - MaterialDocumento23 páginasS14.s1 - MaterialAndre Huayta RivasAún no hay calificaciones
- S04.s1 - MaterialDocumento27 páginasS04.s1 - MaterialAndre Huayta RivasAún no hay calificaciones
- S05 S1-EjerciciosDocumento2 páginasS05 S1-EjerciciosAndre Huayta RivasAún no hay calificaciones
- S03 S1-MaterialDocumento15 páginasS03 S1-MaterialAndre Huayta RivasAún no hay calificaciones
- S15.s1 - SEGUNDA - LEYDocumento28 páginasS15.s1 - SEGUNDA - LEYAndre Huayta RivasAún no hay calificaciones