Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Termodin Ímica
Termodin Ímica
Cargado por
mariaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Termodin Ímica
Termodin Ímica
Cargado por
mariaCopyright:
Formatos disponibles
Termodinámica.
Un proceso fisiológico sólo puede llevarse a cabo sino incumple los principios termodinámicos
elementales. La magnitud termodinámica que gobierna la transferencia de sustancias a través
de una membrana se denomina potencial electroquímico del soluto, el cual se define como la
variación de energía libre que ocurre cuando se transporta un mol de soluto a través de una
membrana:
Si Au es negativo, el transporte es exergónico, y no requiere aporte de energía externa para
llevarse a cabo; si Au es positivo, el transporte es endergónico, y requiere un aporte externo
de energía
. Es decir, se requiere un proceso exergónico que suministre la energía necesaria y un
mecanismo de acoplamiento que transfiera la energía desde el proceso exergónico al
transporte endergónico.
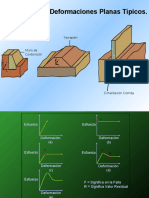
Muestra un ejemplo de difusión pasiva simple, donde el soluto es suficientemente soluble en
la membrana como para atravesarla sin problemas de forma espontánea , en este transporte
la velocidad de entrada o salida del soluto es proporcional a la diferencia de potencial
electroquímico del sustrato. Sin embargo, podemos ver que esta recta cambia para el
transporte activo, centrándonos en simporte, ya que este requiere un transporte endergónico
acoplado al transporte exergónico de otro soluto.
Para especies que experimentan simporte, los flujos continuos en condiciones de no equilibrio
están relacionados con las fuerzas mediante las siguientes ecuaciones:
Donde de las fuerzas impulsoras serían:
Para el flujo del soluto sin carga
Para el transporte exergónico del ión que permite el
acoplamiento del transporte endergónico.
Los coeficientes fenomenológicos directos son Ls,s y Lion,ion. Ls,s representa el acoplamiento
de las fuerzas del sustrato a su flujo y el coeficiente Lion,ion representa el acoplamiento de las
fuerzas del ión a su flujo. Por otra parte, los coeficientes fenomenológicos cruzados serían
Ls,ion y Lion,s. Ls,ion representa como el flujo de s se relaciona con la fuerza del ion y Lion, s
relaciona el flujo del ion acoplado a las fuerzas de s.
A continuación, debemos tener en cuenta las relaciones de Onsanger que expresan que los
coeficientes fenomenológicos cruzados son simétricos, de forma que:
Y, por otra parte, el Coeficiente de acoplamiento, que representa el número de moles de iones
que son transportados por mol de sustrato, viene dado por:
En células que acumulan sustrato en su interior como resultado de la condición experimental
impuesta de que hay un flujo descendente del ión de fuera hacia adentro:
Dentaríamos que el valor absoluto del término que representa como el
flujo de S se acoplan con la fuerzas motrices del ión, debe ser mayor que el término
representado por el coeficiente directo del sustrato.
En base a ello, se puede deducir que el gradiente de concentración de ión que es transportado
de forma exergónica permite al acoplamiento de otro transporte endergónico.
Ejemplos de simporte:
En cuanto a la concentración de algunos iones en el líquido intracelular y extracelular podemos
encontrar algunas diferencias. En el interior celular hay mayor concentración de K, mientras
que en el exterior hay mayor concentración de Na, Cl y Ca. Es por ello que en condiciones
normales, el K tenderá a salir de la célula y el Na, Ca y Cl tenderán a entrar, por lo que estos
cuatro iones son los que con mayor frecuencia intervienen en los mecanismos de simporte,
permitiendo que un trasnporte endergónico se acople con su transporte exergónico.
-Simporte de glucosa y sodio en el intestino
-Simporte de sodio y yodo en las células tiroideas
-Simporte sodio-potasio-2cloro en el asa de Henle de la nefrona del riñón
-Simporte de sodio y aminoácidos
Escriba aquí laecuación .►
También podría gustarte
- 2 G - Afeo-03 PDFDocumento68 páginas2 G - Afeo-03 PDFDiego Evaristo0% (1)
- APLICACIONES DE LOS ANTIBI+ôTICOSDocumento9 páginasAPLICACIONES DE LOS ANTIBI+ôTICOSmariaAún no hay calificaciones
- EjerciciosTema14 - Pavón Carrasco MaríaDocumento4 páginasEjerciciosTema14 - Pavón Carrasco MaríamariaAún no hay calificaciones
- Articulo NatureDocumento1 páginaArticulo NaturemariaAún no hay calificaciones
- Tema 9 Resumen Función HepáticaDocumento11 páginasTema 9 Resumen Función HepáticamariaAún no hay calificaciones
- Práctica 1 Recogida de GasesDocumento6 páginasPráctica 1 Recogida de GasesmariaAún no hay calificaciones
- ELECTROIMDocumento8 páginasELECTROIMYim ACAún no hay calificaciones
- Analisis de Fallas y Control de Protecciones Como Prevencion de Riesgos ElectricosDocumento131 páginasAnalisis de Fallas y Control de Protecciones Como Prevencion de Riesgos ElectricosItalo Leiva100% (1)
- Informe Leyes de KirchhoffDocumento8 páginasInforme Leyes de KirchhoffYovany Alexander Albino Cote0% (1)
- TD SILENT (S&P) Helicocentrifugos.Documento12 páginasTD SILENT (S&P) Helicocentrifugos.jodsanchezsaAún no hay calificaciones
- Ley de ArquímedesDocumento7 páginasLey de ArquímedessaasassAún no hay calificaciones
- Informe Maquina de Induccion Faltan Curvas y ConclusionesDocumento17 páginasInforme Maquina de Induccion Faltan Curvas y ConclusionesJhoanelis Marcano SAún no hay calificaciones
- PC7 GraficasDocumento2 páginasPC7 Graficascharlton28290615Aún no hay calificaciones
- Recursostic - Educacion.es Secundaria Edad 3esofisicaquimica Impresos Quincena12Documento25 páginasRecursostic - Educacion.es Secundaria Edad 3esofisicaquimica Impresos Quincena12Sheylla Arias PinedaAún no hay calificaciones
- ColisionesDocumento2 páginasColisionesDANIEL FELIPE CAPERA LEONAún no hay calificaciones
- Taller 1. La Carga Electrica y La Ley de CoulombDocumento3 páginasTaller 1. La Carga Electrica y La Ley de CoulombInterventorias y Construcciones Ltda INCON LTDA100% (1)
- FORMULARIO de Turbinas Francis y KaplanDocumento6 páginasFORMULARIO de Turbinas Francis y KaplanGustavo Quispe LimachiAún no hay calificaciones
- Guía de Momento de Inercia TDocumento5 páginasGuía de Momento de Inercia TJOSE LUIS TICONA OCORURO0% (1)
- Tarea 1-Cristian OrtegaDocumento4 páginasTarea 1-Cristian OrtegaJesús Ángel Garcia GonzalezAún no hay calificaciones
- Flexion BiaxialDocumento8 páginasFlexion BiaxialJuan Diego Valdivia Heredia100% (1)
- Introducción Ensayo 3Documento10 páginasIntroducción Ensayo 3José Ramón Cisneros de LeónAún no hay calificaciones
- Reduccion de FuerzasDocumento19 páginasReduccion de FuerzassmithAún no hay calificaciones
- Sistema de UnidadesDocumento11 páginasSistema de UnidadesSantiago RodriguezAún no hay calificaciones
- 2 Taller-Fisica 2Documento1 página2 Taller-Fisica 2Wilson MarcilloAún no hay calificaciones
- ENERGIADocumento7 páginasENERGIAKaren SalazarAún no hay calificaciones
- Seminario Estructura TPDocumento2 páginasSeminario Estructura TPGuillermo PujanteAún no hay calificaciones
- Conductividad TermicaDocumento11 páginasConductividad TermicaJho CarrascoAún no hay calificaciones
- 2.1 - Comportamiento Termico de Los Polímeros - 2020Documento57 páginas2.1 - Comportamiento Termico de Los Polímeros - 2020Mayte Olenka Miranda BandaAún no hay calificaciones
- Informe V Fuerzas de Friccion en Fluidos PDFDocumento24 páginasInforme V Fuerzas de Friccion en Fluidos PDFAldo Benjamin Becerra Gaytan100% (1)
- MicrocanicoDocumento6 páginasMicrocanicoElisa RaúlAún no hay calificaciones
- Esfuerzo de Una Masa de SuelosDocumento45 páginasEsfuerzo de Una Masa de SuelosCesar CortezAún no hay calificaciones
- Respuesta Actividad 4Documento4 páginasRespuesta Actividad 4Arnoldo Mondragon ValenciaAún no hay calificaciones
- Guia-Esfuerzo DeformacionDocumento5 páginasGuia-Esfuerzo DeformacionCristian Niviayo MedinaAún no hay calificaciones
- Conversion EsDocumento8 páginasConversion EsSERGIO ANDRES GONZALEZ MINDIOLAAún no hay calificaciones
- Bertha Dioselina Begazo PalominoDocumento4 páginasBertha Dioselina Begazo PalominoAna Luz MamaniAún no hay calificaciones