Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Enlaces Quimicos
Cargado por
gaby-010 calificaciones0% encontró este documento útil (0 votos)
26 vistas28 páginasquimica CBC UBA
Título original
enlaces_quimicos
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoquimica CBC UBA
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
26 vistas28 páginasEnlaces Quimicos
Cargado por
gaby-01quimica CBC UBA
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF o lea en línea desde Scribd
Está en la página 1de 28
A ENLACES QUiMICOS
1. INTRODUCCION
Los electrones de valencia
La naturaleza de los enlaces quimicos
2, CONCEPCION DE LOS ENLACES QUIMICOS Y SIMBOLOS DE LEWIS
3. EL ENLACE IONICO
4. EL ENLACE COVALENTE
Polaridad de los enlaces
Carécter iénico parcial
5. EL ENLACE METALICO
6. ESTRUCTURAS DE LEWIS DE SUSTANCIAS MOLECULARES Y SUSTANCIAS IONICAS
Sustancias moleculares
Las estructuras de Lewis y Ia regla de! acteto
ones y compuestos iénicos
Resonancia
Enlaces Quimicos
13
4. INTRODUCCION
En esto capitulo estuciaremos fa
rneturaleza de fas unions quimi:
‘cas, a través de los distintos on.
laces que se pueden establecer
contre las partioulas que se unen.
cap. 4
14
En el mundo que nos rodea estamos en cortacto con infinidad de sustancias que se encucn~
tran en distintos estados de agregacién, Sabemos que estas sustancias estin formadas por molé-
clas 0 bien por reticulos cristalinos. Asi, tenemos susiancias moleculares cuyas moléculas
estén formadas por dtomos del mismo elemento como Hz, Ny, Cly, 0 de elementos distintos
como HO, COs, NHy, También hay sélidas como el diamante, la sal de mesa (NaC?) 0 los
-metales, que son agregados de numerosos étomos o iones. La existencia de todas estas susta
cias nos lleva @ suponer que de alguna manera los atomos de los diversos elementos se unen
cent si para formar sustancias diferentes,
Las primeras ideas acerca de la formacién de los enlaces quimicos fueron aportadas por
Berzelius hacia 1812, Segin su teoria, los dtortos de los distintos elementos poseian polos eléc~
tricos predominantemente positivos 0 negativos, La union se establecia entre [os tomos con
polos de signo contrario, Sin embargo, esta teorix no podia explicar la existencia de moléculas
formadas por Stomos del mismno elemento, como Hy, Np 0 Cly, y@ que sus toms tendrian
polos" del mismo signo y no se atracrian,
Una de las claves que permitié establecer la naturaleza de los enlaces quimieos con mayor
precision, fue el estudio del comportamiento de los gases nobles. Los gases nobles presentan
fescasa reactividad quimica, a tal punto que sus moléculas son todas monoatomicas; esta “inac-
tividad" quimiea de los gases nobles se arrihuye a que sus dtomos tienen su nivel mas externo
‘completo con 8 eleetrones cada uno (2 electranes en el caso del helio)
‘Actualmente, el modelo orbital sugiere para estos étomos una C.E.E. nsnp®, donde n es el
nimero cudntico principal del nivel mas extemo (1s? para cl helio). En virtud de esta caracte-
ristica de Ia estructura electronica mas externa, Kossel y Lewis sugirieron en 1916 que en una
‘gran vatiedad de compuestos quimicos los itomos de muchos elementos (en particular los
representativos de los periodos | y 2 de la Tabla Periésdica) se hallan combinados de modo tal
‘que sus estructuras electtOnicas mis externas tienen 8 electrones, salvo el hidrSgeno que adop-
‘a la configuracién del helio con solo 2 electrones.
Lewis llamé a esta caracteristica “Ia regla de ocho” y Langmuir -quien en 1919 hizo apor:
taciones may importantes a la concepcisn de enlace quimico de Lewis- la denomind “regla del
‘cteto”, tal como se la conoce hoy.
“Lewis postulé que estos electrones, sea que participen en enlaces quimicos 0 no, estén orga
nizados de a pares, Ilamando a esta earacteristica la “regla de dos”, Se conocen muy pocas
excepciones a esta regla, salvo, naturalmente, en compuestos cuyas particulas constituyentes
tienen nimero impar de electrones, y las hay muchisimas a la regla del octeto (en particular,
‘cuando estin presentes elementos de los periods 3 y mayores de la Tabla Periédica). En le
actualidad los cientificos utilizan modelos pera comprender el enlazamiento quimico basados
cen a Mecanica Cusintica, en especial cvandl se requiere informacion cuantitativa, Para estudios
‘cuslitativos suele ser suficiente un tratamiento mas simple y deseriptivo como el aportado pot
Kossel, Lewis y Langmuir y que describiremos en este capitulo, imitando nuestras considera
cones 2 los elementos representativos.
Capitulo 5
Los electrones de valencia
Hemos deserito que los étomos de los elementos de un mismo Grupo de la Tabla Peviéai
‘a excepcidn del helio, tienen jgual nimero de electrones en su nivel mas externa. Dado que las
propiedades quimicas de los clementos de un Grupo son similares, pademos infer que hay une
relacidn entre las propiedades quimicas y el nimero de electrones mas extemnos. Slo esos elec-
‘tones parecen intervenir en Ia formacién de los enlaces quimicos y se Ios suele denominar elec-
trones de valencia. En los elementos representativos los electeones de valene'a son los que
constituyen la configuracién electrénica externa (C.E.E.)
En la Tabla 5.1 sc muestra Ia expresion general de la C.E.E. y ol miimero de electrones de
valencia, pare los Grupos que comprenden a los elementos representativos. Como podemos
observar, los atomos de los elementos de un mismo Grupo tienen igual mimero de electrones en
su nivel mas extemo, que ademas coincide con el ihimo digito del Grupo.
Grupo 1 2 | 3
CEE ns! ns? | ns*np!
| Plectrones de valencia | 1 2 3
Tabla 6.1: ExprosiOn general de la CEE y del auimero de electrones de valencia de los elemen-
‘os representativos, donide n es e/ admero cusintico principal dol nivel mas extemo.
La naturaleza de los enlaces quimicos
La formacién de una unién quimica implica un reordenamiento de los electrenes de valen-
cia de los étomos que se unen, para dar lugar a una estructura de menor energia y por lo tanto
inds estable. Esto significa que en el proceso de unién entre dos atomos se liber cierta cant
dad de energia (energia de enlace). Por ejemplo, cuando dos dtomos A y B cuyas energias son
E; y By, se unen para formar una sustanicia AB, la energia final Ep es menor que la de los éto-
os inviduales
En las uniones quimicas existe fueras de naturtezaelectrostitca, debidas ainteracciones ®
entre particulas cargadas. Como sabemos, las fuerzas pueden ser de repulsién (cergas de igual Ey
Signo) o de atraceib(cargas de sign opuesto). =
El enlazamiento quimico es, en buena medida, de naturaleza eleetrostitica. Los “cores” de
‘ambos dtomos que participan en el enlace, a una cierta distancia entre si, pudlen atracrse tanto
con sus propios electtones de valereia como con los eletroncs de valencia del co tomo. Y ce)
Soke oh dune paso ibe cero eles GS
#1 predominio dela infracein atractiva oeurset hasta que ambas entidades 2tén Io sui- E
cicntemente cerca como para que opeten fuerzas electrostaticas de repulsién entre los “cores” racion del eniace
(ambos con carga positiva) y/o entre los electrones (todos con carga negativa). La distancia orien det eniees 42:
Enlaces Quimicos
Gilbert Newton Lewis
Nacié el 23 de octubre de 1875
(Weymouth, EEUU). Transcurié fa
‘mayor parte de su vila siendo
profesor de Fisicoquimica en fa
Universidad de California en
Berkeley Murié en su laboratoro,
23 de marzo de 1946.
‘Se destacé par ous teoriae acerca
de las unions quimicas y también
por sus aportes a la toorla del
‘comgortamionto de los &cidos y
de las bases.
“core-core” donde la energia es minima se denomina fongitud de enlace y la energia que
. La con
figuracién de gas noble en los elementos de estos tres grupos puede ser aleanzada compartien-
do elecirones con otros dtomos.
En principio, hay dos maneras por las cuales un tomo puede adquirir la configuracién elec-
trénica de gas noble:
+ Cuando se comparten electrones entre dos tomes,
+ Cuando un tomo transfiere electrones a otro.
Estas ideas condujeron @ los cientificos 9 establecer una afitmacién conocida como regla
del octeto,
Los atomos de los elementos tienden a unirse entre si compartiondo o transfiriendo
olectrones, de manera que su nivel més externo se complete con ocho electrones
sta regla indica que cuando los ftomos se unen, tienden @ transferir © compartir el mime
ro necesario de clectrones para tener ocho en su capa més extema, Si bien Ia validez de esta
‘egla no es universal, pues como veremos existen excepciones, constituye una buena aproxima-
cién para una explicacién elemental de como se establecen las uniones quimica.
Capitulo 5
Las explicaciones anteriores -hasadas en Ia concepei6n de Lewis del enlace quitico- no
bastan para explicar todas las formas en que los dtomos de todos los elementos de la Tabla
Periddica se combinan quimicamente, pero constituyen una buena aproximacién para una des-
cripeién elemental del enlace quimico. Como representaciones sinabélicas se dibujan la llama-
das estnicturas de Lewis, a partir de los simbolos de Lewis ya descritos.
Para ordenar su catacterizacién, es habitual clasificar a los enlaces quimivos, por ejemplo,
segin la diferencia de tas clectronegatividades entre los étomos enlazads y asi eran descritos
cen las seeciones siguientes para los elementos representativos:
+ Enlace iénico, cuando dicha diferencia es grande ({ipicamente involuera a no metales de
clectronegatividad alta y a metales)
+ Bnlace covalente, cuando dicha diferencia es pequefa o nul ¢ involuera a no metales
+ Enlace metilico, cuando dicha diferencia es pequetia o nula ¢ involuera a metales
Dacio que las diferencias de eleetronegatividades abarcan un rango continuo de valores, tam
bién hay un rango continuo de enlaces que van desde el predominantemente iénico hasta el
covalente no polarizado o el metilico. Los casos intermedios consisten en enlaces polarizados,
A excepcin de casos extremes, no hay limites provisos para predecir cuando un enlace tend
ccaracteristicas de un tipo determinado debido a que esta clasificacidn, como cualquier otra, es
necesariamente arbitraria. Sin perjuicio de esto, daremos ejemplos que preserten la menor
ambigitedad posible,
3. EL ENLACE IONICO
Como hemos descrito, los slidos iénicos estén formados por redes cristalinas que contienen
ioncs de signo opuesto, Por ejemplo, el cloruro de sodio es un reticulo cristalino constituide por
‘gual mimero de iones Na* y de iones CI, ya que el sistema debe ser elgctricamente neutro.
‘Si escribimos las respectivas configuraciones electrGnicas, destaeando en negrita las CEE,
memos:
Na: 1s22s?2p63st Ck: 1522s22p63s23ps
1oNe: 1522526 aeAt: 18?2322p63923p6
E] tomo de sodio tiene un solo electrén en su nivel més extemo (351), y si se le entrega la
energia de ionizacién necesaria, puede transformarse en el catién sodio, cuya configuracién
clectrOnica es igual a la del neén. Es decir, el Na* y el Ne son isoelectrdnicos
£1 dtomo de cloo, que tiene sete electrones extemos,tende a capar un eles para edquii fa cone
Figuracién del aryén, convirtizndoseenel anién Cr, que esiselectonico con el arzén. Sin stom de socio
‘2 acerca suficientemente a uno de cloro, puede transerine su clostrén mis extemo, formendose simi
‘neamente ls iones Nar y Cr’. Este hecho podemos visualizario mediante el siguiente diagrama de caja:
Cop.2
Enlaces Quimicos
139
nNa Is
.E
ul Is
CE.
Reticulo cristatino
dol NaC
ENLACE IONICO
160
an as N 2p | tL | te | th | 38 v
se 2s 2p8 3s!
N | as | ty | ap | te] te n| as | Nap | Tet
Is 28° 2p? 3s" 3p
‘Ambos itomos adquieren simulténeamente una estructura estable, originando los tones Nat
con diez electrones y CT’ con 18, que tienen ¢ mismo niimero de electrones que los atomos de
los gases nobles Ne y Ar, respectivamente. El proceso de atraccién entre ambos iones podemos
representarlo segiin:
El catign Nay el anién CI se mantienen unidos por un enlace idnico. Notemos que el par
Na* CY se simbolizd con una estructura de Lewis: ala izquierda se escribié el simbolo de Lewis
del catién sodio, ¢] cual es el simbolo quimmico del elemento y su carga y ningn punto o cruz,
ya que dicho catidn no tiene electrones dle valencia, y el simbolo de Lewis del anién eloruro,
‘donde se explicitan sus 8 electzones de valenca y a la que se encierra entre corchetes y se escri~
bre la carga por fuera de ellos como superindie derecho, dado que los electrones son indi
‘guibles y la carga pertenece al eloruro y no esté adsoripta a un electr6n individual.
En la representacién anterior se considers, por simplicidad, a un cation sodio atrayéndose
ccon un solo anién cloruro, pero debemos aclarar que el catién atraert a tantos aniones como
pueda, y lo mismo el anién, respecto de los cationes. En particular, en un cristal de cloruro de
Sodio, cada catidn sodio se rodea de 6 aniones cloruro y cada anién cloruro se rodea de 6 catio-
nes Sodio. El nimero de iones de carga opuesia alrededor de cada ion del cristal depende, entre
‘otros factores, de Ia carga de cada ion y de sus tamaiios relatives.
Es el que se produce entre lones con carga opuesta
‘eamos el ejemplo del fuoruro de calcio, cuya formula empirica es CaF. La CEE del eal-
cio es 4s? y la de thor es 2s?2p5. Es decir, el étomo de ealeio pose dos eleetrones externos
mientras que el de Mor posee site, Esto ms indica que para adquiri Ia configuracion de!
‘tomo del gas noble argon, el dtomo de caleio debe ceder sus dos electrones extemos. Por st
parte, cada itomo de flior necesita captar un electton, para Iograr la configuraci6n del tomo
el gas noble ned. Se producen dos enlaces idnicos que podentos representa
Capitulo 5
De esta manera, se forma una unidad de CaF, el ion C
nen unides por fuerzas de atraccién electrostaticas,
y los dos iones F, se mi
Fl enlace idnico se producird entre cationes de elementos de baja energia ce ionizacién y
aniones de elementos que sean muy electronegativos. En efecto, la mayoria de los compues-
{os ténicos binarios estin formados por la combinacién de elementos de los grupos 1 y 2
(metales) con los de los grupos 16 y 17 (no metales).
4. EL ENLACE COVALENTE
Existen muchas moléculas formadas por atomos cuyos valores de electronegatividad son
similares (0 iguales, como en las moléeulas de las sustancias simples Hy, F, ob). Las prime-
"as ideas para explicar cémo se unen estos itomos fueron aportadas por G. N. Lewis, quien pro-
puso lo siguiente:
Cuando los dtamas se unen, pueden aleanzar wna configuracion de gar nobie compurtien-
ddo entre si pares de electrones,
El enlace covalente es la unién que se produce entre dos étomas cuando comparten
uno 0 més pares de electrones de valencia
El enlace covalente generalmente se presenta entre dtomos de elementos de alta y similar
¢lectronegatividad, como los elementos no metilicos.
‘Mediante diagramas de puntos, Lewis representé la estructura de muchas mcléculas senci
las unidas por enlaces covalentes. Esta forma de representar las molécules se conoce como far=
‘mula o estructura de Lewis. A continuacién mostraremos distintos ejemplos sencilles de molé-
culas con enlaces eovalentes y sus estructuras de Lewis,
+ La molécula de hidrégeno
El hidrgeno (Ht) es un gas en condiciones ambientales, formado por moléeulas diatomicas,
«8 decir, constituidas por dos ftomos. Cada dtoma de hidrégeno posee un niicleo con un protin
(on carga positiva) y un tnico eleetrén (con carga negativa) que se halla en un otbital Is.
Cuando dos dtomos de hidrégeno se aproximan aparecen fuerzas de repulsién nticleo-
niicleo y electrén-electrin y fuctzas de atraccién ndeleo-electrén, como se riuestra en la
figura lateral de Ia pagina siguiente,
Sean un modelo sencillo, podemos suponcr que el enlace se produce eutando ambos ato
‘mos se aproximan hasta llegar a una distancia dptima. Cuando se alcanza esta distancia dptima
ENLACE COVALENTE
ENLACES COVALENTES
‘SIMPLES
Emaces Quinicos
161
fosfirico hay cuatro enlaces simples P-O y 3 simples O-H. Las estructuras de Lewis y la regla del octeto La denominada regla del octeto ticne validez limitada, yo que en general, puede aplicarse satisfactoriamente para los elementos representativos de los periodos I y 2. Adn en moléculas formadas por étomos de elementos representativos, hay dtomos a cuyo alrededor bay un niime~ 10 menor © mayor de ocho electrones. ‘Veamos casos donde el étemo central no quede con C.E.E, de gas noble: 9) Atomos con menos de acho electrones Los atomos que tienen un nimero de electrones de valencia menor que cuatto, suelen for- ar enlaces covalentes con menos de ocho electrones a su alrededor, Ea el segundo period tenemos dos ejemplos tipicos: el belo yel boro, que forman compuestos covalentes come el loruro de berilio (BeC!,)y el tictoruro de boro (BCI). Sus estrucuras de Lewis se mucsttan en Jos diagrams adjuntos. donde podemos observar que el itome de berilio able tiene nats electrones a su alrededor y el de boro seis, Por otra parte, en las motéculas en las cuales el nimero total de eletrones externos es impr, también hay étomos a cuyo alrededor hay menos de ocho elecirones, Ejemplos de este tipo de moléculas, son el monéxido de nitzbgeno (NO) cuyo nimeto total de electrones extemos ¢s 11 1 dibxido de nitrogeno (NO) con un total de 17 y el dibxido de cloro (C103) con 19. Sus esiracturas de Lewis se obtienen aproximéndose lo mis posible ala rela del oct. En general, las moléculas que poseen uno 0 mis electroncs no aparealas, como 1s tes ite ‘mos ejemplos, son atraidas por un campo magnético y se las denomina paramagnéticas b) Atomos con mis de ocho clectrones Hay algunas moléculas en las que un dtomo central estéligado a mas de cuato stomos por enlaces covalentes y esté radeado por més de ocho electrones. A partir del tercer period, hay algunos elementos cuyos étomos coastituyen moléculas estables en las cuales tienen més de ocho electrones a su alrededor. Fl peatacloruro de fisforo (PCl,) y el hexafluoraro de azure (SF.6) son dos ejemplos de tales motéculas. En ellas, et fostoro y el azure estin rodeados por cinco y seis pares de electrones respectivamente Apesar de estas excepeiones que limitan el uso de la regla de octeto, debemnas eonvenit que igualmente es de gran utilidad pars obtener las formulas desamroliadas de muchas sustan explicar de manera sencilla sus enlaces, Enlaces Quimicos Gen + Be: Cl clonuro de borilo hexafluoruro de azutie 173 be Estructura do Lewis del jon sulfura pe) anion hidséxido Estructura de Lewis del {on nitrato ° ONO Esquema 1 fo wo] Esquema 2 [> wf Esquema 3 174 lones y compuestos iénicos + Tones monoatémicos Los eationes monoaiémicos, que han perdido sus electrones de valencia, se indican mediante su simbolo y la carga positiva como superindice. Por ejemplo: K*, Ca? La estructura de Lewis de a ann monoa'Smice, se escribe representando mediante pun- tos los electrones de valencia, de a pares, alrededor del simbolo del étomo. Luego se encie- fra el conjunto entre corchetes, indicando la carga del ion como superindice. Por ejemplo, el ‘ain sulfuro (S?) que se forma cuando el toro de azufre gana dos eleetrones, tiene dos car- tus nepativas. Como el dtomo de azure tiene seis eletrones de valencia, el nimero total de tlectrones del ion sulfuro es ocho, que se distnbuyen de a pares alrededor del siribolo del azue fic, Suestructura de Lewis se eseribe encerrande el conjunto entre paréntesis ¢ indicando Ia carwa negativa como se muestra en Ia figura adjunts, + Tones poliatémicos Fl procedimicnto para escribir las formuls de Lewis de iones poliatomicas (dos o ms Atomo$), no differe esencialmente del descripto para escribir las de las moléculas, Aniones Elion hidrOxido (OH"), tiene una carga negativa; el tomo de oxigeno tiene seis electrones do valencia y el del hidrgeno uno, y el nsimers total de electrones del aniOn es ocho, Estos elec- trones, representados mediante simbolos, los cistribuimos de manera que haya ocho electrones alrededor del tomo de oxigeno y dos alrededer del tomo de hidrogeno. El electtn que le con fiere la carga al anién ests representado en este ejemplo por un circulo, el del hidrOgeno por u cruz y los del oxigeno mediante puntos, Se eneierra el conjunto entre corehtes indicando la carga negativa como superindice ara escribir las estructuras de Lewis de aniones constituidos por mis de dos atomos, como por ejemplo el ion nitrato (NO3"), es conventente seguir los siguientes pasos 1) Colocar el dtomo de nitrdgena en el centro rodeado en forma simétrica pot los tres ‘itomos de oxigeno (Esquema 1). 2) Considerar el nimero de electrones de valencia de cada tomo. Elétomo de nitrogen tiene cinco electrones de valencia y cada dtomo de oxfgeno seis. Por tratarse de un anién mono: velente hay ademas un electron en exceso, que le confiere al anin la carga negativa 3) Colocar un electrin (mediante un circtlo) por cada carga negativa del anién en los éto- ‘mos de oxigeno, sin que patticipe en la anion con el nitrdgeno, En nuestro ejemplo cl ion tiene una sola carga negativa pot To que colacamos un electron del Indo externo del ox!- geno de la derecha. Luego, encerrar el grupo de itomos entre corchetes indicando la carga del anign con un signo (-) como superindice (Esquema 2). Caputo 5 4) Representar mediante puntos ls electrones de valencia del étomo de oxigeno que comtie- ne el electrén en exceso colocado en el paso anterior. En nuestro ejemplo ubicamos los seis electrones de valencia del oxigeno de la derecha (Esquema 3), 5) Representar con cruces los electrones de valencia del étomo central. De esta forma el fitomo de oxigeno que tiene la carga en exceso completa su octeto y alrededor del étomo de nitrégeno hay seis electrones, faltandole dos para llegar a los ocho (Esqueme 4), 6) Colocar con puntos los electrones de valencia de los atomos de oxigeno restantes, de ‘manera que con un par electronico de uno de ellos se complete el octeto del nitrogen, formandose el enlace covaiente doble N ~ 0, De esta manera obtenemos la estructura de Lewis, donde todos los étomos quedan con ‘ocho clectrones a su alrededor. (Esquema 5), Cationes ‘Neamos como se procede para escribir la estructura de Lewis de un eatin poliatémico como por ejemplo, el ion amonio (NF{,"). Esta formado por un dtomo de nitrégeno, cuatro de hidrd- geno y tiene una carga positiva. Como el atomo de nitrégeno tiene cinco eleetrores extemnos y los cuatro étomos de hidrdgeno uno cada uno, habria que distribuir nueve electrones de valen- cia. Sin embargo la carga positiva del ion indica que uno de los atomos de hidrogeno ha perdi- Go su electrén y por lo tanto sélo aportan un elected cada vin de los tres restantes. Para escribir Ia estructura de Lewis de este ion podemos seguir la siguiente s:cuencia 1) Eseribir el atomo de nitrdyeno en el centro rodeado por los cuatro dtomos de hidrégeno (Esquema 1). 2) Escribir mediante puntos un electron por cada uno de los tres dtomos de hidgeno y luego cencerrar el grupo de atomos entre corchetes indicando la carga positiva coy un signa (+) ‘como superindice (Esquema 2) 3) Colocar los cinco electrones de valencia del étomo de nitrOgeno a su alrededor de manera ‘que complete sv octeto, De esta manera quedan ocho electrones alrededor det dtomo de nitrégeno y dos alrededor de cada atomo de hidrSgeno. (Esquema 3) + Hidréxidos Los hidr6xidos son compuestos sélidos cristalinos formados por un catién metalico unido a aniones hidrOxidos y se representan mediante su formula minima Para escribir la estructura de Lewis det hidréxido de caleio; Ca(OH), debamos tener en ‘cuenta que el reticulo cristalino de este compuesto esta forrado por ua relacién sninima de un jon Ca?" y dos iones OW, La estructura de Lewis del hidréxido de calcio se escribe representanclo €. cation Ca en el centro y a ambos lados los dos aniones hidroxido entre corchetes con su carga como Emiaces Quimicos Estructura de Lowis do} jon amonio H HN H H Esquema 1 Hoyt IKON oH H Esquema 2 Hoqt eNH Ui Esquema 3 [am][s 2[eB en] ce Estructuras de Lewis del ‘idroxido do calelo superindice, como se muestra en la figura. También puede escribirse en forma més simpli- ficada, indicando el mimero de antones hidrixido mediante el nimero 2. + Oxosales Las oxosales son sales oxigenadas que estén formadas por teticulos cristalinos que contie~ ‘nen cationes metélicos y aniones formados por un no metal y oxigeao, Para escribir la estruc- tura de Lewis de una oxosal debemos tener en cuenta que el metal code electrones transforman- dose en un cation y estos electrones, a su vez generan un ani “ b Se Para escribir la estructura de Lewis del sulfato de sodio debemos tener en cuenta que la Nat 23a net frmuila minima de esta oxosal es Na,SOy. Este formada por una retacion de 2 eationes Brae sodio (Na*) y un anion sufato (50,2). Os a estrus et sul eo esentand el anién sulfio entre pean re eT aC La estructura de Lewis del sulfate de sodio se eseribe representando el at a corchstes con su canga como superindice y los dos jones Na* & ambos lados, como se muestra en Ia figura. Para eseribir la estructura de Lewis del Fe(NOx)>, seguiremos los siguientes pasos: 1) Idenficar el metal asignarie las cargas positivas de acuerdo a su estado de oxidacin. Fi ‘ese conapasto.l hiermn, qe ex el metal, tiene estado de oxidacion +2 v io escribimos Fe? 2) Escribir fa estructura de Lewis del oncaniém (NO) sein los pasos descritos anterior ‘mente 3) Bseribir ia estructura de Lewis de la axosal eolocando en ta forma mas simétrica posible Jos aniones y cationes. [sackeae] | La estructura de Lewis también puede escribirse en forma mis abrevinda de la siguiente manera 76 ‘Capituo 5 Resonancia Tin le estrctura de Lewis del didxido de aze (S0,) representada ala derech, uaa de las Uuniones entre el tome de austey ef de oxigeno es simple, mientras qu la ota es doble. Sin embargo, datos experimentales de distancia y de energia de enlace sugieten que ambos enlaces son equivalentes La estructura de Lewis propuesta 0 coneuerda con el hecho experimental y por lo tanto no representa correctamente cl enlace en la molécula. Para superar esta dificultad y conscrvar esta hherramienta Sencilia de representacidn suelen eseribirse dos estnucturas de Lewis cistintas, conec ‘adas por una flecha de doble sentido donde el enlace simple y el dabie estin intereambiados: (0 bien mediamte tas frmulas desarolledes O-S=0 <—» 0=s-0 Ninguna dc las dos estructuras por separado representa el enlace en la molécula de $03, ni ‘ainpoco se trata de un intercambio entre estructura, sino que se considera que le molécula real es una combinacién o “aibrida” de amhas a la ver, Cuando pueden eseribirse dos o més estructuras de Lewis para una misma especie, se dice ue existe resonancia y esas estructuras se denominan estructuras resonantes, Para el ion nitrato (NO;") pueden dlbujarse tres estructuras resonantes que difieren en la posicién del enlace covalenie doble: [t.] Orss0 Estructura de Lewis del $0 Enaces Quinicos 7 Hi a A a tH Benceno 5 ‘La molécula de benceno, cuya férmula molezular es C,H, tiene la estructura de un anillo for~ ‘mado por seis toms de carbone situados en el mismo plano, con tres dobles ligaduras altemadss ‘con tres simples, Sin embargo, datos experimertales indican que todos los enlaces entre fos sto- mos de carbono tienen la misma longitud (que es intermedia entre la de uno simple y uno doble). Es posible eseribir dos estructuras de resonancia del benceno, mediante anillos, donde cada ‘uno de su vértices representa un tomo de earbeno unide a un tome de hidrSgeno, con Tos enla- ces dables ubicados en distinto lugar: oo De esta manera, los seis enlaces entre los itomos de carbono pueden considerarse equiva lentes. Elion avetalo (CHjCOO") también se representa con dos estructaras resonantes, que difier rem en la posicién del enlace doble carbon ~ axigeno: oO o ¢ Z CHC, CH,-C, wy vy Capiudo 5 EJERCICIOS 1__Dadas las siguientes afirmaciones, indicar si son verdaderas o falsas: 4) cl enlace covalente se establece entre un elemento metilico y uno ne metilico, 5) el enlace covalente simple se produce por un par de electrones compartidos entre dos dtomos, ©) en una unin idnica se considera que los cationes y los aniones comoatten electrones 2_Eseribir los simbolos de Lewis de los siguientes étomos DAL bjCl |P DSi QNe HSe grHe 3. Escribir las estructuras de Lewis y las formulas desarrolladas de las siguientes especies 2) fluoruro de caleio (CaF) ©) sulfuro de sodin (Na;S) ») tetractoruro de carbono (CCI,) 1) H,0* «c) metano (CH,) 9 Clo> 4) amoniaco (NH) 4_ Ordenar los siguientes enlaces segin su polaidad creciente,indicanda sobre qué étomo esti desplazado cl par electrnico de la unién a0H bHF 90d gHC 5_Colocat los siguientes compuestos en orden creciente de carécter idnico: a) AIF; bY AIR) ) AIC, 6 Indicar ual de tos siguientes compuestor ee mis polar: a) HCI by TIE HBr 7_Dado el ion sulfato (S042 4) escribir su esructure de Lewis. +) determinar el numero total de electrones. ©) indicar cud es e1niimero total de protones de todos los nics del ion, 8_Completar el siguiente cuadro, en cuyas primeras columnas figuran letras que epresentan los simbolos de los elementos, jemento 2% [lemento) 2 |rormula Ptructurade x 2] ¥ | 9 | Mer, Rk iWw| Tt {a eae BE 8] M H 1 1 | 33 | (ee | Emaces Quimicos 9 9_ Elaimero total de protones presentes en el anién tetrat6mica formado por fos clementos R y T ¢s 40. T pertenece al grupo 16 de la clasificacién periédica y la CBE de R es 38?3p. Eseribir fa estructura de Lewis del anidin. 10_ Bscrbir ls estructuras de Lewis y las formulas desarroladas de las moléculas de las siguientes sustancias a) diéxido de earbono (CO3) 4) tidxido de dicloro (C103) b)etileno (CH) ©) pentoxido de difésforo (Ps) ©) amoniaco (NH) 1) sulfuro de litio (LixS) 11_Rscrbie la estructura de Lewis de los iones siguientes: a) ion amonio (NH,") 4) ion nitrato (NOS) ») ion ortofosfato (PO) ¢} ion carbonate (CO?) ©) fon perclorato (C10,") 12_Escrbir las estracturas de Lewis y las formalas desarrolladas de las moléculas o unidades formula correspondientes 2 las siguientes sustancias, indicando el tipo de enlace: a)HNO, —-B)HSO, HCI, HPO, &) HCO K,S0, g) CaCO, A) KCIO,_—i) Bay(PO,) jf) MgSO, 13_ Dadas las siguientes especies, escribir sus estructuras de Lewis, y discutir la validez de la regla del octeto @)NO; 6)SO, BE, ACN’) SIF, SF 14_Eserbir estrcturas de resonancia para las siguientes especies: 20; 4) 80; NO" -A)CO;* —e) HCOO™ 15_ Eseribir los nombres de las sales formadas por los cationes que figuran en cada colurmna con Tos aniones que figuran en cad file. tilizar el Apéndice de este Capitulo. KT | Ca” | NP | Fe* a 1{2i[3ale Br s | 6 f7[s s 9 | 0 | uj 2 nos 13 | 14 | 15 | 16 soe 21 | 2 | 2 | 28 Boy 29 | 30 | 31 | 32 aso, 33 | 34 | 35 | 36 Capitulo 5
También podría gustarte
- Acidos YbasesDocumento49 páginasAcidos Ybasesgaby-01Aún no hay calificaciones
- Moleculas InteraccionesDocumento32 páginasMoleculas Interaccionesgaby-01Aún no hay calificaciones
- Ecuaciones DiferencialesDocumento8 páginasEcuaciones Diferencialesgaby-01Aún no hay calificaciones
- Reacciones QuimicasDocumento35 páginasReacciones Quimicasgaby-01Aún no hay calificaciones
- Soluciones QuimicasDocumento36 páginasSoluciones Quimicasgaby-01Aún no hay calificaciones
- Colores Ggplot2Documento14 páginasColores Ggplot2gaby-010% (1)
- Poster Paleontologia Evolucion Humana 01Documento1 páginaPoster Paleontologia Evolucion Humana 01gaby-01Aún no hay calificaciones
- Resume N Latex PedroDocumento8 páginasResume N Latex Pedrogaby-01Aún no hay calificaciones
- Resumen Contabilidad2Documento2 páginasResumen Contabilidad2gaby-01Aún no hay calificaciones
- Apunte TeledeteccionDocumento3 páginasApunte Teledetecciongaby-01Aún no hay calificaciones
- Funciones Estadísticas 3 - LibreOffice CalcDocumento6 páginasFunciones Estadísticas 3 - LibreOffice Calcgaby-01Aún no hay calificaciones
- Funciones Estadísticas 4 - LibreOffice CalcDocumento12 páginasFunciones Estadísticas 4 - LibreOffice Calcgaby-01Aún no hay calificaciones
- Ecologia Condiciones y RecursosDocumento9 páginasEcologia Condiciones y Recursosgaby-01Aún no hay calificaciones
- Parametros de Calidad de AguaDocumento21 páginasParametros de Calidad de Aguagaby-01Aún no hay calificaciones
- Funciones de Hojas de Calculo - LibreOffice CalcDocumento15 páginasFunciones de Hojas de Calculo - LibreOffice Calcgaby-01Aún no hay calificaciones
- Funciones Estadísticas - LibreOffice CalcDocumento13 páginasFunciones Estadísticas - LibreOffice Calcgaby-01Aún no hay calificaciones
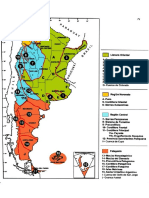
- Mapa de Las Provincias Geologicas ArgentinasDocumento1 páginaMapa de Las Provincias Geologicas Argentinasgaby-01100% (1)
- Variables Fisico QuimicasDocumento9 páginasVariables Fisico Quimicasgaby-01Aún no hay calificaciones