Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Primer Parcial 2020 - 1
Cargado por
Susana OriaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Primer Parcial 2020 - 1
Cargado por
Susana OriaCopyright:
Formatos disponibles
UNIVERSIDAD DE ANTIOQUIA
FACULTAD DE INGENIERÍA
ESCUELA AMBIENTAL
PROCESOS FISICOQUÍMICOS
PRIMER PARCIAL: UNIDADES 1-2-3
PROFESOR Darío Naranjo Fernández
CORREO ELECTRÓNICO dario.naranjo@udea.edu.co
OFICINA 20-412
HORARIO DE ATENCION WV 14-16
ESTUDIANTES
INSTRUCCIONES:
El parcial es para realizarse en grupos de máximo dos (2) personas.
Sólo se acepta un documento único en formato .pdf.
La hora máxima de entrega es 10:00 a.m. (GMT-5).
Use la información suministrada y consulte sólo lo necesario en otras fuentes.
Muestre claramente los cálculos que llevan a los resultados.
Parciales similares entre diferentes parejas serán anulados.
Un sistema de potabilización de un pequeño pueblo se abastece de dos fuentes subterráneas diferentes
y tiene una característica particular, se encuentran altas concentraciones de zinc y muy bajas
concentraciones de otros cationes polivalentes. Una caracterización de las fuentes mezcladas se
presenta a continuación:
Q = 0,8 L/s pH = 7,0
T = 20 °C OD = 0,3 mg O2/L
Alcalinidad (HCO3-) = 80 mg CaCO3/L [Zn+2] = ¿?
[SO42-] = 26,5 mg SO42-/L [Na+] = 17,3 mg Na+/L
[Cl-] = 21,2 mg Cl-/L [CO2] = 40 mg CaCO3/L
De acuerdo a la información presentada, determine:
1. (10%) La concentración de saturación de oxígeno disuelto (mg/L) si la presión barométrica del lugar
es de 700 mm Hg y la temperatura es de 20 °C. (KH 25°C = 1,3x10-3 mol/L.atm; nO2/nT = 0,2095; ∆H O2(g)
= 0; ∆H O2(ac) = -11,71 kJ/mol).
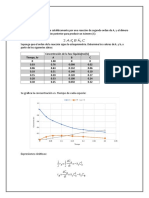
2. (20%) El coeficiente volumétrico de transferencia de oxígeno (min-1) si en un ensayo con el agua
cruda mezclada se obtuvieron los siguientes resultados:
ATENCIÓN: Sólo se acepta un procedimiento con estos datos y con la ecuación de la ley de Fick sin
integrar [dC/dt = KLa(Cs – C)]. ¡Piensen y propongan!
t (min) C (mg O2/L)
0,00 0,85
0,33 0,96
0,67 1,03
1,00 1,11
1,33 1,22
1,67 1,33
2,00 1,45
2,50 1,64
3,00 1,79
3,50 1,92
4,00 2,07
4,50 2,23
5,00 2,35
6,00 2,61
7,00 2,80
8,00 3,02
9,00 3,23
10,00 3,40
12,00 3,73
14,00 4,06
16,00 4,32
18,00 4,55
20,00 4,73
3. (20%) La concentración de ion zinc en la mezcla que abastece al sistema de potabilización si una de
las fuentes aporta un caudal de 0,5 L/s con [Zn2+] = 98,5 mg Zn2+/L y la otra un caudal de 0,3 L/s con
[Zn2+] = 10,5 mg Zn2+/L. (MAZn = 65,4 g/mol)
4. (10%) Las durezas total, carbonácea y no carbonácea.
5. (10%) El mejor anión, entre carbonato e hidroxilo, para la remoción de zinc. (Kps ZnCO3 = 1,46x10-10 y
Kps Zn(OH)2 = 7,68x10-17, supuestas a 20 °C)
6. (30%) Las cantidades requeridas (kg/d) de cal [Ca(OH)2] al 75% de pureza y soda (Na2CO3) al 90%
de pureza para el proceso de ablandamiento, presentando claramente el procedimiento y las
reacciones involucradas. (Nota: en el diagrama de barras de especies hipotéticas, la sal de
bicarbonato es menos soluble que la sal de sulfato).
También podría gustarte
- Po1 5Documento24 páginasPo1 5Susana OriaAún no hay calificaciones
- SP10 1Documento11 páginasSP10 1Susana OriaAún no hay calificaciones
- PO315 OkDocumento12 páginasPO315 OkSusana OriaAún no hay calificaciones
- Planilla Agua Potable Antioquia 2019Documento26 páginasPlanilla Agua Potable Antioquia 2019Susana OriaAún no hay calificaciones
- Taller 3Documento12 páginasTaller 3Susana OriaAún no hay calificaciones
- Actividad Evaluativa 29 de AgostoDocumento3 páginasActividad Evaluativa 29 de AgostoSusana OriaAún no hay calificaciones
- Prog Fister 2018 1Documento5 páginasProg Fister 2018 1Susana OriaAún no hay calificaciones
- Taller Parcial III 2016-I Con Cuadriláteros PDFDocumento10 páginasTaller Parcial III 2016-I Con Cuadriláteros PDFSusana OriaAún no hay calificaciones
- Taller de Funciones VectorialesDocumento3 páginasTaller de Funciones VectorialesSusana OriaAún no hay calificaciones
- Taller de Límites y Derivadas Parciales VNDocumento7 páginasTaller de Límites y Derivadas Parciales VNSusana Oria0% (1)
- SoluciónParcial - 1 Calculo - IntegralCarta - 20161Documento2 páginasSoluciónParcial - 1 Calculo - IntegralCarta - 20161Susana OriaAún no hay calificaciones
- Taller 1G.E.2015-1 PDFDocumento15 páginasTaller 1G.E.2015-1 PDFSusana OriaAún no hay calificaciones
- Laboratorio Microbiología CLDocumento13 páginasLaboratorio Microbiología CLDaniela HenriquezAún no hay calificaciones
- Ejer Cici OsDocumento3 páginasEjer Cici OsIrvin VizurragaAún no hay calificaciones
- Problema 2.3 CarberryDocumento4 páginasProblema 2.3 CarberryAbner LugoAún no hay calificaciones
- Unidades Físicas de ConcentraciónDocumento7 páginasUnidades Físicas de ConcentraciónPaula GordillpAún no hay calificaciones
- BP Termologia-NumeradoDocumento8 páginasBP Termologia-NumeradoJackeline Ortuño RamírezAún no hay calificaciones
- Actividad de Puntos Evaluables - Escenarios 6 - SEGUNDO BLOQUE-CIENCIAS BASICAS - FUNDAMENTOS DE QUIMICA - (GRUPO10)Documento5 páginasActividad de Puntos Evaluables - Escenarios 6 - SEGUNDO BLOQUE-CIENCIAS BASICAS - FUNDAMENTOS DE QUIMICA - (GRUPO10)Víctor Manuel0% (1)
- GUIA Entropia y Energia Libre de GibbsDocumento9 páginasGUIA Entropia y Energia Libre de GibbsluzmooreAún no hay calificaciones
- INFORME PRÁCTICA REFRIGERACIÓN Falta 1 GraficaDocumento10 páginasINFORME PRÁCTICA REFRIGERACIÓN Falta 1 GraficaYalexiAún no hay calificaciones
- Termometria Gal 03Documento4 páginasTermometria Gal 03Fabricio ValenciaAún no hay calificaciones
- Ejercicios - Masas Molares y MolesDocumento1 páginaEjercicios - Masas Molares y MolesLuisAún no hay calificaciones
- Calor Integral de SolucionDocumento7 páginasCalor Integral de SolucionOscar PortilloAún no hay calificaciones
- Calculo de Parametros EnergeticosDocumento13 páginasCalculo de Parametros EnergeticosABRAHAM JARAMILLO SANCHEZAún no hay calificaciones
- Quimica 1°año IiiDocumento24 páginasQuimica 1°año IiiOscar Rodríguez GómezAún no hay calificaciones
- Tema 2-IIDocumento34 páginasTema 2-IIFabiana Elizabeth FeijooAún no hay calificaciones
- Descenso TérmicoDocumento7 páginasDescenso TérmicoalexisAún no hay calificaciones
- Ejercicios de EstequiometríaDocumento32 páginasEjercicios de EstequiometríaMaddox Parra RoperoAún no hay calificaciones
- Problemas de DisolucionesDocumento3 páginasProblemas de Disolucionesbastian arias moralesAún no hay calificaciones
- Sesion 7-Intro A La Estequiometría y Clasificación de ReaccionesDocumento25 páginasSesion 7-Intro A La Estequiometría y Clasificación de ReaccionesIgnacio MejiaAún no hay calificaciones
- Ejercicios ConcentracionesDocumento8 páginasEjercicios ConcentracionesIALCAún no hay calificaciones
- Unidades Químicas de Masa 21-09-2021Documento7 páginasUnidades Químicas de Masa 21-09-2021Carlos Andrés Clausen AlíAún no hay calificaciones
- Disminucion de Presion de VaporDocumento1 páginaDisminucion de Presion de VaporSponja75Aún no hay calificaciones
- PFR Adiabatico y Con Intercambio de CalorDocumento4 páginasPFR Adiabatico y Con Intercambio de CalorJazbeth JimenezAún no hay calificaciones
- Determinación Del Calor de Solución Por El Método de SolubilidadDocumento10 páginasDeterminación Del Calor de Solución Por El Método de SolubilidadPIPOCHICHITO100% (1)
- Aplicación de Modelos TermodinámicosDocumento24 páginasAplicación de Modelos TermodinámicosLalo Cortes EspinosaAún no hay calificaciones
- Manual Del Octano - Diagrama P-HDocumento24 páginasManual Del Octano - Diagrama P-HLeticia ChávezAún no hay calificaciones
- 2do PROBLEMARIO 3er DEP - MAYO'22Documento6 páginas2do PROBLEMARIO 3er DEP - MAYO'22guillermoAún no hay calificaciones
- Practica #9 Capacidad CalorificaDocumento15 páginasPractica #9 Capacidad CalorificaCarlos Manuel Fernandez100% (1)
- EstequiometríaDocumento19 páginasEstequiometríaErick VasquezAún no hay calificaciones
- Prueba de Química Propiedades Coligativas Coeficiente 1 Fila ADocumento4 páginasPrueba de Química Propiedades Coligativas Coeficiente 1 Fila AFelipe Alejandro Jara67% (3)
- Simulador - ProblemasDocumento8 páginasSimulador - ProblemasYus AssafAún no hay calificaciones
- Cómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaDe EverandCómo hacer que te pasen cosas buenas: Entiende tu cerebro, gestiona tus emociones, mejora tu vidaCalificación: 5 de 5 estrellas5/5 (1875)
- La revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaDe EverandLa revolución de la glucosa: Equilibra tus niveles de glucosa y cambiarás tu salud y tu vidaCalificación: 5 de 5 estrellas5/5 (203)
- Psicología oscura: Una guía esencial de persuasión, manipulación, engaño, control mental, negociación, conducta humana, PNL y guerra psicológicaDe EverandPsicología oscura: Una guía esencial de persuasión, manipulación, engaño, control mental, negociación, conducta humana, PNL y guerra psicológicaCalificación: 4.5 de 5 estrellas4.5/5 (766)
- Recupera tu mente, reconquista tu vidaDe EverandRecupera tu mente, reconquista tu vidaCalificación: 5 de 5 estrellas5/5 (9)
- Yo Pude, ¡Tú Puedes!: Cómo tomar el control de tu bienestar emocional y convertirte en una persona imparable (edición revisada y expandida)De EverandYo Pude, ¡Tú Puedes!: Cómo tomar el control de tu bienestar emocional y convertirte en una persona imparable (edición revisada y expandida)Calificación: 5 de 5 estrellas5/5 (9)
- Batidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoDe EverandBatidos Verdes Depurativos y Antioxidantes: Aumenta tu Vitalidad con Smoothie Detox Durante 10 Días Para Adelgazar y Bajar de Peso: Aumenta tu vitalidad con smoothie detox durante 10 días para adelgazar y bajar de pesoCalificación: 5 de 5 estrellas5/5 (2)
- Tus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadDe EverandTus Zonas Erroneas: Guía Para Combatir las Causas de la InfelicidadCalificación: 4.5 de 5 estrellas4.5/5 (1833)
- Resetea tu mente. Descubre de lo que eres capazDe EverandResetea tu mente. Descubre de lo que eres capazCalificación: 5 de 5 estrellas5/5 (196)
- El poder del optimismo: Herramientas para vivir de forma más positivaDe EverandEl poder del optimismo: Herramientas para vivir de forma más positivaCalificación: 5 de 5 estrellas5/5 (16)
- Resumen de Pensar rápido pensar despacio de Daniel KahnemanDe EverandResumen de Pensar rápido pensar despacio de Daniel KahnemanCalificación: 4.5 de 5 estrellas4.5/5 (64)
- La violencia invisible: Identificar, entender y superar la violencia psicológica que sufrimos (y ejercemos) en nuestra vida cotidianaDe EverandLa violencia invisible: Identificar, entender y superar la violencia psicológica que sufrimos (y ejercemos) en nuestra vida cotidianaCalificación: 4 de 5 estrellas4/5 (2)
- DMT: La molécula del espíritu (DMT: The Spirit Molecule): Las revolucionarias investigaciones de un medico sobre la biologia de las experiencias misticas y cercanas a la muerteDe EverandDMT: La molécula del espíritu (DMT: The Spirit Molecule): Las revolucionarias investigaciones de un medico sobre la biologia de las experiencias misticas y cercanas a la muerteCalificación: 4.5 de 5 estrellas4.5/5 (19)
- La metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceDe EverandLa metamedicina. Cada síntoma es un mensaje: La curación a tu alcanceCalificación: 5 de 5 estrellas5/5 (8)
- Contra la ansiedad: Una guía completa para manejar emociones difícilesDe EverandContra la ansiedad: Una guía completa para manejar emociones difícilesCalificación: 5 de 5 estrellas5/5 (58)
- Tu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaDe EverandTu cerebro emocional: Saca partido de lo que sientes y transforma tu vidaCalificación: 5 de 5 estrellas5/5 (2)
- Influencia. La psicología de la persuasiónDe EverandInfluencia. La psicología de la persuasiónCalificación: 4.5 de 5 estrellas4.5/5 (14)
- The Coaching Habit: Las 7 preguntas clave para liderar equipos y organizaciones del siglo XXIDe EverandThe Coaching Habit: Las 7 preguntas clave para liderar equipos y organizaciones del siglo XXICalificación: 4.5 de 5 estrellas4.5/5 (166)