0% encontró este documento útil (0 votos)
274 vistas19 páginasCálculo de Separación en Columna de Destilación
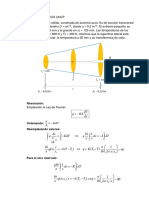
Este documento presenta los cálculos para resolver un problema de separación de una mezcla de cuatro componentes (A, B, C, D) en una columna de destilación a una presión de 300 psi. Incluye tablas para calcular los puntos de burbuja y rocío de la mezcla, el balance de materia, la temperatura de operación del condensador y otros parámetros necesarios para el diseño de la columna. El objetivo es encontrar la razón de reflujo óptima que minimice el costo total anual de operación de la columna.
Cargado por
Jezie Paul ReyesDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd
0% encontró este documento útil (0 votos)
274 vistas19 páginasCálculo de Separación en Columna de Destilación
Este documento presenta los cálculos para resolver un problema de separación de una mezcla de cuatro componentes (A, B, C, D) en una columna de destilación a una presión de 300 psi. Incluye tablas para calcular los puntos de burbuja y rocío de la mezcla, el balance de materia, la temperatura de operación del condensador y otros parámetros necesarios para el diseño de la columna. El objetivo es encontrar la razón de reflujo óptima que minimice el costo total anual de operación de la columna.
Cargado por
Jezie Paul ReyesDerechos de autor
© © All Rights Reserved
Nos tomamos en serio los derechos de los contenidos. Si sospechas que se trata de tu contenido, reclámalo aquí.
Formatos disponibles
Descarga como DOCX, PDF, TXT o lee en línea desde Scribd