Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Teoría Atómica
Cargado por
lacasitaazulTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Teoría Atómica
Cargado por
lacasitaazulCopyright:
Formatos disponibles
Teora atmica
Teora atmica
En fsica y qumica, la teora atmica es una teora de la naturaleza de la materia, que afirma que est compuesta por pequeas partculas llamadas tomos. La teora atmica comenz hace miles de aos como un concepto filosfico y fue en el siglo XIX cuando logr una extensa aceptacin cientfica gracias a los descubrimientos en el campo de la estequiometra. Los qumicos de la poca crean que las unidades bsicas de los elementos tambin eran las partculas fundamentales de la naturaleza y las llamaron tomos (de la palabra griega atomos, que significa "indivisible"). Sin embargo, a finales de aquel siglo, y mediante diversos experimentos con el electromagnetismo y la radiactividad, los fsicos descubrieron que el denominado "tomo indivisible" era realmente un conglomerado de diversas partculas subatmicas (principalmente electrones, protones y neutrones), que pueden existir de manera separada. De hecho, en ciertos ambientes, como en las estrellas de neutrones, la temperatura extrema y la elevada presin impide a los tomos existir como tales. El campo de la ciencia que estudia las partculas fundamentales de la materia se denomina fsica de partculas.
Varios tomos y molculas segn John Dalton, en su libro A New System of Chemical Philosophy (Nuevo Sistema de Filosofa Qumica, 1808).
Teora atmica de Dalton
Durante el siglo XVIII y los primeros aos del siglo XIX, en su afn por conocer e interpretar la naturaleza, los cientficos estudiaron intensamente las reacciones qumicas mediante numerosos experimentos. Estos estudios permitieron hallar relaciones muy precisas entre las masas de las sustancias slidas o entre los volmenes de los gases que intervienen en las reacciones qumicas. Las relaciones encontradas se conocen como leyes de la qumica. Entre las leyes fundamentales de la Qumica, hay algunas que establecen las relaciones entre masas, llamadas leyes gravimtricas y otras que relacionan volmenes, denominadas leyes volumtricas. John Dalton desarroll su modelo atmico, en la que propona que cada elemento qumico estaba compuesto por tomos iguales y exclusivos, y que aunque eran indivisibles e indestructibles, se podan asociar para formar estructuras ms complejas (los compuestos qumicos). Esta teora tuvo diversos precedentes. El primero fue la ley de conservacin de la masa, formulada por Antoine Lavoisier en 1789, que afirma que la masa total en una reaccin qumica permanece constante. Esta ley le sugiri a Dalton la idea de que la materia era indestructible. El segundo fue la ley de las proporciones definidas. Enunciada por el qumico francs Joseph Louis Proust en 1799, afirma que, en un compuesto, los elementos que lo conforman se combinan en proporciones de masa definidas y caractersticas del compuesto. Dalton estudi y ampli el trabajo de Proust para desarrollar la ley de las proporciones mltiples: cuando dos elementos se combinan para originar diferentes compuestos, dada una cantidad fija de uno de ellos, las diferentes cantidades del otro se combinan con dicha cantidad fija para dar como producto los compuestos, estn en relacin de nmeros enteros sencillos. En 1803, Dalton public su primera lista de pesos atmicos relativos para cierta cantidad de sustancias. Esto, unido a su rudimentario material, hizo que su tabla fuese muy poco precisa. Por ejemplo, crea que los tomos de oxgeno
Teora atmica eran 5,5 veces ms pesados que los tomos de hidrgeno, porque en el agua midi 5,5 gramos de oxgeno por cada gramo de hidrgeno y crea que la frmula del agua, en estado gaseoso, era HO (en realidad, un tomo de oxgeno es 16 veces ms pesado que un tomo de hidrgeno). La ley de Avogadro permiti deducir la naturaleza diatmica de numerosos gases, estudiando los volmenes en los que reaccionaban. Por ejemplo: el hecho de que dos litros de hidrgeno reaccionasen con un litro de oxgeno para producir dos litros de vapor de agua (a presin y temperatura constantes), significaba que una nica molcula de oxgeno se divide en dos para formar dos partculas de agua. De esta forma, Avogadro poda calcular estimaciones ms exactas de la masa atmica del oxgeno y de otros elementos, y estableci la distincin entre molculas y tomos. Ya en 1784, el botnico escocs Robert Brown, haba observado que las partculas de polvo que flotaban en el agua se movan al azar sin ninguna razn aparente. En 1905, Albert Einstein tena la teora de que este movimiento browniano lo causaban las molculas de agua que "bombardeaban" constantemente las partculas, y desarroll un modelo matemtico hipottico para describirlo. El fsico francs Jean Perrin demostr experimentalmente este modelo en 1911, proporcionando adems la validacin a la teora de partculas (y por extensin, a la teora atmica).
Descubrimiento de las partculas subatmicas
Hasta 1897, se crea que los tomos eran la divisin ms pequea de la materia, cuando J.J Thomson descubri el electrn mediante su experimento con el tubo de rayos catdicos.[1] El tubo de rayos catdicos que us Thomson era un recipiente cerrado de vidrio, en El tubo de rayos catdicos de Thomson, en el que el cual los dos electrodos estaban separados por un vaco. Cuando observ la desviacin de los rayos catdicos por un se aplica una diferencia de tensin a los electrodos, se generan campo elctrico. rayos catdicos, que crean un resplandor fosforescente cuando chocan con el extremo opuesto del tubo de cristal. Mediante la experimentacin, Thomson descubri que los rayos se desviaban al aplicar un campo elctrico (adems de desviarse con los campos magnticos, cosa que ya se saba). Afirm que estos rayos, ms que ondas, estaban compuestos por partculas cargadas negativamente a las que llam "corpsculos" (ms tarde, otros cientficos las rebautizaran como electrones). Thomson crea que los corpsculos surgan de los tomos del electrodo. De esta forma, estipul que los tomos eran divisibles, y que los corpsculos eran sus componentes. Para explicar la carga neutra del tomo, propuso que los corpsculos se distribuan en estructuras anilladas dentro de una nube positiva uniforme; ste era el modelo atmico de Thomson o "modelo del plum cake".[2] Ya que se vio que los tomos eran realmente divisibles, los fsicos inventaron ms tarde el trmino "partculas elementales" para designar a las partculas indivisibles.
Teora atmica
Descubrimiento del ncleo
El modelo atmico de Thomson fue refutado en 1909 por uno de sus estudiantes, Ernest Rutherford, quien descubri que la mayor parte de la masa y de la carga positiva de un tomo estaba concentrada en una fraccin muy pequea de su volumen, que supona que estaba en el mismo centro. En su experimento, Hans Geiger y Ernest Marsden bombardearon partculas alfa a travs de una fina lmina de oro (que chocaran con una pantalla fluorescente que haban colocado rodeando la lmina).[3] Dada la mnima como masa de los electrones, la elevada masa y momento de las partculas alfa y la distribucin uniforme de la carga positiva del modelo de Thomson, estos cientficos esperaban que todas las partculas alfa atravesasen la lmina de oro sin desviarse, o por el contrario, que fuesen absorbidas. Para su asombro, una pequea fraccin de las partculas alfa sufri una fuerte desviacin. Esto indujo a Rutherford a proponer el modelo planetario del tomo, en el que los electrones orbitaban en el espacio alrededor de un gran ncleo compacto, a semejanza de los planetas y el Sol.[4]
Descubrimiento de los istopos
En 1913, Thomson canaliz una corriente de iones de nen a travs de campos magnticos y elctricos, hasta chocar con una placa fotogrfica que haba colocado al otro lado. Observ dos zonas incandescentes en la placa, que revelaban dos trayectorias de desviacin diferentes. Thomson concluy que esto era porque algunos de los iones de nen tenan diferentes masas; as fue como descubri la existencia de los istopos.[5]
Experimento de la lmina de oro Arriba: Resultados esperados: las partculas alfa pasan sin problemas por el modelo atmico de Thomson. Abajo: Resultados observados: una pequea parte de las partculas se desva, lo que revela la existencia de un lugar en el tomo donde se concentra la carga positiva.
Descubrimiento del neutrn
En 1918, Rutherford logr partir el ncleo del tomo al bombardear gas nitrgeno con partculas alfa, y observ que el gas emita ncleos de hidrgeno. Rutherford concluy que los ncleos de hidrgeno procedan de los ncleos de los mismos tomos de nitrgeno.[6] Ms tarde descubri que la carga positiva de cualquier tomo equivala siempre a un nmero entero de ncleos de hidrgeno. Esto, junto con el hecho de que el hidrgeno el elemento ms ligero tena una masa atmica de 1, le llev a afirmar que los ncleos de hidrgeno eran partculas singulares, constituyentes bsicos de todos los ncleos atmicos: se haba descubierto el protn. Un experimento posterior de Rutherford mostr que la masa nuclear de la mayora de los tomos superaba a la de los protones que tena. Por tanto, postul la existencia de partculas sin carga, hasta entonces desconocidas ms tarde llamadas neutrones, de donde provendra este exceso de masa. En 1928, Walther Bothe observ que el berilio emita una radiacin elctricamente neutra cuando se le bombardeaba con partculas alfa. En 1932, James Chadwick expuso diversos elementos a esta radiacin y dedujo que sta estaba compuesta por partculas elctricamente neutras con una masa similar la de un protn.[7] Chadwick llam a estas partculas "neutrones".
Teora atmica
Modelos cunticos del tomo
El modelo planetario del tomo tena sus defectos. En primer lugar, segn la frmula de Larmor del electromagnetismo clsico, una carga elctrica en aceleracin emite ondas electromagnticas, y una carga en rbita ira perdiendo energa y describira una espiral hasta acabar cayendo en el ncleo. Otro fenmeno que el modelo no explicaba era por qu los tomos excitados slo emiten luz con ciertos espectros discretos. La teora cuntica revolucion la fsica de comienzos del siglo XX, cuando Max Planck y Albert Einstein postularon que se emite o absorbe una leve cantidad de energa en cantidades fijas llamadas cuantos. En 1913, Niels Bohr incorpor esta idea a su modelo atmico, en el que los electrones slo podran orbitar alrededor del ncleo en rbitas circulares determinadas, con una energa y un momento angular fijos, y siendo proporcionales las distancias del ncleo a los respectivos niveles de energa.[8] Segn este modelo, los tomos no podran describir espirales hacia el ncleo porque no podran perder energa de manera continua; en cambio, slo podran realizar "saltos cunticos" instantneos entre los niveles fijos de energa.[9] Cuando esto ocurre, el El modelo de Bohr. tomo absorbe o emite luz a una frecuencia proporcional a la diferencia de energa (y de ah la absorcin y emisin de luz en los espectros discretos).[9]Arnold Sommerfeld ampli el tomo de Bohr en 1916 para incluir rbitas elpticas, utilizando una cuantificacin de momento generalizado. El modelo de Bohr-Sommerfeld ad hoc era muy difcil de utilizar, pero a cambio haca increbles predicciones de acuerdo con ciertas propiedades espectrales. Sin embargo, era incapaz de explicar los tomos multielectrnicos, predecir la tasa de transicin o describir las estructuras finas e hiperfinas. En 1924, Louis de Broglie propuso que todos los objetos particularmente las partculas subatmicas, como los electrones podan tener propiedades de ondas. Erwin Schrdinger, fascinado por esta idea, investig si el movimiento de un electrn en un tomo se podra explicar mejor como onda que como partcula. La ecuacin de Schrdinger, publicada en 1926,[10] describe al electrn como una funcin de onda en lugar de como una partcula, y predijo muchos de los fenmenos espectrales que el modelo de Bohr no poda explicar. Aunque este concepto era matemticamente correcto, era difcil de visualizar, y tuvo sus detractores.[11] Uno de sus crticos, Max Born, dijo que la funcin de onda de Schrdinger no describa el electrn, pero s a muchos de sus posibles estados, y de esta forma se podra usar para calcular la probabilidad de encontrar un electrn en cualquier posicin dada alrededor del ncleo.[12] En 1927, Werner Heisenberg indic que, puesto que una funcin de onda est determinada por el tiempo y la posicin, es imposible obtener simultneamente valores precisos tanto para la posicin como para el momento de la partcula para cualquier punto dado en el tiempo.[13] Este principio fue conocido como principio de incertidumbre de Heisenberg. Este nuevo enfoque invalidaba por completo el modelo de Bohr, con sus rbitas circulares claramente definidas. El modelo moderno del tomo describe las posiciones de los electrones en un tomo en trminos de probabilidades. Un electrn se puede encontrar potencialmente a cualquier distancia del ncleo, pero dependiendo de su nivel de energa tiende a estar con ms frecuencia en ciertas regiones alrededor del ncleo que en otras; estas zonas son conocidas como orbitales atmicos.
Los cinco orbitales atmicos de un tomo de nen, separados y ordenados en orden creciente de energa. En cada orbital caben como mximo dos electrones, que estn la mayor parte del tiempo en las zonas delimitadas por las "burbujas".
Teora atmica
Importancia
La importancia de esta teora no puede ser exagerada. Se ha dicho (por ejemplo el premio Nobel Richard Feynman) que la teora atmica es la teora ms importante en la historia de la ciencia. Esto se debe a las implicaciones que ha tenido, tanto para la ciencia bsica como por las aplicaciones que se han derivado de ella. Toda la qumica y bioqumica modernas se basan en la teora de que la materia est compuesta de tomos de diferentes elementos, que no pueden transmutarse por mtodos qumicos. Por su parte, la qumica ha permitido el desarrollo de la industria farmacutica, petroqumica, de abonos, el desarrollo de nuevos materiales, incluidos los semiconductores, y otros avances.
Notas
[1] J.J. Thomson (1897), Cathode rays (http:/ / web. lemoyne. edu/ ~GIUNTA/ thomson1897. html), Philosophical Magazine [2] J.J. Thomson (Marzo de 1904), On the Structure of the Atom: an Investigation of the Stability and Periods of Oscillation of a number of Corpuscles arranged at equal intervals around the Circumference of a Circle; with Application of the Results to the Theory of Atomic Structure (http:/ / dbhs. wvusd. k12. ca. us/ webdocs/ Chem-History/ Thomson-Structure-Atom. html), Philosophical Magazine Serie 6, Vol 7, N 39 [3] H Geiger (1910), The Scattering of the -Particles by Matter (http:/ / dbhs. wvusd. k12. ca. us/ webdocs/ Chem-History/ Geiger-1910. html), Proceedings of the Royal Society Series A 82: 495500 [4] Ernest Rutherford (1911), The Scattering of and Particles by Matter and the Structure of the Atom (http:/ / dbhs. wvusd. k12. ca. us/ webdocs/ Chem-History/ Rutherford-1911/ Rutherford-1911. html), Philosophical Magazine Serie 6, vol. 21 [5] J.J. Thomson (1913), Rays of positive electricity (http:/ / web. lemoyne. edu/ ~giunta/ canal. html), Proceedings of the Royal Society, A 89, 1-20 [6] Ernest Rutherford (1919), Collisions of alpha Particles with Light Atoms. IV. An Anomalous Effect in Nitrogen. (http:/ / web. lemoyne. edu/ ~GIUNTA/ rutherford. html), Philosophical Magazine, 6 serie, 37, 581 [7] James Chadwick (27 de febrero de 1932), Possible Existence of a Neutron (http:/ / dbhs. wvusd. k12. ca. us/ webdocs/ Chem-History/ Chadwick-neutron-letter. html), Nature Magazine [8] Bohr, N. (1913). On the constitution of atoms and molecules. Philosophical Magazine, 26, 1-25 (http:/ / dbhs. wvusd. k12. ca. us/ webdocs/ Chem-History/ Bohr/ Bohr-1913a. html)] [9] Bohr, N. On the constitution of atoms and molecules. [10] Erwin Schrodinger (1926), Quantisation as an Eigenvalue Problem, Annalen der Physik [11] Dr Subodh Mahanti, Erwin Schrodinger: The Founder of Quantum Wave Mechanics (http:/ / www. vigyanprasar. gov. in/ scientists/ ESchrodinger. htm), Vigyan Prasar [12] Dr Subodh Mahanti, Max Born: Founder of Lattice Dynamics (http:/ / www. vigyanprasar. gov. in/ scientists/ MBorn. htm), Vigyan Prasar [13] ISCID, Heisenberg Uncertainty Principle (http:/ / www. iscid. org/ encyclopedia/ Heisenberg_Uncertainty_Principle)
Enlaces externos
Atomismo antiguo (http://plato.stanford.edu/entries/atomism-ancient/) Descubrimiento del neutrn (http://www.chemcases.com/nuclear/nc-01.htm) Atom: The Incredible World (http://library.thinkquest.org/19662/low/eng/main.html)
Fuentes y contribuyentes del artculo
Fuentes y contribuyentes del artculo
Teora atmica Fuente: http://es.wikipedia.org/w/index.php?oldid=65978494 Contribuyentes: .Sergio, 3coma14, 4lex, Acratta, Airunp, Ale flashero, Alvaro qc, Andreasmperu, Antn Francho, Aipni-Lovrij, Baiji, Banfield, Comae, Dalton2, Danilo Andres Ramirez, David0811, Davius, Diego danilo vargas, Diegusjaimes, Diosa, Dodo, Dorieo, Durst21, Eduardosalg, Emiduronte, Equi, Erfil, FAL56, Fdvfvdv, Ferbr1, Fmariluis, Foundling, Furti, Ganmedes, Ggenellina, HUB, Halfdrag, Helmy oved, Humberto, JABO, Jarfil, Jarisleif, Javierito92, Jkbw, Jorge c2010, Kurtan, Kvnbarragan, Laura Fiorucci, Leonpolanco, Leugim1972, Linux65, Lucien leGrey, MadriCR, Magister Mathematicae, Maldoror, Manuelt15, Manw, MarcoAurelio, Matdrodes, Mel 23, Montgomery, Mortadelo2005, Mr.Ajedrez, Mushii, Netito777, Nicop, Nioger, Obelix83, Ortisa, Oscar ., Pan con queso, Pedro Nonualco, Perez17, Plux, Queninosta, Raulshc, Rodolfo Javier Buitrago Holmquist, RoyFocker, Rubpe19, Rudolph, Rge, Saloca, Savh, Sebrev, Snakeyes, Soulreaper, SuperBraulio13, Superzerocool, Technopat, Tigerfenix, Tirithel, Tomatejc, Tothinio, Travelour, Truor, UA31, Vic Fede, Vitamine, Waka Waka, Xoacas, Yeza, 562 ediciones annimas
Fuentes de imagen, Licencias y contribuyentes
Archivo:A New System of Chemical Philosophy fp.jpg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:A_New_System_of_Chemical_Philosophy_fp.jpg Licencia: Public Domain Contribuyentes: haade Archivo:JJ Thomson exp2.png Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:JJ_Thomson_exp2.png Licencia: Public Domain Contribuyentes: Kurzon Image:Gold foil experiment conclusions.svg Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Gold_foil_experiment_conclusions.svg Licencia: Public Domain Contribuyentes: Kurzon Archivo:Modelo de Bohr.png Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Modelo_de_Bohr.png Licencia: GNU Free Documentation License Contribuyentes: Belfer00, Hidaspal, Pilaf Archivo:neon orbitals.JPG Fuente: http://es.wikipedia.org/w/index.php?title=Archivo:Neon_orbitals.JPG Licencia: Public Domain Contribuyentes: Benjah-bmm27, Mortadelo2005, 1 ediciones annimas
Licencia
Creative Commons Attribution-Share Alike 3.0 Unported //creativecommons.org/licenses/by-sa/3.0/
También podría gustarte
- Qué Es El VerboDocumento5 páginasQué Es El Verbojuva2000-1100% (2)
- Cuadro de Las Funciones Yoicas Segun L BellakDocumento1 páginaCuadro de Las Funciones Yoicas Segun L Bellakpsicologos91189% (19)
- Escritos Del Último CriolloDocumento205 páginasEscritos Del Último CriolloDefensor ArcanoAún no hay calificaciones
- School Brass 2Documento13 páginasSchool Brass 2my domp100% (1)
- La LocomotoraDocumento11 páginasLa LocomotoraBrenda DíazAún no hay calificaciones
- Febrero Planeacion AdaptaciónDocumento52 páginasFebrero Planeacion AdaptaciónNathalyAún no hay calificaciones
- Analisis de Caso Bimbo Una Empresa RespDocumento4 páginasAnalisis de Caso Bimbo Una Empresa RespDaniel SCAún no hay calificaciones
- Mate 4Documento4 páginasMate 4Cielo Gonzales HAún no hay calificaciones
- Modelo Kaizen para La Solución de Problemas - V5Documento86 páginasModelo Kaizen para La Solución de Problemas - V5Edwin DZAún no hay calificaciones
- Normas para La Descripción de Vasijas Cerámicas - Capítulo II. Términos TécnicosDocumento20 páginasNormas para La Descripción de Vasijas Cerámicas - Capítulo II. Términos TécnicosHerber Cahuana SegoviaAún no hay calificaciones
- Nutrición y Dieta para Diabetes y Problemas de Tiroides - Nutrición y SaludDocumento3 páginasNutrición y Dieta para Diabetes y Problemas de Tiroides - Nutrición y SaludLuis GalvezAún no hay calificaciones
- DIBUJOnDEnINGENIERnnAnv21 76608b4b4eda086Documento391 páginasDIBUJOnDEnINGENIERnnAnv21 76608b4b4eda086Jaider Calderon BarreraAún no hay calificaciones
- Lab1-Doblador y EnclavadorDocumento3 páginasLab1-Doblador y Enclavadormeeduma67% (3)
- Anexo-A NUESTRO PADRE CREADOR TÚPAC AMARUDocumento3 páginasAnexo-A NUESTRO PADRE CREADOR TÚPAC AMARUabrahanmauriciosahuaAún no hay calificaciones
- Modelo de Acta Constitutiva de Asociación Cooperativa AgrícolaDocumento10 páginasModelo de Acta Constitutiva de Asociación Cooperativa AgrícolaEnder PiñaAún no hay calificaciones
- El Pie Diabético Ulcerado, Un Desafío Aún en El Siglo XXIDocumento5 páginasEl Pie Diabético Ulcerado, Un Desafío Aún en El Siglo XXIadreadnalinaAún no hay calificaciones
- Caracterizacion de Proceso Control Interno DisciplinarioDocumento5 páginasCaracterizacion de Proceso Control Interno DisciplinarioCAROLINAAún no hay calificaciones
- Axiomas de La ComunicaciónDocumento21 páginasAxiomas de La ComunicaciónCAROLINA AGUILAR BEDOYAAún no hay calificaciones
- Día de Los Difuntos-1Documento6 páginasDía de Los Difuntos-1Karla GuachaminAún no hay calificaciones
- CuentoDocumento4 páginasCuentokenia lindaoAún no hay calificaciones
- Eval 3 FGL-144 (IND-GRP)Documento9 páginasEval 3 FGL-144 (IND-GRP)Sebastián R. DuránAún no hay calificaciones
- Cómo Orientamos El Proceso de Apropiación Del Código Escrito en Lengua Originaria Como Lengua MaternaDocumento64 páginasCómo Orientamos El Proceso de Apropiación Del Código Escrito en Lengua Originaria Como Lengua MaternacamilaAún no hay calificaciones
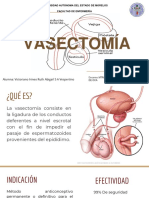
- VASECTOMÍADocumento9 páginasVASECTOMÍARuth Abigail Victoriano IrineoAún no hay calificaciones
- Organigrama Septiembre 14 de 2020Documento17 páginasOrganigrama Septiembre 14 de 2020Andrea Hernández MAún no hay calificaciones
- Fijacion de MuestrasDocumento8 páginasFijacion de MuestrasSabina MelloAún no hay calificaciones
- Mapa Conceptual 2Documento1 páginaMapa Conceptual 2Juan LopezAún no hay calificaciones
- Actividad 4 Evidencia 2Documento3 páginasActividad 4 Evidencia 2laura liliana perez salazarAún no hay calificaciones
- Allanamiento de MoradaDocumento6 páginasAllanamiento de MoradaDannylitow Lopez50% (2)
- Características de Los Fluidos Reales e IdealesDocumento24 páginasCaracterísticas de Los Fluidos Reales e IdealesHrnanDz IsaacAún no hay calificaciones
- Evidencia 2 Actividad No. 23Documento10 páginasEvidencia 2 Actividad No. 23Jose Luis Gonzalez100% (3)