Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Reactor de Acido Sulfurico
Cargado por
Doriannys Subero Rivadulla0 calificaciones0% encontró este documento útil (0 votos)
255 vistas10 páginasDerechos de autor
© Attribution Non-Commercial (BY-NC)
Formatos disponibles
DOCX, PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Attribution Non-Commercial (BY-NC)
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
255 vistas10 páginasReactor de Acido Sulfurico
Cargado por
Doriannys Subero RivadullaCopyright:
Attribution Non-Commercial (BY-NC)
Formatos disponibles
Descargue como DOCX, PDF, TXT o lea en línea desde Scribd
Está en la página 1de 10
14.1.
5 Ejemplo: Oxidacin de dixido de azufre
1. Produccin de cido sulfrico.
En la produccin de cido sulfrico a partir de azufre, el primer paso es la
combustin de azufre para producir dixido de azufre:
S + O
2
SO
2
Posteriormente el SO
2
se convierte en trixido de azufre, utilizando un catalizador:
SO
2
+ 1/2O
2
SO
3
En la Fig. 1 se muestra un diagrama de flujo de una planta de produccin de cido
sulfrico por el mtodo de contaco. Es el convertidor el que vamos a tratar en este
problema.
Aunque el catalizador de platino de ha utilizado en la produccin de cido sulfrico,
es el vanadio soportado el nico catalizador que se utiliza hoy en da en su produccin.
Para nuestro problema utilizaremos el catalizador estudiado por Eklun, cuyo trabajo fue
seguido de forma extensa por Donovan en su descripcin de la cintica de oxidacin del
SO
2
. El catalizador estudiado por Eklun fue en catalizador soportado de V
2
0
5
. Las
partculas catalticas de forma cilndrica tenan un dimetro de 8 mm y una longitud de
8 mm, con una densidad de 33.8 lb/ft
3
. Entre 818 y 1029 F, la ley de velocidad para la
oxidacin de SO
2
sobre este catalizador en particular fue:
Ec. 1
en la que P
i
es la presin parcial de la especie i. Esta ecuacin se puede utilizar
cuando la conversin es superior al 5%. Para el resto de conversiones superiores al 5%,
la velocidad es esencialmente la correspondiente al 5% de conversin.
En el proceso de produccin de cido sulfrico se utilizan diferentes tipos de
reactores. Quizs el tipo ms comn es el reactor dividido en diferentes secciones
adiabticas con enfriamiento entre ellas (ver Fig. 2). Otro tipo de reactor est dispuesto
con tubos de enfriamiento embebidos en la mezcla de reaccin. El reactor que se
muestra en la Fig. 3 utiliza gas entrante para enfriar la mezcla de reaccin. En el proceso
de la Fig. 3, el gas se saca del convertidor para ser enfriado entre etapas, utilizndolo
para recalentar la caldera de agua, producir vapor, superheat vapor, y recalentar el gas
fro, todo ello para incrementar la eficiencia energtica del proceso.
Una tpica planta de produccin de cido sulfrico de los aos 70 produce entre 1000
y 2400 toneladas de cido sulfrico el da. Utilizando los nmeros de Kastens y
Hutchinson, una planta que produce 1000 ton/da de cido sulfrico tiene una
alimentacin de SO
2
en el convertidor de 7900 lb mol/h, consistente en 11% SO
2
, 19%
O
2
Y 79% en inertes (principalmente N
2
). Utilizaremos estos valores para desarrollar el
problema.
Vamos a calcular la conversin de reaccin para dos situaciones diferentes y
posteriormente compararemos los resultados obtenidos:
a) El primer caso se refiere a un reactor de lecho fijo cataltico cilndrico, con sus
paredes enfriadas a temperatura constante por un lquido hirviendo.
b) El segundo caso hace referencia a un reactor comercial adiabtico en dos etapas.
2. Cantidades de catalizador
Harrer afirma que la velocidad de flujo volumtrico en un convertidor adiabtico de
SO
2
, medida en condiciones normales de presin y temperatura, es normalmente
alrededor de 75 a 100 ft
3
/min ft
2
de rea de convertidor. Tambin afirma que el lecho de
catalizador en el converidor debe ser entre 20 y 50 in de profundidad.
Es conveniente utilizar una velocidad msica baja a travs del lecho para minimizar
los requerimientos de energa, por lo que utilizaremos un valor de 75 ft
3
/min ft
2
.
Normalmente en convertiddores adiabticos se consiguen conversiones del 70% en la
primera etapa y una conversin adicional del 18% en la segunda. Utilizando el
catalizador del trabajo de Eklun, para estas conversiones se requiere 1550 ft
3
(23 in de
profundidad de lecho) en la primera etapa y 2360 ft
3
(35 in de profundidad de lecho) en
la segunda. Atendiendo a estos resultados, en nuestro reactor tubular refrigerado,
utilizaremos un volumen total de catalizador de 3910 ft
3
.
3. Configuracin del reactor
El catalizador se dispone en tubos, y los tubos se colocan en intercambiadores donde
se enfriarn por un lquido a ebullicin. El dimetro exterior de los tubos ser de 3 in.
Se han observado severos gradientes de temperatura en la oxidacin de SO
2
, aunque
estos sistemas utilizaban platino como catalizador y se desarrollaron en condiciones
destintas a las consideradas aqu. El tubo de 3 in de dimetro se ha tomado como
compromido entre la minimizacin de los posibles gradientes de temperatura y el
mantenimiento de un nmero de tubos bajo. Para este propsito se han elegido tubos de
0.109 in de espesor y un dimetro interno de 2.782 in. Se utilizarn tubos de 20 ft de
longitud, como compromiso entre la disminucin de los requerimientos de
energa(tubos de pequea longitud) y la disminucin de los costes de material(pocos
tubos de gran longitud). Para un total de catalizador de 3910 ft
3
, el nmero de tubos que
se requerir ser de:
Ec
. 2
El rea transversal total de los tubos es:
Ec. 3
El coeficiente global de transferencia de calor entre la mezcla de reaccin gaseosa y
el lquido hirviendo se toma como 10 Btu/h ft
2
F. Este valor est cerca del lmite
superior del rango de coeficientes de transferencia de calor para estas situaciones tal
como lo describen Colburn y Bergelin.
4. Condiciones de operacin.
Los convertidores de dixido de azufre operan a presiones slo ligeramente
superiores a la atmosfrica. Utilizaremos una presin absoluta de 2 atm en nuestros
diseos. La temperatura de entrada al reactor se ajustar de forma que obtengamos la
mxima conversin. Introduciremos ahora dos restricciones.
La velocidad del catalizador de V
2
O
3
es despreciable por debajo de
aproximadamente 750 F, y la temperatura del reactor no debe exceder de 125 F
aproximadamente en ningn punto. Es necesario ensayar una serie de temperaturas de
entrada, y aquella que por encima de 760 F de la mxima conversin, sin que el reactor
nunca exceda de 1120 C, ser la adecuada pra llevar a cabo la reaccin.
La sustancia utilizada como refrigerante debe operar a elevada temperatura, con el fin
de mejorar la eficiencia trmica. La sustancia ms adecuada parece ser el Dowtherm A,
con una temperatura de ooperacin lmite de aproximadamente 750 F.
Utilizando los valores de JANAF para la Kp a 700 y 900 K, la conversin de
equilibrio a cualquier temperatura T tiene la expresin:
Ec. 4
(Kp en atm
-1/2
, T en R)
A 1600 R,
Kp = 7.8 atm
-1/2
Para la constante de velocidad, los datos de Eklun se pueden correlacionar muy bien
mediante la ecuacin:
Ec. 5
(k en lb mol SO
2
/lb cat s atm, t en R)
Existen efectos difusionales presentes en el catalizador a las temperaturas de trabajo,
y la Ec. 5 se puede interpretar como una ecuacin emprica que predice la constante de
velocidad de reaccin efectiva en el rango de temperaturas indicadas por Donovan(entre
815 y 1138 F).
De las tablas JANAF se pueden obtener los valores de las capacidades calorficas y la
entalpa de reaccin de los compuestos que intervienen en la reaccin.
AH
R
(800 F) = -42471 Btu/lb mol
SO
2
Ec. 6
Cp
SO3
= 7.208 + 5.633x10
-3
T - 1.343x10
-6
T
2
Ec. 7
Cp
O
= 5.731 + 2.323x10
-3
T - 4.886x10
-7
T
2
Ec. 8
Cp
SO3
= 8.511 + 9.517x10
-3
T - 2.325x10
-6
T
2
Ec. 9
Cp
N2
= 6.248 + 8.778x10
-4
T - 2.13x10
-8
T
2
Ec. 10
5. Procedimiento general de diseo del reactor
El procedimiento general de diseo que vamos a desarrollar para llevar a cabo el
diseo del reactor estar constituido de las siguientes etapas:
a. Aplicacin de la ecuacin de diseo de un reactor de flujo pistn, para
relacionar el peso de catalizador,velocidad de reaccin y conversin.
Utilizaremos las relaciones estequiomtricas y las condiciones de
alimentacin especificadas para expresar la ley de velocidad como
funcin de la conversin.
b. Aplicacin del balance de energa, para establecer la relacin entre el
peso de catalizador y la temperatura.
c. Utilizacin de la ecuacin de Ergun, para calcular la cada de presin
como funcin del peso de catalizador.
d. Establecer los valores apropiados para las variables del sistema (k,
Kp,AH
R
(T
R
),Cpi,...) y sus correspondientes dependencias con la
temperatura para poder llevar a cabo los clculos correspondientes.
e. Integrar numricamente la ecuacin de diseo, balance de energa y
ecuacin de Ergun de forma simultnea, para determinar la conversin y
temperatura de salida asa como los perfiles de concentracin.
5.1 Ecuacin de diseo
La ecuacion del balance molar general, en su forma diferencial (ecuacin de diseo),
basada en el peso de ctalizador se expresa segn la ecuacin:
Ec. 11
5.2 Ley de velocidad
La ley de velociadad propuesta por Eklun, como ya indic anteriormente, tiene la
expresin:
5.3 Relaciones estequiomtricas. Expresin de como funcin de la conversin,X.
La relacin que tiene lugar en el convertidor es:
Si A representa la especie SO2, y vi el coeficiente estequiomtrico de la especie i,
podemos escribir
Ec. 12
sustituyendo las presiones parciales de cada una de las especies con la Ec. 12 en la
ecuacin de velocidad, Ec. 1, y combinando el resultado con la Ec. 11, obtenemos la
siguiente expresin:
Ec
.
13
donde
c = -0.055
P
A0
= 0.22 atm
u
SO2
= 1.0
u
O2
= 0.91
u
SO3
= 0.0
u
N2
= 7.17
F
T0
= 7900 lb mol/h
F
A0
= 869 lb mol/h
Por tubo tendremos:
peso de catalizador en un tubo = W =
c
tD
2
L/4 = 28.54 lb cat/tubo
F
A0
= 869/4631 = 0.188 lb mol/h tubo
Sustituyendo los valores obtenidos en la Ec. 13 se obtiene:
Ec.
14
es decir, obtenemos una ecuacin diferencial de la forma:
Ec. 15
Los lmites de integracin irn desde cero hasta el peso de catalizador en un
tubo,28.54 lb.
5.4 Balance de energa
Para una operacin en estado estacionario y despreciando el trabajo shaft work , el
balance de energa expresado en trminos del peso de catalizador toma la siguiente
expresin:
Ec. 16
5.5 Evaluacin de los parmetros del balance de energa.
Calor de reaccin
AH
R
(T) = AH
o
R
(T
R
) + Ao(T-T
R
) + A|/2(T
2
-
T
2
R
) + A/3(T
3
-T
3
R
)
Ec. 17
Para la oxidacin del
SO
2
,
Ao = o
SO3
- 1/2o
O2
- o
SO2
= 8.511 - (0.5)(5.731) - 7.208 = -1.563
de forma similar se obtiene,
A
|
= 0.00273
A
= 0.738*10
6
Sustituyendo los valores obtenidos en la Ec. 16 teniendo en cuenta que T
R
= 1260 R,
tenemos que:
AH
R
(T) = 42471 -
(1.563)(T-1260) +
(1.36x10
-3
)(T
2
-
1260
2
)-(2.459x10
-
7
)(T
3
-1260
3
)
Ec.18
(AH
R
en Btu/lb ml, T en R)
Ec. 19
Trmino correspondiente al coeficiente de transmisin de calor
Sustituyendo los valores obtenidos en la Ec. 15, correspondiente al balance de
energa, obtenemos:
Ec. 20
es decir, obtenemos una ecuacin diferencial con la siguiente funcionalidad
Ec. 21
5.6 Cada de presin a traves del lecho
Para calcular la cada de presin a travs del lecho, vamos a considerar la ecuacin de
Ergun, que tiene la siguiente expresin:
donde
;(M
i
= peso molecular de la especie i)
G = 1307.6 lb/ft
2
h
A
c
= rea de la seccin transversal del tubo, tD
2
/4
Teniendo en cuenta que:
W =
c
A
c
L
podemos expresar la expredin anteror correspondiente a la cada de presin en funcin
del peso de catalizador, en lugar de la distancia del reactor,L.
Ec. 22
Como la viscosidad de la fase gaseosa es una funcin dbil de la temperatura,
vamos a considerar que la viscosidad es independiente de la temperatura. Al igual que
anteriormente, hemos llegado hasta una ecuacin diferencial con la siguiente
funcionalidad:
Ec. 23
5.7 Evaluacin de los parmetros de la cada de presin
Sustituyendo los valores adecuados en la Ec. 21 obtenemos:
Ec. 24
Vamos a estimar un orden de magnitud para la cada de presin. Para obtener esta
estimacin, vamos a considerar que la reaccin se lleva a cabo isotrmicamente con c =
0,
Integrando entre los lmites
P
0
= 2 atm en W = 0 y P = P en W = 28.54 lb de catalizador, se otiene:
(p
2
-4)/2 = -0.0432(0-28.54)/p>
P = 1.239 atm ; AP = 2-1.24 = 0.76 atm
5.8 Procedimiento de solucin
Tenemos tres ecuaciones diferenciales acopladas que tendremos que resolver de
forma simultnea:
Balance
molar
Ec. 15
Balance de energa
Ec. 21
Balance de presin
Ec. 23
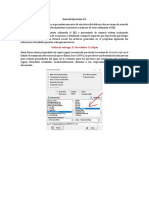
Para llevar a cabo la solucin de este sistema de tres ecuaciones diferenciales,
haremos uso del simulador ISIM. Desarrollaremos a continuacin el procedimiento
numrico general para el clculo del reactor y pposteriormente veremos cmo, con la
ayuda de ISIM, la solucin del problema se simplifica notablemente.
5.8 Procedimiento numrico general
La velocidad de reaccin es independiente de la conversin entre X = 0.0 y X =
0.005 y la velocidad de desaparicin de SO
2
en el rango de conversiones anterior ser
igual a la velocidad de reaccin a X = 0.05, es decir:
Ec. 25
Los pasos a seguir sern los siguientes:
1. Dar los valores de X = 0.00, T = T
0
y P = P
0
2. Calcular k de la Ec. 5
3. Calcular Kp de la Ec. 4
4. Si X<0.05,
calcular
de la Ec. 25. Si X>0.05,
calcular
de la Ec. 1
5. Calcular f
1
(X, T, P), f
2
(X, T, P), f
3
(X, T, P) de las ecuaciones 15, 21 y 23
respectivamente
6. Calcular x, T y P numricamente por medio de las expresiones
También podría gustarte
- Termonidamica de Gases y VaporesDocumento54 páginasTermonidamica de Gases y VaporesGenaro Jauregui67% (12)
- Ejercicios de Ciclos TermodinámicosDocumento30 páginasEjercicios de Ciclos TermodinámicosReed Daniels89% (56)
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Simulación Reactor Lecho para Producir Anhídrido MaleicoDocumento6 páginasSimulación Reactor Lecho para Producir Anhídrido MaleicoLuis Jesús Díaz ManzoAún no hay calificaciones
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSDe EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Actividad 1 React EspañolDocumento4 páginasActividad 1 React Españolsamara navasAún no hay calificaciones
- Cantidad de Calor y Capacidad CaloríficaDocumento5 páginasCantidad de Calor y Capacidad CaloríficaMartin Ac100% (1)
- Ejercicios del Capítulo 8 de Fogler - Problema 4: Explosión de nitrato de amonioDocumento57 páginasEjercicios del Capítulo 8 de Fogler - Problema 4: Explosión de nitrato de amonioKarina100% (2)
- Ejercicios de EvaporacionDocumento2 páginasEjercicios de EvaporacionErick Joel Loayza AraujoAún no hay calificaciones
- Proceso de Extracción de La PlataDocumento19 páginasProceso de Extracción de La Platajose daniel ramirezAún no hay calificaciones
- Ejercicios Disoluciones ChangDocumento8 páginasEjercicios Disoluciones Changsgpizarro20% (5)
- Informe de ReactoresDocumento15 páginasInforme de ReactoresCarlos A. GomezAún no hay calificaciones
- Calculos So2Documento10 páginasCalculos So2MichaelAún no hay calificaciones
- Taller 1 Oxidacion de Dioxido de AzufreDocumento8 páginasTaller 1 Oxidacion de Dioxido de AzufreAlejandro MatsonAún no hay calificaciones
- Problemaanhidridoftalico 15470Documento3 páginasProblemaanhidridoftalico 15470CarlosAlfonsoRiosAlanisAún no hay calificaciones
- TP 6 Tecnología Del CalorDocumento4 páginasTP 6 Tecnología Del CalorMilagros FornesAún no hay calificaciones
- Disen - o de Reactores ProblemasDocumento5 páginasDisen - o de Reactores ProblemasEvanStoneAún no hay calificaciones
- Guía Extraordinario TMTDocumento6 páginasGuía Extraordinario TMTheber mollinedoAún no hay calificaciones
- Cinetica IIDocumento4 páginasCinetica IILeo Sandro Huaman PachecoAún no hay calificaciones
- Calentadores de JugoDocumento12 páginasCalentadores de JugoLissette Jeri Amao100% (5)
- Capitulo 22Documento26 páginasCapitulo 22AgustinVenturaAún no hay calificaciones
- Diseño de Procesos - Manual de ApoyoDocumento13 páginasDiseño de Procesos - Manual de ApoyoDiana Catalina Molano BayonaAún no hay calificaciones
- Segunda Ley Termodinamica Pares-DeberDocumento19 páginasSegunda Ley Termodinamica Pares-DeberWendy Dávila Arteaga33% (3)
- Trabajo Completo Sintesis de AmoniacoDocumento77 páginasTrabajo Completo Sintesis de Amoniacoleynisg67% (6)
- Edoc - Tips Cantidad de Calor y Capacidad CaloraficaDocumento5 páginasEdoc - Tips Cantidad de Calor y Capacidad CaloraficaJimmy Vargas ArteagaAún no hay calificaciones
- Problemas de TermoDocumento8 páginasProblemas de Termomisterio32133% (3)
- Cinética Del Soplado A Cobre en Un Convertidor PeirceDocumento10 páginasCinética Del Soplado A Cobre en Un Convertidor Peircefabi721Aún no hay calificaciones
- Discusion 5Documento3 páginasDiscusion 5elbetoavila0% (2)
- Termodinámica II - Ciclo de potencia de vapor y ciclo de refrigeración por compresión de vaporDocumento2 páginasTermodinámica II - Ciclo de potencia de vapor y ciclo de refrigeración por compresión de vaporHenry OjedaAún no hay calificaciones
- Guía N°3-EESDocumento4 páginasGuía N°3-EESAlan PérezAún no hay calificaciones
- Guia 4 Ppios 1 (Balance de Energía Sin Reacción)Documento6 páginasGuia 4 Ppios 1 (Balance de Energía Sin Reacción)carlos hernandezAún no hay calificaciones
- TT 2023-1S TALLER C Ejercicios Segunda Ley ProcesosDocumento4 páginasTT 2023-1S TALLER C Ejercicios Segunda Ley ProcesosNicolas Torres0% (1)
- Guía de Aprendizaje - Ley I de Termodinámica Sistema Abiertos EstacionariosDocumento8 páginasGuía de Aprendizaje - Ley I de Termodinámica Sistema Abiertos EstacionariosDaniela TorresAún no hay calificaciones
- Guia n3 Ejercicios TermodinamicaDocumento6 páginasGuia n3 Ejercicios TermodinamicaArriarán Camila ConstanzaAún no hay calificaciones
- Practico 2010Documento11 páginasPractico 2010Jose Leobardo Santiago GonzalezAún no hay calificaciones
- EntropíaDocumento4 páginasEntropíaROXAS PLAYAún no hay calificaciones
- Proyecto Final de SimulacionDocumento11 páginasProyecto Final de SimulacionRichard RondónAún no hay calificaciones
- Trabajo Práctico #5Documento4 páginasTrabajo Práctico #5Carli CastilloAún no hay calificaciones
- Inter Cambi AdoresDocumento4 páginasInter Cambi AdoresZarai GarciaAún no hay calificaciones
- Diapositiva 4 CSTR SeguridadDocumento56 páginasDiapositiva 4 CSTR SeguridadDENIS LEYVAAún no hay calificaciones
- Ejercicios Capitulo 8Documento7 páginasEjercicios Capitulo 8Emmanuel CarciniAún no hay calificaciones
- Termodinamica EjerciciosDocumento17 páginasTermodinamica Ejerciciosjose.perezgomez54Aún no hay calificaciones
- termodinamica capitulo 7Documento10 páginastermodinamica capitulo 7p4gkpmpjz8Aún no hay calificaciones
- Ciclo Rankine Ejercicios ResueltosDocumento7 páginasCiclo Rankine Ejercicios ResueltosJorge OlacheaAún no hay calificaciones
- GIM IT Problemas Cap3 Análisis EntrópicoDocumento5 páginasGIM IT Problemas Cap3 Análisis EntrópicoSergio Alberto Fajardo SantanaAún no hay calificaciones
- Columnas de DestilaciónDocumento19 páginasColumnas de DestilaciónToño MzAraizaAún no hay calificaciones
- Balances de Energía. Visión General Del Tema.Documento20 páginasBalances de Energía. Visión General Del Tema.ADRIANA LUCIA GONZALEZ LEONAún no hay calificaciones
- Serie1 10357 PDFDocumento2 páginasSerie1 10357 PDFahsimAún no hay calificaciones
- Lista de Ejercicios Be-2022-1Documento2 páginasLista de Ejercicios Be-2022-1Josselyn GrimaldoAún no hay calificaciones
- Final 2 PracticaDocumento20 páginasFinal 2 PracticamarianaAún no hay calificaciones
- Problemario de Ingeneria de ReactoresDocumento32 páginasProblemario de Ingeneria de ReactoresJavier Benítez100% (1)
- Ejercicicios de Intercambiadores de Calor (Operaciones Unitarias)Documento3 páginasEjercicicios de Intercambiadores de Calor (Operaciones Unitarias)Theo AltuveAún no hay calificaciones
- Enl 5Documento5 páginasEnl 5Herlin Velasquez AguilarAún no hay calificaciones
- Guia Reactores No IsotérmicosDocumento4 páginasGuia Reactores No IsotérmicosAlexContrerasFonseca0% (1)
- EjerciciosEntregables22 23Documento4 páginasEjerciciosEntregables22 23Fabio Alfaro DiazAún no hay calificaciones
- Taller Intercambiadores 201801Documento5 páginasTaller Intercambiadores 201801David ParradoAún no hay calificaciones
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- El Mejor Libro de Preparación Para Tu Examen De Licencia De Operador De CalderaDe EverandEl Mejor Libro de Preparación Para Tu Examen De Licencia De Operador De CalderaAún no hay calificaciones
- Flujo de fluidos e intercambio de calorDe EverandFlujo de fluidos e intercambio de calorCalificación: 1 de 5 estrellas1/5 (1)
- Eficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108De EverandEficiencia energética en las instalaciones de calefacción y acs en los edificios. ENAC0108Aún no hay calificaciones
- Entropía Diferencial para Distribuciones ContinuasDocumento6 páginasEntropía Diferencial para Distribuciones ContinuasEduardo Franco Sotelo BazanAún no hay calificaciones
- Practica 1 Molienda y Tamizado PDFDocumento10 páginasPractica 1 Molienda y Tamizado PDFElvis Amerlin Condori Ch.Aún no hay calificaciones
- Informe de EstaticaDocumento2 páginasInforme de Estaticajorge_capri_97Aún no hay calificaciones
- Líneas de TransmisiónDocumento7 páginasLíneas de TransmisiónRoa Revolledo JhonchitoAún no hay calificaciones
- Estado Del Arte Modelacion Probabilista Del RiesgoDocumento140 páginasEstado Del Arte Modelacion Probabilista Del RiesgoReynaldo Reyes RoqueAún no hay calificaciones
- Cajas de distribución PES para concentración de medidoresDocumento18 páginasCajas de distribución PES para concentración de medidoresJv Omar SaYsAún no hay calificaciones
- Ejercicios Quimica OrganicaDocumento4 páginasEjercicios Quimica OrganicaHaydee Zapata Lpda0% (1)
- Informe de Lab. Circuitos II - Corrección Del Factor de PotenciaDocumento10 páginasInforme de Lab. Circuitos II - Corrección Del Factor de PotenciaMontalvo Cavides GerbertAún no hay calificaciones
- Puntos Cardinales CartesianosDocumento5 páginasPuntos Cardinales CartesianosPeter AlorAún no hay calificaciones
- FS3Documento20 páginasFS3Alejandra Miranda DíazAún no hay calificaciones
- P. Circunferencia 7°Documento3 páginasP. Circunferencia 7°Benji Zapata TorresAún no hay calificaciones
- Informe LimitesDocumento15 páginasInforme LimiteswilsonAún no hay calificaciones
- Estequiometria LaboratorioDocumento6 páginasEstequiometria LaboratorioGerson de la CruzAún no hay calificaciones
- Fig 5semGIDocumento22 páginasFig 5semGIluis camargoAún no hay calificaciones
- Anders CelsiusDocumento10 páginasAnders Celsiuslocosebas_23Aún no hay calificaciones
- Solucionario Boletin 8 Ciclo AnualDocumento15 páginasSolucionario Boletin 8 Ciclo AnualCharlieAún no hay calificaciones
- Caratulas PucpDocumento19 páginasCaratulas PucpStewart Lopez OtinianoAún no hay calificaciones
- Capitulo 22 Apnb 777 PDFDocumento3 páginasCapitulo 22 Apnb 777 PDFelrojoerik100% (1)
- Análisis de Iluminación UniformeDocumento15 páginasAnálisis de Iluminación UniformeFernando MagosAún no hay calificaciones
- 3.5 - Cond. Cu Protegido CPIDocumento6 páginas3.5 - Cond. Cu Protegido CPIJherson Quispe ChavezAún no hay calificaciones
- NitrotiofenoDocumento3 páginasNitrotiofenoGaby RodriguezAún no hay calificaciones
- Exámenes FyQ 3º ESODocumento62 páginasExámenes FyQ 3º ESOJuan Carlos Rodríguez Pérez100% (1)
- Diseno Ventilador Axial 0 25 HPDocumento15 páginasDiseno Ventilador Axial 0 25 HPFrancisco LaraAún no hay calificaciones
- Tarea1 Quimica General UnadDocumento26 páginasTarea1 Quimica General UnadFabian Mejia33% (6)
- Industria Del Cemento GGDocumento17 páginasIndustria Del Cemento GGDeyby Gutierrez SosaAún no hay calificaciones
- Fisica Mru AslyDocumento15 páginasFisica Mru AslyDanferSernaqueIman100% (1)
- Cotamanía - Vectores PDFDocumento3 páginasCotamanía - Vectores PDFGermain VilcapazaAún no hay calificaciones
- Conservación de La Energía en La Caída LibreDocumento3 páginasConservación de La Energía en La Caída LibrePedro Ibarbo PerlazaAún no hay calificaciones