Documentos de Académico
Documentos de Profesional
Documentos de Cultura
9412 Tarea 01
Cargado por
Jose Carlos GonzalezDescripción original:
Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
9412 Tarea 01
Cargado por
Jose Carlos GonzalezCopyright:
Formatos disponibles
Universidad de Sonora
Departamento de Ingenierı́a Quı́mica y Metalurgia
Termodinámica II (9412)
Tarea 1
Lee con atención el caso1 que se presenta a continuación y después realiza lo que se solicita.
Un metro cúbico de un gas ideal a 600 K y 1000 kPa se expande hasta alcanzar cinco veces su
volumen inicial mediante dos maneras: (a) por un proceso adiabático mecánicamente reversible
y (b) por un proceso adiabático irreversible en el cual la expansión se hace contra una presión
de frenado de 100 kPa. CP = 21 J mol−1 K−1 .
1. [5 puntos] Calcula el trabajo asociado al proceso (a) en kJ.
2. [10 puntos] Calcula el trabajo asociado al proceso (b) en kJ.
3. [5 puntos] Explica por qué el trabajo del proceso (a) es mayor que el del proceso (b).
Lee con atención el caso2 que se presenta a continuación y después realiza lo que se solicita.
Un recipiente rı́gido con un volumen de 0.06 m3 contiene un gas ideal CV = (5/2)R a 500 K y
1 bar.
4. [20 puntos]Calcula el cambio de entropı́a del gas en J/K, si se le transfieren 7500 J de
calor.
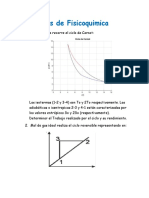
5. [10 puntos] Dibuja la trayectoria seguida por el sistema en un diagrama P T , si la trans-
ferencia de calor ocurre de manera reversible.
Lee con atención el caso3 que se presenta a continuación y después realiza lo que se solicita.
Se tiene un ciclo reversible en el que participa un mol de gas ideal para el que CP = (5/2)R.
Al inicio el gas se encuentra a T1 = 700 K y P1 = 1.5 bar. Enseguida, el gas se enfrı́a a presión
constante hasta T2 = 350 K. Después, se comprime isotérmicamente hasta la presión P3 . El gas
regresa a su estado original a lo largo de una trayectoria donde el producto P T es constante.
6. [20 puntos] Dibuja los procesos del ciclo en un diagrama P V .
7. [10 puntos] Calcula el cambio de entropı́a en J/K de la reserva térmica (alrededores) en
contacto con el sistema en el proceso isotérmico.
8. [20 puntos] Calcula el valor de la eficiencia térmica4 del ciclo.
1
Adaptado del problema 3.29, SVNAS 8.a
2
Adaptado del problema 5.9, SVNAS 8.a
3
Adaptado del problema 5.25, SVNAS 8.a
4
Se define como el cociente del valor absoluto del trabajo neto del ciclo entre el calor suministrado.
También podría gustarte
- 2-Practica Calificada FTA 2019-IDocumento7 páginas2-Practica Calificada FTA 2019-IMarco Antonio100% (1)
- NNNMDocumento13 páginasNNNMredyz huamanAún no hay calificaciones
- Problemario de Ingeneria de ReactoresDocumento32 páginasProblemario de Ingeneria de ReactoresJavier Benítez100% (1)
- Primer Taller 1-2011Documento8 páginasPrimer Taller 1-2011China LqmAún no hay calificaciones
- Trabajo Práctico #5Documento4 páginasTrabajo Práctico #5Carli CastilloAún no hay calificaciones
- Hoja 3Documento3 páginasHoja 3Jony GarciaAún no hay calificaciones
- Enunciados Ejercicios Entregados en Clase Examen 1Documento6 páginasEnunciados Ejercicios Entregados en Clase Examen 1Jennifer YataAún no hay calificaciones
- Hoja 1 NewDocumento3 páginasHoja 1 NewJony GarciaAún no hay calificaciones
- Guia de Problemas - Capitulo 5Documento17 páginasGuia de Problemas - Capitulo 5Víctor Vázquez0% (1)
- MMMMMDocumento3 páginasMMMMMCristina GranizoAún no hay calificaciones
- H3-EFECTOS - TERMICOS - EN - REACTORES - IDEALES-2014-2015 CampusDocumento5 páginasH3-EFECTOS - TERMICOS - EN - REACTORES - IDEALES-2014-2015 CampusCenaida ColinaAún no hay calificaciones
- Examenes Finales TermodinamicaDocumento34 páginasExamenes Finales TermodinamicaMafer Mabel GalarzaAún no hay calificaciones
- Actividad 3-2 ProblemarioDocumento3 páginasActividad 3-2 ProblemarioKenia SegoviaAún no hay calificaciones
- Parctica 2 2p-2Documento4 páginasParctica 2 2p-2Noel Condori100% (1)
- Ejercicios Propuesto TermodinámicaDocumento12 páginasEjercicios Propuesto TermodinámicaPilar UsonAún no hay calificaciones
- Xdoc - MX Termodinamica Guzlop EditorasDocumento10 páginasXdoc - MX Termodinamica Guzlop Editorasnewton bardajesAún no hay calificaciones
- Serie de Problemas2 - Termo-MasterDocumento3 páginasSerie de Problemas2 - Termo-MasterAltair PerezAún no hay calificaciones
- AaaDocumento10 páginasAaaLizbeth AbrilAún no hay calificaciones
- Termo Tpnº3 2021Documento4 páginasTermo Tpnº3 2021Juan Octavio BustoAún no hay calificaciones
- ProbtermoDocumento3 páginasProbtermoroncada-series.0rAún no hay calificaciones
- TermoquimicaDocumento5 páginasTermoquimicaHenry OjedaAún no hay calificaciones
- 7645guía02 2C23Documento4 páginas7645guía02 2C23lautaro razzettiAún no hay calificaciones
- 1o LeyDocumento4 páginas1o LeyneedformaxAún no hay calificaciones
- Guia 1 Termo 119 UTALDocumento3 páginasGuia 1 Termo 119 UTALDANU45364Aún no hay calificaciones
- Práctica 01 de Termodinámica II 2-2017Documento4 páginasPráctica 01 de Termodinámica II 2-2017Nadia CondeAún no hay calificaciones
- GIM IT Problemas Cap3 Analisis Entropico PDFDocumento5 páginasGIM IT Problemas Cap3 Analisis Entropico PDFMikel MénderzonAún no hay calificaciones
- Listado Certamen TERMODINAMICA UDECDocumento9 páginasListado Certamen TERMODINAMICA UDECGustavo Padilla Maldonado0% (2)
- TP03 BECerr 2023Documento3 páginasTP03 BECerr 2023Daniel Roman CoronelAún no hay calificaciones
- 08-Tema IVDocumento6 páginas08-Tema IVDani MestreAún no hay calificaciones
- TP 4Documento4 páginasTP 4Gabii Van CauwenbergheAún no hay calificaciones
- Colección de Problemas TTyTC - 2020 - 2021Documento12 páginasColección de Problemas TTyTC - 2020 - 2021Laura VercherAún no hay calificaciones
- Pablo Diaz Examenes UsbDocumento65 páginasPablo Diaz Examenes UsbJulio César Borjas Celis0% (1)
- Ejercicios W y Q. Primera Ley 2020-IDocumento7 páginasEjercicios W y Q. Primera Ley 2020-IOleggValVilAún no hay calificaciones
- Problemas Tema 2Documento2 páginasProblemas Tema 2José Rafael GuillénAún no hay calificaciones
- Serie de Problemas #1 Termodinamica IIDocumento4 páginasSerie de Problemas #1 Termodinamica IIFrank C. Flores100% (1)
- TermoDocumento13 páginasTermoEsTefanii R'cAún no hay calificaciones
- Termodinamica 3 ParcialDocumento8 páginasTermodinamica 3 ParcialLAún no hay calificaciones
- Segundo Taller Unificado 2017-II Calor y Onda - Copia (1) - 1Documento16 páginasSegundo Taller Unificado 2017-II Calor y Onda - Copia (1) - 1Paola MurilloAún no hay calificaciones
- Problemario QeaDocumento8 páginasProblemario QeaJesus Escalera GuerraAún no hay calificaciones
- Guias FQI 2019 6 A 9 v2Documento12 páginasGuias FQI 2019 6 A 9 v2Christian Iván Silva GarcíaAún no hay calificaciones
- 3 - Prob RFP 11-12 23-35Documento4 páginas3 - Prob RFP 11-12 23-35adonis aguero pajueloAún no hay calificaciones
- Term Odin A MicaDocumento23 páginasTerm Odin A MicaDiego NavarroAún no hay calificaciones
- Problemas Resueltos en Clase 20-21Documento2 páginasProblemas Resueltos en Clase 20-21Javier Rosero0% (1)
- PROBLEMAS DE FISICOQUÍMICA (Termod)Documento1 páginaPROBLEMAS DE FISICOQUÍMICA (Termod)gerson alarconAún no hay calificaciones
- Segunda Ley Termodinamica Pares-DeberDocumento19 páginasSegunda Ley Termodinamica Pares-DeberWendy Dávila Arteaga33% (3)
- Practica Domiciliaria 6Documento6 páginasPractica Domiciliaria 6Julio Soto LovonAún no hay calificaciones
- Tarea 6Documento2 páginasTarea 6Paola VillalobosAún no hay calificaciones
- Ejercicios FisicoquímicaDocumento8 páginasEjercicios FisicoquímicaAndreslass100% (1)
- PARCIALDocumento2 páginasPARCIALnataliAún no hay calificaciones
- Problemas IntercambiadoresDocumento2 páginasProblemas IntercambiadoresAlejandro Javier AcostaAún no hay calificaciones
- Tac No Isotermico - 2022Documento6 páginasTac No Isotermico - 2022Juan Esteban ZarzaAún no hay calificaciones
- Ejercicios Segunda Ley 2020-IIDocumento2 páginasEjercicios Segunda Ley 2020-IIStefany Elizabeth Crisostomo QuispeAún no hay calificaciones
- Ejercicios Segunda Ley 2020-IIDocumento2 páginasEjercicios Segunda Ley 2020-IIStefany Elizabeth Crisostomo QuispeAún no hay calificaciones
- RFPDocumento2 páginasRFPAndres CentellaAún no hay calificaciones
- Final 2 PracticaDocumento20 páginasFinal 2 PracticamarianaAún no hay calificaciones
- Seminario de TermodinamicaDocumento2 páginasSeminario de TermodinamicaJGibson FiestasAún no hay calificaciones
- 00 Determin BMDocumento2 páginas00 Determin BMDaniel SalazarAún no hay calificaciones
- Discusion 5Documento3 páginasDiscusion 5elbetoavila0% (2)