Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Práctica 5 - Presencial
Práctica 5 - Presencial
Cargado por
Elizabeth TacillaTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Práctica 5 - Presencial
Práctica 5 - Presencial
Cargado por
Elizabeth TacillaCopyright:
Formatos disponibles
UNIVERSIDAD PRIVADA DEL NORTE
Facultad de Ingeniería
Curso:
Química Analítica y Análisis Instrumental
Docente:
M.Sc. Ing Gladys Sandi Licapa Redolfo
Tema:
Práctica Nº 5: Determinación Gravimétrica de cloruro
Alumno:
• Alvarado Tacilla, Yuliza Elizabeth
• Fernández Bardales, Kimberly Jheraldine
• Poma de la Cruz, Paulo Cesar
PERÚ
Práctica Nº 5: Determinación Gravimétrica de cloruro
Facultad de Ingeniería Semestre 2022-I
1. OBJETIVOS:
- Realizar una precipitación cuantitativa del analito (Cl -) y mediante la determinación de
la masa del compuesto formado (cloruro de plata) obtendrá el contenido del analito en
la muestra problema.
- Determinar el factor gravimétrico y el porcentaje de cloruro en una muestra.
2. Fundamento teórico
1. Descripción del Análisis Gravimétrico:
El análisis gravimétrico se basa en la determinación del contenido de analito en una
muestra mediante operaciones de pesada. Los métodos gravimétricos pueden clasificarse
en dos categorías:
Métodos de precipitación: El analito se separa de los demás constituyentes de la muestra
por formación de un compuesto insoluble. El peso del analito en la muestra se determina a
partir del peso del compuesto obtenido inicialmente, o de un compuesto producido
posteriormente por calentamiento. El resto del tema se referirá a este tipo de métodos.
2. Características de los precipitados:
La precipitación debe ser cuantitativa, o lo que es lo mismo, la solubilidad del precipitado
debe ser suficientemente pequeña para que la cantidad perdida no afecte al resultado. Para
ello, un precipitado para su uso en análisis gravimétrico debe cumplir las siguientes
características:
• El precipitado debe ser suficientemente insoluble para asegurar que el proceso sea
cuantitativo y para reducir perdidas en el lavado del mismo. Elegir condiciones
experimentales (pH y temperatura) para Ks’ pequeña. Puede añadirse exceso de 2
precipitante para forzar la precipitación por efecto de ion común, aunque no siempre
puede utilizarse un exceso de reactivo para incrementar la cuantitatividad, ya que puede
producirse la redisolución por formación de complejos, o la impurificación del
precipitado con el reactivo precipitante.
• El precipitado debe ser puro, no debe estar contaminado por otros compuestos presentes en
la disolución.
• Debe poder transformarse en una especie de estequiometría exactamente conocida, estable
(que no adsorba H2O o CO2), no higroscópica y a ser posible de peso molecular alto
(factor gravimétrico bajo).
• Debe tener un tamaño de partícula adecuado para poder ser filtrado sin atravesar los poros
del filtro. El tamaño de partícula puede aumentarse controlando las condiciones de
precipitación y realizando la digestión del precipitado.
3.- Etapas de un método gravimétrico de precipitación las etapas de que consta un método
gravimétrico de precipitación son:
• precipitación
• digestión del precipitado
• separación del precipitado (filtración)
• lavado del precipitado
• conversión a una forma de pesada adecuada
• pesada
• cálculos
Facultad de Ingeniería Semestre 2022-I
Son pocos los precipitados que cumplen los requisitos necesarios para que cada etapa se
cumpla con éxito. De ahí que existan pocos métodos descritos que proporcionen buenos
resultados, aunque algunos de ellos son muy utilizados.
Precipitación: La formación de un precipitado tiene lugar en tres etapas:
• La nucleación, en la que se forman agregados estables de unos pocos iones de precipitado
• El crecimiento cristalino, donde nuevos iones se unen a los núcleos aumentando su
tamaño.
• El envejecimiento durante el cual el precipitado evoluciona hacia formas más insolubles.
3. Materiales, Equipos y Reactivos
- Beakers
- Varrillas
- Matraz
- Pipeta
- Embudo
- Papel filtro
- Propipeta
- NaCl
- AgNO3
- Agua Destilada
4. Procedimiento experimental.
a) Obtener la muestra desconocida. En un vaso de precipitados de 250 mL, añadir 5g
de un cloruro XCl desconocido.
b) Añadir agua a la muestra de XCl. Llenar el vaso con 100 mL de agua, agitar la
disolución hasta que la muestra quede totalmente disuelta.
c) Añadir ácido nítrico concentrado. Añadir 1 mL de ácido concentrado a la disolución
de XCl.
d) Añadir AgNO3 1M. Obtener una probeta de 100 mL y llenarla con la disolución de
AgNO3 1M, añadir AgNO3 a la disolución de XCl, en incrementos de 5 a 25 mL.
Aparecerá un precipitado de AgCl que se irá depositando gradualmente en el fondo.
Continuar añadiendo AgNO3 hasta que no se forme más precipitado.
e) Preparar el sistema de filtrado utilizando un embudo, matraz Erlenmeyer de 250 ml
y papel filtro.
f) Filtrar y pesar el AgCl. Dejar que el contenido del filtrado llene el vaso de
precipitado.
g) Retirar el filtro del sistema de filtrado y colocar el contenido sólido en una luna de
reloj y secar en una estufa por un periodo de 15 minutos
h) Pesar el precipitado en una balanza analítica y anotar el valor (descontando el peso
de la luna de reloj).
i) Calcular el porcentaje de cloruro en la muestra.
5. Resultados y Discusión.
• Papel filtro: 1.0901g
• Papel filtro sobre recipiente (crisol): 53.2802g
• Recipiente (crisol): 52.1901g
Facultad de Ingeniería Semestre 2022-I
• Papel filtro con precipitado (Ag𝐶𝑙 − ) sobre recipiente (crisol): 56.048g
• Precipitado (Ag𝐶𝑙− ) + Papel filtro = 1.2066g
𝑃𝑟𝑒𝑐𝑖𝑝𝑖𝑡𝑎𝑑𝑜 + 1.0901𝑔 = 1.2066g
𝑃𝑟𝑒𝑐𝑖𝑝𝑖𝑡𝑎𝑑𝑜 = 0.1165g
• Precipitado (Ag𝐶𝑙 − ): 0.1165g
• Factor gravimétrico: 0.2473g
𝑀 𝐶𝑙 35.5
𝐹. 𝐺 = = = 0.2473𝑔
𝑀 𝐴𝑔𝐶𝑙 143.5
• Masa del cloruro:
𝑚𝐶𝑙− = 𝐹. 𝐺 𝑥 𝑚𝑎𝑠𝑎 𝑑𝑒 𝑚𝑢𝑒𝑠𝑡𝑟𝑎
𝑚𝐶𝑙− = 0.2473 𝑥 0.1165
𝑚𝐶𝑙− = 0.02881g
• Porcentaje de cloruro (%𝐶𝑙 − ):
𝑚𝐶𝑙 −
%𝐶𝑙− = 𝑥100
𝑚𝑁𝑎𝐶𝑙 −
0.0281𝑔
%𝐶𝑙− = 𝑥100 = 1.4405𝑔
2𝑔
Masa de la muestra desconocida (g): 2 g
Masa del precipitado de AgCl: 0.1165g
Volumen aproximado de disolución de AgNO3 añadido (mL): 10 ml
Calcular el factor gravimétrico: 0.2473g
Calcular la masa de cloruro: 0.02881 g
Calcular el % 𝐶𝑙− = 1.4405%
En la técnica de determinación de cloruro en el libro de Arthur Vogel (Química Analítica
Cualitativa) nos indica que se agrega ácido nítrico concentrado a la disolución de agua con
cloruro de sodio para posteriormente agregar lentamente nitrato de plata 0.1N, hasta que haya un
exceso. También nos confirma lo que se nos indicó a la hora de presenciar un cambio de
coloración debido a la presencia de luz, ya que nos dice que la determinación se efectuará con
una iluminación débil.
En nuestro informe no usamos ácido nítrico concentrado, pero sí se llegó a apreciar la reacción
que tuvo la disolución debido a la presencia de luz (una iluminación débil).
De igual manera nos habla de una técnica distinta realizada en el laboratorio . El cuál nos dice
que después del lavado del precipitado con ácido nítrico muy diluido, se lavarán las paredes del
crisol cinco o seis veces, con volúmenes pequeños de alcohol puro y que mediante una pipeta
pequeña o de un tubo estirado para continuar lavando unas cuantas veces con volúmenes de éter
anhidro. Se seca el precipitado, pero esta vez con una trompa de agua durante unos 10 minutos,
se frotarán las paredes externas del crisol con un repasador de hilo limpio; se dejará en un
desecador al vacío durante 10 minutos para luego pesar el AgCl.
En la práctica del laboratorio se calentó la muestra a unos 120℃ por unos 15 min apróx
mientras que Arthur Vogel nos indica que su muestra lo llevo a una estufa a 130-150℃ durante
1 hora.
Facultad de Ingeniería Semestre 2022-I
6. Cuestionario.
a. ¿Cuál es la diferencia entre decantación y precipitación?
• Una precipitación ocurre
En una decantación no existe cuando una reacción
Una reacción química. química
Ya que tenemos compuestos • Compuesto con mayor
densidad donde se
Mezclados con diferentes
encuentran los reactantes
Densidades
• En lo cual se producen que
Por efectos de la gravedad se se deposite al fondo
Van depositando en el fondo
Conforme su densidad • Precipitación se usa mucho
en análisis cualitativo o
cuantitativo
Podemos usar este proceso
para dos líquidos inmiscibles y • La forma controladora para
una mezcla de un líquido y identificar elementos o para
un sólido (una suspensión) identificar puntos de
equilibrio
Esto puede separar el líquido
menos denso del líquido
de alta densidad.
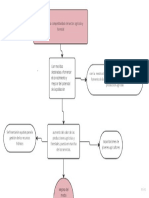
b. Qué técnicas de separación de mezclas homogéneas y heterogéneas más comunes se
utilizan en los laboratorios de análisis
Facultad de Ingeniería Semestre 2022-I
filtración
Técnicas de separación
disolución
Separa mezclas evaporación decantación destilación
heterogéneas
Separa mezclas
homogéneas
Formadas
Por
Formadas
Sólido y
Por
liquido
Funcionamiento Sólido y
liquido
Un filtro retiene
el sólido y deja
pasar el liquido Funcionamiento
Se evapora el
líquido y queda
el solido
Facultad de Ingeniería Semestre 2022-I
c. Defina los siguientes conceptos en sus propias palabras: disolución saturada, disolución
sobresaturada, nucleación, crecimiento cristalino, digestión del precipitado,
precipitación, y Kps.
Una solución saturada es aquella en la que el mismo número de
Disolución partículas o solutos y solvente están presentes en la solución. de un
disolvente es que puede ser líquido, sólido o gaseoso, aunque los
saturada disolventes suelen ser líquidos. El solvente más común es el agua; El
factor que tiene mayor influencia en la velocidad de disolución es la
cantidad de soluto ya disuelto en la solución. Otro hecho que afecta la
solubilidad es la temperatura. La solubilidad aumenta al aumentar la
temperatura del disolvente. Además, la presión y la naturaleza del
soluto y el solvente también pueden afectar la solubilidad.
disolución Una solución está sobresaturada cuando no puede agregar solutos y
sobresaturada disolverse. Por otro lado, una solución sobresaturada es una solución
en la que la cantidad de soluto es mayor en relación con una solución
saturada. Un solvente contiene más soluto del que puede disolver a
una temperatura dada.
la nucleación es el proceso por el cual cambia el estado de la materia,
nucleación como la formación de un gas o un cristal a partir de un líquido. Se
puede ver en la condensación por evaporación de gotas o burbujas en
líquidos hirviendo. Otro momento de nucleación ocurre cuando
pequeñas burbujas en el gas se unen en burbujas más grandes. En
general, la nucleación es la formación de nuevas estructuras a partir
de un núcleo base.
crecimiento La cristalización Cuando ocurre la recombinación condiciones dentro
cristalino del medio solución, fundida o vaporizada, en Temperatura, presión y
sobresaturación dado, es energéticamente favorable Composición
Juntas permanentes.
La digestión del precipitado es un proceso de purificación y mejora
digestión del del tamaño de partícula que consiste en poner en contacto el sólido
recién precipitado con la solución de la que se obtuvo durante un
precipitado, período de tiempo previo a la filtración. Para que se realice las altas
temperaturas, lo que da como resultado la formación de cristales más
grandes y regulares que son más fáciles de filtrar y más puros, la
pérdida de iones pequeños en cristales grandes, la reorganización de
iones en la red cristalina, la desaparición de defectos puede haber
cambios químicos
precipitación La precipitación es el proceso de obtención de un sólido a partir de
una solución. Puede lograrse mediante reacciones químicas,
evaporación de solventes, enfriamiento repentino de soluciones
calientes o cambios en la polaridad del solvente. El sólido así
obtenido se denomina precipitado y puede contener impurezas.
Generalmente, es necesario cristalizarlo y recristalizarlo.
Kps. El valor Ksp representa la solubilidad de un compuesto iónico, es
decir, cuanto menor es su valor, menos soluble es el compuesto.
También es fácil observar que si aumentamos la concentración de un
componente o ion, alcanzando nuevamente un estado de equilibrio de
disolución, la concentración del otro ion disminuirá debido al efecto
del ion común. El equilibrio de solubilidad es un equilibrio
heterogéneo, por lo tanto, para calcular la constante de equilibrio, la
fase sólida siempre debe estar presente, incluso en cantidades muy
pequeñas.
Facultad de Ingeniería Semestre 2022-I
d. ¿Cuántos tipos de contaminación en el proceso gravimétrico existen y como pueden
eliminarse?
Los precipitados contienen con frecuencia impurezas que son solubles en las aguas madres en las
condiciones en las que se ha realizado la precipitación. La incorporación de este tipo de impurezas solubles
en las condiciones experimentales se denomina coprecipitación. Cuando la contaminación ocurre después de
formarse el precipitado, se tiene la coprecipitación. La contaminación de precipitados se debe,
principalmente, lo que anteriormente dijimos a la coprecipitación de sustancias solubles arrastradas debido:
Adsorción en la superficie: Aumenta con la superficie. (Suspensiones coloidales).
Absorción en el interior del cristal por:
Formación de cristales mixtos: El ion contaminante sustituye a un ion de analito en la red cristalina
del precipitado.
Oclusión de bolsas de disolvente: lones extraños disueltos quedan atrapados
dentro de un cristal en crecimiento.
La contaminación según Kolthalt puede dividirse en dos grandes grupos:
• Coprecipitación: El precipitado fundamental y el contaminante se originan al mismo tiempo,
pudiéndose distinguir entre dos tipos: por adsorción y por oclusión. Por adsorción consiste en un
arrastre de impurezas en la superficie del precipitado mientras que, en la oclusión, el arrastre de las
impurezas se realiza en el interior de las partículas primarias del precipitado.
• Posprecipitación: El precipitado fundamental estaba inicialmente puro. produciéndose la
contaminación después que la precipitación ha terminado. Este fenómeno se favorece con el tiempo
de agitación y con la elevación de la temperatura, pudiendo llegar a un aumento del 100% en el peso
del precipitado puro,
e. Calcule la Kps para el AgCl sabiendo que la concentración en el equilibrio de los iones es
de 1.34x10-5.
AgCl (s) Ag+ + Cl-
Kps= [𝑨𝒈+ ][𝑪𝒍− ]
Kps = (𝟏. 𝟑𝟒𝒙𝟏𝟎−𝟓 )(𝟏. 𝟑𝟒𝒙𝟏𝟎−𝟓 )
Kps = 𝟏𝟕𝟗. 𝟓𝟔𝒙𝟏𝟎-12
Facultad de Ingeniería Semestre 2022-I
f. ¿Qué masa de yodato de plata se pude obtener a partir de 0,50 g de yodato de sodio?
Suponga que la solubilidad del AgIO3 en agua es despreciable.
1 mol NalO3 1 mol NalO3 2.82.767 g AgIO3
0.50g NalO3 { }( }( )
197.8924 𝑔 NalO3 1 mol NalO3 1 mol AgIO3
= 0.7144 AgIO3
g. ¿Qué sucede con el exceso de AgNO3 añadido a la disolución?
✓ El exceso de AgNO3, puede reaccionar con las demás sustancias, generando el precipitado,
Que es la sustancia blanca en el fondo del vaso.
✓ Cuando se coloca un exceso de este compuesto a una disolución tenemos que se precipitan los
aniones y además se estudia por el método de retroceso al exceso que quede de Ag+.
✓ Se da a notar un cambio de coloración, debido a que el AgNO3 es fotosensible y con una ligera
iluminación tiende a realizar este tipo de reacción.
✓ Los iones de AgNO3 van a reaccionar con el NaCl dando como resultado un desplazamiento doble en
la cual se observara que el catión Ag+ se unirá con anión Cl- y el anión NO3- se unirá con el catión
Na+.
𝐴𝑔𝑁𝑂3(𝑎𝑞) + NaCl(aq) AgCl(s) + NaNO3(aq)
Referencia:
Mejia, j. (12 de septiembre de 2019). scribd. Obtenido de
https://es.scribd.com/document/425584891/Preci-Pita-Dos
s.a. (25 de marzo de 2015). sawakinome. Obtenido de
https://es.sawakinome.com/articles/analytical-chemistry/difference-between-sedimentation-
and-decantation.html
S.A. (ABRIL de 24 de 2021). Obtenido de yumpu:
https://www.yumpu.com/es/document/read/15228017/capitulo-9-gravimetria
Zagal, C. (03 de mayo de 2016). academia edu . Obtenido de
GRAVIMETRIA_En_Química_Analítica_cualitativa_y_cuantitativa_los_procesos_de_separaci
ón_pueden_llevarse_a_cabo_de_varias_formas_ellas_son_Precipitación_Volatilización_Extracc
ión_Deposición_electrolítica_Complejación_Adsorción
Zambrano, S. (10 de abril de 202). departamento de biologia. Obtenido de
https://institutonacional.cl/wp-content/uploads/2020/03/7-CIENCIAS-NATURALES-GUIA-
1_Mezclas.pdf
Arthur Vogel, Química Analítica Cuantitativa (1983), Editorial Buenos aires.
Facultad de Ingeniería Semestre 2022-I
Anexos:
1. 2.
3. 4.
5.
Facultad de Ingeniería Semestre 2022-I
También podría gustarte
- Propuesta Economica - Mineria &construcción SRLDocumento1 páginaPropuesta Economica - Mineria &construcción SRLElizabeth TacillaAún no hay calificaciones
- 6 - PPP VC Semana 1 - Introducción - Juan GonzalesDocumento19 páginas6 - PPP VC Semana 1 - Introducción - Juan GonzalesElizabeth TacillaAún no hay calificaciones
- Universidad Privada Del Norte: Facultad de Ingeniería AmbientalDocumento23 páginasUniversidad Privada Del Norte: Facultad de Ingeniería AmbientalElizabeth TacillaAún no hay calificaciones
- Informe 4Documento44 páginasInforme 4Elizabeth TacillaAún no hay calificaciones
- Record de NotasDocumento6 páginasRecord de NotasElizabeth TacillaAún no hay calificaciones
- Informe de Guia para El MuestreoDocumento14 páginasInforme de Guia para El MuestreoElizabeth TacillaAún no hay calificaciones
- Actividades de Minería Artesanal: Canchis, Chinchipe (Parte Alta) - San Ignacio (Yacimiento: Placeres)Documento1 páginaActividades de Minería Artesanal: Canchis, Chinchipe (Parte Alta) - San Ignacio (Yacimiento: Placeres)Elizabeth TacillaAún no hay calificaciones
- Universidad Privada Del Norte: Facultad de Ingeniería AmbientalDocumento12 páginasUniversidad Privada Del Norte: Facultad de Ingeniería AmbientalElizabeth TacillaAún no hay calificaciones
- Jueves PresentarDocumento8 páginasJueves PresentarElizabeth TacillaAún no hay calificaciones
- Práctica #02: Conductividad en SuelosDocumento6 páginasPráctica #02: Conductividad en SuelosElizabeth TacillaAún no hay calificaciones
- Jueves Presentar OficialDocumento9 páginasJueves Presentar OficialElizabeth TacillaAún no hay calificaciones
- Metales Pesados en Minerias (Perú)Documento1 páginaMetales Pesados en Minerias (Perú)Elizabeth TacillaAún no hay calificaciones
- Laboratorio 2Documento20 páginasLaboratorio 2Elizabeth TacillaAún no hay calificaciones
- Laboratorio 1 Tecnologias de Tratamiento de SuelosDocumento23 páginasLaboratorio 1 Tecnologias de Tratamiento de SuelosElizabeth TacillaAún no hay calificaciones
- Protocolo de Seguridad de LaboratorioDocumento14 páginasProtocolo de Seguridad de LaboratorioElizabeth TacillaAún no hay calificaciones
- Biocompost Final PDFDocumento20 páginasBiocompost Final PDFElizabeth TacillaAún no hay calificaciones
- JP - Rúbrica de Evaluación Informes de Trabajo - Ing. Gerzon Fernando Dominguez Silva - Contaminación de SuelosDocumento2 páginasJP - Rúbrica de Evaluación Informes de Trabajo - Ing. Gerzon Fernando Dominguez Silva - Contaminación de SuelosElizabeth TacillaAún no hay calificaciones
- UntitledDocumento1 páginaUntitledElizabeth TacillaAún no hay calificaciones
- Habilidades Geologia - PDF JsatDocumento1 páginaHabilidades Geologia - PDF JsatElizabeth TacillaAún no hay calificaciones
- Número Cuenta Más FacturaDocumento2 páginasNúmero Cuenta Más FacturaElizabeth TacillaAún no hay calificaciones
- Laboratorio de SuelosDocumento5 páginasLaboratorio de SuelosElizabeth TacillaAún no hay calificaciones
- Habilidades GeologiaDocumento1 páginaHabilidades GeologiaElizabeth TacillaAún no hay calificaciones
- Semana 37 Razonamiento Matemático.Documento6 páginasSemana 37 Razonamiento Matemático.Elizabeth TacillaAún no hay calificaciones
- ResultadosDocumento4 páginasResultadosElizabeth TacillaAún no hay calificaciones
- ACTIVIDAD 08. 1° y 2° TANGRAMDocumento8 páginasACTIVIDAD 08. 1° y 2° TANGRAMElizabeth TacillaAún no hay calificaciones
- Habilidades Geologia - PDF JsatDocumento1 páginaHabilidades Geologia - PDF JsatElizabeth TacillaAún no hay calificaciones
- VVVVVVVVDocumento14 páginasVVVVVVVVElizabeth TacillaAún no hay calificaciones
- Anexos Informe de LaboratorioDocumento3 páginasAnexos Informe de LaboratorioElizabeth TacillaAún no hay calificaciones
- 2012 CastroFrancoMELAFISDocumento16 páginas2012 CastroFrancoMELAFISElizabeth TacillaAún no hay calificaciones
- T1-Adelgazamiento de La Capa de Ozono en El Territorio AntárticoDocumento4 páginasT1-Adelgazamiento de La Capa de Ozono en El Territorio AntárticoElizabeth TacillaAún no hay calificaciones