Documentos de Académico
Documentos de Profesional
Documentos de Cultura
T - Sem 09 - Ses 10 - MicroTaller 05
Cargado por
Alderan 512Título original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
T - Sem 09 - Ses 10 - MicroTaller 05
Cargado por
Alderan 512Copyright:
Formatos disponibles
GRUPO 01 INTEGRANTES:
ANGIE CARITO GARCÍA CONCHA.
ANDERSON JAVIER CERNA CASTILLO.
ALDO ANDRE MARTINEZ SANCHEZ.
DONA JOANA SALAZAR
QUÍMICA INORGÁNICA
S10.s1 – Micro Taller 05
Primera Ley de la Termodinámica
1. Calcula el trabajo que desarrolla el gas encerrado en un cilindro cuando sufre una
expansión de 50 cm3 sometido a la presión constante de 5 atm. Expresa el resultado en
julios.
2. Un sistema recibe 200 cal del ambiente y realiza un trabajo de 500 J sobre sus
alrededores. Calcula la variación de energía interna del sistema.
3. Un mol de un gas ideal se expande contra un pistón que soporta una presión de 0,2 atm. Si
la presión inicial del gas es de 10 atm y la presión final es de 0,4 atm, manteniéndose la
temperatura constante a 0ºC, calcula:
a) El cambio en la energía interna del gas.
b) El calor transferido en el cambio.
4. Determina el cambio en la energía interna, el calor y el trabajo realizado, por un mol de un
gas ideal al ser sometido a un proceso a volumen constante desde un estado 1, donde P1 =
2,0 atm y T1 = 546,0 K hasta un estado 2, donde P 2 = 1,0 atm y T2 = 273 K.
5. Un gas se comprime a una presión constante de 0,8 atm de 9 L a 2 L. En el proceso, 400 J
de energía salen del gas por calor.
(a) ¿Cuál es el trabajo realizado sobre el gas?
(b) ¿Cuál el cambio en su energía interna?
1 Química Inorgánica
También podría gustarte
- Examen de Entrada FQ - FISICOQUIMICA (37137)Documento3 páginasExamen de Entrada FQ - FISICOQUIMICA (37137)Miguel BaldeonAún no hay calificaciones
- U4 - S5.Ficha de Trabajo 5 - TermodinamicaDocumento3 páginasU4 - S5.Ficha de Trabajo 5 - TermodinamicaJair ItmeAún no hay calificaciones
- S - Sem12 - Ses24 - Integrales Triples Mediante Coordenadas Esféricas-1Documento2 páginasS - Sem12 - Ses24 - Integrales Triples Mediante Coordenadas Esféricas-1Josh Patrick Miranda Castillo0% (1)
- T Sem 11 Ses 11 TermoquímicaDocumento1 páginaT Sem 11 Ses 11 TermoquímicaARANZA ALIAGA CARHUAMACAAún no hay calificaciones
- U1 - S1.Ficha de Trabajo 1 - Estequiometria Con RedoxDocumento2 páginasU1 - S1.Ficha de Trabajo 1 - Estequiometria Con RedoxAlexander Caceres Lopez50% (4)
- Micro Taller 2 - Quimica Inorganica - Sala 1Documento4 páginasMicro Taller 2 - Quimica Inorganica - Sala 1Rodrigo AndrésAún no hay calificaciones
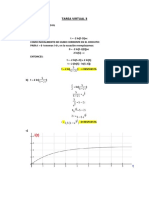
- Circuito RL: Resolución de ecuaciones para corriente i(tDocumento2 páginasCircuito RL: Resolución de ecuaciones para corriente i(teduardoAún no hay calificaciones
- U3 - S5 - Ejercicios Electroquímica CDDocumento10 páginasU3 - S5 - Ejercicios Electroquímica CDmaicot donayreAún no hay calificaciones
- S02.s3 - Taller N°2Documento1 páginaS02.s3 - Taller N°2Katherine Villegas CuadrosAún no hay calificaciones
- UTP Guia de Practica PA Estructura Secuencial 1Documento4 páginasUTP Guia de Practica PA Estructura Secuencial 1Erwinga Gamarra LeonAún no hay calificaciones
- Corte y Sección: Conceptos GeneralesDocumento4 páginasCorte y Sección: Conceptos GeneralesAlejandra PobleteAún no hay calificaciones
- Utp Evaluacion Calificada en Linea 1Documento7 páginasUtp Evaluacion Calificada en Linea 1SusanRCAún no hay calificaciones
- Tarea Mate2Documento5 páginasTarea Mate2Beren Kaya YamanAún no hay calificaciones
- Ficha de Trabajo 3 - Equilibrio QuimicoDocumento3 páginasFicha de Trabajo 3 - Equilibrio QuimicoRodrigo CiezaAún no hay calificaciones
- U5 - S7.Ficha de Trabajo 7 - Electroquimica PDFDocumento5 páginasU5 - S7.Ficha de Trabajo 7 - Electroquimica PDFjegonugaAún no hay calificaciones
- S04 s2-REPASO+PARCIALDocumento10 páginasS04 s2-REPASO+PARCIALfaftAún no hay calificaciones
- Formato de Trabajo Final CAF2Documento4 páginasFormato de Trabajo Final CAF2Angelica GoñiAún no hay calificaciones
- T - Sem 08 - Ses 08 - Taller Examen ParcialDocumento3 páginasT - Sem 08 - Ses 08 - Taller Examen ParcialjuancitoAún no hay calificaciones
- (ACV-S02) Evaluación en Línea 1 - EP - QUIMICA GENERAL (4104)Documento5 páginas(ACV-S02) Evaluación en Línea 1 - EP - QUIMICA GENERAL (4104)Lo AnguAún no hay calificaciones
- S16.s1 - Material. Solucion en Serie de PotenciasDocumento27 páginasS16.s1 - Material. Solucion en Serie de PotenciasluisAún no hay calificaciones
- Ficha de Trabajo 1 - Estequiometria Con Redox PDFDocumento2 páginasFicha de Trabajo 1 - Estequiometria Con Redox PDFYeison Lujan RamosAún no hay calificaciones
- Ejercicios de Taller 5 Caf1Documento2 páginasEjercicios de Taller 5 Caf1Gabii Jhoyzy CamposAún no hay calificaciones
- U4 - S5.Ficha de Trabajo 5 - TermodinamicaDocumento1 páginaU4 - S5.Ficha de Trabajo 5 - TermodinamicaRoberto Quispe Escarcena0% (1)
- SimuladorCeldasGalvánicasDocumento6 páginasSimuladorCeldasGalvánicasPercy TorresAún no hay calificaciones
- Trabajo Final 1 PDFDocumento5 páginasTrabajo Final 1 PDFantonioAún no hay calificaciones
- Examen - EXAMEN PARCIAL - CÁLCULO APLICADO A LA FÍSICA 3 - AGOSTO 2022 - IIadrDocumento6 páginasExamen - EXAMEN PARCIAL - CÁLCULO APLICADO A LA FÍSICA 3 - AGOSTO 2022 - IIadrAdrian RamosAún no hay calificaciones
- S03.s1. - (ACV-S03) Autoevaluación 3 - FISICOQUIMICA (8837)Documento9 páginasS03.s1. - (ACV-S03) Autoevaluación 3 - FISICOQUIMICA (8837)xiomara chavezAún no hay calificaciones
- Introducción a la TermodinámicaDocumento47 páginasIntroducción a la TermodinámicaCesar Rojas BordaAún no hay calificaciones
- S05s1 Evaluacion Virtual 02Documento3 páginasS05s1 Evaluacion Virtual 02ronny rojas villacrezAún no hay calificaciones
- Guia Tercera Practica QGDocumento4 páginasGuia Tercera Practica QGCajamarca Ninalaya Yerson0% (1)
- Mmicro Taller 2-FiquiDocumento1 páginaMmicro Taller 2-FiquiNayely Alexandra Diaz LujanAún no hay calificaciones
- S04.s1 - Informe Final Del Laboratorio 2 PDFDocumento5 páginasS04.s1 - Informe Final Del Laboratorio 2 PDFAngelAún no hay calificaciones
- Huawei Y330-U05 V100r001c00b126custc40d001 Update Guide 2.1Documento5 páginasHuawei Y330-U05 V100r001c00b126custc40d001 Update Guide 2.1Liz Estefani Condori CamposAún no hay calificaciones
- Resuelto - (ACV-S02) Cuestionario de Laboratorio Calificado 1 - FISICOQUIMICA (8608)Documento5 páginasResuelto - (ACV-S02) Cuestionario de Laboratorio Calificado 1 - FISICOQUIMICA (8608)cristianAún no hay calificaciones
- CG-Sem13-Problemas de ElectroquímicaDocumento1 páginaCG-Sem13-Problemas de ElectroquímicaJosé Luis GamboaAún no hay calificaciones
- Solucion Ejercicios 8 FiquiDocumento3 páginasSolucion Ejercicios 8 FiquiYanela CamargoAún no hay calificaciones
- U4 S6 Fichadetrabajo6 CalculosEstequiométricosDocumento2 páginasU4 S6 Fichadetrabajo6 CalculosEstequiométricosEver Panca HuamaniAún no hay calificaciones
- Plantilla-Para-La-Revista-Eciperu Nivel de Contaminacion de La Quebrada Mananay Por Aguas Residuales - Afluente Del Rio Ucayali - Provincia de Coronel Portillo, 2017Documento4 páginasPlantilla-Para-La-Revista-Eciperu Nivel de Contaminacion de La Quebrada Mananay Por Aguas Residuales - Afluente Del Rio Ucayali - Provincia de Coronel Portillo, 2017Jaime Alberto Mori CastroAún no hay calificaciones
- Matemática para Ingenieros I - Evaluación Permanente 1Documento8 páginasMatemática para Ingenieros I - Evaluación Permanente 1milagrosss03100% (1)
- Separata03 - Unidad01 (1) ALGORITMOSDocumento3 páginasSeparata03 - Unidad01 (1) ALGORITMOSAndres PeñaAún no hay calificaciones
- (Acv-S05) Autoevaluación 5 - Fisicoquimica (8608) - 2Documento5 páginas(Acv-S05) Autoevaluación 5 - Fisicoquimica (8608) - 2Gimar2Aún no hay calificaciones
- (ACV S03) TareaCalificada1EP1 PDFDocumento11 páginas(ACV S03) TareaCalificada1EP1 PDFPatrick ChacchiAún no hay calificaciones
- PDF Acv s06 Laboratorio N 3 Simulador Conductividad de Soluciones Ionicas DDDocumento9 páginasPDF Acv s06 Laboratorio N 3 Simulador Conductividad de Soluciones Ionicas DDOlger Aragon BerlangaAún no hay calificaciones
- Asientos ContaDocumento9 páginasAsientos ContaMarilyn Rofner FloresAún no hay calificaciones
- S03.s1 - Microtaller 02Documento1 páginaS03.s1 - Microtaller 02Geoffrey CoronadoAún no hay calificaciones
- Actividades de La Semana 2 B - ResueltaDocumento2 páginasActividades de La Semana 2 B - ResueltaJosé Urday100% (1)
- Calculo toma decisiones PC2Documento6 páginasCalculo toma decisiones PC2Selene Supo PérezAún no hay calificaciones
- S04 - Taller para PC1Documento9 páginasS04 - Taller para PC1Miguel Angel Romero CruzAún no hay calificaciones
- Dibujo para Ingeniería: Ejercicios de instrumentos, AutoCAD y modelado 3DDocumento8 páginasDibujo para Ingeniería: Ejercicios de instrumentos, AutoCAD y modelado 3DLeonardo CoaguilaAún no hay calificaciones
- PRACTICA DE QUIMICA Soluciones y RedoxDocumento3 páginasPRACTICA DE QUIMICA Soluciones y Redoxgaby181107Aún no hay calificaciones
- Proyecto Lab. FISICA-200Documento6 páginasProyecto Lab. FISICA-200Miguel Potosí MndzAún no hay calificaciones
- S10.s1 RESOLVER EJERCICIOSDocumento1 páginaS10.s1 RESOLVER EJERCICIOSBrayam Stalyn Bonifacio AyalaAún no hay calificaciones
- Calculo para La Toma de DecisionesDocumento6 páginasCalculo para La Toma de DecisionesBrenda PAAún no hay calificaciones
- S18.s1 - Archivo Presentación Del Trabajo FinalDocumento10 páginasS18.s1 - Archivo Presentación Del Trabajo Finalgalleta oreoAún no hay calificaciones
- Avance 1 Caf2Documento5 páginasAvance 1 Caf2junior james fernandoAún no hay calificaciones
- S11.s2 - Poner en PrácticaDocumento4 páginasS11.s2 - Poner en PrácticaMarcelo Adrian GonzalesAún no hay calificaciones
- T - Sem 09 - Ses 10 - MicroTaller 05Documento2 páginasT - Sem 09 - Ses 10 - MicroTaller 05Alexander Gutiérrez ChacaliazaAún no hay calificaciones
- T Sem 09 Ses 10 MicroTaller 05Documento1 páginaT Sem 09 Ses 10 MicroTaller 05juancitoAún no hay calificaciones
- T - Sem 10 - Ses 10 - MicroTaller 05 - 1era Ley TDDocumento1 páginaT - Sem 10 - Ses 10 - MicroTaller 05 - 1era Ley TDsantiagoAún no hay calificaciones
- B TermodinamicaDocumento2 páginasB TermodinamicaOscar OcsaAún no hay calificaciones
- S07.s1 - Resolver EjerciciosDocumento1 páginaS07.s1 - Resolver EjerciciosAlderan 512Aún no hay calificaciones
- S07.s1 - Resolver EjerciciosDocumento2 páginasS07.s1 - Resolver EjerciciosAlderan 512Aún no hay calificaciones
- S08.s1 - Resolver EjerciciosDocumento5 páginasS08.s1 - Resolver EjerciciosAlderan 512Aún no hay calificaciones
- S02.s2 - Resolver EjerciciosDocumento4 páginasS02.s2 - Resolver EjerciciosAlderan 512Aún no hay calificaciones
- La historia y aplicaciones de los cuadrados mágicosDocumento22 páginasLa historia y aplicaciones de los cuadrados mágicostaty_paredes_2Aún no hay calificaciones