Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Informe de Laboratorio PH EN SOLUCIONES ÁCIDAS Y BÁSICAS
Cargado por
Santy PerezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Informe de Laboratorio PH EN SOLUCIONES ÁCIDAS Y BÁSICAS
Cargado por
Santy PerezCopyright:
Formatos disponibles
LABORATORIO DE BIOQUÍMICA
pH EN SOLUCIONES ÁCIDAS Y BÁSICAS
Fajardo Martínez Jose Andrés
Moreno Valencia Sebastián Alejandro
Patichoy Calpa Santiago
Pérez Ramírez Santiago
Facultad de Ingeniería
Ingeniería de Procesos
Universidad Mariana
RESUMEN
El pH o su nombre más largo potencial de hidrógeno sirve para entablar el grado de acidez o de
alcalinidad de una disolución, en la práctica laboratorio con ayuda de un pH-metro se pudo medir el
grado de acidez de varias sustancias y disoluciones y clasificarlas por su pH en ácidas, neutras y
básicas, sustancias líquidas, como zumo de limón y de tomate y disoluciones de HCl y NaOH,
analizando los resultados obtenidos se llega a la conclusión de que el pH de una solución va a variar
respecto a la concentración del reactivo mezclado con un solvente (en este caso agua destilada) en los
ácidos se evidencia que cada vez que baja su concentración, el pH aumenta y en los resultados de la
base, los datos salieron dispersos diferentes a lo pensado, esto se dio debido a una posible
contaminación del tubo por parte de otro reactivo no deseado; Sin embargo este error se aprendió a
mejorar la atención y sacar nuevas conclusiones.
Palabras Clave: pH, acidez, alcalinidad, pH-metro, sustancias.
1. INTRODUCCIÓN Se expresa como el logaritmo negativo de
base 10 de la concentración de iones
El concepto de pH es muy importante para hidrógeno. La siguiente ecuación representa
comprender muchos procesos químicos como esta definición:
las reacciones de óxido reducción, la
estructura de las biomoléculas
(particularmente de las proteínas), la
estabilidad de coloides, la cinética química, los
mecanismos de reacción, la polución, el
estudio de ecosistemas, la agricultura, la
tecnología de alimentos y cosmética, etc.
(Ocampo, 2018)
Ecuación 1: Ecuaciones para calcular pH y POH.
¿Qué es el pH? Por otro lado, el pOH es una medida de la
concentración de iones hidroxilo en una
El pH es una medida que sirve para entablar el disolución. Se expresa como el logaritmo
grado de acidez o alcalinidad de una negativo de base 10 de la concentración de
disolución. La “p” es por “potencial”, por esa iones hidroxilo y, a diferencia del pH, se usa
razón el pH se denomina: potencial de para medir el grado de alcalinidad de una
hidrógeno. disolución.
¿Qué relación existe entre el nivel de acidez 2. MATERIALES
y el pH?
Reactivos: ácido clorhídrico (0.01 M),
Las disoluciones ácidas poseen una alta hidróxido de sodio (0.01 M) y agua destilada.
proporción de iones hidrógeno. Esto quiere Materiales: 1 gradilla + 20 tubos de ensayo, 2
decir que poseen bajos valores de pH (ver goteros, 5 beakers de 50 mL, 10 mL de zumo
ecuación 1) y, por consiguiente, su grado de de limón, 10 mL de zumo de tomate, 10 mL de
acidez es elevado. De esta forma, una clara de huevo, 10 mL de vinagre y 10 mL de
disolución va a ser más ácida o menos ácida leche.
dependiendo de la proporción de iones Equipos: pH-metro
hidrógeno que tenga.
3. MÉTODOS
Por otro lado, las disoluciones simples
(alcalinas) poseen bajas porciones de iones Ensayo 1.
hidrógeno. Esto quiere decir que poseen altos Primeramente, se tomaron 4 tubos de ensayo
valores de pH (ver ecuación 1) y, por debidamente numerados (1-4).
consiguiente, su grado de acidez es bajo. En el tubo de ensayo #1 se depositó 1 mL de
(Ondarse, 2015) ácido clorhídrico (0.01M) junto con 5mL de
agua destilada (previamente agitada
vigorosamente).
Figura 1: Escala del pH
La escala de pH va desde el valor 0 hasta el 14.
Ejemplificando, las sustancias con costo de
pH=0 son las más ácidas (menos básicas), las
que poseen pH=7 son neutras, y las que poseen Figura 2: Ácido clorhídrico
pH=14, son las menos ácidas (más básicas).
(Ondarse, 2015) Seguido a esto se depositó en todos los tubos
5mL de agua destilada junto con 1mL de la
solución del tubo anterior (Tubo #2 contiene 5
mL de agua destilada y 1 mL de solución del
tubo 1) y así sucesivamente hasta llegar al tubo
Ecuación 2: Ecuación de equilibrio ácido base. 4.
Ensayo 2.
Primeramente, se tomaron 4 tubos de ensayo
debidamente numerados (5-8).
Ecuación 3: La constante de equilibrio o constante de En el tubo de ensayo #5 se depositó 1 mL de
disociación. hidróxido de sodio (0.01M) junto con 5mL de
agua destilada (previamente agitada
vigorosamente) .
Ecuación 3: La ecuación de Henderson – Hasselblach,
relaciona el pH de una disolución con la proporción base
conjugada/ácido sin disociar.
Figura 3: Hidróxido de sodio.
Seguido a esto se depositó en todos los tubos
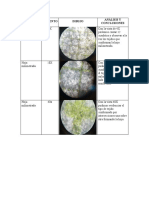
Figura 5: Beakers 1-5
5mL de agua destilada junto con 1mL de la
solución del tubo anterior (Tubo #6 contiene 5
Posteriormente a esto se midió el pH de cada
mL de agua destilada y 1 mL de solución del
solución en los beakers con ayuda de un pH-
tubo 5), y así sucesivamente hasta llegar al
metro.
tubo 8.
Ensayo 3.
Se toma un tubo de ensayo marcado con el
número nueve, Inmediatamente se depositaron
2.5 mL de la solución del tubo 1 y 2.5 mL de
la solución del tubo 5.
Figura 6: pH-metro
4. RESULTADOS
Figura 4: Tubo de ensayo #9 1. El pH fue aumentando a medida que
el ácido HCl se iba diluyendo, como
Posteriormente se midió el pH de la solución. se puede apreciar en la gráfica.
Ensayo 4.
Primeramente, se tomaron 5 beakers de 50mL
debidamente numerados.
Seguido a esto, en el beaker #1 se depositaron
10 mL de zumo de limón, en el beaker #2 10
mL de zumo de tomate,en el beaker #3 10 mL
de clara de huevo, en el beaker #4 10 mL de
vinagre y en el beaker #5 10 mL de leche.
Figura 7: Gráfica Concentración por
pH, ensayo de ácidez
2. Se obtuvieron valores de pH muy
dispersos a medida que se iba 4.CONCLUSIONES Y
diluyendo la base NaOH. RECOMENDACIONES
● Se logró cumplir con los objetivos
propuestos al inicio de la práctica, el
cual era medir el pH de diferentes
sustancias de origen orgánico e
inorgánico para así determinar su
compuesto (ácido, básico o neutro) y
de la misma manera interpretar las
Figura 8: Gráfica Concentración por variaciones de pH.
pH, ensayo de ácidez
● Los resultados obtenidos en el ensayo
3. Al mezclar solución del tubo 1 y 1 permiten concluir que el ácido al irse
solución del tubo 5 se obtiene una disolviendo en cada tubo de ensayo
solución completamente alcalina. fue reduciendo su concentración y por
ende el aumento del pH, que se puede
4. Tabla con el nombre de la sustancia y evidenciar de otra forma en la gráfica
su pH respectivo. realizada.
● Los resultados del ensayo 2 salen
Nombre de pH Compuesto dispersos al objetivo principal debido
la sustancia que, como el agua es neutra y si se
agrega una base debería aumentar la
T. Ensayo 1 3.2 Ácido alcalinidad de la solución y en este
caso en algunos tubos de ensayo
T. Ensayo 2 4.1 Ácido aumentó y disminuyó el pH y se llegó
a la conclusión que posiblemente los
T. Ensayo 3 5.3 Ácido tubos de ensayo fueron contaminados
accidentalmente con un ácido y por
T. Ensayo 4 6.1 Neutro esta razón el pH no aumentó en todos
los tubos y el resultado fue la
T. Ensayo 5 7.2 Neutro neutralización en 3 de ellos.
T. Ensayo 6 9.8 Básico
● Recomendamos que al momento de
T. Ensayo 7 8.1 Neutro realizar un ensayo de pH básicos
tengan todas sus herramientas
T. Ensayo 8 7.8 Neutro totalmente libres de impurezas o con
restos de reactivos diferentes a los
T. Ensayo 9 9.8 Básico utilizados en el ensayo, para evitar
resultados erróneos o confusión en su
B1:Limón 2.8 Ácido práctica realizada.
B2:Tomate 4.1 Ácido
B3:Huevo 8.4 Neutro
B4:Vinagre 2.9 Ácido
B5:Leche 6.7 Neutro
5. REFERENCIAS
Ocampo, J. C. (2018). Enseñanza-aprendizaje
del concepto de acidez y pH en grado décimo,
bajo la metodología de la ingeniería didáctica.
188.
https://repositorio.unal.edu.co/handle/unal/69
270%0Ahttp://bdigital.unal.edu.co/70911/1/1
016012755.2018.pdf
Ondarse, D. (2015). pH. Concepto.De.
https://concepto.de/ph/
También podría gustarte
- Informe Quimica General 7 - 9 (Reparado)Documento30 páginasInforme Quimica General 7 - 9 (Reparado)Dianita Rodriguez100% (1)
- Determinación de puntos de fusión, ebullición, densidad y solubilidadDocumento32 páginasDeterminación de puntos de fusión, ebullición, densidad y solubilidadSergio Andres Rincon Rodriguez100% (1)
- Sistemas Buffer: Estudio de Ácidos y BasesDocumento13 páginasSistemas Buffer: Estudio de Ácidos y BasesNataly MendozaAún no hay calificaciones
- Pre - Informe Medicion de Propiedades Fisicas de Los Estados Solido y LiquidoDocumento4 páginasPre - Informe Medicion de Propiedades Fisicas de Los Estados Solido y LiquidoJenny chavesAún no hay calificaciones
- Informe de Laboratorio PH y Soluciones AmortiguadorasDocumento7 páginasInforme de Laboratorio PH y Soluciones AmortiguadorasJuan FernandezAún no hay calificaciones
- Informe 1 - Permeabilidad de La Membrana Citoplasmatica (Osmosis)Documento13 páginasInforme 1 - Permeabilidad de La Membrana Citoplasmatica (Osmosis)Lizzet Xiomara Vargas Torres100% (1)
- Informe Lab FisicoquimicaDocumento40 páginasInforme Lab FisicoquimicaCARMENZA100% (1)
- Informe 03 Punto de Ebullicion Del ToluenoDocumento13 páginasInforme 03 Punto de Ebullicion Del ToluenoJimmy Jiménez0% (1)
- Contenido de agua en tejidos biológicosDocumento10 páginasContenido de agua en tejidos biológicosFaiver RemolinaAún no hay calificaciones
- Laboratorio de BiologiaDocumento8 páginasLaboratorio de Biologiaduvarantonio100% (3)
- Diálisis a través de membrana de celofánDocumento4 páginasDiálisis a través de membrana de celofánMario MolinaAún no hay calificaciones
- Parámetros para medir contaminantes en aguas residuales urbanasDocumento3 páginasParámetros para medir contaminantes en aguas residuales urbanascristian mendoza quispeAún no hay calificaciones
- Cuestionario 1Documento8 páginasCuestionario 1Berenice S. OleaAún no hay calificaciones
- Informe Práctica 1Documento20 páginasInforme Práctica 1DianaAún no hay calificaciones
- Determinación de errores de medición en análisis químicoDocumento5 páginasDeterminación de errores de medición en análisis químicoAna Maria Guerrero AgudeloAún no hay calificaciones
- Preinforme Quimica 4 5 6Documento16 páginasPreinforme Quimica 4 5 6Patricia Gomez Daza33% (3)
- Practica 3Documento6 páginasPractica 3JAWERAún no hay calificaciones
- Fundamentos TeoricosDocumento2 páginasFundamentos TeoricosJuan Sebastian Buitrago Ramos0% (1)
- Propiedades físicas de compuestos orgánicosDocumento61 páginasPropiedades físicas de compuestos orgánicosmonica acosta100% (1)
- Práctica 3. Determinación Del PH de Soluciones Ácidas, Básicas y NeutrasDocumento6 páginasPráctica 3. Determinación Del PH de Soluciones Ácidas, Básicas y NeutrasSalomon BonillaAún no hay calificaciones
- Pre InformeDocumento8 páginasPre InformeEdnaJazminOtero0% (1)
- Preinformes Laboratorio Quimica GeneralDocumento65 páginasPreinformes Laboratorio Quimica GeneralDante Lopez70% (10)
- Informe Laboratorio 2 BioquimicaDocumento7 páginasInforme Laboratorio 2 BioquimicaROMER SABOGAL VARGASAún no hay calificaciones
- 1 Informe PH y Soluciones AmortiguadorasDocumento4 páginas1 Informe PH y Soluciones AmortiguadorasJean B. Garcia100% (1)
- Entrenamiento Practico Unidad 3 - QUIMICA GENERAL UNADDocumento7 páginasEntrenamiento Practico Unidad 3 - QUIMICA GENERAL UNADAlexandraAhumada100% (1)
- Tarea 3 Estados de Agregacion y DisolucionesDocumento15 páginasTarea 3 Estados de Agregacion y DisolucionesANDREA ALVAREZ DIAZAún no hay calificaciones
- Solubilidad Orgánica vs InorgánicaDocumento1 páginaSolubilidad Orgánica vs InorgánicaHugo VargasAún no hay calificaciones
- Informe Quimica General Practicas 4,5 y 6Documento30 páginasInforme Quimica General Practicas 4,5 y 6Yenifer De Rozo75% (8)
- Preparación y medición de pH de solucionesDocumento6 páginasPreparación y medición de pH de solucionesAnita Zarza BandaAún no hay calificaciones
- Rasgos Genéticos en El HombreDocumento18 páginasRasgos Genéticos en El HombreUSMP FN ARCHIVOS73% (11)
- Reporte de Practica 3 Ley de CharlesDocumento16 páginasReporte de Practica 3 Ley de CharleslizAún no hay calificaciones
- Informe Quimica 1Documento9 páginasInforme Quimica 1Criadero San FransiscoAún no hay calificaciones
- Componente Practico Microbiología Dairon SanchezDocumento32 páginasComponente Practico Microbiología Dairon SanchezPallares Estrd Miguel100% (1)
- Identificacion de Proteinas Mediante La Reaccion de BiuretDocumento9 páginasIdentificacion de Proteinas Mediante La Reaccion de BiuretAnonymous IG3Pj6AwAún no hay calificaciones
- Química General - Practica No. 9 - Estequiometria de Reacciones Que Involucran Gases y SolucionesDocumento5 páginasQuímica General - Practica No. 9 - Estequiometria de Reacciones Que Involucran Gases y Solucionessvenson1875% (4)
- Balanza analíticaDocumento3 páginasBalanza analíticapolo1526Aún no hay calificaciones
- Preinforme de PHDocumento4 páginasPreinforme de PHAndrey ArizaAún no hay calificaciones
- Practica de Laboratorio 7 y 8 Biologia UnadDocumento11 páginasPractica de Laboratorio 7 y 8 Biologia UnadFernanda PalaciosAún no hay calificaciones
- ConstFísOrgDocumento13 páginasConstFísOrgRichard Antonio QuitianAún no hay calificaciones
- Informe 2 - Constantes FísicasDocumento16 páginasInforme 2 - Constantes FísicasAllison ArevaloAún no hay calificaciones
- Análisis bioquímico de aminoácidos y proteínasDocumento12 páginasAnálisis bioquímico de aminoácidos y proteínasRica3652100% (1)
- Determinación del reactivo limitante en la reacción de formación de carbonato de plomoDocumento7 páginasDeterminación del reactivo limitante en la reacción de formación de carbonato de plomoTatianita HerreraAún no hay calificaciones
- Preparación de Disoluciones AcuosasDocumento22 páginasPreparación de Disoluciones AcuosasPedro YAún no hay calificaciones
- INFORME PRACTICA No 4 POTENCIOMETRIADocumento11 páginasINFORME PRACTICA No 4 POTENCIOMETRIAWilmer Stevens Mena Quintero100% (3)
- Preinforme de Práctica 5Documento5 páginasPreinforme de Práctica 5danielAún no hay calificaciones
- Informe de Laboratorio Sobre SolubilidadDocumento22 páginasInforme de Laboratorio Sobre SolubilidadERWIN ANDRES NAVARRO GOMEZAún no hay calificaciones
- Preinforme 5 de LaboratorioDocumento5 páginasPreinforme 5 de LaboratorioAngie CruzAún no hay calificaciones
- Muestre Todos Los Cálculos Que Se Requieren para Preparar Cada Una de Las Soluciones AnterioresDocumento2 páginasMuestre Todos Los Cálculos Que Se Requieren para Preparar Cada Una de Las Soluciones AnterioresNorela PicoAún no hay calificaciones
- Practicas2 3 4 y 6 Laboratorio Quimica General UnadDocumento37 páginasPracticas2 3 4 y 6 Laboratorio Quimica General UnadWillian PintoAún no hay calificaciones
- Determinacion Del Acido CitricoDocumento6 páginasDeterminacion Del Acido CitricoAaron Huillcas Sullcaray100% (1)
- PRACTICA No 6 Extracción de ADNDocumento14 páginasPRACTICA No 6 Extracción de ADNmarioAún no hay calificaciones
- Reconocimiento de Los Tipos de Reacciones Quimicas Practica-8Documento10 páginasReconocimiento de Los Tipos de Reacciones Quimicas Practica-8Wendy Peralta HerreraAún no hay calificaciones
- Practica N°3: Reconocimiento en Material Biologico de Lipidos y ProteinasDocumento11 páginasPractica N°3: Reconocimiento en Material Biologico de Lipidos y ProteinasCaroTaAr75% (8)
- Diagrama Practica Acidos y Bases Fuerte S y DebilesDocumento2 páginasDiagrama Practica Acidos y Bases Fuerte S y DebilesSara VenturaAún no hay calificaciones
- Informe Prácticas 4, 5 y 6 Del Curso de Biología - Grupo Laboratorio 6Documento35 páginasInforme Prácticas 4, 5 y 6 Del Curso de Biología - Grupo Laboratorio 6Richar Castañeda50% (2)
- Anexo - Tarea 3Documento8 páginasAnexo - Tarea 3Andres Fabian Fonseca Tellez0% (3)
- Medir pH y caracterizar ácidos y basesDocumento9 páginasMedir pH y caracterizar ácidos y basesWillian PintoAún no hay calificaciones
- Guía de Práctica # 1Documento4 páginasGuía de Práctica # 1YefersonAún no hay calificaciones
- g9. Determinación Experimental de PHDocumento4 páginasg9. Determinación Experimental de PHjacobAún no hay calificaciones
- Bioquímica Pra - Informe N°1Documento8 páginasBioquímica Pra - Informe N°1Gianella GarcésAún no hay calificaciones
- Informe de Inorganica II #1 (Hito 4)Documento8 páginasInforme de Inorganica II #1 (Hito 4)LAURA CECILIA COLQUE QUINTANAAún no hay calificaciones
- Guia y Laboratorio 1Documento9 páginasGuia y Laboratorio 1Jeremmy Ernesto Estrada LópezAún no hay calificaciones
- Ejemplos - Co Ejemplos de Calor Específico Sensible y LatenteDocumento8 páginasEjemplos - Co Ejemplos de Calor Específico Sensible y LatenteSanty PerezAún no hay calificaciones
- Practicas LaboratorioDocumento23 páginasPracticas LaboratorioSanty PerezAún no hay calificaciones
- Examen Final 1Documento3 páginasExamen Final 1Santy PerezAún no hay calificaciones
- PérezRamirezSantiago ABPDocumento8 páginasPérezRamirezSantiago ABPSanty PerezAún no hay calificaciones
- Proteina Limpia PDFDocumento37 páginasProteina Limpia PDFJohnattan ElíasAún no hay calificaciones
- Guia StandartDocumento6 páginasGuia StandartdabianaAún no hay calificaciones
- Iglesia y poder eclesiástico en Marsilio de PaduaDocumento105 páginasIglesia y poder eclesiástico en Marsilio de PaduaSanty PerezAún no hay calificaciones
- PolioxometalatoDocumento2 páginasPolioxometalatoVictorAún no hay calificaciones
- FICHA Compuestos-NitrogenadosDocumento9 páginasFICHA Compuestos-NitrogenadosMauricio Valdez MamaniAún no hay calificaciones
- Quimica Organica 5to AñoDocumento5 páginasQuimica Organica 5to AñoAnonymous kEC3kiy100% (2)
- Todos Los Ejercicios Cap 11 RaynerDocumento8 páginasTodos Los Ejercicios Cap 11 RaynerCINDY STEPHANY LEAL SANABRIAAún no hay calificaciones
- Int. A La Experimentacion en Quimica Inorganica y Quimica OrganicaDocumento9 páginasInt. A La Experimentacion en Quimica Inorganica y Quimica Organicatrue storyAún no hay calificaciones
- 4°año-Explica-Guia 4 El CarbonoDocumento4 páginas4°año-Explica-Guia 4 El CarbonoJean De Los SantosAún no hay calificaciones
- Unidad 2. Grupos Funcionales IDocumento21 páginasUnidad 2. Grupos Funcionales IEsteban RamirezAún no hay calificaciones
- Quimica Superint Ii Prim21 01 1Documento3 páginasQuimica Superint Ii Prim21 01 1juan pupucheAún no hay calificaciones
- AI-1 U2-Estequimetría 4IV2 E7Documento6 páginasAI-1 U2-Estequimetría 4IV2 E7GONZALEZ RIOS ANA VALERIAAún no hay calificaciones
- Reglas NomenclaturaDocumento9 páginasReglas NomenclaturaAnita Aldás CárdenasAún no hay calificaciones
- MVDocumento3 páginasMVDiego Emmanuel Sánchez CalderónAún no hay calificaciones
- Acido Sulfonico Ficha de SeguridadDocumento4 páginasAcido Sulfonico Ficha de SeguridadluisAún no hay calificaciones
- Quimica FinalDocumento16 páginasQuimica FinalJuan DelgadoAún no hay calificaciones
- Que Es Una ProteínaDocumento5 páginasQue Es Una ProteínaGuillermina OrdoñoAún no hay calificaciones
- Fundamentos de Manufactura ModernaDocumento12 páginasFundamentos de Manufactura ModernaHernandez Hernandez JavierAún no hay calificaciones
- Nomenclatura Oxidos y Estados Oxidacion TallerDocumento3 páginasNomenclatura Oxidos y Estados Oxidacion TallerFrancisco Pinchao Velez100% (1)
- Reacciones químicas de los monosacáridosDocumento15 páginasReacciones químicas de los monosacáridosJose Luis S GarciaAún no hay calificaciones
- Determinación Mercurimétrica de Cloruros en SangreDocumento3 páginasDeterminación Mercurimétrica de Cloruros en SangreGabriela TorresAún no hay calificaciones
- Ejercicios de RepasoDocumento4 páginasEjercicios de RepasoEnrique PuenteAún no hay calificaciones
- Cinetica Química (Chang)Documento49 páginasCinetica Química (Chang)Cristina Durand RubioAún no hay calificaciones
- Informe Shampoo EmersonDocumento10 páginasInforme Shampoo EmersonJhonatan Vill SejasAún no hay calificaciones
- Tabla Grupos Funcionales - Química OrgánicaDocumento1 páginaTabla Grupos Funcionales - Química OrgánicaAmbar AlmarazAún no hay calificaciones
- Presentación Planta de Amoniaco y Urea (20-05-2016) PDFDocumento23 páginasPresentación Planta de Amoniaco y Urea (20-05-2016) PDFEdson EcosAún no hay calificaciones
- Cuadernillo de Trabajo - MIII - 23-23Documento81 páginasCuadernillo de Trabajo - MIII - 23-23Alex OdkfnAún no hay calificaciones
- Quimica Listo 3Documento8 páginasQuimica Listo 3FABIÁN Ponce Gómez100% (1)
- 0-Práctica de Titulación 2022Documento2 páginas0-Práctica de Titulación 2022Azael MartinAún no hay calificaciones
- Sintesis Del Fenol 1. AntecedentesDocumento19 páginasSintesis Del Fenol 1. AntecedentesFabritzio- KunAún no hay calificaciones
- Práctica #11 Colirios IIIDocumento13 páginasPráctica #11 Colirios IIIEdy CalsinAún no hay calificaciones