Documentos de Académico
Documentos de Profesional
Documentos de Cultura
ESTEQUIOMETRIA
Cargado por
nahum androssiDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
ESTEQUIOMETRIA
Cargado por
nahum androssiCopyright:
Formatos disponibles
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
ESTEQUIOMETRIA
Uno de los núcleos conceptuales de la química, la estequiometría, se ocupa de los aspectos
cuantitativos de la reacción química, entendida como un proceso en el cual una sustancia o varias
sustancias se forman a partir de otra u otras. La química se interesa por la composición y la cantidad
de las sustancias que reaccionan o se producen en un proceso químico. La estequiometría aborda
las relaciones cuantitativas de la química sobre una base cualitativa, conceptual. Resolver
situaciones sobre estequiometría implicaría la comprensión de los conceptos de fórmula química,
reacción química, ecuación química, reactivos y productos, subíndices y coeficientes
estequiométricos. (Raviolo y Lerzo, 2016).
Leyes de combinaciones químicas
Las leyes que rigen toda reacción química son: Leyes ponderales y las leyes volumétricas
1. Leyes Ponderales.
1-a. Ley de conservación de la masa o ley de conservación de la masa. Enunciada en 1875 por
A. L. Lavoisier. En toda transformación química, permanece constante la masa total de las
sustancias que intervienen en toda la reacción.
Ejemplo
2 CH3OH (l) + 3 O2 (g) → 2 CO2 (g) + 4 H2O (l)
2 moles 3 moles 2 moles 4 moles
160 g 160 g
1-b. Ley de las proporciones definidas. Establecida en 1799 por J. L. Proust. Cuando dos o más
elementos se unen para formar un mismo compuesto, lo hacen siempre en una proporción fija.
Ejemplo:
El exceso no reacciona
1-c. Ley de las proporciones múltiples. Esta ley fue enunciada por J. Dalton. Las cantidades de
un mismo elemento que se combinan con una cantidad fija de otro, para formar varios
compuestos, están en la relación a los números enteros y sencillos.
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
1-d. Ley de las proporciones equivalentes o proporciones reciprocas. Fue esbozada en 1792 por
J. B. Richter y completada más tarde por C. F. Wenzel. Los pesos de los cuerpos que reaccionan
con un mismo peso de otro cuerpo, son los mismos que reaccionan entre sí, si la reacción es
posible, o estarán en una relación sencilla.
2Na (s) + Cl2 (g) → 2 NaCl (s) 1ra reaction
46 g 71 g
H2 (g) + Cl2 (g) → 2 HCl (g) 2 da reaccion
2g 71 g
2 Na (s) + H2 (g) → 2 NaH(s) 3 ra reacciòn
46 g 2g
2. Leyes Volumétricas.
Ley de los volúmenes de combinación. Fue establecida en 1808 por J. L. Gay-Lussac. La relación
volumétrica de las sustancias gaseosas que intervienen en una reacción química, pueden
expresarse por números enteros y sencillos.
N2 (g) + 3 H2 (g) → 2 NH3 (g)
1 mol 3 moles 2 moles
1V 3v 2V
22.4 L 3(22.4L) 2 (22.4L) a CN
Relaciones masa a masa
El metanol (CH3OH) se quema en aire de acuerdo con la siguiente ecuación:
2 CH3OH (l) + 3 O2 (g) → 2 CO2 (g) + 4 H2O (l)
Si se utilizan 209 g de metanol en un proceso de combustión, ¿cuál será la masa de agua producida?
2 CH3OH (l) + 3 O2 (g) → 2 CO2 (g) + 4 H2O (l)
64 g 72 g
72 g H2O
209 g CH3OH x = 235 .13 g H2O
64 g CH3OH
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
Relaciones masa a volumen
El metanol (CH3OH) se quema en aire de acuerdo con la siguiente ecuación:
2 CH3OH (l) + 3 O2 (g) → 2 CO2 (g) + 4 H2O (l)
Si se utilizan 209 g de metanol en un proceso de combustión a condiciones normales ¿cuál será el
volumen de oxido de carbono (IV) producido?
2 CH3OH (l) + 3 O2 (g) → 2 CO2 (g) + 4 H2O (l)
2 moles 2 moles
64 g 44.8 L
2 mol CO2 22.4 L
3.27 moles CH3OH x = 146.5 L CO2
x
1 mol CH3OH 1 mol CO2
Relaciones volumen a volumen
A partir de la siguiente ecuación
Calcule los litros de NO a CN que se produce cuando reaccionan 22.4 L de amoniaco
4 moles 4 moles
89.6 L 89.6 L
22.4 L x
Rpta = 22.4L de NO
Porcentaje de pureza
Cuando se realizan cálculos estequiometricos es necesario tener en cuenta el porcentaje de pureza
de los reactivos con los que se trabaja, por ejemplo:
Una piedra caliza tiene una pureza en CaCO3 del 92%. ¿Cuántos gramos de cal viva (CaO) se
obtendrán por descomposición térmica de 200 g de la misma?
CaCO3 (s) + calor → CaO (s) + CO2 (g)
100 g 56 g
184 g X
Rpta= 103 g de CaO
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
Reactivo Limitante
Fuente: Chang y Goldsby (2017) Química. Duodécima edición
Fuente: Chang y Goldsby (2017) Química. Duodécima edición
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
Ejemplo de aplicación
RENDIMIENTO DE REACCION
La cantidad de reactivo limitante determina el rendimiento de una reacción, es decir la cantidad de
producto que se obtendrá cuando reaccione todo el reactivo limitante. Se determina mediante la
siguiente ecuación:
𝑟𝑒𝑛𝑑𝑖𝑚𝑖𝑒𝑛𝑡𝑜 𝑟𝑒𝑎𝑙
𝑃𝑜𝑟𝑐𝑒𝑛𝑡𝑎𝑗𝑒 𝑑𝑒 𝑟𝑒𝑛𝑑𝑖𝑚𝑖𝑒𝑛𝑡𝑜 = 𝑥 100
𝑟𝑒𝑛𝑑𝑖𝑚𝑖𝑒𝑛𝑡𝑜 𝑡𝑒𝑜𝑟𝑖𝑐𝑜
El rendimiento real es casi siempre menor que el rendimiento teórico debido a que algunas
reacciones son reversibles y no se completan al 100 % , y aunque sea al 100% es difícil recuperar
todo el producto del medio de la reacción y en algunas reacciones complicada una vez obtenidos los
productos estos siguen reaccionando entre si o con los reactivos.
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
EJERCICIOS
1. La sosa cáustica, NaOH, suele prepararse industrialmente con la reacción de carbonato de sodio, con
cal apagada Ca(OH)2 ¿Cuántos gramos de NaOH se pueden obtener al hacer reaccionar 1 kg de
carbonato de calcio con cal apagada?(Schaum)
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
2. ¿Cuántos gramos de Ca3(PO4)2 se pueden obtener mezclando una disolución que contiene 5?00 g de
cloruro de calcio con otra que contiene 8.00 g de fosfato de potasio? La reacción es:
3CaCl2 + 2K3PO4 → Ca3(PO4)2 + 5KCl
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
3. El nonano es un componente de la gasolina y se encontró en un incendio que, se sospecha, fue provocado.
a) Escriba la ecuación balanceada de la combustión de nonano, C9H20, en el aire
b) ¿Cuántos gramos de oxígeno, O2, se requieren para quemar 500 g de nonano?
c) Si 32 g de O2 ocupan 22.4 L a 0°C y 1 atm, ¿qué volumen de oxígeno bajo esas condiciones
se requiere para quemar el nonano?
4. El cianuro de hidrógeno gaseoso es un gas que se usaba como método de pena de muerte. Se dejaban caer
pastillas de cianuro de potasio en una disolución de HCl para formar el HCN.
a) Escriba la reacción balanceada de producción de HCN de esta manera.
b) ¿Qué masa de KCN produce 4 moles de HCN gaseoso?
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
5. El disulfuro de carbono, CS2, se puede obtener a partir del dióxido de azufre, SO2, un producto de desecho en
muchos procesos industriales. ¿Cuánto CS2 puede obtenerse a partir de 450 kg de SO2 con exceso de coque, si la
conversión de SO2 tiene 82% de eficiencia? La reacción total es
5C + 2SO2 → CS2 + 4CO
6.
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
La nitroglicerina (C3H5N3O9) es un explosivo muy potente. Su descomposición se puede
representar mediante la siguiente ecuación:
4C3H5N3O9 → 6 N2 + 12CO2 + 10 H2O + O2
Esta reacción genera una gran cantidad de calor y muchos productos gaseosos. La velocidad de
formación de estos gases, así como su rápida expansión, es lo que causa la explosión:
a) ¿Cuál es la máxima cantidad de O2 en gramos que se obtendrá a partir de 2.00 x 102
g de nitroglicerina?
b) Calcule el porcentaje de rendimiento de esta reacción si se encuentra que la cantidad
de O2 producida fue de 6.55 g.
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
UNIVERSIDAD NACIONAL DE SAN ANTONIO ABAD DEL CUSCO
QUIMICA GENERAL E INORGANICA
Bibliografía
Chang y Goldsby (2017) Química. Duodécima edición. McGRAW-HILL/INTERAMERICANA
EDITORES, S.A. DE C.V. México
Raviolo, A., y Lerzo, G. (2016). Enseñaanza de la estequiometría: uso de analogías y comprensión
conceptual. Recuperado de: http://dx.doi.org/10.1016/j.eq.2016.04.003
Rosenberg, J. (2009). Química. Novena edición. McGRAW-HILL/INTERAMERICANA EDITORES,
S.A. DE C.V. Mexico.
Mstro. Juana Graciela Torres Polanco Ciclo de Verano 2020-2V
También podría gustarte
- Experiment oDocumento9 páginasExperiment ogiselxAún no hay calificaciones
- Problemas Analisis 8.3Documento3 páginasProblemas Analisis 8.3Adri EmmaAún no hay calificaciones
- Resutados y AnalisisDocumento4 páginasResutados y Analisismauricio pinedaAún no hay calificaciones
- Sistemas de oxidación-reducción: reacciones redox y celdas electroquímicasDocumento14 páginasSistemas de oxidación-reducción: reacciones redox y celdas electroquímicasMontserrat Concepción Portilla MarínAún no hay calificaciones
- Efecto de Ion ComúnDocumento1 páginaEfecto de Ion ComúnuniversoexactoAún no hay calificaciones
- Halogenos Obtencion y PropiedadesDocumento15 páginasHalogenos Obtencion y PropiedadesEber Juan Chira CanchosAún no hay calificaciones
- PLANCHASSDocumento5 páginasPLANCHASSRobinsonAún no hay calificaciones
- Informe Viscosímetro HopplerDocumento3 páginasInforme Viscosímetro HopplerKarina GarciaAún no hay calificaciones
- Trabajo Grupal 5Documento1 páginaTrabajo Grupal 5Richard Qvispe CAún no hay calificaciones
- Propiedades Mecánicas de Los MetalesDocumento44 páginasPropiedades Mecánicas de Los MetalesKarin AndersonAún no hay calificaciones
- QA 02 Complejos Problemas01Documento6 páginasQA 02 Complejos Problemas012112mariaAún no hay calificaciones
- Aporte 2 Parcial 1 Nov2019Documento2 páginasAporte 2 Parcial 1 Nov2019LanderPerezAún no hay calificaciones
- Jcasleon - Problemas GravimetríaDocumento3 páginasJcasleon - Problemas GravimetríaLuis Felipe Vega RodriguezAún no hay calificaciones
- Taller de Gravimetria y VolumetriaDocumento2 páginasTaller de Gravimetria y VolumetriaKristian Zubiria PerezAún no hay calificaciones
- Taller Titulaciones Acido BaseDocumento5 páginasTaller Titulaciones Acido BaseMartinoliAún no hay calificaciones
- Ejercicios QuimicaDocumento7 páginasEjercicios QuimicaZHARICK VANESSA SALDAÑA MEJIAAún no hay calificaciones
- Ejerci Reacc Disol AcuosaDocumento4 páginasEjerci Reacc Disol AcuosaalejandroAún no hay calificaciones
- Informe - Grupo de La Plata FherDocumento6 páginasInforme - Grupo de La Plata FherGC FernandoAún no hay calificaciones
- AnitaDocumento6 páginasAnitaCèsar Eduardo Vásquez VásquezAún no hay calificaciones
- Teorema Pi BuckinghamDocumento2 páginasTeorema Pi BuckinghamAlejandro_Fuen_96090% (1)
- Reporte P2 - Lab - TermodinamicaDocumento15 páginasReporte P2 - Lab - TermodinamicaAnnel AquinoAún no hay calificaciones
- Taller SolucionesDocumento5 páginasTaller SolucionesJANIS RIVERA DIAZAún no hay calificaciones
- Qui Gen Gui8Documento8 páginasQui Gen Gui8Ale MAún no hay calificaciones
- Taller de FisicoquimicaDocumento8 páginasTaller de FisicoquimicaDaniel Santos GarciaAún no hay calificaciones
- Problemas de Combustion y TostaciónDocumento17 páginasProblemas de Combustion y TostaciónEdwin Cirilo ChaucaAún no hay calificaciones
- Balance de materia y energía en reacciones químicasDocumento1 páginaBalance de materia y energía en reacciones químicasVDAún no hay calificaciones
- Informe 1 - 92GDocumento19 páginasInforme 1 - 92GJhon Paul Sanchez100% (1)
- Disoluciones No Ideales - FQDocumento29 páginasDisoluciones No Ideales - FQFrank León La CruzAún no hay calificaciones
- QA Problemas de QuímicaDocumento22 páginasQA Problemas de Químicagr4ndeunicornAún no hay calificaciones
- CV-T4 Geogebra y SymbolabDocumento14 páginasCV-T4 Geogebra y SymbolabSebastian Vargas García100% (1)
- Tarea Nº3Documento34 páginasTarea Nº3R RodríguezAún no hay calificaciones
- CineticaDocumento28 páginasCineticaCarlos Abarca GamboaAún no hay calificaciones
- Problemas Fisicoquímica U1Documento19 páginasProblemas Fisicoquímica U1Diego Andrade AlemanAún no hay calificaciones
- Taller 4 Aplicaciones de Las Valoraciones Acido-S BaseDocumento1 páginaTaller 4 Aplicaciones de Las Valoraciones Acido-S BaseCarolina posadaAún no hay calificaciones
- Informe de LaboratorioDocumento7 páginasInforme de Laboratorioaleven quispeAún no hay calificaciones
- Masa atómica magnesioDocumento6 páginasMasa atómica magnesioHenry Giampiere Reyna RamosAún no hay calificaciones
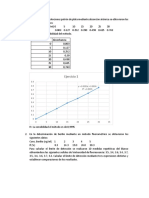
- Análisis de plata y berilio mediante absorción atómica y fluorometríaDocumento2 páginasAnálisis de plata y berilio mediante absorción atómica y fluorometríaNatasha VargasAún no hay calificaciones
- Determinación Del Calor de NeutralizaciónDocumento11 páginasDeterminación Del Calor de NeutralizaciónLUIS ALBERTO PEREZ GARCIA100% (1)
- Taller 2 PDFDocumento6 páginasTaller 2 PDFsebastian gonzalezAún no hay calificaciones
- EJERCICIOS GasesDocumento3 páginasEJERCICIOS Gasesmary kely chambi choque100% (1)
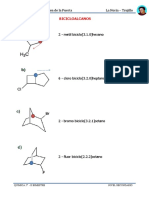
- BicicloalcanosDocumento3 páginasBicicloalcanosGrecia NicolleAún no hay calificaciones
- Taller #3 de Quimica Analitica Universidad de Cartagena Facultad de Ingeniería, Programa de Ingeniería Química Cuarto SemestreDocumento5 páginasTaller #3 de Quimica Analitica Universidad de Cartagena Facultad de Ingeniería, Programa de Ingeniería Química Cuarto SemestreJuanito Alcachofa100% (1)
- Laboratorio de Química - Informe de Práctica sobre EstequiometríaDocumento16 páginasLaboratorio de Química - Informe de Práctica sobre EstequiometríaDiana Supo OsorioAún no hay calificaciones
- Ejercicios Estequiometria 29102 PDFDocumento47 páginasEjercicios Estequiometria 29102 PDFWendy AvilaAún no hay calificaciones
- Entalpia Casos de EstudioDocumento3 páginasEntalpia Casos de EstudioRobert Joaquin Medina RamosAún no hay calificaciones
- Tallerdeunidadesdeconcentración2020 IDocumento4 páginasTallerdeunidadesdeconcentración2020 ILuis Enrique LagunaAún no hay calificaciones
- Laboratorio Analítica Práctica 9Documento10 páginasLaboratorio Analítica Práctica 9Ever Tola FloresAún no hay calificaciones
- Obtención de metano a través de descarboxilación por fusión alcalinaDocumento9 páginasObtención de metano a través de descarboxilación por fusión alcalinaDaniela AlvarezAún no hay calificaciones
- Progra Tarea 4Documento20 páginasProgra Tarea 4Rodriguez Mamani100% (1)
- 1er Parcial SolucionDocumento6 páginas1er Parcial SolucionZambrana Ocaña Jorge LuisAún no hay calificaciones
- EJERCICIDocumento11 páginasEJERCICIGega123Aún no hay calificaciones
- Problemario U2Documento6 páginasProblemario U2JUAN GERARDO CIGARROA RENDONAún no hay calificaciones
- Transferencia de CalorDocumento2 páginasTransferencia de CalorWoody33Aún no hay calificaciones
- Analitica ComplejosDocumento6 páginasAnalitica ComplejosJesus David PerezAún no hay calificaciones
- Taller SolubilidadDocumento2 páginasTaller SolubilidadJulian Alvarez0% (1)
- USO DE COORDENADAS RECTANGULARES Y POLARESDocumento11 páginasUSO DE COORDENADAS RECTANGULARES Y POLARESlucio RAún no hay calificaciones
- Problemas de ErroresDocumento4 páginasProblemas de ErroresAraceli67% (3)
- MG 5° EstequiometriaDocumento24 páginasMG 5° EstequiometriaPhoto MemoriesAún no hay calificaciones
- 13.1. Tema EstequiometríaDocumento21 páginas13.1. Tema EstequiometríaDaniel AcostaAún no hay calificaciones
- Tema 10 - La Reaccion QuimicaDocumento9 páginasTema 10 - La Reaccion Quimicaapi-3810262100% (2)
- Shrek - Wikipedia, La EnciclopediaDocumento14 páginasShrek - Wikipedia, La Enciclopedianahum androssiAún no hay calificaciones
- Sarita Colonia, santa popular peruana venerada por sus milagrosDocumento10 páginasSarita Colonia, santa popular peruana venerada por sus milagrosnahum androssiAún no hay calificaciones
- George Gurdjieff - WikipediaDocumento17 páginasGeorge Gurdjieff - Wikipedianahum androssiAún no hay calificaciones
- La DAO (Organización)Documento11 páginasLa DAO (Organización)nahum androssiAún no hay calificaciones
- Problemas Propuestos y Resueltos Dinc3a1mica CircularDocumento5 páginasProblemas Propuestos y Resueltos Dinc3a1mica Circularnahum androssiAún no hay calificaciones
- Yin y Yang - Wikipedia, La EnciclopedieDocumento10 páginasYin y Yang - Wikipedia, La Enciclopedienahum androssiAún no hay calificaciones
- Qi en la medicina chinaDocumento8 páginasQi en la medicina chinanahum androssiAún no hay calificaciones
- Prácticas Sexuales Taoístas - WikieDocumento9 páginasPrácticas Sexuales Taoístas - Wikienahum androssiAún no hay calificaciones
- Samael Aun Weor - WikipediaDocumento21 páginasSamael Aun Weor - Wikipedianahum androssiAún no hay calificaciones
- Mantak Chia - WikipediaDocumento6 páginasMantak Chia - Wikipedianahum androssiAún no hay calificaciones
- Resist Materiales ExDocumento5 páginasResist Materiales Exnahum androssiAún no hay calificaciones
- Cuerpo Astral - WireDocumento11 páginasCuerpo Astral - Wirenahum androssiAún no hay calificaciones
- Equilibrio IonicoDocumento4 páginasEquilibrio Ioniconahum androssiAún no hay calificaciones
- QUI-UNSAAC-SILABO-QUIMICADocumento7 páginasQUI-UNSAAC-SILABO-QUIMICAnahum androssiAún no hay calificaciones
- Mecanica Clasica e LazoDocumento277 páginasMecanica Clasica e LazoEliezer Vladimir CastroAún no hay calificaciones
- Topografia para Ing CivilesDocumento191 páginasTopografia para Ing CivilesJavier Gonzalez Gamez100% (1)
- Edgar Cayce Sobre Canalizando Su Yo Superior (Henry Reed)Documento242 páginasEdgar Cayce Sobre Canalizando Su Yo Superior (Henry Reed)Dennis Alexéi100% (2)
- FUERZA RELATIVA DE LOS ACIDOS Y BASES-pH-pOH-pK-Ka-KbDocumento13 páginasFUERZA RELATIVA DE LOS ACIDOS Y BASES-pH-pOH-pK-Ka-Kbnahum androssiAún no hay calificaciones
- 1 Temario o Sílabus Walter Lauro PerezDocumento9 páginas1 Temario o Sílabus Walter Lauro Pereznahum androssiAún no hay calificaciones
- Principio de Le ChatelierDocumento9 páginasPrincipio de Le Chateliernahum androssiAún no hay calificaciones
- ELECTROQUIMICADocumento13 páginasELECTROQUIMICAnahum androssiAún no hay calificaciones
- Aplicaciones de MovimientoDocumento36 páginasAplicaciones de MovimientoDiego VargasAún no hay calificaciones
- EL AGUA-propiedades - Tipos-DurezaDocumento5 páginasEL AGUA-propiedades - Tipos-Durezanahum androssiAún no hay calificaciones
- Poleas PDFDocumento25 páginasPoleas PDFDiana CordobaAún no hay calificaciones
- Conceptos Acido-BaseDocumento3 páginasConceptos Acido-Basenahum androssiAún no hay calificaciones
- MINEROLOGIADocumento49 páginasMINEROLOGIAnahum androssiAún no hay calificaciones
- Contaminacion Del Aire-Agua y SueloDocumento26 páginasContaminacion Del Aire-Agua y Suelonahum androssiAún no hay calificaciones
- Los Siete RayosDocumento87 páginasLos Siete RayosXavierFdz100% (1)
- Maria Ejemplo A SeguirDocumento77 páginasMaria Ejemplo A Seguirnahum androssiAún no hay calificaciones
- Informe de Investigacion EstresDocumento43 páginasInforme de Investigacion EstresAlexander TomeAún no hay calificaciones
- Grupo 81 Trabajo de PotenciaDocumento11 páginasGrupo 81 Trabajo de PotenciajenniferAún no hay calificaciones
- Evaluación Heurística de InterfacesDocumento26 páginasEvaluación Heurística de InterfacesENMANUEL NERI USCUVILCA LOAYZAAún no hay calificaciones
- El Amor Que SantificaDocumento6 páginasEl Amor Que SantificaAguas de Mar CartagenaAún no hay calificaciones
- Qué Es La MotivaciónDocumento4 páginasQué Es La MotivaciónMaggie AMAún no hay calificaciones
- EA-Unidad 1Documento33 páginasEA-Unidad 1LADY CAROLINA BETANCUR CÁRCAMOAún no hay calificaciones
- La Evaluacion Formativa en El Plan de Estudios 2022 Resumen e InstrumentosDocumento15 páginasLa Evaluacion Formativa en El Plan de Estudios 2022 Resumen e InstrumentosSandy GuzmanAún no hay calificaciones
- Arqueologia Actividad 6Documento3 páginasArqueologia Actividad 6Maria Caicedo EnríquezAún no hay calificaciones
- Langostinos - Martin 1Documento26 páginasLangostinos - Martin 1Katherine Llerena CalderónAún no hay calificaciones
- Problemas de fluidos mecánicos: caudales, presiones y pérdidas de cargaDocumento10 páginasProblemas de fluidos mecánicos: caudales, presiones y pérdidas de cargaJolehisy Acevedo MedinaAún no hay calificaciones
- Proyecto de Mejora de Jornada ContinuaDocumento26 páginasProyecto de Mejora de Jornada Continuaelsextopisoblog100% (1)
- Manual de RefrigeradoraDocumento12 páginasManual de RefrigeradoraMarlon ChavezAún no hay calificaciones
- El Pacto MatrimonialDocumento2 páginasEl Pacto Matrimoniallfhpublicidad100% (1)
- Tarea 3 Jorge JuarezDocumento5 páginasTarea 3 Jorge JuarezPepe Sepulveda Yañez100% (1)
- Dios Otero David CD Tarea1.7Documento3 páginasDios Otero David CD Tarea1.7David DiosAún no hay calificaciones
- Sistemas de conservación de forrajeDocumento6 páginasSistemas de conservación de forrajeFelipe FernándezAún no hay calificaciones
- CARBOHIDRATOSDocumento14 páginasCARBOHIDRATOSjesus alejandroAún no hay calificaciones
- Facultad de Ciencias Naturales Y MatemáticasDocumento120 páginasFacultad de Ciencias Naturales Y MatemáticasAndres BalcazarAún no hay calificaciones
- Estructura curricular del Bachillerato Tecnológico en la carrera de Técnico en Construcción y Reparación NavalDocumento97 páginasEstructura curricular del Bachillerato Tecnológico en la carrera de Técnico en Construcción y Reparación NavalJavith DeJesús Pertuz RicardoAún no hay calificaciones
- Diseño Mecanico de MotorreductorDocumento16 páginasDiseño Mecanico de MotorreductorEduardoAún no hay calificaciones
- Sesion 1 Soldadura de Estruct Segun Aws D1.1 PDFDocumento43 páginasSesion 1 Soldadura de Estruct Segun Aws D1.1 PDFBrayan ChagllaAún no hay calificaciones
- Valvulas Ventosas PDFDocumento8 páginasValvulas Ventosas PDFhomero_parraAún no hay calificaciones
- Proapsi080302 Tratamiento Del Trastorno Límite de La Personalidad Con Antagonistas OpioidesDocumento56 páginasProapsi080302 Tratamiento Del Trastorno Límite de La Personalidad Con Antagonistas OpioidesEzequiel BollatiAún no hay calificaciones
- Practica Calificada Nro. 2-DINAMICADocumento21 páginasPractica Calificada Nro. 2-DINAMICAFernando David Siles NatesAún no hay calificaciones
- Alte BrueDocumento22 páginasAlte BrueFrançoiseIvonneCareauMeraAún no hay calificaciones
- Informe PsicológicoDocumento2 páginasInforme PsicológicoMomita AlitaAún no hay calificaciones
- Gestion FinancieraDocumento16 páginasGestion FinancieraGloria GRAún no hay calificaciones
- Plantilla Inicial PacientesDocumento3 páginasPlantilla Inicial PacientesMIGUEL MATEUS TORRADO MARTINEZAún no hay calificaciones
- Dualist ADocumento2 páginasDualist AangryvikingAún no hay calificaciones
- ReseñaDocumento6 páginasReseñajoseantonioaar0% (1)