Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Resumen de Soluciones para Los Alumnos
Cargado por
Alfredo FernandezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Resumen de Soluciones para Los Alumnos
Cargado por
Alfredo FernandezCopyright:
Formatos disponibles
Universidad Nacional de Piura Química General
TEMA: SOLUCIONES
En química, una solución o disolución (del latín disoluto) es una mezcla
homogénea, a nivel molecular de una o más especies químicas que no
reaccionan entre sí; cuyos componentes se encuentran en proporción que varía
entre ciertos límites.
Gran parte de los líquidos que conocemos o que manejamos habitualmente son
soluciones o disoluciones. El agua de mar, la saliva, la orina, la lavandina, el
vinagre y al agua que bebemos son ejemplos de soluciones.
“Una solución es un sistema homogéneo formado por dos o más
sustancias puras, que no reaccionan entre sí”.
COMPONENTES DE UNA SOLUCION
El termino solución se usa en química para describir un sistema en la cual una o
mas sustancias están mezcladas homogéneamente o disueltas, en otra sustancia.
Por la cual decimos que una solución simple tiene dos componentes importantes
los cuales son:
SOLUTO
Componente minoritario de una disolución. Los solutos pueden ser sólidos,
líquidos o gaseosos. Un ejemplo de soluto sólido son las sales, o el azúcar,
disueltos en agua. Un soluto líquido es el etanol disuelto en agua, como ocurre en
el vino y los licores. Un soluto gaseoso, por ejemplo, puede ser el anhídrido
carbónico disuelto en agua, caso de las bebidas carbónicas.
Una disolución está formada por el disolvente y uno o más solutos.
Generalmente llamamos disolvente a la sustancia que se encuentra en mayor
proporción y llamamos solutos a las sustancias restantes. La solución se presenta
en el mismo estado físico que el solvente.
Ej. : Si se disuelve 2 g de glucosa, C6O6H12, en 10 mL de agua se obtiene una
solución líquida (estado físico del agua). El azúcar es el soluto y el agua el
solvente:
Soluto + solvente = solución
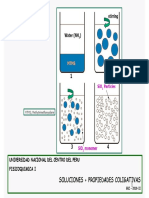
En la figura se da un ejemplo de una disolución
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
líquida: azúcar – agua. Los círculos blancos representan las moléculas de agua y
los grises, las de azúcar. Las moléculas de azúcar se distribuyen
homogéneamente en el solvente agua y el sistema presenta las mismas
propiedades intensivas en todos los puntos del mismo.
Aunque es frecuente asociar la palabra disolución con el hecho de disolver una
sustancia sólida en un líquido, generalmente agua, existen otras clases de
disoluciones. Por ejemplo: soluciones sólidas como el acero, que es una mezcla
homogénea de hierro, carbono y otros metales, o soluciones gaseosas como el
aire, que es una mezcla de nitrógeno, oxígeno, dióxido de carbono y otros gases
en menor proporción.
CLASIFICACIÓN DE LAS SOLUCIONES
a) Por su estado agregación:
Sólidas: Sólido en sólido: aleaciones como zinc en estaño (latón);
gas en sólido: hidrógeno en paladio; líquido en sólido: mercurio en
plata (amalgama).
Líquidas: líquido en líquido: alcohol en agua; sólido en líquido: sal en agua
(salmuera); gas en líquido: oxígeno en agua
Gaseosas: gas en gas: oxígeno en nitrógeno; gas en líquido: gaseosas,
cervezas; gas en sólido: hidrógeno absorbido sobre superficies de
Ni, P.D., Pt, etc.
b) sus componentes:
SOLUCIÓN DISOLVENTE SOLUTO EJEMPLOS
Gaseosa Gas Gas Aire
Líuida Líquido Líquido Alcohol en agua
Líquida Líquido Gas O2 en H2O
Líquida Líquido Sólido NaCl en H2O
c) Por su concentración y/o Solubilidad:
Solución no saturada (insaturada): Solución que contiene una
cantidad de soluto menor que la que el solvente puede disolver a esa
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
presión y esa temperatura. Es aquella en donde la fase dispersa y la
dispersante no están en equilibrio a una temperatura dada; es decir,
ellas pueden admitir más soluto hasta alcanzar su grado de saturación.
Estas a su vez pueden ser:
Soluciones diluidas
Soluciones Concentradas.
Ejemplo: a 0ºC, 100g de agua disuelven 37,5 NaCl, es decir, a la
temperatura dada, una disolución que contengan 20g NaCl en 100g de
agua, es no saturada.
Solución saturada: Solución que contiene la máxima cantidad de soluto
que el solvente puede disolver a esa presión y esa temperatura. En esta
disolución hay un equilibrio entre la fase dispersa y el medio dispersante,
ya que a la temperatura que se tome en consideración, el solvente no es
capaz de disolver más soluto.
Ejemplo: una disolución acuosa saturada de Nací es aquella que
contiene 37,5g disueltos en 100g de agua 0ºC.
Si se le agrega más soluto no lo disuelve: si es un sólido en un solvente
líquido, el exceso sedimenta; si es un líquido en solvente líquido, el
exceso queda separado del solvente por encima o por debajo según su
densidad relativa; si es un gas en un solvente líquido, el exceso de
soluto escapa en forma de burbujas.
En una solución saturada de un sólido en un líquido, el proceso de
disolución tiene la misma velocidad que el proceso de precipitación.
Solución sobre saturada: es aquella solución que representa un tipo de
disolución inestable, ya que presenta disuelto más soluto que el
permitido para la temperatura dada. Para preparar este tipo de
disolución se agrega soluto en exceso, a elevada temperatura y luego se
enfría el sistema lentamente. Esta disolución es inestable, ya que al
añadir un cristal muy pequeño del soluto, el exceso existente precipita;
de igual manera sucede con un cambio brusco de temperatura.
PROPIEDADES DE LAS SOLUCIONES
Sus propiedades físicas dependen de su concentración:
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Disolución HCl (ácido clorhídrico) 12 mol/L Densidad = 1,18 g/cm 3
Disolución HCl (ácido clorhídrico) 6 mol/L Densidad = 1,10 g/cm 3
Las propiedades químicas de los componentes de una solución no se
alteran.
Las propiedades físicas de la solución son diferentes a las del solvente
puro:
La adición de un soluto a un solvente aumenta su punto de ebullición y
disminuye su punto de congelación; la adición de un soluto a un solvente
disminuye la presión de vapor de éste.
Sus componentes se separan por cambios de fases, como la fusión,
evaporación, condensación, etc.
Tienen ausencia de sedimentación, es decir al someter una disolución a un
proceso de centrifugación las partículas del soluto no sedimentan debido a
que el tamaño de las mismas son inferiores a 10 Ángstrom (ºA).
El hecho de que las disoluciones sean homogéneas quiere decir que sus
propiedades son siempre constantes en cualquier punto de la mezcla.
Las propiedades que cumplen las disoluciones se llaman propiedades
coligativas.
El soluto permanece distribuido uniformemente en toda la solución y no se
asienta con el transcurso del tiempo.
Generalmente se puede separar del soluto del solvente solo con medios
físicos; por ejemplo la evaporación.
Las partículas de soluto tienen tamaño iónico o molecular.
Cuando se añade un soluto a un solvente, se alteran algunas propiedades
físicas del solvente.
Al aumentar la cantidad del soluto, sube el punto de ebullición y desciende
el punto de solidificación. Así, para evitar la congelación del agua utilizada
en la refrigeración de los motores de los automóviles, se le añade un
anticongelante (soluto). Pero cuando se añade un soluto se rebaja la
presión de vapor del solvente.
Otra propiedad destacable de una solución es su capacidad para ejercer
una presión osmótica. Si separamos dos soluciones de concentraciones
diferentes por una membrana semipermeable (una membrana que permite
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
el paso de las moléculas del solvente, pero impide el paso de las del
soluto), las moléculas del solvente pasarán de la solución menos
concentrada a la solución de mayor concentración, haciendo a esta última
más diluida. Estas son algunas de las características de las soluciones:
Las partículas de soluto tienen menor tamaño que en las otras clases de
mezclas.
Presentan una sola fase, es decir, son homogéneas.
Si se dejan en reposo durante un tiempo, las fases no se separan ni se
observa sedimentación, es decir las partículas no se depositan en el fondo
del recipiente.
Pueden ser totalmente transparentes, es decir, permiten el paso de la luz.
Sus componentes o fases no pueden separarse por filtración
FACTORES QUE INFLUYEN EN LA VELOCIDAD DE DISOLUCIÓN:
a) tamaño de las partículas del soluto;
b) naturaleza física del soluto;
c) naturaleza física del solvente;
d) temperatura; y
e) grado de agitación del soluto y del solvente.
SOLUBILIDAD
La solubilidad es la cantidad máxima de un soluto que puede disolverse en una
cantidad dada de solvente a una determinada temperatura.
“La solubilidad es la medida o magnitud que indica la cantidad máxima de soluto
que puede disolverse en una cantidad determinada de solvente y a una
temperatura dada”.
La solubilidad es una medida de la capacidad de una determinada sustancia para
disolver en un líquido. Puede expresarse en moles por litro, en gramos por litro, o
en porcentaje de soluto; en algunas condiciones se puede sobrepasarla,
denominándose solución sobresaturada.
En la solubilidad, el carácter polar o apolar de la sustancia influye mucho, ya que,
debido a estos la sustancia será más o menos soluble, por ejemplo: Los
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
compuestos con más de un grupo funcional presentan gran polaridad por lo que
no son solubles en éter etílico. Entonces para que sea soluble en éter etílico ha de
tener poca polaridad, es decir no ha de tener más de un grupo polar el
compuesto. Los compuestos con menor solubilidad son los que presentan menor
reactividad como son: las parafinas, compuestos aromáticos y los derivados
halogenados.
El término solubilidad se utiliza tanto para designar al fenómeno cualitativo del
proceso de disolución como para expresar cuantitativamente la concentración de
las soluciones. La solubilidad de una sustancia depende de la naturaleza del
disolvente y del soluto, así como de la temperatura y la presión del sistema, es
decir, de la tendencia del sistema a alcanzar el valor máximo de entropía. Al
proceso de interacción entre las moléculas del disolvente y las partículas del
soluto para formar agregados se le llama solvatación y si el solvente es agua,
hidratación.
Las unidades de expresión para la solubilidad son variadas, en general se
expresa en g/l (gramos/litros).
Ejemplo: La solubilidad de la sal común (cloruro de sodio) es de 360 g/l en agua a
20ºC.
Este valor indica que en un litro de agua (1000 CC) a 20ºC, la cantidad máxima
de cloruro de sodio que se puede disolver es 360 gramos.
Pueden presentarse dos situaciones en particular para la solubilidad:
Si dos solutos son solubles en un mismo solvente, dependiendo de las
cantidades (pequeñas) pueden disolverse ambos sin ninguna dificultad, pero en
general la sustancia de mayor solubilidad desplaza de la solución a la de menor
solubilidad, ejemplo: al agregar azúcar o sal a una bebida, inmediatamente se
produce el escape del gas disuelto en ella.
Si un soluto es soluble en dos solventes inmiscibles (no se mezclan) entre sí, el
soluto se disuelve en ambos solventes distribuyéndose proporcionalmente de
acuerdo a sus solubilidades en ambos solventes
La solubilidad en un líquido dado, depende de la naturaleza del soluto y del
solvente, de la temperatura y de la presión. Las variaciones del valor de la presión
atmosférica solo producen cambios despreciables en la solubilidad de los líquidos
o de los sólidos en líquidos.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
En cambio la solubilidad de los gases en los líquidos varía en proporción directa
de la presión parcial del gas que se solubiliza. En los sólidos y líquidos la mayoría
de las solubilidades aumentan con la temperatura.
Factores que afectan la solubilidad:
Los factores que afectan la solubilidad son:
a) Superficie de contacto: La interacción soluto-solvente aumenta cuando hay
mayor superficie de contacto y el cuerpo se disuelve con más rapidez
(pulverizando el soluto).
b) Agitación: Al agitar la solución se van separando las capas de disolución que
se forman del soluto y nuevas moléculas del solvente continúan la disolución
c) Temperatura: Al aument6ar la temperatura se favorece el movimiento de las
moléculas y hace que la energía de las partículas del sólido sea alta y puedan
abandonar su superficie disolviéndose.
d) Presión: Esta influye en la solubilidad de gases y es directamente
proporcional
FACTORES QUE CONDICIONAN O MODIFICAN LA SOLUBILIDAD.
Solubles: si su solubilidad es 0,1 M o >.
Poco Solubles: si su solubilidad se sitúa entre 0,1 M y 0,001 M
Insolubles: si su solubilidad no llega a 0,001 M
Como se ha comprobado mediante experiencias cotidianas, hay sustancias muy
solubles en agua (azúcar), otras muy poco solubles y otras prácticamente
insolubles (aceite), por lo tanto la solubilidad no posee siempre valor fijo o
constante sino que depende de ciertos factores que harán de la solubilidad un
valor que puede ser aumentado o disminuido según sea el factor modificante y
éstos son los siguientes:
La Temperatura:
Este factor solo modifica la solubilidad de solutos sólidos y gaseosos, los líquidos
no sufren ninguna alteración en su solubilidad, solo hasta que sean miscibles
entre sí (que se mezclen).
En el caso de los sólidos: en general un aumento de la temperatura provocará un
aumento de la solubilidad aunque existen casos donde la solubilidad sufre una
pequeña variación e incluso casos donde al aumentar la temperatura la
solubilidad disminuye.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
En el caso de los gases: un aumento de la temperatura produce siempre una
disminución de la solubilidad y vise-versa. Si se coloca en un recipiente una
pequeña cantidad de bebida gaseosa, al ser calentada, se observa
inmediatamente una efervescencia derivada del escape de gas (dióxido de
carbono) de la solución. Si se calienta agua, esta pierde el aire disuelto en ella.
La Presión:
Este factor no produce alteración alguna en las solubilidades de sólidos y líquidos.
La presión modifica considerablemente la solubilidad de un gas y actúa de la
siguiente forma: “Un aumento de la presión producirá siempre un aumento de la
solubilidad del gas y vise-versa, siempre que la temperatura permanezca
constante” (la temperatura también modifica la solubilidad de un gas. Esta
mitificación se conoce con términos matemáticos como “ley de Henry” que dice:
“La solubilidad de un gas es directamente proporcional a la presión del gas sobre
la superficie del líquido a temperatura constante”.
Esto se puede comprobar fácilmente con la siguiente experiencia:
Las bebidas y el champagne, contienen un gas disuelto (dióxido de carbono) a
una alta presión, sobre todo el champagne, de ahí que al abrirlos se produzca una
disminución de la presión y el gas escapa violentamente de la solución.
Esto se puede evitar un cierto grado enfriando, ya que como uno puede darse
cuenta fácilmente en el caso de los gases, su solubilidad varía en forma contraria
con la presión y la temperatura.
Naturaleza Química del Soluto y el Solvente:
Este factor podemos tomarlo en términos sencillos en el siguiente sentido:
“Una sustancia podrá ser muy soluble en un determinado solvente, pero esto no
permite asegurar que lo sea en otros solventes”, para ejemplificar lo dicho, hay
que observar la solubilidad del azúcar y el yodo (en g/100g de solvente a 20ºC),
utilizando como solventes agua y alcohol.
SOLVENTE AZUCAR YODO
AGUA 179 0.029
ALCOHOL 0.9 20.5
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
La concentración es la magnitud física que expresa la cantidad de un elemento o
un compuesto por unidad de volumen. En el SI se emplean las unidades mol·m-3.
Cada sustancia tiene una solubilidad que es la cantidad máxima de soluto que
puede disolverse en una disolución, y depende de condiciones como la
temperatura, presión, y otras substancias disueltas o en suspensión.
En química, para expresar cuantitativamente la proporción entre un soluto y el
disolvente en una disolución se emplean distintas unidades: molaridad,
normalidad, molalidad, formalidad, porcentaje en peso, porcentaje en volumen,
fracción molar, partes por millón, partes por billón, partes por trillón, etc. También
se puede expresar cualitativamente empleando términos como diluido, para bajas
concentraciones, o concentrado, para altas.
MEDIDA DE LAS CONCENTRACIONES
Concentración química:
La concentración de las soluciones es la cantidad de soluto contenido en una
cantidad determinada de solvente o solución. Los términos diluidos o
concentrados expresan concentraciones relativas. Para expresar con exactitud la
concentración de las soluciones se usan sistemas como los siguientes:
LA MOLARIDAD
La molaridad (M) es el número de moles de soluto por litro de disolución. Por
ejemplo, si se disuelven 0,5 moles de soluto en 100 mL de disolución, se tiene
una concentración de ese soluto de 5,0 M (5,0 molar).
Para preparar una disolución de esta concentración normalmente se disuelve
primero el soluto en un volumen menor, por ejemplo 30 mL, y se traslada esa
disolución a un matraz aforado, para después rellenarlo con más disolvente hasta
los 100 mL.
Es el método más común de expresar la concentración en química sobretodo
cuando se trabaja con reacciones químicas y relaciones estequiométricas.
Sin embargo, tiene el inconveniente de que el volumen cambia con la
temperatura.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
EJEMPLO:
* Cuántos gramos de AgNO3, se necesitan para preparar 100 cm3 de solución
1M?
Previamente sabemos que:
El peso molecular de AgNO3 es: 170 g= masa de 1 mol AgNO3 y que 100 de H20
cm3 , equivalen a 100 mL. H20
Usando la definición de molalidad, se tiene que en una solución 1M hay 1 mol de
AgNO3 por cada Litro (1000 ml ) de H2O (solvente) es decir:
Utilizando este factor de conversión y los datos anteriores tenemos que:
Se necesitan 17 g de AgNO3 para preparar una solución
LA MOLALIDAD
La molalidad (m) es el número de moles de soluto por kilogramo de disolvente.
Para preparar disoluciones de una determinada molalidad en un soluto, no se
emplea un matraz aforado como en el caso de la molaridad, sino que se puede
hacer en un vaso de precipitados y pesando con una balanza analítica, previo
peso del vaso vacío para poderle restar el correspondiente valor.
La principal ventaja de este método de medida respecto a la molaridad es que
como el volumen de una disolución depende de la temperatura y de la presión,
cuando éstas cambian, el volumen cambia con ellas. Gracias a que la molalidad
no está en función del volumen, es independiente de la temperatura y la presión, y
puede medirse con mayor precisión.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
EJEMPLO:
* Cuántos gramos de AgNO3 , se necesitan para preparar 100 cm3 de solución
1m?
Previamente sabemos que:
El peso molecular de AgNO3 es: 170 g = masa de 1 mol AgNO3 y que 100
de H20 cm3 equivalen a 100 gr. H20
Usando la definición de molalidad, se tiene que en una solución 1m hay 1 mol de
AgNO3 por cada Kg. (1000 g) de H2O (solvente) es decir:
Utilizando este factor de conversión y los datos anteriores tenemos que:
Se necesitan 17 g de AgNO3 para preparar una solución 1 m, observe que debido
a que la densidad del agua es 1.0 g/ml la molaridad y la molalidad del AgNO 3 es la
misma
Es menos empleada que la molaridad.
Formalidad) (F): Es el cociente entre el número de pesos fórmula gramo (pfg) de
soluto que hay por cada litro de solución. Peso fórmula gramo es sinónimo de
peso molecular.
La molaridad (M) y la formalidad (F) de una solución son numéricamente iguales,
pero la unidad formalidad suele preferirse cuando el soluto no tiene un peso
molecular definido, ejemplo: en los sólidos iónicos.
La formalidad (F) es el número de peso-fórmula-gramo por litro de solución.
F = # PFg / volumen (litro solución)
El número de peso-fórmula-gramo tiene unidad de g / PFg.
Normalidad
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
La normalidad (N) es el número de equivalentes (n) de soluto (s.f.) por litro de
disolución (SC).
EJEMPLO:
Cuántos gramos de AgNO3 , se necesitan para preparar 100 cm3 de solución 1N?
Previamente sabemos que:
El peso molecular de AgNO3 es: 170 g = masa de 1 mol AgNO3 y que 100
de H20 cm3 equivalen a 100 gr. H20
Usando la definición de molalidad, se tiene que en una solución 1N hay 1 mol de
AgNO3 por cada Kg. (1000 g) de H2O (solvente) es decir:
Utilizando este factor de conversión y los datos anteriores tenemos que:
El peso equivalente de un compuesto se calcula dividiendo el peso molecular del
compuesto por su carga total positiva o negativa.
Concentraciones Físicas:
Peso por volumen (w/v)
Se pueden usar también las mismas unidades que para medir la densidad aunque
no conviene confundir ambos conceptos.
La densidad de la mezcla es la masa de la solución entre el volumen de esta
mientras que la concentración en dichas unidades es la masa de soluto entre el
volumen de la disolución. Se suelen usar los gramos por litro (g/l).
Porcentaje por masa:
Masa de soluto por cada cien partes de solución.
Porcentaje por volumen:
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Expresa el volumen de soluto por cada cien unidades de volumen. Se suele usar
para mezclas gaseosas en las que el volumen es un parámetro importante a tener
en cuenta.
Porcentaje peso a peso (% P/P): indica el peso de soluto por cada 100 unidades
de peso de la solución.
Porcentaje volumen a volumen (% V/V): se refiere al volumen de soluto por
cada 100 unidades de volumen de la solución.
Porcentaje peso a volumen (% P/V): indica el número de gramos de soluto que
hay en cada 100 ml de solución.
Ejemplo: Calcula el porcentaje peso / volumen de soluto de una solución
formada por 80 [ g ] de soluto disueltos en 500 [ ml ] de solución.
Si la densidad de la solución es 1,1 [g / mL ], calcula el porcentaje peso /
volumen de solvente.
100 × 80
( P / V ) soluto = ————– = 16 %
500
m solución = 500 × 1,1 = 550 [ g ]
m solvente = 550 – 80 = 470 [ g ]
100 × 470
( P / V ) solvente = ————— = 94 %
500
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Si los volúmenes son aditivos:
( V / V ) soluto + ( V / V ) solvente = 100 ( soluciones binarias )
Donde:
( % V / V ) soluto : porcentaje volumen / volumen de soluto
( % V / V ) solvente : porcentaje volumen / volumen de solvente
Ejemplo:
300 [ ml ] de una cierta solución acuosa contienen 60 [ ml ] de CH 3CH2OH .
Calcula el porcentaje volumen / volumen de soluto. Si los volúmenes son aditivos,
calcula el porcentaje volumen / volumen de solvente.
100 × 60
( V / V ) soluto = ————– = 20 %
300
V solvente = 300 – 60 = 240 [ ml ]
100 × 240
( V / V ) solvente = ————– = 80 %
300
Normalidad ácido-base
Es la normalidad de una solución cuando se la utiliza para una reacción como
ácido o base.
Por esto suelen titularse utilizando indicadores de pH.
En este caso, los equivalentes pueden expresarse de la siguiente forma:
n = moles * H + para un ácido, o n = moles * HO − para una base.
Donde:
n: es la cantidad de equivalentes.
moles: es la cantidad de moles.
H+: Es la cantidad de protones cedidos por un mol del ácido.
HO-: Es la cantidad de hidroxilos cedidos por un mol de la base.
Por esto, podemos decir lo siguiente:
N = M * H + para un ácido, o N = M * HO − para una base.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Donde:
N: es la normalidad de la solución.
M: es la molaridad de la solución.
H+: Es la cantidad de protones cedidos por un mol del ácido.
HO-: Es la cantidad de hidroxilos cedidos por un mol de la base.
Ejemplos:
Una solución 1 M de HCl cede 1 M de H+, por lo tanto, es igual a 1 N.
Una solución 1 M de Ca (OH)2 cede 2 M de HO-, por lo tanto, es igual a 2 N.
En este caso, los equivalentes pueden expresarse de la siguiente forma:
n = moles * e −.
Donde:
n: es la cantidad de equivalentes.
Moles: es la cantidad de moles.
e-: Es la cantidad de electrones intercambiados en la hemireacción de oxidación o
reducción.
Por esto, podemos decir lo siguiente:
N = M * e −.
Donde:
N: es la normalidad de la solución.
M: es la molaridad de la solución.
e-: Es la cantidad de electrones intercambiados en la hemireacción de oxidación o
reducción.
Ejemplos:
En el siguiente caso vemos que el anión nitrato en medio ácido (por ejemplo el
ácido nítrico, puede actuar como oxidante,
Donde una solución 1 M,
Es 3 Nox.
4 H+ + NO3-1 + 3 e- ↔ NO + 2 H2O
En el siguiente caso vemos que el anión ioduro, puede actuar como reductor,
donde una solución 1 M, es 1 Nrd.
2 I- - 2 e- ↔ I2
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
En el siguiente caso vemos que el catión argéntico, puede actuar como oxidante,
donde una solución 1 M, es 1 Nox.
1 Ag+ + 1 e- ↔ Ag0
Partes por millón (ppm), Partes por billón (ppb) y Partes por trillón (ppt)
Para expresar concentraciones muy pequeñas, trazas de una sustancia muy
diluida en otra, es común emplear las relaciones partes por millón (ppm), partes
por "billón" (ppb) y partes por "trillón" (ppt). El millón equivale a 10 6, el billón
estadounidense, o millar do, a 109 y el trillón estadounidense a 1012.
Es de uso relativamente frecuente en la medición de la composición de la
atmósfera terrestre. Así el aumento de dióxido de carbono en el aire debido al
calentamiento global se suele dar en dichas unidades.
Las unidades más comunes en las que se usan son las siguientes:
pmm = μg·g-1
pmv = μg·ml-1
pbm = ng·g-1
pbv = ng·ml-1
ptm = pg·g-1
ptv = pg·ml-1
Nota: Se pone una m o una v al final según se trate de partes en volumen o en
masa.
Sin embargo, a veces se emplean otras unidades.
Por ejemplo:
1 ppm de CO2 en aire podría ser, en algunos contextos, una molécula de CO 2 en
un millón de moléculas de aire.
También se habla a veces de relaciones más pequeñas, por ejemplo "cuatrillón".
Sin embargo son concentraciones excesivamente pequeñas y no se suelen
emplear.
La IUPAC desaconseja el uso de estas relaciones (especialmente en el caso de
masa entre volumen) y recomienda usar las unidades correspondientes.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
CONVERSIONES ÚTILES
Molalidad a fracción molar ( m→Xst )
Fracción molar a molalidad ( Xst→m ),
Se define como la relación entre las moles de un componente y las moles totales
presentes en la solución, recordando que Xst + Xsv = 1
Molalidad a molaridad ( m→M )
Molaridad a molalidad ( M→m )
Donde:
Psv = Peso molar del solvente (g/mol)
Pst = Peso molar del soluto (g/mol)
d = densidad (g/m)
Otras formas de indicar la concentración
Para ciertas soluciones muy usadas (por ejemplo ácido sulfúrico, hidróxido de
sodio, etc.) se indica la concentración de otras formas:
LA DENSIDAD:
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Si bien la densidad no es una forma de expresar la concentración, ésta es
proporcional a la concentración (en las mismas condiciones de temperatura y
presión).
Por esto en ocasiones se expresa la densidad de la solución a condiciones
normales en lugar de indicar la concentración; pero se usa más prácticamente y
con soluciones utilizadas muy ampliamente.
También hay tablas de conversión de densidad a concentración para estas
soluciones; aunque el uso de la densidad para indicar la concentración es una
práctica que está cayendo en desuso.
VOLUMENES:
Si bien el volumen no es una forma de expresar la concentración, el volumen de
algún producto o sustrato es proporcional a la concentración del mismo, o de otro.
(En las mismas condiciones de temperatura y presión.)
Esta forma es práctica cuando se liberan gases, como en el caso del agua
oxigenada. En este último caso, se expresa la concentración como los volúmenes
de oxígeno que puede liberar un volumen de agua oxigenada.
Verifica este ejemplo:
Ej: se preparan dos soluciones de la forma que se indica a continuación *se pesan
5g de cloruro de sodio (NaCl) en cada caso *se agrega agua hasta 50 mL(sol A) y
200 mL(sol B) . *se agita hasta disolución completa La solución A es la más
concentrada ( 10% en volumen), y la solución B es la más diluída (2,5% en
volumen) Para transformar la solución 10% en una 2,5% basta con agregar 150
mL de solvente agua. Para transformar los 200 mL de solución B (que contiene 5
g de soluto) en solución A (10%) puede agregarse 15 g de NaCl o bien someter el
sistema a evaporación reduciendo el volumen de la solución hasta 50 mL.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
GRUPO DE EJERCICIOS 01
1) ¿Qué cantidad de Na2CO3 se debe disolver para obtener 120 mL de solución al
2,5 %? Respuesta: 3 g
2) Se disuelven 24 g de Ca(OH)2 en agua hasta obtener 150 mL de solución.
¿Cuál es el % m/v de la solución? Respuesta: 16 g/100 mL
3) ¿Cuántos moles de soluto hay en 300 mL de solución de HCl concentrado 12
M?
Respuesta: 3,6 moles
4) Determinar la molaridad de las siguientes soluciones:
a) 5 g de Na2SO4 en 250 mL de solución acuosa.
b) 40 g de KOH en 150 mL de solución acuosa.
c) 34 g de NH3 en 500 mL de solución acuosa.
Respuesta: 0,14 M; 4,76 M; 4,00 M
5) ¿Cuántos gramos de soluto se necesitan para preparar: a-500 cm 3 de solución
0,25 M de Li2SO4 ? b-1 dm3 de solución 0,15 M de Al2(SO4)3 ?
Respuesta: 13,7 g; 51,30 g
6) ¿Qué cantidad de sustancia se debe pesar para preparar 300 mL de una
solución 1,24 M de CuCl2 ?
a) Si se dispone de droga anhidra.
b) Si se dispone de CuCl2·2H2O
Respuesta: 50g; 63,4 g
7) ¿Qué cantidad de sustancia hay que pesar para preparar 450 cm 3 de las
siguientes soluciones acuosas?: a)Ba(OH) 2 0,2 M a partir de Ba(OH)2.8H2O
b)ZnSO4 5 % a partir de ZnSO4.6H2O Respuesta: 28,4 g ; 37,6 g
8) Se tienen 20 mL de H2SO4 al 25 % (25 g de H2SO4 en 100 mL de solución) y
se llevan a 50 mL de solución con agua destilada. ¿Cuál es el porcentaje en
volumen de la solución resultante, y cuál es su molaridad (M)?.
Respuesta: 10%; 1,02 M
9) ¿Cuántos mL de solución de NaCl 2M deben medirse para preparar 400mL de
una solución 0,5M?
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Respuesta: 100 mL
10) A 450 ml de solución de Pb(NO3)2 al 1,8 % se le agregan 50 ml de agua.
¿Cuál es la concentración % de la nueva solución?
Respuesta: 1,62 %
11) Se tienen 200 mL de ácido concentrado 12 M. ¿A qué volumen hay que llevar
con agua para obtener un ácido 6 M ?
Respuesta: 400 mL
12) Se tienen 300 mL de solución de KCl al 3 % y se mezclan con 200 mL de
solución de KCl 0,2 M.¿ Cuál es la concentración final de la nueva solución
expresada en molaridad?
Respuesta: 0,32 M
13) Se pesaron 3,0 g de BaCl2.2H2O y se disolvieron en agua hasta un volumen
final de 500 mL. ¿ Cuál es la concentración final de la solución en %
(expresada como droga anhidra) y cuál la molaridad? Respuesta: 0,51 %,
0,024 M
14) ¿Qué volumen de una disolución de NaOH al 12% m/v contiene el mismo
número de gramos de soluto que 100 cm3 de una disolución 2M de NaOH?.
Respuesta: 66,7 mL
15) En 300 mL de una disolución de HCl hay 12 gramos de HCl. Determina: a) el
número de moles de HCl. b) la Molaridad de la disolución.
Respuesta: 0,33 moles; 1,1 M
16) Se disuelven 12 gramos de LiCl en 250 mL de agua, completándose la
disolución. Calcula: a) El número de moles de soluto; b) la concentración de
la disolución en moles/litro
Respuesta: 0,28 moles; 1,13M
17) Un operador pesó 61 gramos de CuSO4·5H2O para preparar una solución
0,98M de CuSO4, ¿Qué volumen de solución preparó?
Respuesta: 250 mL
18) Se somete a evaporación 200 mL de una solución de Na2SO4 al 6%, hasta
reducir su volumen a 150 mL. a) ¿La nueva solución será más concentrada o
más diluída que la solución original? ; b) Calcula la concentración final en
%m/v.
Respuesta: 8 % m/v
19) Completa el siguiente cuadro:
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
Soluto mL solución % m/v M
1 g. ZnCl2 100
1g. NaCl 100
1g. Na2SO4 100
1 g. KNO3 100
GRUPO DE EJERCICIOS 02
1. Una lejía blanqueadora consiste en una disolución de hipoclorito de Sodio
(NaOCl) cuya densidad es 74.5 g/L. Determinar la normalidad y molaridad de
esta solución.
a) 0.40 y 0.40
b) 0.20 y 0.40
c) 0.44 y 0.44
d) 0.10 y 0.10
e) 1.00 y 1.00
2. Una solución de H2SO4 contiene 50% de H2SO4 y tiene una densidad de
1.4 g./cm3. Exprese su concentración en términos de molaridad, normalidad y
molalidad.
a) 7.50 M 14.50 N 10.50 m
b) 7.15 M 14.50 N 10.10 m
c) 7.14 M 14.28 N 10.20 m
d) 7.14 M 14.20 N 10.80 m
e) 7.14 M 14.25 N 10.35 m
3. Se dispone de un ácido fosfórico al 50% en peso cuya densidad es de 1.4
g./cm3 y se desea preparar 5 L. de un ácido fosfórico 3 N hallar el volumen
del ácido concentrado que debe tomarse.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
a) 0.4 L
b) 0.3 L
c) 0.5 L
d) 0.7 L
e) 0.9 L
4. Calcular la molalidad de una solución que resulta de mezclar 100 g. de
H2SO4 de 76.5% y 100 g. de H2SO4 83.3%
a) 40.10 m
b) 40.20 m
c) 40.56 m
d) 40.80 m
e) 40.90 m
5. Se disolvieron 13.5 g. de sacarosa (C 12H22O11) en suficiente agua hasta
completar 100 mL. la densidad de esta solución es de 1.050 g/mL.
Determinar la molaridad y la molalidad.
a) 0.395 m, 0.5 m
b) 0.400 m, 0.435 m
c) 0.395 m, 0.432 m
d) 0.415 m, 0.438 m
e) N.A
6. Calcular la normalidad de una solución de Al2(SO4)3 0.12 M.
a) 0.12 N
b) 0.60 N
c) 0.72 N
d) 0.15 N
e) 0.5 N
7. El análisis de una muestra de aire da como resultado la sgte. Composición
13.44 g de oxigeno 43.68 gr. de Nitrógeno y 0.8 gr. de Argon. Calcular la
fracción molar de los diferentes componentes del aire.
a) 0.21 0.78 0.01
b) 0.50 0.1 0.40
c) 0.30 0.21 0.21
d) 0.40 0.30 0.21
e) N.A.
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
8. Calcular la molaridad de una solución de etanol C 2H5OH en agua, si se
parte de 2 litros de una solucion concentrada 4 M del etano, y se desea
preparar 8 litros de la nueva solucion.
a) 2M
b) 1M
c) 0.5 M
d) 0.25 M
9. En la etiqueta de una botella de HCl c.c. figuran los siguientes datos:
d =1.2g/cm3 %HCl=36.5 determinar los gramos de HCl en cada cm 3 de HClcc
a) 0.438
b) 0.538
c) 0.338
d) 0.212
e) N.A
10. Se adicionan 35 g de HCl puro a 500 mL de HCl 3.5 M, supóngase que el
volumen sigue siendo 500 mL(se evapora agua) ¿Cuál es la concentración
final?
a) 7.0
b) 6.42
c) 5.42
d) 5.50
e) 6.50
11. Cuantas mL de una solución 0.25 M de hidróxido de Sodio se necesitan
para neutralizar 100 mL de una solución 0.40 M de ácido sulfúrico.
a) 320 mL
b) 350 mL
c) 400 mL
d) 500 mL
e) 600 mL
12. Se prepara solución disolviendo 15.2 g. de NaCl en 197 g de Agua, la
densidad de la solución resultante es 1.012 g/mL. calcular la fracción molar
de NaCl, la molalidad y la molaridad de la solución resultante.
a) 0.025 1.40 m 1.50 M
b) 0.020 1.35 m 1.50 M
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
c) 0.023 1.32 m 1.24 M
d) 0.023 1.32 m 1.75 M
e) 0.023 1.38 m 1.24 M
13. Se mezclan 1 L. de HNO3 de densidad 1.380 g/mL y 62.70% con 1L de
HNO3 de densidad 1.130 g/Ml y 22.38%. Determinar la concentración y el
volumen del acido que se forma si la densidad del acido resultante es 1.276
g/mL.
a) 44.5% y 2 L
b) 44.0% y 2 L
c) 45.5% y 2.5 L
d) 44.0% y 2 L
e) N.A.
14. Al añadir AgNO3 en exceso a 25 mL de una solución de HCl cuya
concentración se desconoce, se forma el precipitado de AgCl que cuando se
seca se encuentra que pesaba 0.538 g. calcular la molaridad de la solución
de HCl suponiendo que todo el ion presenta precipitado en forma de AgCl.
a) 0.20
b) 2.5
c) 0.15
d) 1.5
e) 10.5
15. Cuando se neutralizan 90 cm3 de una solución deHNO3 con NaOH 0.234 M
se requieren 42.8 cm3 de base ¿Cuál es la molaridad del HNO3
a) 2.1 M
b) 1.111 M
c) 0.10 M
d) 0.101 M
e) 0.111 M
16. Si 0.03 mol de Ca(OH)2 se diluyen a 500 cm3 ¿Con cuantos cm3 de H2SO4
0.2 N reaccionarán.
a) 300 cm3
b) 400 cm3
c) 500 cm3
Ingº. A. Fernández Reyes
Universidad Nacional de Piura Química General
d) 550 L.
e) ayd
17. A que volumen deben diluirse 250 cm 3 de H2SO4 1.4 M para dar una
solución 0.35 N.
a) 2000 L
b) 200 L
c) 20 L
d) 2L
e) ayb
18. Se tiene una solución de HCl 0.1255 M ¿Qué cantidad de H 2O debe
añadirse a 750 cm3 de este ácido para obtener una disolución exactamente a
0.1 M?
a) 191.21 cm3
b) 941.25 cm3
c) 650 m3
d) 650 Lt.
e) N.A.
19. Se disuelven 7 g. de NaCl en 43 g de agua. Calcular la concentración de la
disolución en tanto por ciento en peso, del soluto y del disolvente.
a) 14% 86%
b) 10% 90%
c) 86% 14%
d) 14% 10%
e) N.A.
20. Se añade 6 g de KCl a 80 g de una solución de KCl al 12%. Hallar el tanto
por ciento en peso del KCl de la solución resultante.
a) 18.14%
b) 18.00%
c) 20%
d) 16.15%
e) N.A.
Ingº. A. Fernández Reyes
También podría gustarte
- Leyes Fundamentales de La QuímicaDocumento4 páginasLeyes Fundamentales de La QuímicaMarian12orAún no hay calificaciones
- 9 Unidad Ix Equilibrio Acido Base PDFDocumento78 páginas9 Unidad Ix Equilibrio Acido Base PDFRocio HuertaAún no hay calificaciones
- Reacciones Analiticas de Los Cationes de Primer Grupo 1Documento11 páginasReacciones Analiticas de Los Cationes de Primer Grupo 1Danny Santana Guerrero0% (1)
- Unidades Químicas de MasaDocumento43 páginasUnidades Químicas de MasaELMER RICARDO SERIN NERYAún no hay calificaciones
- 10 Clase HalogenosDocumento60 páginas10 Clase HalogenosClaudiaAún no hay calificaciones
- Reactivo Limitante y en ExcesoDocumento33 páginasReactivo Limitante y en ExcesoAgu NunesAún no hay calificaciones
- Guia 2 - Concepto de Mol y Numero de AvogadroDocumento7 páginasGuia 2 - Concepto de Mol y Numero de Avogadrojose cuesta100% (2)
- Tabla Prioridades Química OrgánicaDocumento2 páginasTabla Prioridades Química OrgánicaCamilo AravenaAún no hay calificaciones
- Taller Soluciones y EstequiometriaDocumento9 páginasTaller Soluciones y EstequiometriaLis Ocoro CaicedoAún no hay calificaciones
- Equilibrio QuímicoDocumento4 páginasEquilibrio Químicojdiazgall9395Aún no hay calificaciones
- Solucionesypropiedadescoligativas 091028082701 Phpapp02Documento54 páginasSolucionesypropiedadescoligativas 091028082701 Phpapp02Lexo MontalvoAún no hay calificaciones
- Soluciones EjercDocumento3 páginasSoluciones Ejercjudit delgado perezAún no hay calificaciones
- Factores Que Afectan La SolubilidadDocumento13 páginasFactores Que Afectan La SolubilidadDinka Zúñiga ValenzuelaAún no hay calificaciones
- Accidos y BasesDocumento24 páginasAccidos y Basesabc1703Aún no hay calificaciones
- Estequiometria Problemas 02Documento1 páginaEstequiometria Problemas 02andres_old_condeAún no hay calificaciones
- Guia de Ejercicios Ecuaciones Redox PDFDocumento2 páginasGuia de Ejercicios Ecuaciones Redox PDFAndrés Quezada PérezAún no hay calificaciones
- Agentes DesecantesDocumento44 páginasAgentes DesecantesRossy Moral100% (1)
- EstequiometríaDocumento6 páginasEstequiometríaLuis F. González AñezAún no hay calificaciones
- F3 SOL Calculos EstequiometricosDocumento7 páginasF3 SOL Calculos EstequiometricosRuben FraguelAún no hay calificaciones
- Química General: Materia, Sistemas Materiales y Estados FísicosDocumento11 páginasQuímica General: Materia, Sistemas Materiales y Estados FísicosAgustin Ganin100% (1)
- Solucion 2da Ev Quimica 2008Documento11 páginasSolucion 2da Ev Quimica 2008Nelson ChiribogaAún no hay calificaciones
- Presentacion SolubilidadDocumento36 páginasPresentacion Solubilidadyho nnyAún no hay calificaciones
- Quimica 2005 RESUELTO PDFDocumento57 páginasQuimica 2005 RESUELTO PDFLuispino SotoAún no hay calificaciones
- Balanceo Ion-Electrón Reacción MnO4- SO3Documento3 páginasBalanceo Ion-Electrón Reacción MnO4- SO3Juanita Marcela Méndez MalagónAún no hay calificaciones
- BROWN Quim11ed Cap15Documento48 páginasBROWN Quim11ed Cap15Carlos AcostaAún no hay calificaciones
- Fórmula Empírica y MolecularDocumento2 páginasFórmula Empírica y MolecularBerthyn Rodrigo TiñiniAún no hay calificaciones
- Tipos de soluciones por abundancia relativa del solutoDocumento6 páginasTipos de soluciones por abundancia relativa del solutoYimi Peralta VegaAún no hay calificaciones
- Soluciones Propiedades ColigativasDocumento75 páginasSoluciones Propiedades ColigativasXiomara ACAún no hay calificaciones
- Cuestionario Resouesta 2Documento9 páginasCuestionario Resouesta 2PAOLA ANDREA QUENALLATA CHIPANAAún no hay calificaciones
- DisolucionesDocumento7 páginasDisolucionesbarlosAún no hay calificaciones
- Quiz de EstequiometriaDocumento4 páginasQuiz de Estequiometriajohnx820Aún no hay calificaciones
- MolalidadDocumento1 páginaMolalidadFlor Martinez100% (1)
- Configuracion-Electronica-Para-Quinto-Grado-de-Secundaria Corteza AtomicaDocumento5 páginasConfiguracion-Electronica-Para-Quinto-Grado-de-Secundaria Corteza AtomicaLeandroCarlosManayayAún no hay calificaciones
- Ecuaciones RedoxDocumento2 páginasEcuaciones Redoxelicetmoreno0% (1)
- Reacciones de Los AlcoholesDocumento7 páginasReacciones de Los Alcoholeslucia alegriaAún no hay calificaciones
- Equilibrio iónico del aguaDocumento19 páginasEquilibrio iónico del aguaALEX CRISTOPHER CJUNO QUISPEAún no hay calificaciones
- Constantes de Ionizacion - PH - POHDocumento2 páginasConstantes de Ionizacion - PH - POHMARCO NICOLAS PACHACAMA FIALLOSAún no hay calificaciones
- Química Analítica: Unidades, Métodos y ObjetivosDocumento68 páginasQuímica Analítica: Unidades, Métodos y ObjetivosEMMAZELAún no hay calificaciones
- Examen CalorimetriaDocumento2 páginasExamen CalorimetriaSegundo Carlos Villegas VienaAún no hay calificaciones
- pH-cálculosDocumento5 páginaspH-cálculosRobert José Lobatón AlvarezAún no hay calificaciones
- Cuestionario de Química - Balanceo de EcuacionesDocumento3 páginasCuestionario de Química - Balanceo de EcuacionesGabriela Paredes HerediaAún no hay calificaciones
- Volumetria IntroduccionDocumento30 páginasVolumetria IntroduccionMishel RamonAún no hay calificaciones
- Guia Estequiometria N° 1Documento4 páginasGuia Estequiometria N° 1mayroAún no hay calificaciones
- Eficiencia de reacción y producción de sulfuro de plata a partir de plata puraDocumento3 páginasEficiencia de reacción y producción de sulfuro de plata a partir de plata puraJuanjose Ruiz SerranoAún no hay calificaciones
- Autoionizacion Del Agua PH y POHDocumento12 páginasAutoionizacion Del Agua PH y POHLizVDiAún no hay calificaciones
- Diferencias Entre Reacción Química y Ecuación QuímicaDocumento2 páginasDiferencias Entre Reacción Química y Ecuación QuímicadanielcapetillogarciaAún no hay calificaciones
- Clase DisolucionesDocumento39 páginasClase DisolucionesMilagros RabanalAún no hay calificaciones
- Informe P1 EquilibrioDocumento9 páginasInforme P1 EquilibrioJORGE LEONARDO FRASSER QUIÑONESAún no hay calificaciones
- HT Balance de Reacciones Quimicas 2014-2-2Documento2 páginasHT Balance de Reacciones Quimicas 2014-2-2Vanessa ValdezAún no hay calificaciones
- Guia Estequiometria ManizalesDocumento10 páginasGuia Estequiometria ManizalesDeyanira Medina RuizAún no hay calificaciones
- Analitica 18Documento2 páginasAnalitica 18Jhenny ZarateAún no hay calificaciones
- Análisis de Una Mezcla de Carbonato y BicarbonatoDocumento7 páginasAnálisis de Una Mezcla de Carbonato y BicarbonatoIsabella Callejas GaviriaAún no hay calificaciones
- Soluciones QuímicasDocumento20 páginasSoluciones QuímicasDavis LiveAún no hay calificaciones
- Informe de SolucionesDocumento17 páginasInforme de SolucionesandersoAún no hay calificaciones
- 02 Teoría SolucionesDocumento17 páginas02 Teoría SolucionesFederico CastilloAún no hay calificaciones
- Monografía de SolucionesDocumento13 páginasMonografía de SolucionesGiulianaAún no hay calificaciones
- PRACTICA #10 Preparación y Valoración de SolucionesDocumento14 páginasPRACTICA #10 Preparación y Valoración de SolucionesFelipeBangiroAún no hay calificaciones
- Soluciones 2022 v2Documento45 páginasSoluciones 2022 v2Secrets UncleAún no hay calificaciones
- SolucionesDocumento45 páginasSolucionesFlorAún no hay calificaciones
- Guia Química. Las DisolucionesDocumento25 páginasGuia Química. Las DisolucionesEymardVivas100% (1)
- Conducción de Calor en Pared Plana-03Documento2 páginasConducción de Calor en Pared Plana-03Alfredo FernandezAún no hay calificaciones
- Juntas y TratadosDocumento28 páginasJuntas y TratadosAlfredo FernandezAún no hay calificaciones
- Conducción de Calor en Pared Plana-05Documento1 páginaConducción de Calor en Pared Plana-05Alfredo FernandezAún no hay calificaciones
- Conducción de Calor en Pared Plana-04Documento2 páginasConducción de Calor en Pared Plana-04Alfredo FernandezAún no hay calificaciones
- ElaguaDocumento40 páginasElaguaAlfredo FernandezAún no hay calificaciones
- Ejercicio DestilaciónDocumento1 páginaEjercicio DestilaciónAlfredo FernandezAún no hay calificaciones
- Collar Perro Grupo 02Documento1 páginaCollar Perro Grupo 02Alfredo FernandezAún no hay calificaciones
- Conducción de Calor en Pared Plana-02Documento2 páginasConducción de Calor en Pared Plana-02Alfredo FernandezAún no hay calificaciones
- Conducción de Calor en Pared Plana-01Documento1 páginaConducción de Calor en Pared Plana-01Alfredo FernandezAún no hay calificaciones
- Leopold JerusalenDocumento5 páginasLeopold JerusalenAlfredo FernandezAún no hay calificaciones
- Balances de Masa y EnergíaDocumento21 páginasBalances de Masa y EnergíaAlfredo FernandezAún no hay calificaciones
- AguaDocumento5 páginasAguaAlfredo FernandezAún no hay calificaciones
- Ejemplo de Problema-Objetivos-Hipotesis-VariableDocumento20 páginasEjemplo de Problema-Objetivos-Hipotesis-VariableAlfredo FernandezAún no hay calificaciones
- Precisión PDFDocumento19 páginasPrecisión PDFAlfredo FernandezAún no hay calificaciones
- Venturi2010 (Reparado) 2009 IIDocumento15 páginasVenturi2010 (Reparado) 2009 IIAlfredo FernandezAún no hay calificaciones
- Diseño AgitadorDocumento6 páginasDiseño AgitadorFav Rodrîgø Jr.Aún no hay calificaciones
- Niveles Criticos de Interpretac de SuelosDocumento2 páginasNiveles Criticos de Interpretac de SuelosAlfredo FernandezAún no hay calificaciones
- Geomorfologia de La SelvaDocumento22 páginasGeomorfologia de La SelvaAlfredo FernandezAún no hay calificaciones
- Glosario de Analisis de AguaDocumento5 páginasGlosario de Analisis de AguaAlfredo FernandezAún no hay calificaciones
- Para Poder Calorifico de CarbonDocumento1 páginaPara Poder Calorifico de CarbonAlfredo FernandezAún no hay calificaciones
- Alteraciones Fisicas Del AguaDocumento1 páginaAlteraciones Fisicas Del AguaAlfredo FernandezAún no hay calificaciones
- Para La Calidad Del AguaDocumento2 páginasPara La Calidad Del AguaAlfredo FernandezAún no hay calificaciones
- Papel Filtro Sin CenizasDocumento1 páginaPapel Filtro Sin CenizasAlfredo FernandezAún no hay calificaciones
- Correccion Del Grado AlcoholicoDocumento6 páginasCorreccion Del Grado AlcoholicoAlfredo FernandezAún no hay calificaciones
- Papel Filtro Sin CenizasDocumento1 páginaPapel Filtro Sin CenizasAlfredo FernandezAún no hay calificaciones
- Patogenos Del AguaDocumento1 páginaPatogenos Del AguaAlfredo FernandezAún no hay calificaciones
- Anexo 10 Factores de Conversion de Nitrogeno en ProteinasDocumento1 páginaAnexo 10 Factores de Conversion de Nitrogeno en ProteinasAlfredo Fernandez0% (1)
- Maximos Permisibles Segun Ley de AguasDocumento1 páginaMaximos Permisibles Segun Ley de AguasAlfredo FernandezAún no hay calificaciones
- Agua PuraDocumento1 páginaAgua PuraAlfredo FernandezAún no hay calificaciones
- Anexo 10 Factores de Conversion de Nitrogeno en ProteinasDocumento1 páginaAnexo 10 Factores de Conversion de Nitrogeno en ProteinasAlfredo Fernandez0% (1)
- Parcial #3RDocumento2 páginasParcial #3RBenigno Vargas G.Aún no hay calificaciones
- 500 Palabras en Ingles y EspañolDocumento21 páginas500 Palabras en Ingles y EspañolLeonardo BolívarAún no hay calificaciones
- Pedido 310719Documento2 páginasPedido 310719Sebastian ChapaAún no hay calificaciones
- Abreviaciones PDFDocumento23 páginasAbreviaciones PDFFrank OrtizAún no hay calificaciones
- CAPITULO I Rio9 NeveriDocumento28 páginasCAPITULO I Rio9 NeveriFjeb23Aún no hay calificaciones
- Fisico Informe 3Documento10 páginasFisico Informe 3Ana Maria Rojas PereaAún no hay calificaciones
- Guía de Talleres Química 10°Documento84 páginasGuía de Talleres Química 10°Laura Maria Ramirez MarinAún no hay calificaciones
- PERCDocumento30 páginasPERCTn MontanaAún no hay calificaciones
- Taller de MaterialesDocumento23 páginasTaller de MaterialesCalcule el caudal de agua que fluye a Través de una tubería de hierro galvanizado67% (3)
- Experimentos Preescolar2018Documento2 páginasExperimentos Preescolar2018Viridiana MoralesAún no hay calificaciones
- Simbologia Inserto FresadoDocumento46 páginasSimbologia Inserto FresadoCristina Maldonado MorenoAún no hay calificaciones
- Las Proteínas, Carbohidratos y Las Grasas Lácteas Son Buenas o Malas para El Consumo Humano.Documento3 páginasLas Proteínas, Carbohidratos y Las Grasas Lácteas Son Buenas o Malas para El Consumo Humano.David HrdzAún no hay calificaciones
- El átomo y la Tabla PeriódicaDocumento32 páginasEl átomo y la Tabla PeriódicaJuan DiegoAún no hay calificaciones
- Analisis Caso Clinico BioquimicaDocumento16 páginasAnalisis Caso Clinico BioquimicaJose Carlos Wild DoriaAún no hay calificaciones
- La Importancia Del AguaDocumento5 páginasLa Importancia Del AguaJenny Bucarey Gonzalez100% (1)
- Tabla Periodica EnsayoDocumento14 páginasTabla Periodica Ensayocrispin100% (1)
- Deber de Temperaturas EjerciciosDocumento3 páginasDeber de Temperaturas EjerciciosJack EcuAún no hay calificaciones
- MONOGRAFIA de SHELL CERAMIC 2022Documento14 páginasMONOGRAFIA de SHELL CERAMIC 2022Meday BaltodanoAún no hay calificaciones
- Quimica de AlimentosDocumento9 páginasQuimica de AlimentosSamuel HernandezAún no hay calificaciones
- Examg6 LDocumento14 páginasExamg6 LRoberto Vera RamosAún no hay calificaciones
- Funcionamiento de Los InyectoresDocumento4 páginasFuncionamiento de Los InyectoresWillian Jose Navarro ZepedaAún no hay calificaciones
- Seminario AinesDocumento58 páginasSeminario AinesJihanBlancoAún no hay calificaciones
- Alimentación BiocompatibleDocumento4 páginasAlimentación BiocompatibleLulu Espino LarraldeAún no hay calificaciones
- Protocolos Antioxidantes - Valor DPPHDocumento7 páginasProtocolos Antioxidantes - Valor DPPHJuan Borja Fajardo100% (1)
- El MaízDocumento10 páginasEl Maízluci mezaAún no hay calificaciones
- SulfitosDocumento6 páginasSulfitostilsonlanderoAún no hay calificaciones
- Propiedades de la materia claveDocumento4 páginasPropiedades de la materia claveSantiago MonsalveAún no hay calificaciones
- Diseño de dosificación de concreto f'c 210 Kg/cm2 para obra de rehabilitaciónDocumento7 páginasDiseño de dosificación de concreto f'c 210 Kg/cm2 para obra de rehabilitaciónEdson Guillermo MoralesAún no hay calificaciones
- Ec 611Documento3 páginasEc 611Dora CordovaAún no hay calificaciones
- Rocas IgneasDocumento45 páginasRocas IgneasRodolfo Vilca100% (2)