Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Práctica 6
Cargado por
Karen9DiazTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Práctica 6
Cargado por
Karen9DiazCopyright:
Formatos disponibles
PRÁCTICA 6
TENSIÓN SUPERFICIAL
OBJETIVO
Determinar la tensión superficial de líquidos usando el método de la burbuja y el
aparato de Otto Stenbach.
Comprender la importancia que tiene el concepto de tensión Superficial de los
líquidos.
INTRODUCCIÓN
Tensión superficial.- La explicación que justifica el hecho de que líquidos
diferentes generen gotas de distinto tamaño, reside en la misma explicación que justifica
que algunos insectos o animales puedan “caminar” sobre la superficie del agua, así
como el uso de servilletas de papel como absorbente, cómo la savia accede desde las
raíces hasta las hojas y porqué el detergente sirve para lavar. Lo que explica todos estos
fenómenos es lo que denominamos como tensión superficial.
a)
b)
Figura 6.1. Ejemplos de cómo insectos a) o animales b) pueden suspenderse en la superficie de los
líquidos debido a la tensión superficial.
Todos los líquidos presentan una cierta tendencia a disminuir su superficie libre, la cual
se comporta de forma parecida a como lo hace una membrana elástica. Dicha propiedad
es debida a la existencia de fuerzas tangenciales a la superficie o fuerzas de tensión, por
lo que se denomina tensión superficial.
Desde un punto de vista molecular, la tensión superficial se explica como debida a la
condición especial de las moléculas situadas en la superficie del líquido. Una molécula
del líquido situada en el interior del mismo es solicitada en todas direcciones por fuerzas
atractivas procedentes de las otras moléculas que la rodean, de modo que, por simetría,
se compensan mutuamente sus efectos (ver fig. 6.2).
En la superficie o en sus proximidades, la simetría se rompe y sólo las moléculas que
están por debajo de la superficie atraen a las de la capa límite, dando lugar a una fuerza
neta dirigida hacia el interior de la masa líquida que tensa la superficie libre y produce
ese efecto de malla o membrana elástica. De aquí que sea necesario consumir cierto
Autor: Alejandro Uría Galicia 1
trabajo para mover las moléculas hacia la superficie venciendo la resistencia de estas
fuerzas, por lo que las moléculas de la superficie tienen más energía que las interiores.
Figura 6.2. Fuerzas que actúan sobre las moléculas de un líquido.
Se define cuantitativamente la tensión superficial como el trabajo que debe realizarse
para llevar moléculas en número suficiente desde el interior del líquido hasta la
superficie para crear una nueva unidad de superficie. Debido a estas fuerzas, la
superficie tiende a contraerse y ocupar el área más pequeña posible, si se trata de una
gota libre, tiende a tomar forma esférica.
Podremos calcular el trabajo necesario dW , para incrementar en dA la
αβ
superficie de la gota como; dW =γ dA
αβ
donde: γ , representa la fuerza neta que apunta al interior de la gota y se denomina
tensión superficial. αβ , representa a la interfase limítrofe (agua y aire).
UnidadesdeEnergía
Las unidades de tensión superficial serían UnidadesdeSuperficie
. Empelando las
J
2
unidades recomendadas por el sistema internacional se expresarían como m .
J N .m N
= =
Si desarrollamos este cociente, se llega a: m2 m2 m
Por lo que a la tensión superficial también se le conoce como la Fuerza por unidad de
longitud = .
Presión producida por la curvatura de una superficie.- Young y Laplace
dedujeron de forma independiente en 1805 la fórmula de la diferencia de presión entre
el interior y el exterior de una superficie esférica de radio R.
La fórmula de Young-Laplace demuestra que la presión en el interior de de una
superficie esférica es siempre mayor que en el exterior, que la diferencia de presión se
Autor: Alejandro Uría Galicia 2
incrementa cuando disminuye el radio de dicha superficie, y que se hace cero cuando la
superficie es plana (radio infinito).
Los líquidos tienden a minimizar su superficie. Por esta razón, las gotas tienen forma
esférica en ausencia de gravedad. La tensión superficial tiende a reducir el área de la
superficie y por tanto, el volumen de la gota. La diferencia de presión tiende a
incrementar el volumen de la gota, la condición de equilibrio se alcanza cuando ambas
tendencias se compensan.
Vamos a mostrar que en el interior de una gota o una burbuja en equilibrio hay una
presión superior a la exterior. Este exceso de presión es debido a la curvatura de la
superficie límite de separación.
Las fuerzas de presión ejercen una fuerza neta o
resultante que es normal a la superficie. (Pi-Pe)dA
Supongamos que la presión en el interior de la
x
burbuja es Pi y en el exterior es Pe, entonces la
fuerza sobre una porción dA de la lámina es (Pi- (Pi-Pe)dA cos
Pe)dA, su componente x es (Pi-Pe) dA cos. Pero
dA cos es la proyección del área sobre un plano dA cos
perpendicular al eje x.
La diferencia de presión entre el interior de la
burbuja y el exterior origina fuerzas sobre la
superficie de la burbuja, perpendiculares a la superficie esférica, tal como indican las
flechas de la derecha de la figura de abajo. Su proyección a lo largo del eje horizontal x,
será el producto de la diferencia de presión (Pi-Pe) por el área proyectada sobre un plano
perpendicular al eje x (la proyección de una semiesfera de radio R, sobre un plano es un
círculo de área R2.
Una burbuja está formada por dos láminas superficiales esféricas muy próximas entre sí.
Consideremos la mitad de la burbuja y busquemos las fuerzas que mantienen a esa
porción en equilibrio.
La fuerza que origina la diferencia de presión es F1 = (Pi-Pe) R2
Fuerza originada por la tensión superficial =
La mitad izquierda de la burbuja (no representada) ejerce una
fuerza hacia la izquierda igual a dos veces la tensión superficial por
el perímetro (flechas hacia la izquierda en la figura) F2=2 ·2 R
En el equilibrio F1 = F2 y
4 γπ R 4 γ
Pi−P e= =
πR2 R
la diferencia de presiones es tanto mayor cuanto menor es el radio
R. Esta expresión es un caso particular de la denominada ley de
Laplace.
El factor cuatro aparece por que una pompa de jabón tiene dos caras: interior y exterior.
En el caso de una gota de agua, solamente hay una cara por lo que la diferencia de
presión se reduce a la mitad.
MATERIAL EMPLEADO
Autor: Alejandro Uría Galicia 3
Aparato de Otto Stenbach
Soluciones de jabón a diferente concentración
PROCEDIMIENTO EXPERIMENTAL
Método de la burbuja.- Este método está basado en la medida de la presión que
tiene la parte cóncava de una burbuja que desciende al líquido problema. Dicha presión
coincide con la presión máxima necesaria para hacer salir una burbuja por un tubo
capilar, de radio “R”, introduciéndolo en un líquido problema a una profundidad
conocida. Esta presión máxima se mide en el manómetro del aparato.
El dispositivo experimental, aparato de Otto Stenbach, se muestra en la figura 6.3 y se
opera de la siguiente manera.
Se inyecta con cuidado aire por el tubo A, las burbujas formadas en el capilar C se
desprenden ascendiendo hasta la superficie del vaso D. El manómetro M mide la
sobrepresión requerida para formar la burbuja.
Para inyectar aire se emplea un embudo E lleno de agua, con una llave L que se abre
muy poco. El agua que cae del embudo va llenando el matraz K y el aire desalojado sale
hacia el dispositivo.
Calculamos la presión en el interior y en el exterior de la burbuja en el momento en el
que se desprende del tubo capilar C:
Presión exterior: La presión exterior a la burbuja es la suma de la presión
atmosférica P0 más la de la columna de líquido de densidad y profundidad h
en el vaso de precipitados.
Pe = P0 + gh
Presión interior: La presión en el interior de la burbuja es la suma de la presión
atmosférica P0 más la que corresponde a la altura máxima hm marcada por el
manómetro que contiene un líquido (líquido manométrico) de densidad m.
Pi = P0 + mghm
Como hemos visto anteriormente, la diferencia de presión entre el interior y el exterior
2γ
Pi−P e=
de una burbuja debido a su curvatura es R
Donde R es el radio de la burbuja o del capilar. El factor dos se debe a que la burbuja
solamente presenta una cara (una pompa de jabón tiene dos caras). Despejando la
tensión superficial llegamos a la siguiente fórmula
Rg
γ= ( ρ h −ρh)
2 m m
Calibración del aparato.- En primer lugar se prepara un capilar C de diámetro
pequeño, lavándolo perfectamente y colocándolo en el dispositivo adecuado del aparato.
Autor: Alejandro Uría Galicia 4
Ahora necesitamos calcular el radio del capilar, para ello llenamos un vaso de
precipitados con agua destilada hasta el afore superior y colocamos el capilar en su
interior hasta que el extremo inferior se encuentre a 2 cm de profundidad. Tomamos
como tensión superficial del agua a la ª a la que se encuentre de la tabla 6.1.
B D
Figura 6.3 Aparato de Otto Stenbach para medir la tensión superficial.
Se abre la llave B hasta igualar la lectura en ambas ramas de la presión. Si al cerrar esta
llave se modifica la lectura, entonces se anota la lectura de las posiciones de ambas
ramas H1 - h1= h0. Se abre la llave L comenzando a desplazarse el líquido de tal manera
que el gas sale por le capilar formándose una pequeña burbuja, cuando ésta se ha
formado y se tiene un rosario discreto y continuo de burbujas se anotan la altura.
La presión máxima necesaria para la formación de la burbuja se calcula como se
muestra en la figura 6.3.
P = g[ hm – h0]
Con la presión máxima y la tensión superficial del agua destilada ya se puede calcular
el radio del capilar, aplicando la siguiente ecuación.
Rg
γ= [ ρ (h −h )− ρh]
2 m m 0
Una vez conocido el radio del capilar se puede calcular ya la tensión superficial de
cualquier sustancia en función de la presión máxima, operando como anteriormente se
explicó, llenando el vaso D con el líquido correspondiente.
NOTA. Cuando es conocido el radio del capilar, conviene realizar la calibración, ya que
si se obtiene un valor similar o igual, al especificado por el fabricante, del radio del
capilar, estamos cerciorándonos que el aparato esta trabajando correctamente, de lo
contrario tendremos que verificar si no existe alguna fuga u obstrucción en el aparato.
RESULTADOS
1.-Con el método de la burbuja determina el radio del capilar, utilizando agua destilada.
La tensión superficial del agua se da en la tabla 6.1.
Autor: Alejandro Uría Galicia 5
2.- Obtén el valor del Radio del capilar en función de las medidas realizadas durante el
experimento, teniendo en cuenta que el líquido manométrico es agua.
3.- Obtén la tensión superficial de diferentes mezclas de agua-detergente a distintas
concentraciones.
4.- Construye una gráfica de tensión superficial (como ordenada) contra la
concentración de jabón (abscisa) y realiza un análisis cualitativo de dicha gráfica.
No se requiere en este caso la ecuación empírica.
dinas T °C dinas T °C dinas T °C
( ) ( ) ( )
cm cm cm
74.07 11 72.75 20 71.35 29
73.93 12 72.59 21 71.18 30
73.78 13 72.44 22 70.38 35
73.64 14 72.28 23 69.56 40
73.49 15 72.13 24 68.74 45
73.34 16 71.97 25 67.91 50
73.19 17 71.82 26 66.18 60
73.05 18 71.66 27 64.42 70
72.90 19 71.50 28 62.61 80
Tabla 6.1. Tensión Superficial del agua en contacto con el aire a varias temperaturas.
Autor: Alejandro Uría Galicia 6
También podría gustarte
- Tensión SuperficialDocumento7 páginasTensión SuperficialOber Sánchez100% (1)
- Tension Superficial Fisica PDFDocumento5 páginasTension Superficial Fisica PDFAnonymous ZewMBS2Aún no hay calificaciones
- Tension Superficial de TodosDocumento43 páginasTension Superficial de TodosAnalyabrilAún no hay calificaciones
- C04 Tension Superficial2006 2Documento9 páginasC04 Tension Superficial2006 2Allisson Corina Muñoz RiveraAún no hay calificaciones
- 20221111071141Documento8 páginas20221111071141Marino GuerreroAún no hay calificaciones
- Tensión Superficial y CapilaridadDocumento16 páginasTensión Superficial y CapilaridadKatia Michelle ArmentaAún no hay calificaciones
- Informe de Laboratorio Virtual 3Documento20 páginasInforme de Laboratorio Virtual 3erickAún no hay calificaciones
- Práctica Tensión SuperficialDocumento16 páginasPráctica Tensión SuperficialManuMadridAún no hay calificaciones
- Informe de Practica Sobre Tensión Superficial y CapilaridadDocumento11 páginasInforme de Practica Sobre Tensión Superficial y CapilaridadCristian ZavaletaAún no hay calificaciones
- Sesion #2Documento65 páginasSesion #2Shei M. BLAún no hay calificaciones
- C04 - Tension SuperficialDocumento8 páginasC04 - Tension SuperficialDante Emilio RMAún no hay calificaciones
- Tención Superficial LUFDocumento10 páginasTención Superficial LUFOmar MonteroAún no hay calificaciones
- TENSION SUPERFICIAL Teoria!!Documento10 páginasTENSION SUPERFICIAL Teoria!!Elvis Henry MoscosoAún no hay calificaciones
- Fenómenos Interfaciales. en Una Fase, Tensión Y Cinética en La Superficie Y Relación Entre Tensión Superficial Y Tensión InterfácialDocumento19 páginasFenómenos Interfaciales. en Una Fase, Tensión Y Cinética en La Superficie Y Relación Entre Tensión Superficial Y Tensión InterfácialEkos RgAún no hay calificaciones
- Tensiòn Superficial Del Agua: ObjetivoDocumento24 páginasTensiòn Superficial Del Agua: ObjetivoMarino GuerreroAún no hay calificaciones
- Mecanica de Fluidos - Tension SuperficialDocumento6 páginasMecanica de Fluidos - Tension SuperficialFelipe CamposAún no hay calificaciones
- Determinación del coeficiente de tensión superficial mediante el método de RayleighDocumento11 páginasDeterminación del coeficiente de tensión superficial mediante el método de RayleighDiego Del CastilloAún no hay calificaciones
- Tensión superficial: concepto, causas, propiedades y métodos de mediciónDocumento6 páginasTensión superficial: concepto, causas, propiedades y métodos de mediciónJhon JefferAún no hay calificaciones
- Tension SuperficialDocumento38 páginasTension SuperficialRoy Juan Mendoza PalmaAún no hay calificaciones
- EXPOTERMODocumento24 páginasEXPOTERMOAaron Chacaliaza RicaldiAún no hay calificaciones
- Tensión Superficial y CapilaridadDocumento38 páginasTensión Superficial y Capilaridadfernando benottiAún no hay calificaciones
- Determinación del coeficiente de tensión superficial de líquidosDocumento30 páginasDeterminación del coeficiente de tensión superficial de líquidosJhony Chacon Robles0% (1)
- Interfase Liquido - GasDocumento40 páginasInterfase Liquido - GasJhon AyalaAún no hay calificaciones
- Tensión superficial: concepto, determinación y ecuación de Katayama-GuggenheimDocumento29 páginasTensión superficial: concepto, determinación y ecuación de Katayama-GuggenheimVale Prado VargasAún no hay calificaciones
- Tension SuperficialDocumento12 páginasTension SuperficialWendyAún no hay calificaciones
- Tensión Superficial y CapilaridadDocumento67 páginasTensión Superficial y CapilaridadFlorValleAún no hay calificaciones
- Tensión SuperficialDocumento7 páginasTensión SuperficialKarin Johanna ColomboAún no hay calificaciones
- Método Dunoy para medir tensión superficialDocumento6 páginasMétodo Dunoy para medir tensión superficialAnonymous iIaMAfVAún no hay calificaciones
- Tension SuperficialDocumento2 páginasTension SuperficialLUISA FERNANDA ZAMBRANO CARDENASAún no hay calificaciones
- Tensión superficial: definición, propiedades, fórmulas y métodos de determinaciónDocumento4 páginasTensión superficial: definición, propiedades, fórmulas y métodos de determinaciónAGUSTÍN LEANDRO DÍAZAún no hay calificaciones
- Tensión SuperficialDocumento8 páginasTensión SuperficialCluisantony Jayco DizeAún no hay calificaciones
- Semana #05Documento14 páginasSemana #05Cristhian Fabian Garcia CruzAún no hay calificaciones
- Marco Teórico Tension SuperficialDocumento9 páginasMarco Teórico Tension SuperficialDOMITILA MEDINA CHAVEZAún no hay calificaciones
- Secme 22399Documento77 páginasSecme 22399Samir CayetanoAún no hay calificaciones
- Fenomenos de SuperficieDocumento8 páginasFenomenos de SuperficieMarieta VargasAún no hay calificaciones
- Tension SuperficialDocumento12 páginasTension SuperficialMiguel Ãngel Durãn BAún no hay calificaciones
- Actividad 3Documento10 páginasActividad 3Evellyn San MartinAún no hay calificaciones
- Mecanica de Fluidos-2Documento35 páginasMecanica de Fluidos-2David TipanAún no hay calificaciones
- Interfase Liquido - GasDocumento40 páginasInterfase Liquido - GasDexhuj0% (1)
- Capitulo IDocumento30 páginasCapitulo IMARLA JOSELEEN MARTINEZ RIOSAún no hay calificaciones
- Tension SuperficialDocumento20 páginasTension SuperficialJoel Cano100% (2)
- Tension SuperficialDocumento5 páginasTension SuperficialjulioAún no hay calificaciones
- Tension SuperficialDocumento5 páginasTension SuperficialHugo Angel VlrAún no hay calificaciones
- SemanaDocumento60 páginasSemanaAlex Taipe0% (1)
- Informe 3 Tension SuperficialDocumento22 páginasInforme 3 Tension Superficialdanielandrade780% (1)
- Determinaciones de tensión superficialDocumento25 páginasDeterminaciones de tensión superficialAriana NoeliaAún no hay calificaciones
- Tema 5. - Presión en LIQUIDOS-1Documento4 páginasTema 5. - Presión en LIQUIDOS-1millylupitaolmedoAún no hay calificaciones
- Trabajo Fisica IIDocumento30 páginasTrabajo Fisica IIJunior Steven Solorzano FabianAún no hay calificaciones
- Tensión SuperficialDocumento7 páginasTensión SuperficialGiuliana RojasAún no hay calificaciones
- 4.1 Fenómeno Capilar y Proceso de ContracciónDocumento16 páginas4.1 Fenómeno Capilar y Proceso de ContracciónErika MartínezAún no hay calificaciones
- Tensión Superficial FinalDocumento12 páginasTensión Superficial FinalWilder Huaman MuñozAún no hay calificaciones
- Resumen: Tension Superficial, Anfifilos y Tensoactivos ParacoroDocumento6 páginasResumen: Tension Superficial, Anfifilos y Tensoactivos ParacoroPablo RamírezAún no hay calificaciones
- Tension Superficial, Metodo Del AnilloDocumento11 páginasTension Superficial, Metodo Del Anillosystematicchaos24Aún no hay calificaciones
- Tension SuperficialDocumento10 páginasTension SuperficialReus DomenicoAún no hay calificaciones
- 2a EvaluaciónDocumento2 páginas2a EvaluaciónKaren9DiazAún no hay calificaciones
- Practica 11Documento3 páginasPractica 11Karen9DiazAún no hay calificaciones
- HOJADocumento6 páginasHOJAKaren9DiazAún no hay calificaciones
- 2a EvaluaciónDocumento2 páginas2a EvaluaciónKaren9DiazAún no hay calificaciones
- Cuestionario CromatografiaDocumento4 páginasCuestionario CromatografiaKaren9DiazAún no hay calificaciones
- Polen 40Documento5 páginasPolen 40Karen9DiazAún no hay calificaciones
- Practica 12 de BotanicaDocumento3 páginasPractica 12 de BotanicaKaren9DiazAún no hay calificaciones
- 2a EvaluaciónDocumento2 páginas2a EvaluaciónKaren9DiazAún no hay calificaciones
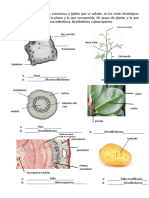
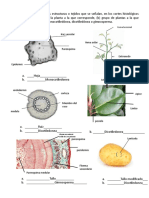
- ESTRUCTURA Y FUNCIONES DE LA HOJADocumento26 páginasESTRUCTURA Y FUNCIONES DE LA HOJAKaren9DiazAún no hay calificaciones
- Características de familias de plantas con interés farmacéuticoDocumento4 páginasCaracterísticas de familias de plantas con interés farmacéuticoKaren9DiazAún no hay calificaciones
- Frutos para RotularDocumento4 páginasFrutos para RotularKaren9DiazAún no hay calificaciones
- HistaminaDocumento5 páginasHistaminaKaren9DiazAún no hay calificaciones
- Cuestionario Practica7Documento2 páginasCuestionario Practica7Karen9DiazAún no hay calificaciones
- Síntesis cloruro ter-butilo SN1 disolvente polaridadDocumento2 páginasSíntesis cloruro ter-butilo SN1 disolvente polaridadKaren9DiazAún no hay calificaciones
- Cuestionario de Ambiente EstudiantilDocumento3 páginasCuestionario de Ambiente EstudiantilKaren9DiazAún no hay calificaciones
- Procesos PoliticosDocumento2 páginasProcesos PoliticosKaren9DiazAún no hay calificaciones
- CUESTIONARIO RecristalizaciónDocumento3 páginasCUESTIONARIO RecristalizaciónKaren9DiazAún no hay calificaciones
- Pract Ica 3 Separ Acion de Una Mezcla TeDocumento1 páginaPract Ica 3 Separ Acion de Una Mezcla TeKaren9DiazAún no hay calificaciones
- Laboratorio 1 Experiencia de ReynoldsDocumento11 páginasLaboratorio 1 Experiencia de ReynoldsRenzo SuarezAún no hay calificaciones
- Instalaciones de AGUADocumento17 páginasInstalaciones de AGUAFranco RufinoAún no hay calificaciones
- VENTILADORESDocumento16 páginasVENTILADORESYordanAún no hay calificaciones
- Clase 2 - HIDRAULICA IDocumento32 páginasClase 2 - HIDRAULICA ILeslie V. ToledoAún no hay calificaciones
- ReologiaDocumento6 páginasReologiajavierAún no hay calificaciones
- Pérdidas de Energía ÁNGELA MARTÍNEZ HB-G3 PDFDocumento17 páginasPérdidas de Energía ÁNGELA MARTÍNEZ HB-G3 PDFAngela Martinez RodriguezAún no hay calificaciones
- Flujo Laminar vs TurbulentoDocumento4 páginasFlujo Laminar vs TurbulentoJohn CahuapazaAún no hay calificaciones
- HidrodinamicaDocumento17 páginasHidrodinamicaRicardo GuachamínAún no hay calificaciones
- Galeria Filtrante ProyectoDocumento3 páginasGaleria Filtrante ProyectorsoyyoAún no hay calificaciones
- Agentes EspumantesDocumento39 páginasAgentes EspumantesEfrainGuzmanAún no hay calificaciones
- Presión capilar laboratorio UNIDocumento15 páginasPresión capilar laboratorio UNIKevin AtochaAún no hay calificaciones
- Perdidas de Carga Locales en Una Tuberias Con AccesoriosDocumento5 páginasPerdidas de Carga Locales en Una Tuberias Con AccesoriosJhon A. CcamaAún no hay calificaciones
- Módulo 1: Principios Básicos de HidraulicaDocumento58 páginasMódulo 1: Principios Básicos de HidraulicaEric Mauricio Solís FritzAún no hay calificaciones
- Cavitación bombas centrifugasDocumento10 páginasCavitación bombas centrifugasRomario Avila MeriñoAún no hay calificaciones
- Iili04038 Tarea 1Documento3 páginasIili04038 Tarea 1Memo CamarenaAún no hay calificaciones
- Componente Práctico - Práctica de LaboratorioDocumento26 páginasComponente Práctico - Práctica de Laboratorioluzamparoninoflorez21Aún no hay calificaciones
- Problemario U4Documento9 páginasProblemario U4MARIO ANDRES MONTOYA HERNANDEZ0% (2)
- Coeficientes de fricción y ecuaciones de flujoDocumento17 páginasCoeficientes de fricción y ecuaciones de flujoJohna M MartínezAún no hay calificaciones
- Precion Mecanica de FluidosDocumento2 páginasPrecion Mecanica de Fluidoseduardo alfaro amadorAún no hay calificaciones
- Capitulo I Flujo Permanente y Uniforme en Canales 2010 - DocDocumento18 páginasCapitulo I Flujo Permanente y Uniforme en Canales 2010 - DocKevin Yangali LimacoAún no hay calificaciones
- Manual de Fluidos, Spanish Chapter 05Documento36 páginasManual de Fluidos, Spanish Chapter 05Ronald Tellez ChoqueAún no hay calificaciones
- Informe de Laboratorio No. 2Documento4 páginasInforme de Laboratorio No. 2maoslhoAún no hay calificaciones
- Evidencias Hidráulica de Canales - Juan Manuel Ocampo RodríguezDocumento30 páginasEvidencias Hidráulica de Canales - Juan Manuel Ocampo RodríguezManuel OcampoAún no hay calificaciones
- Reynols Practica 4Documento10 páginasReynols Practica 4Orlando MoralesAún no hay calificaciones
- Flujo de Fluidos en TuberíasDocumento12 páginasFlujo de Fluidos en TuberíasJorge Alberto Uribe RamírezAún no hay calificaciones
- Mecánica de FluidosDocumento4 páginasMecánica de FluidosVANESSA CATALINA BUITRAGO SOLORZANOAún no hay calificaciones
- Ecuación de Colebrook-WhiteDocumento4 páginasEcuación de Colebrook-WhitealejandroAún no hay calificaciones
- Experimeto de Los HuevosDocumento17 páginasExperimeto de Los HuevosCRISTIAN DANIEL ZUÑIGA FLORESAún no hay calificaciones
- 165095Documento76 páginas165095Anonymous YuMZpKAún no hay calificaciones
- Tension InterfacialDocumento31 páginasTension InterfacialBilliyoAún no hay calificaciones