Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Taller 3 IRQ-I-2020
Cargado por
Angie PinillaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Taller 3 IRQ-I-2020
Cargado por
Angie PinillaCopyright:
Formatos disponibles
INGENIERÍA DE LAS REACCIONES QUÍMICAS 2015716-2
Taller 3. Cinética química – análisis de datos experimentales
Juan Guillermo Cadavid Estrada
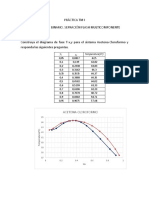
Problema 1. Para realizar el estudio cinético de la producción de amoniaco se utilizó un reactor por
lotes equipado con un dispositivo sensible para la medida de la presión. Se realiaron dos ensayos a
diferentes temperaturas, en ambos casos el reactor se evacuó y se cargó con nitrógeno e hidrógeno,
dicha operación se efectuó a 20 C, temperatura suficientemente baja para que la reacción no
transcurra en extensión apreciable. Posteriormente, la temperatura se elevó rápidamente a la
condición propuesta para el ensayo introduciendo el reactor dentro de un horno equipado con
control de temperatura, obteniéndose los datos dados de las Tablas 1 y 2. Obtenga la ecuación
cinética completa, utilice al menos dos de los métodos presentados en clase (método integral,
método diferencial y ajuste por mínimos cuadrados), explique claramente el procedimiento, así
como las suposiciones que haga.
Tabla 1. Datos Ensayo 1.
Temperatura de reacción: 327 C
Alimentación estequiométrica
Presión del sistema a 20 C : 100 atm Tabla 2. Datos Ensayo 2.
t (min) P (atm) Temperatura de reacción: 450 C
0 Alimentación: yN2i = 0,05
0,6 200,1 Presión del sistema a 20 C : 200 atm
1,4 195,0 t (min) P (atm)
1,9 191,6 0
2,9 186,8 0,5 472,0
3,7 183,2 1,2 456,7
4,7 179,1 2 449,2
12,2 161,7 3 445,7
33,3 142,8 5 444,2
173,9 121,3 20 444,0
1090 110,0
∞
Problema 2. Para realizar el estudio cinético de la esterificación de ácido acético con etanol, se
utilizó un reactor por lotes sumergido dentro de un baño termostático. Se realizaron dos ensayos,
uno a 60 C y el otro a 75 C. En ambos casos se cargaron cantidades equimolares de los dos reactivos
y se tomaron muestras de 0,5 ml cada cierto tiempo, como se indica en las siguientes tablas, las
cuales fueron valoradas con una solución de hidróxido de potasio en isopropanol 0,1 M. Suponiendo
que la reacción es elemental, determine la ecuación cinética completa, explique claramente el
procedimiento, así como las suposiciones que haga.
Tabla 2. Datos Problema 2.
Ensayo 1. T = 60 C Ensayo 2. T = 75 C
t (min)
VKOH (ml) VKOH (ml)
0 43,2 43,2
1 41,4 40,6
4 37,0 34,3
10 30,2 26,6
15 26,3 22,9
20 23,4 20,6
30 19,4 18,0
45 15,8 16,5
60 13,8 16,0
120 11,0 15,8
∞ 10,4 15,8
Información adicional
(kg m-3) MW
A: Ácido acético 1049 60
B: Etanol 789 46,1
C: Agua 1000 18
D: Acetato de etilo 901 88,1
También podría gustarte
- REACCIONES QUIMICAS II REACTOR BATCHDocumento9 páginasREACCIONES QUIMICAS II REACTOR BATCHYeraldin PachecoAún no hay calificaciones
- Clase 11-1Documento4 páginasClase 11-1Jose HumeresAún no hay calificaciones
- Equivalente Eléctrico Del CalorDocumento5 páginasEquivalente Eléctrico Del CalorCamila VelandiaAún no hay calificaciones
- Practica 4 Electricidad Grupo 5Documento12 páginasPractica 4 Electricidad Grupo 5Trostky GuerreroAún no hay calificaciones
- PROBLEMAS PROPUESTOS: TERMODINÁMICA QUÍMICADocumento4 páginasPROBLEMAS PROPUESTOS: TERMODINÁMICA QUÍMICAFlorPerettiAún no hay calificaciones
- Laboratorio de Hidráulica 2Documento3 páginasLaboratorio de Hidráulica 2Fernando AyalaAún no hay calificaciones
- Informes de Viscosidad y DensidadDocumento18 páginasInformes de Viscosidad y DensidadXflk lsbtAún no hay calificaciones
- Actividad 2 Completo 1Documento20 páginasActividad 2 Completo 1KATTERIN PAOLA ALVEAR MORENOAún no hay calificaciones
- Problemas A Desarrollar en Clase PG UnacDocumento1 páginaProblemas A Desarrollar en Clase PG UnacCrinny Urpi Chaska0% (1)
- Lab 7 de QMC1206Documento7 páginasLab 7 de QMC1206AllenWalkerAún no hay calificaciones
- Sistema de AguaDocumento16 páginasSistema de AguaRoxana Copa VasquezAún no hay calificaciones
- PRÁCTICO 3 Melanie Lucia Mansilla Cardozo - Natasha Belén Lombardo Morena - Federico Bello Ureta - Paulo Blanco RodriguezDocumento5 páginasPRÁCTICO 3 Melanie Lucia Mansilla Cardozo - Natasha Belén Lombardo Morena - Federico Bello Ureta - Paulo Blanco RodriguezElianaAún no hay calificaciones
- 3er Informe Presión de Vapor de Un Líquido PuroDocumento5 páginas3er Informe Presión de Vapor de Un Líquido PuroAlejandro González33% (3)
- Carga capacitorDocumento8 páginasCarga capacitorJhonatan YapitaAún no hay calificaciones
- Informe Bombas CentrifugasDocumento17 páginasInforme Bombas CentrifugasYarisbelAún no hay calificaciones
- Informe Filtro PrensaDocumento5 páginasInforme Filtro PrensaMiguel Peña OsorioAún no hay calificaciones
- Hidrólisis ácida del acetato de etiloDocumento14 páginasHidrólisis ácida del acetato de etiloJazmin LeonAún no hay calificaciones
- PracticaFlash30 08 2018Documento5 páginasPracticaFlash30 08 2018Kevin Javier QuispeAún no hay calificaciones
- 3er Examen Parcial - 2023 - 1 - ProblemasDocumento6 páginas3er Examen Parcial - 2023 - 1 - ProblemasJimena GarcíaAún no hay calificaciones
- Sistema agua-hidrocarburo: Contenido de agua y temperatura de hidratación gas naturalDocumento19 páginasSistema agua-hidrocarburo: Contenido de agua y temperatura de hidratación gas naturalMarco Antonio Campos VeraAún no hay calificaciones
- Transferencia de Masa II PDFDocumento28 páginasTransferencia de Masa II PDFAndrade Oscco L. Jose100% (1)
- Practicas Primer Parcial de IngDocumento14 páginasPracticas Primer Parcial de IngramiroAún no hay calificaciones
- Ejercicios Resueltos #1Documento11 páginasEjercicios Resueltos #1Ronald100% (2)
- Informe Cinetica de La Descomposicion Del Peroxido FinalDocumento8 páginasInforme Cinetica de La Descomposicion Del Peroxido FinalJuanesVascoAún no hay calificaciones
- Granizo-EspinosaC. Labo CoreolisDocumento11 páginasGranizo-EspinosaC. Labo CoreolisGabriel GranizoAún no hay calificaciones
- Propiedades Del Agua y Tablas de VaporDocumento31 páginasPropiedades Del Agua y Tablas de VaporMartin Balladares OrellanaAún no hay calificaciones
- Practica 2 Cinetica EsiqieDocumento12 páginasPractica 2 Cinetica EsiqieJesús Yair Mejía SánchezAún no hay calificaciones
- Tarea3 TRANSPORTEDocumento6 páginasTarea3 TRANSPORTEJuan Carlos Flores100% (1)
- Informe Destilacion BinariaDocumento17 páginasInforme Destilacion BinariaDenisse DiazAún no hay calificaciones
- Cinética de La Descomposición Del Peróxido de HidrógenoDocumento9 páginasCinética de La Descomposición Del Peróxido de HidrógenoMaríaAún no hay calificaciones
- Informe Sistemas TernariosDocumento6 páginasInforme Sistemas TernariosVictor CrossAún no hay calificaciones
- Informe Tuvo de VenturiDocumento5 páginasInforme Tuvo de VenturiOskar Kamilo KaroAún no hay calificaciones
- Fase 4 Orieta Patricia OchoaDocumento33 páginasFase 4 Orieta Patricia OchoaEsteban IsazaAún no hay calificaciones
- Taller Cinéticas de Reacción SubirDocumento3 páginasTaller Cinéticas de Reacción SubirLüis Santacruz VillaAún no hay calificaciones
- Experiencia de Lab N°6Documento11 páginasExperiencia de Lab N°6Sofia Victoria Olmos TorresAún no hay calificaciones
- Torres EmpacadasDocumento8 páginasTorres Empacadasvalerie samaanAún no hay calificaciones
- Filtración de caldos: Problemas y cálculos de parámetrosDocumento2 páginasFiltración de caldos: Problemas y cálculos de parámetrosD-Rod GarciaAún no hay calificaciones
- Taller Sustancias Puras Melissa Camargo y Steven MoraDocumento10 páginasTaller Sustancias Puras Melissa Camargo y Steven MorastevenAún no hay calificaciones
- Laboratorio 6 Relajacion ExponencialDocumento8 páginasLaboratorio 6 Relajacion ExponencialFabián ZuñigaAún no hay calificaciones
- Grupo 1 - Informe 2Documento18 páginasGrupo 1 - Informe 2Gabriel FreitesAún no hay calificaciones
- Determinación de la AEPT, número de etapas teóricas y número de unidades de transferencia en una columna de destilación con rellenoDocumento14 páginasDeterminación de la AEPT, número de etapas teóricas y número de unidades de transferencia en una columna de destilación con rellenoMauricio MerlanAún no hay calificaciones
- Efecto del tiempo de residencia en la conversión de reactores CSTR en serieDocumento11 páginasEfecto del tiempo de residencia en la conversión de reactores CSTR en seriePaul Vallejo PossoAún no hay calificaciones
- Fisicoquímica Ejercicios 2 y 6Documento5 páginasFisicoquímica Ejercicios 2 y 6paola lancherosAún no hay calificaciones
- Laboratorio 8Documento17 páginasLaboratorio 8Jhonatan Rimache ArotomaAún no hay calificaciones
- Quiz 3 - 2023-1Documento3 páginasQuiz 3 - 2023-1Angela Lorena DíazAún no hay calificaciones
- Cuarta Práctica Calificada de Estadística Aplicada A La Ingeniería - 2017 IIDocumento1 páginaCuarta Práctica Calificada de Estadística Aplicada A La Ingeniería - 2017 IIanon_285939503Aún no hay calificaciones
- Documento Sin TítuloDocumento5 páginasDocumento Sin TítuloSebastian MerchanAún no hay calificaciones
- Laboratorio N°4Documento6 páginasLaboratorio N°4Noelia SosaAún no hay calificaciones
- Energia Interna y Trabajo ElectricoDocumento7 páginasEnergia Interna y Trabajo ElectricoMelany Vanessa Berrio TabordaAún no hay calificaciones
- Caracterización de fracción de crudo mediante ensayos ASTM D-86 y D-287Documento31 páginasCaracterización de fracción de crudo mediante ensayos ASTM D-86 y D-287estefaniAún no hay calificaciones
- Calculo Practica#8Documento7 páginasCalculo Practica#8Rosalia Pacheco CastroAún no hay calificaciones
- Serie de ejercicios de organización y economía de la producciónDocumento8 páginasSerie de ejercicios de organización y economía de la producciónBárbaraAún no hay calificaciones
- CONDUCTIMETRIADocumento10 páginasCONDUCTIMETRIAFabian Alejandro SanchezAún no hay calificaciones
- Solucionario Levenspiel Cap 3 TRABAJO de INGE 3Documento12 páginasSolucionario Levenspiel Cap 3 TRABAJO de INGE 3Roy Quispe HuayllapumaAún no hay calificaciones
- Formato de Informe Práctica Medida de CaudalDocumento7 páginasFormato de Informe Práctica Medida de CaudalARRA NOMINAAún no hay calificaciones
- Sedimentadores DiscontinuosDocumento16 páginasSedimentadores DiscontinuosJANY VILELAAún no hay calificaciones
- Problemas resueltos de Hidráulica de CanalesDe EverandProblemas resueltos de Hidráulica de CanalesCalificación: 4.5 de 5 estrellas4.5/5 (7)
- Guía de laboratorio de mecánica de fluidosDe EverandGuía de laboratorio de mecánica de fluidosAún no hay calificaciones
- Ingeniería química. Soluciones a los problemas del tomo IDe EverandIngeniería química. Soluciones a los problemas del tomo IAún no hay calificaciones
- Modelado fenomenológico del proceso de combustión por difusión diéselDe EverandModelado fenomenológico del proceso de combustión por difusión diéselAún no hay calificaciones
- Parcial 1, 15-04-2020Documento2 páginasParcial 1, 15-04-2020Angie PinillaAún no hay calificaciones
- Tarea 1Documento2 páginasTarea 1Angie PinillaAún no hay calificaciones
- MasaDocumento1 páginaMasaAngie PinillaAún no hay calificaciones
- Taller 2 - Mecanismos de Reacción PDFDocumento2 páginasTaller 2 - Mecanismos de Reacción PDFCamila TorresAún no hay calificaciones
- Estequiometría y cinética químicaDocumento3 páginasEstequiometría y cinética químicaAngie PinillaAún no hay calificaciones
- MetodosDocumento5 páginasMetodosAngie PinillaAún no hay calificaciones
- Informe 5 - PorosidadDocumento9 páginasInforme 5 - PorosidadEdwin Cirilo ChaucaAún no hay calificaciones
- PDF Lista de Piezas Orbitrol DLDocumento4 páginasPDF Lista de Piezas Orbitrol DLESTACIÓN DE JUEGOAún no hay calificaciones
- Clase N - 2 Requerimientos CaloricosDocumento19 páginasClase N - 2 Requerimientos CaloricosMijael Vega AcuñaAún no hay calificaciones
- Mitos y Supersticiones PDFDocumento312 páginasMitos y Supersticiones PDFMateo Palacio100% (1)
- PDF Modificacion Del Estudio de Impacto Ambiental Del Proyecto de Expansion A 3300 TMD Unidad Minera Pachapaqui CompressDocumento160 páginasPDF Modificacion Del Estudio de Impacto Ambiental Del Proyecto de Expansion A 3300 TMD Unidad Minera Pachapaqui CompressKEN INGAún no hay calificaciones
- Espacios Normados IntroducciónDocumento9 páginasEspacios Normados IntroducciónLuis Arce GonzálezAún no hay calificaciones
- Informe de Laboratorio de Me 05Documento4 páginasInforme de Laboratorio de Me 05Kevin Medina VillagomezAún no hay calificaciones
- Anual SM Guía Nº21 (CB)Documento13 páginasAnual SM Guía Nº21 (CB)MaxAltairSceneAún no hay calificaciones
- Consideraciones de La Ley de DarcyDocumento3 páginasConsideraciones de La Ley de DarcyEnrique Uicab AlcocerAún no hay calificaciones
- Foro Tematico Calificlable F & QDocumento3 páginasForo Tematico Calificlable F & QNick Arthur Sebastian CarrascalAún no hay calificaciones
- Resumen de La Dieta WWDocumento33 páginasResumen de La Dieta WWMarta Perpiñán0% (1)
- Acido-Formico 2Documento6 páginasAcido-Formico 2Valeria Isabel Flores TamaraAún no hay calificaciones
- Dichos Con Bichos PDFDocumento98 páginasDichos Con Bichos PDFducadeliaAún no hay calificaciones
- Introducción Modelos de Probabilidad en Ingeniería Eléctrica y de La ComputaciónDocumento17 páginasIntroducción Modelos de Probabilidad en Ingeniería Eléctrica y de La ComputaciónNelson ReyesAún no hay calificaciones
- Método de La AutoobservaciónDocumento4 páginasMétodo de La AutoobservaciónRodrigo Vargas PérezAún no hay calificaciones
- Reflejos Primitivos 1Documento1 páginaReflejos Primitivos 1Jorge Luis Rodriguez MejiaAún no hay calificaciones
- Información Del Elemento TelurioDocumento2 páginasInformación Del Elemento TelurioDaniel ParkerAún no hay calificaciones
- Sea Por Siempre Ensalzado El Santo Nombre Del Supremo CreadorDocumento2 páginasSea Por Siempre Ensalzado El Santo Nombre Del Supremo Creadorluis naranjo100% (1)
- Técnicas de Corte Por Oscar ColomboDocumento2 páginasTécnicas de Corte Por Oscar ColomboAbraham MezaAún no hay calificaciones
- Cementaciones Con TFDocumento39 páginasCementaciones Con TFjomarlucaAún no hay calificaciones
- Ruiz Limon Ramon - Historia de La Psicologia Y Sus AplicacionesDocumento169 páginasRuiz Limon Ramon - Historia de La Psicologia Y Sus AplicacionesPsicoem75% (4)
- Semana 2: Egiptología (Egyptology)Documento182 páginasSemana 2: Egiptología (Egyptology)jeycy1002Aún no hay calificaciones
- La Quema de CombustiblesDocumento14 páginasLa Quema de CombustiblesLenin Yasig100% (1)
- Actividad Evaluativa Eje 4 - SISTEMA FINANCIERO INTERNACIONALDocumento4 páginasActividad Evaluativa Eje 4 - SISTEMA FINANCIERO INTERNACIONALAndres Mauricio Lopez GonzalezAún no hay calificaciones
- Apuntes Diseño de CanalesDocumento1 páginaApuntes Diseño de CanalesErick GiovaniAún no hay calificaciones
- Unidad Educativa Franciscana San AntonioDocumento23 páginasUnidad Educativa Franciscana San Antoniomajo arellanoAún no hay calificaciones
- UNAM Química de Coordinación Tarea Previa 3Documento2 páginasUNAM Química de Coordinación Tarea Previa 3Judas IscarioteAún no hay calificaciones
- SaDocumento91 páginasSaLevi JohnstonAún no hay calificaciones
- La CiguapaDocumento5 páginasLa CiguapaYoel Del RosarioAún no hay calificaciones
- Impresora 3DDocumento6 páginasImpresora 3DChristina DunnAún no hay calificaciones