Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Guia de Practicas Farmacologia II 2017-1
Cargado por
Anonymous q3hUTATítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Guia de Practicas Farmacologia II 2017-1
Cargado por
Anonymous q3hUTACopyright:
Formatos disponibles
3B-2
GUÍA DE PRÁCTICAS
Unidad académica: EAP DE FARMACIA Y BIOQUÍMICA
FARMACOLOGÍA II
DOCENTES: Q.F. Máximo C. NAVARRO TORRES.
Q.F. Manuel HERNANDEZ AGUILAR.
Q.F. José Rafael PACHECO FELIX.
Q.F. Milagritos R. PEREZ ALVAREZ.
2017
F-CV3-3B-2 Rev. Enero 2011
INTRODUCCIÓN
La Farmacología es la ciencia encargada del estudio de las propiedades de los fármacos o
medicamentos, cuando éstos interactúan con los sistemas biológicos (células, mitocondrias,
enzimas, entre otros) para calmar, curar, controlar, prevenir o diagnosticar las enfermedades. En
forma general se dice que estudia las propiedades de los fármacos en los seres vivos con particular
referencia al hombre.
Fármaco es toda sustancia que administrada a un organismo vivo provoca en éste un cambio en la
actividad bioquímica o funcional de las células originando una respuesta y se utiliza para calmar o
mitigar, curar, tratar, prevenir o diagnosticar enfermedades.
La farmacología es una ciencia fundamentalmente descriptiva que utiliza la observación y
experimentación (método experimental) para explicar la acción de los fármacos sobre los sistemas
biológicos.
La investigación y desarrollo de un nuevo fármaco es un proceso largo y complejo, que no termina
con la aprobación del mismo para su comercialización, sino que continúa durante todo el tiempo de
su uso terapéutico. El estudio de los fármacos se divide en dos partes:
Farmacología experimental o pre-clínica que se encarga del estudio farmacocinético,
farmacodinámico y toxicológico de los fármacos en modelos biológicos animales más adecuados.
Farmacología Clínica estudia la farmacocinética y farmacodinamia de los fármacos en el hombre
sano o enfermo. Su objeto de estudio no se limita a los nuevos medicamentos, sino que incluye la
búsqueda de nuevas formas de presentación, vías de administración o nuevos usos terapéuticos.
Esta parte de estudio se divide a su vez en cuatro fases; para la realización de las tres primeras, es
decir, las fases I, II y III se requieren la autorización de las autoridades sanitarias, mientras que,
para llevar a cabo la fase IV es necesario la aprobación de la comercialización del fármaco y dura
todo el periodo de vigencia del fármaco.
La farmacología no podía desarrollarse como ciencia hasta que no lo hiciera la química, esto recién
ocurrió hasta fines del siglo XVIII y comienzos del XIX, en que empiezan aislar los principales
alcaloides y glucósidos.
Francisco Magendie (1778-1850) escribió en 1821 un formulario que incluía las nuevas sustancias
puras recién descubiertas, fue el primero en impulsar el método experimental en el estudio de la
acción de los fármacos. Claudio Bernard fue su mejor discípulo y su trabajo sobre el lugar de acción
del curare es verdadera obra maestra.
F-CV3-3B-2 Rev. Enero 2011
El Primer Laboratorio de Farmacología Experimental fue establecido en Dorpat (Estonia) por
Rudolf Bucheim (1820-1879). Su obra se continuó con Oswald Schmiedeberg (1838-1921), profesor
de farmacología en Dorpat y posteriormente en Estrasburgo, contribuyó al estudio de la digital y
muscarina.
El propulsor de la Farmacología en América fue J. J. Abel (1857-1938) fundador de la Journal of
Pharmacology and Experimental Therapeutics y del primer laboratorio de Farmacología en Ann-
Arbor.
En el Perú, el inició de la Farmacología Experimental se debe a Tomas de Moreno y Maíz egresado
de la Facultad de Medicina de la UNMSM de Lima en 1869.
El método que mejor se adapta para el desarrollo de las prácticas de farmacología, así como para
las demás ciencias de la salud es el método de aprendizaje por redescubrimiento.
Mediante la parte práctica de farmacología, el estudiante:
Diseña y ejecuta experiencias que le permitan observar las respuestas en los modelos biológicos
“in vivo”, “in situ” e “in vitro” como consecuencia de la acción de los fármacos utilizados en
situaciones experimentalmente inducidas.
Analiza e Interpreta estos efectos observados aplicando los conocimientos teóricos, adquiridos en
las correspondientes clases o mediante investigaciones bibliográficas.
El estudiante de farmacología, es el futuro profesional Químico-Farmacéutico, quién al desarrollar
competencias en esta asignatura estará en la capacidad de convertirse en un especialista de la
información farmacológica, analizando e interpretando esquemas farmacoterapéuticos y apoyando
en forma eficaz y efectiva al equipo de salud en el uso razonado y adecuado de los medicamentos
en los pacientes.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 01 (SEMANA 01)
GENERALIDADES Y PREPARACION DE SOLUCIONES EN FARMACOLOGÍA
1.1. MARCO TEÓRICO
EL LABORATORIO DE FARMACOLOGIA
El laboratorio de Farmacología es el ámbito de trabajo que sirve a esta ciencia para alcanzar sus
objetivos, mediante la investigación práctica, a través de la aplicación de los fármacos en
organismos vivos y/o órganos aislados.
Elementos del laboratorio
Equipos, material quirúrgico y modelo biológico (animales de experimentación).
Equipos
El tipo de aparatos que requiere la experimentación farmacológica depende de la clase de estudio,
por lo general requiere el siguiente equipo:
1. Balanzas para animales.
2. Balanzas de precisión sensibles al 0.1 mg.
3. Aparatos de sujección:
Mesas de Bernard o de Brodie para perros.
Mesas de fijación para gato y conejo.
Tablas de fijación para rana, rata y ratón.
Dispositivos para la inyección en la cola de rata y ratón.
Cajas de anestesia para gato y conejo.
4. Baño para órganos aislados.
5. Tambores de marey.
6. Bombas a de respiración artificial.
7. Oncómetro.
8. Miógrafo.
9. Espirómetros de Roser.
10. Cánulas de Straub, Clark y Francois Frank.
11. Material de vidrio.
12. Baño de maría de diferente capacidad.
13. Quimógrafos.
14. Agujas de Raverdin.
15. Dispositivos de registro: En la mayoría de los experimentos, el efecto a medir es un cambio
de longitud, de tensión, volumen o del monto de fluido a través de un tejido. Entre estos tipos
de dispositivos tenemos:
a) La palanca inscriptora
Es el dispositivo más simple para medir el cambio de longitud, puede magnificar una respuesta
entre 5 a 7 veces. La tensión de la palanca puede ser de 0.5 a 4 g. Los registros que se realizan
sobre papel ahumado se fijan con un barniz plástico.
Si la respuesta es lenta puede ser necesario adaptar un vibrador en el montaje para prevenir que
la punta inscriptora se pegue; si la respuesta es muy rápida, como la contracción del músculo
cardiaco, deberá usarse una palanca con resorte delgado. Con otras respuestas, como la
contracción de una pieza de íleon, es adecuada una palanca simple en posición frontal; la
respuesta aparece como una línea recta en el papel ahumado. Sin embargo, la relación de la
F-CV3-3B-2 Rev. Enero 2011
contracción del tejido y la longitud del trazo no guarda una relación fija, ni el trazo permanece
constante. En la palanca “auxotónica, el peso ha sido deliberadamente determinado para
aumentarlo a medida que la contracción sea mayor.
Para un registro isotónico verdadero, en donde el peso permanece constante en cualquier
contracción, los dispositivos eléctricos son a menudo superiores, siendo la única manera de
obtener un registro isométrico y registro del aumento de extensión, cuando la longitud del tejido
permanece constante.
En los experimentos de farmacología la imperfección de los dispositivos de registro no es tan
seria, como sucede en fisiología. El farmacólogo se interesa en comparar solamente
concentraciones de diferentes fármacos que producen respuestas similares y no es
extremadamente crítico, si el registro de éstas, no es perfecto, ya que todas ellas van ha ser
afectadas de la misma forma.
La inercia de una palanca de inscripción, limita seriamente su utilidad en experimentos con
tejidos de concentración rápida, tal como la aurícula aislada.
b) Registro de flotación.
El cambio de volumen puede ser detectado con un simple dispositivo de flotación, que registra
su variación mediante una palanca inscriptora. Ej. En el caso que se desee detectar el cambio de
volumen en un segmento de intestino; cuando ocurre el peristaltismo, el fluido en el interior del
intestino retrocede hacía un reservorio que hace mover a su vez un flotador conectado a una
aguja inscriptora. Una línea hacía arriba, indicará una disminución de volumen en la luz
intestinal y viceversa. Estos aparatos son difíciles de operar con pequeños cambios de volumen,
siendo mejores los detectores eléctricos de presión.
c) Manómetros de mercurio.
Los cambios de presión arterial de animales grandes como el perro, gato, conejo pueden ser
registrados con un manómetro de mercurio que consta de un tubo en U, generalmente de 5 mm.
de diámetro interno, el que va adosado a una regla graduada en 0.1 cm.
Para los animales pequeños, el manómetro cuyo diámetro interno mide 2.5 mm es el más
conveniente. La presión puede leerse directamente, porque el cero es virtualmente constante;
las ventajas de estos equipos es su bajo precio, simplicidad de uso, lectura directa y amplio
rango; las desventajas son su gran inercia y el considerable volumen de sangre que pasa al
aparato con la posibilidad de formar coágulos en la cánula.
Empleando registradores eléctricos (transducers), se tienen los cambios de volumen mínimos, el
sistema tiene baja inercia, pero son más caros, de uso complicado y no dan una lectura directa;
siendo la amplitud total del registro de sólo 5 cm.
d) Registros electro-mecánicos.
A fin de graficar los cambios de longitud o tensión y los cambios de presión arterial, se usan los
registradores electro-mecánicos tipo “resistencia”. Estos dispositivos son cintas o espirales cuya
resistencia eléctrica se alteran cuando se tensan. El dispositivo es incorporado a uno de los
cuatro brazos de un puente de Wheatsjone en el que se descarga un voltaje. Cuando se aplica
una fuerza al dispositivo se produce un cambio en la resistencia y se establece una diferencia de
potencial a través del puente. Esta se magnifica por un amplificador DC.
16.estimuladores.
En gran número de experimentos, se necesita estimular eléctricamente la preparación. La forma
y duración del impulso es muy importante, particularmente cuando se trata de nervio y músculo
voluntario. Para ello son esenciales los estimuladores, que producen impulsos de ondas
rectangulares de corta duración.
Los electrodos para estimular nervios son los de platino forrados en plástico (perpspex) que
deberán limpiarse inmediatamente después del uso con un papel absorbente.
17.Material quirúrgico
La selección del material depende del criterio del operador, generalmente se usan los siguientes:
a) Tijeras grandes de punta fina y roma, de hoja recta y curva (18 cm. de largo). Se utilizan
en cirugía general. Útil para cortar la piel de animales medianos (gato, perro, conejo).
b) Tijeras medianas de hoja curva o recta (15 cm.) se utilizan para cortar suturas gruesas.
F-CV3-3B-2 Rev. Enero 2011
c) Tijeras medio-finas de hoja recta y/o medio curva, sirven para cortar vasos sanguíneos
(gato, perro, conejo) e hilos de sutura finos. Las más recomendables son las de punta
extrafina de 12 cm.
d) Tijeras finas, se utilizan para cortar vasos sanguíneos, tal como arteria carótida, arteria
femoral o arteria lingual. Algunas tienen las asas en ángulo con las hojas, esto permite que la
punta vaya hacía arriba, lo que es una ventaja cuando se corta tejido conectivo alrededor de
los vasos.
e) Pinzas gruesas son necesarios para el trabajo en general, especialmente las de pico de
flauta son las más convenientes; algunos encuentran mejor las de punta dentada, que asegura
firmemente la piel o una masa de tejido, pero puede producir desgarramiento.
f) Pinzas medianas curvas, convenientes para la disección o para pasar ligaduras sobre la
tráquea o grandes vasos sanguíneos.
g) Pinzas medianas curvas finamente dentadas son convenientes para asegurar pequeñas
porciones de tejido conectivo o muscular.
h) Pinzas medianas finamente dentadas utilizadas para disecar tráquea, pasar hilos
alrededor de los vasos sanguíneos de ala mayoría de animales.
Las de punta de flauta curvas son las más usadas.
i) Pinzas rectas medio finas se usan para disecciones delicadas (tipo oftalmología).
j) Pinzas grandes hemostáticas con punta recta o curva, se requieren para presionar
grandes vasos sanguíneos o masas de tejidos en gato o rata.
Tanto las pinzas grandes como medianas tienen un diente de seguridad.
k) Pinzas hemostáticas pequeñas con punta recta o curva, se utilizan para la oclusión
temporal de vasos (de 3 cm. son usadas para conejos y de 2 cm. para ratas).
l) Escalpelo grande para cortar piel.
m) Escalpelo medio para cortar pequeñas áreas de piel y para abrir la tráquea.
n) Agujas curvas son utilizadas para suturar piel y paquetes musculares (la Nº 3 para
animales pequeños).
o) Agujas de Raverdin útil para toda sutura en cirugía experimental.
Bioterio
Es el lugar donde se crían los “modelos biológicos” que se necesitarán para realizar las
experiencias farmacológicas, esto nos permitirá asegurar que los animales empleados presenten
perfectas condiciones de salud, que será muy importante para obtener resultados óptimos. Se crían
ratas, ratones, hamster y conejos cuya cantidad debe regularse de acuerdo a las necesidades.
El bioterio deberá estar situado en un lugar relativamente aislado, con ventilación, humedad y
temperatura adecuados, tendrá fácil acceso para la realización de la limpieza, y presentará
suministro continuo de agua potable. Se dispondrá de cilindros para almacenar los alimentos de los
animales.
La crianza de los “modelos biológicos” se realizará en ambientes diferentes para cada especie,
protegidos del ingreso de roedores e insectos.
Reproducción y cría
Requisito indispensable para la adecuada realización de bioensayos es la buena alimentación y el
alojamiento higiénico.
Los animales se alojaran en jaulas lo suficientemente espaciosas que faciliten:
Su ejercicio físico.
Su vigilancia constante.
El fácil acceso para su limpieza y alimentación .
F-CV3-3B-2 Rev. Enero 2011
Conejos
El mejor sistema para su crianza consiste en disponer a las hembras en jaulas especiales con un
pequeño compartimento en los que se le pone en el momento oportuno paja o viruta para que
construyan su nido.
Un semental basta para 10 ó 12 hembras.
El intervalo de los estros es de tres semanas.
La gestación dura 31 días.
Promedio de crías es de 5 a 6.
El mínimo de partos de 3 a 4 al año.
Los animales se encuentran maduros y en condiciones de procrear a los seis meses y se descarta
a los 3 años.
Ratas y Ratones
Las ratas usadas usualmente en investigaciones de tipo farmacológico pertenecen a la raza albina,
pero algunos investigadores utilizan ratas cruzadas.
El número de animales dedicados a la cría es fácil de calcular, teniendo en cuenta, que tanto las
ratas como los ratones:
Tienen un parto cada dos o tres meses.
Promedio de crías es de 8 a 10 para las ratas y cinco a siete para los ratones.
El número de especímenes que habrá de dedicar a la cría puede determinarse de la siguiente
forma:
Si se necesitan, por ejemplo, 600 ratas mensualmente, el cálculo ha realizar será el siguiente:
600 x 3 = 225
8
Habrá que tener, por tanto 225 madres con los machos en número de uno por cada tres hembras. En
consecuencia se necesitan 75 machos y en total 300 adultos.
En el caso de los ratones, el número de madres tendrá que ser mayor por el número de crías más
reducido en cada parto; tomando como termino medio cinco, el número de madres necesarias para
obtener 600 crías mensuales será de:
600 x 3 = 360
5
A éstas habrá que añadir los machos correspondientes en la misma proporción, que para las ratas,
es decir uno por cada tres hembras.
Para la cría se ponen un macho con tres hembras. Con el objeto de descubrir a las hembras
preñadas, se examinan una vez por semana el aumento del volumen del vientre; éstas se separan a
otra jaula, donde se les pone abundante viruta y trozos de algodón, para que puedan formar su
nido, la duración de preñez es de tres semanas y el número de crías es variable, dependiendo en
gran parte del cuidado, alimentación y temperatura a que estén sometidos.
En buenas condiciones pueden obtenerse hasta diez o doce crías por parto.
El peso de las ratas al nacer oscila entre 4 y 5 g. y los ratones entre 0.5 y 1 g.; debiendo
permanecer las crías con las madres hasta los 23 a 25 días después del parto, luego se separan de
ellas, colocándolas en otra jaula, en la que se anotará la fecha de nacimiento, el número de
hembras y machos. La madre se reintegra a la jaula de donde procedía.
Es muy conveniente anotar en las fichas , la fecha en que ha sido reintegrada a su jaula, pues de
esta forma, se puede determinar aproximadamente, la fecha del próximo parto.
Importante: durante el tiempo de permanencia de las crías con la madre, no se cambia la paja, por
lo menos en las primeras semanas, de esta forma ala madre las cuida mejor.
F-CV3-3B-2 Rev. Enero 2011
Sapo y Rana
Se mantienen en estanque de concreto abierto, con tapa de malla de alambre, con islotes de
piedras para que puedan reposar y con agua corriente.
Se les alimenta con hígado de res triturado, que se les da dos veces por semana, colocándoles en la
boca y haciéndoles deglutir.
Enfermedades más comunes, prevención
Hay que evitar en cuanto sea posible, la introducción en el criadero de agentes infectantes. Si las
jaulas no presentan las condiciones debidas, al menos ha de procurarse que estén libres de moscas,
ratones y ratas salvajes, que pueden ser los vehículos y los reservorios de las infecciones. Conviene
instruir a los encargados, para que detecten a los animales con los primeros signos de enfermedad,
para que avisen a la persona responsable del criadero y tomen las medidas oportunas de aislamiento
y cuarentena, debiendo ser cuidadas por personas distintas, que no tengan contacto con los no
enfermos o sospechosos.
Los siguientes signos deber ser considerados como sospechosos:
Alteraciones de la piel, enrojecimiento, alopecia, ulceraciones y erizamiento del pelo.
Falta de movilidad y apetito.
Pérdida de peso.
Presencia de exudados en ojo, boca y nariz.
Restos de heces fecales en la proximidad del ano.
Paresias o parálisis de las extremidades.
Presencia de parásitos, entre otros.
Cuando un animal enfermo no se puede curar, se le eliminará realizando la autopsia y la
investigación bacteriológica.
Enfermedades Infecciosas
Infecciones Agudas y Crónicas del Aparato Respiratorio
Pueden aparecer en todo tiempo en los animales de laboratorio, pero tienen menos prevalencia, en
general en los meses de verano. Las manifestaciones clínicas en muchas de estas enfermedades no
son claras, al contrario son de incierta significación diagnóstica.
El Estreptococo hemolítico produce con frecuencia, neumonías letales en el cobayo, en la misma
enfermedad puede encontrarse con frecuencia, en cultivo puro, la “Br. bronchiséptica”
especialmente en los meses de invierno y primavera. Durante varios días los animales presentan
secreción nasal, lomo arqueado, enrojecimiento de la piel y respiración agitada.
En la autopsia se encuentra hepatización del lóbulo medio del pulmón o de los borde inferiores de
los otros lóbulos.
El Catarro Nasal de los Conejos
Producido por la “Pasteurella plepiséptica” solo o asociada a la “Br. bronchiséptica”, es más
frecuente en los meses de invierno. Los primeros síntomas que presentan son: estornudos, secreción
nasal, secreción mucopurulenta, seguidos de la inmovilidad del animal, emaciación y debilidad; la
enfermedad puede evolucionar rápidamente hacía una neumonía, pericarditis, pleuresía y con
relativa frecuencia otitis media y abscesos cutáneos producidos por la “P. plepiséptica”.
Se han encontrado casos aislados de neumonía en conejos y cobayos producidas por el neumococo
del tipo XIX.
Una alimentación adecuada, evitar los cambios bruscos de temperatura y las oportunas medidas de
aislamiento pueden llegar a controlar las infecciones.
El conejo puede sufrir de abscesos subcutáneos que pueden ser limitados a diversas áreas del
cuerpo (las mamas de las hembras que lactan) o múltiples y diseminados. En todos los casos es
esencial el aislamiento de los enfermos para evitar las epizootias.
Los cobayos y los ratones son afectados con frecuencia de graves epizootias causadas por
microorganismos, tales como del cuerpo paralíticoenteriditis, constituyendo el tifus de los ratones y
la enfermedad denominada seudotuberculosis de los cobayos; designación que debe quedar
reservada a la infección producida en estos animales por el B pseudotuberculosis.
F-CV3-3B-2 Rev. Enero 2011
Los síntomas en el cobayo son: enrojecimiento de la piel, pérdida del apetito y postración; el curso
de la enfermedad puede ser tan rápido, que los animales mueren antes de presentar algún síntoma.
En el ratón el enrojecimiento de la piel es más visible y sufre diarrea; en la autopsia, los hallazgos
varían, pero con bastante frecuencia se encuentra hipertrofia del bazo de variable intensidad, y en
los casos de larga duración se aprecian abscesos múltiples en este órgano y más raramente en el
hígado.
A veces algunos animales se curan y se hacen portadores; los tipos de bacterias causantes de esta
enfermedad caen generalmente en dos grupos distintos: Salmonella enteriditis, aislada con
frecuencia en cobayos y ratones, y tiphimurium, que producen las más graves epizootias. La
aparición repentina de esta infección se debe a que las jaulas o cajas han estado saltadas de
colonias de microorganismos durante años en estado latente.
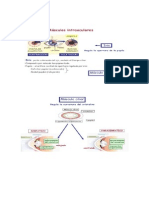
PRINCIPIOS Y MÉTODOS GENERALES DE EXPERIMENTACIÓN
Existen por lo menos tres tipos de experimentación farmacológica:
“In vivo”
Son las experiencias de farmacológicas realizadas en los organismos intactos, en ella el efecto
farmacológico es la consecuencia de la acción del fármaco en muchos sitios del organismo de
manera simultánea. La acción del fármaco, en estos casos esta influenciada por una serie de
factores entre ellos, vías de administración, absorción, distribución, biotransformación y
excreción, por lo que la acción farmacológica será casi inmediatamente o después de un periodo
prolongado.
Este tipo de experiencias tienen la ventaja de indicar los efectos farmacológicos de una sustancia,
pero es difícil predecir su modo de acción.
“In vitro”
En este tipo de experimentación se debe realizar una preparación aislada de un órgano específico,
como estómago, útero, corazón. El efecto farmacológico observado es consecuencia de la acción
directa de la droga administrada en una concentración conocida y en un tiempo determinado sobre
un segmento de tejido.
“In situ”
Es un tipo de experimentación alternativo a la preparación intacta o aislada, ya que el órgano no es
separado del cuerpo del animal, si no es identificado y liberado de sus aponeurosis. Luego en el
lugar donde se encuentran se hacen las conexiones necesarias para administrar y registrar los
efectos de las fármacos en ensayo.
Sistema de Órganos Aislados o Baño de Magnus
Es un conjunto de materiales, equipos y reactivos para mantener en condiciones vitales un órgano o
un segmento de éste, donde es necesario proporcionar todos los elementos indispensables para su
mantenimiento y estabilidad, tales como:
Electrolitos esenciales para la vida, proporcionados por el líquido nutricio. Su composición es
específica según el origen y tipo de órgano a aislar.
Material Energético (glucosa) necesario para que el trabajo del tejido sea por largo tiempo. Se
adiciona al líquido nutricio, al momento de su uso, de otro modo constituiría un excelente medio
de cultivo de microorganismos.
pH, que esta determinado por el fosfato y bicarbonato.
Temperatura adecuada, es uno de los factores a tener en cuenta para estos trabajos, se debe
considerar según el tejido. Así por ejemplo en el caso de los anfibios, se puede usar una
temperatura baja o ambiental, ya que estos pueden sobrevivir por largos periodos a esta
temperatura. En cambio los tejidos de mamíferos necesitan una temperatura de 37°C +/- 1° C,
sin embargo pueden durar más tiempo a menor temperatura (30°C), pero su sensibilidad a los
fármacos es alterada por cambios mínimos (rango de 1°C)., por lo cual es indispensable trabajar
con temperatura constante, que suele ser mantenida por un termostato.
Es necesario tener ciertas precauciones al añadir la solución de la droga, tal como, no añadirla
fría, ni directamente sobre el órgano o tejido, además el volumen debe estar de acuerdo con la
F-CV3-3B-2 Rev. Enero 2011
capacidad de la cámara que contiene el órgano. Se recomienda que el solvente debe ser el suero
nutricio con que se trabaja.
Disección
Consiste en separar y dejar libre de su aponeurosis a los diferentes órganos para su estudio. Es un
buen principio evitar la exposición innecesaria del tejido profundo, lo que deterioraría la
preparación.
Se realiza el siguiente procedimiento:
Afeitar el área escogida.
Cortar longitudinalmente la piel con un escalpelo o se extrae una porción longitudinal de piel
con tejido subyacentes, cauterizando los vasos sangrantes o bloqueándolos con pinzas
hemostáticas, para luego ser ligadas con hilos. Puede utilizarse la diatermia quirúrgica para
cortar la piel en lugar del escalpelo o las tijeras, esto produce menor hemorragia, siendo
necesaria esta técnica cuando se han utilizado altas dosis de anticoagulantes.
Se debe tratar de separar los tejidos siguiendo las líneas de unión, utilizando las tijeras punta
roma, pinzas o sondas. Una vez separado el plano muscular se procede a la liberación de las
aponeurosis que envuelven los diferentes órganos, para ello se utilizan pinzas romas y se corta
con tijeras finas, dejando así al descubierto, el órgano elegido para la experiencia.
Canulación
Consiste en la inserción de tubos especiales, llamados cánulas o sondasen determinados órganos,
tales como la tráquea, los vasos sanguíneos , entre otros.
Para la inserción en la tráquea se prefieren las cánulas de vidrio, por su transparencia y porque son
fáciles de limpiar.
Para arterias y venas se usan cánulas más finas, siendo el plástico el material más conveniente; en
este caso para evitar la formación de coágulos es importante llenarlos con solución salina fisiológica
conteniendo heparina 50 U/ml.
1.2. COMPETENCIAS
Manipula, marca y pesa correctamente animales de experimentación.
Prepara correctamente las concentraciones de las soluciones de trabajo; y determina
correctamente los volúmenes de administración de fármacos.
1.3. MATERIALES Y EQUIPOS
Jeringas descartables 1 cc 12 unid
Ratas 04 unid
Ratones 06 unid
Balanza mecánica 02 unid
Guantes gruesos 01 par
Beaker 100 ml 04 unid
Pipetas 1 ml 04 unid
Pipetas 10 ml 03 unid
Fenobarbital sódico 10 % 30 ml
Sodio cloruro 0.9 % 150 ml
1.4. PROCEDIMIENTO
MANIPULACIÓN DE LOS MODELOS EXPERIMENTALES
Por razones científicas y éticas, es muy importante que los animales de laboratorio, sean
manipulados con mucho cuidado y siempre con actitud amable, nunca maltratarlos, porque de ello
dependerá obtener resultados de calidad.
La incógnita del reactivo biológico ofrece para nosotros el mayor interés y nuestra constante
preocupación debe ir orientada siempre a evitar en lo posible su variabilidad.
En un mismo ensayo conviene emplear animales de una sola raza, y a veces se utiliza una
determinada, según el tipo de experiencia.
F-CV3-3B-2 Rev. Enero 2011
El tipo de sexo también es factor decisivo en los resultados. En ciertas ocasiones es preciso utilizar
animales de un mismo sexo, tal es el caso, cuando se estudia la valoración de ciertas hormonas; en
cambio en otro tipo de experiencias se pueden emplear animales de ambos sexos.
Como la mayor parte de las experiencias se lleva a cabo con animales vivos, se recomienda realizar
cualquier intervención quirúrgica o maniobra dolorosa, bajo anestesia general o local, para evitarles
sufrimientos innecesarios. Si la naturaleza del estudio exige que el animal siga viviendo, se tendrá
que adaptar la técnica más indicada, de lo contrario se le dará muerte piadosa al término de la
observación.
El tratamiento post-operatorio debe reducir al mínimo las molestias de esta etapa, se les mantendrá
en condiciones confortables para su bienestar, empleando las mejores prácticas médicas y
quirúrgicas que se aplican en las clínicas para animales.
Batracios
Pese a lo pequeño de su tamaño y a sus diferencias anatómicas, sirven en muchos casos para
demostrar efectos farmacológicos que son posibles en los mamíferos y aún en el hombre.
Para los batracios existen mesas de fijación especial que favorecen su manipulación y que constan
de una plataforma de corcho puesta sobre madera, presentando perforaciones en serie, que
faciliten la adaptación de abrazaderas.
Ratón
Animal de suma utilidad para determinar la dosis y toxicidad de una droga, cuyo manejo es
relativamente fácil con un poco de práctica.
Para la administración de fármacos se le sujeta de la cola con la mano derecha, permitiéndole
sujetarse con sus miembros anteriores a una malla de alambre, con la yema de los dedos pulgar e
índice de la mano izquierda tomarlo del cuello, sujetando luego la cola con el dedo meñique de la
misma mano, quedando de esta manera la mano derecha libre para la inyección. En el caso que esta
fuera intravenosa, se emplea un tubo de vidrio, uno de cuyos extremos se encuentra cerrado con un
tapón por donde se retiene la cola.
Rata
Siempre que sea posible deberán ser manipuladas dentro de sus respectivas cajas, así como los
ratones, las ratas pueden ser cogidas por la cola, siguiendo igual procedimiento al anterior y de esta
forma estarán seguras y aptas para inyectarlas. No deberán ser tratadas rudamente, ya que se
vuelven ariscas y muy difíciles de manipular.
Para las intervenciones quirúrgicas de estos animales Levine y Kugel recomiendan una pequeña
mesa de operaciones por la que circula agua caliente.
Se las prefiere en experiencias sobre el aparato digestivo, no siendo adecuado para estudiar las
alteraciones del ritmo cardiaco por el excesivo número de latidos.
Marcación de ratas y ratones
En algunos ensayos biológicos en que se emplean elevado número de ratas o ratones, es necesario
identificarlos. Si el ensayo se lleva a cabo en no más de tres días y el número de animales es
relativamente pequeño, la marcación se hace por medio de colorantes: rojo, anaranjado, amarillo,
verde, azul y violeta (colores del espectro), solubles en acetona.
La identificación es numérica, de acuerdo con el color y el lugar del animal en que se practica la
tinción, en la forma siguiente:
Rojo : 1-10 Verde : 31-40
Anaranjado : 11-20 Azul : 41-50
Amarillo : 21-30
En cada serie realizar la marcación en el orden es el siguiente:
Ratón Nº 1: Cabeza. Ratón Nº 6: Las dos patas delanteras.
F-CV3-3B-2 Rev. Enero 2011
Ratón Nº 2: Pata delantera derecha. Ratón Nº 7: Las dos patas traseras.
Ratón Nº 3: Pata delantera izquierda. Ratón Nº 8: El lomo.
Ratón Nº 4: Pata trasera derecha. Ratón Nº 9: El costado derecho.
Ratón Nº 5: Pata trasera izquierda. Ratón Nº 10: El costado izquierdo.
Cobayo
El conejillo de indias es un animal muy dócil, y permite una fácil manipulación.
Son extremadamente sensibles a la infección, de allí, que deberá trabajarse con material estéril en
las intervenciones quirúrgicas. El intestino de cobayo es muy usado en los experimentos de órganos
aislados.
Conejo
Es fácil de adquirir, por ello es bastante empleado para algunas experiencias de farmacología. Para
sujetarlo se emplean cajas de sujeción de 49 x 35 x 20 cm. provistos de una cubierta corrediza, que
en el extremo tiene un corte semicircular, que se corresponde con otro corte igual en el borde de
la caja, adaptado a la dimensión ordinaria del cuello.
Para transportarlos, se les lleva de la piel del cuello, no deben ser levantados de ninguna manera de
las orejas, teniendo en cuenta que normalmente no emiten sonidos, salvo dolor extremo. Para
identificarlos se hace un tatuado numérico con tinta china en la cara ventral de la caja.
Gato
Para sujetarlos se necesitan dos personas, una que sostenga firmemente la piel del cuello y las
patas delanteras y la otra las patas posteriores. Se recomienda utilizar un paño para envolver las
extremidades y evitar rasguños.
Se caracteriza por tener un sistema nervioso y circulatorio semejante al humano, además tiene un
ojo altamente sensible a los fármacos simpáticos y responde fácilmente a los fármacos eméticos.
Perro
Para inmovilizarlo se utiliza la mesa de sujeción de Bernard, en la que se fija sobre el dorso, el
vientre, para facilitar las intervenciones quirúrgicas. El perro se debe manejar siempre atado del
cuello, con un bozal para evitar su acometida.
Gracias a su ritmo pausado de su sistema respiratorio es recomendado para el estudio de las
alteraciones respiratorias provocadas por los fármacos, igualmente de la fatiga y los cambios
metabólicos. Debido a la facilidad de adquirirlo, es que son frecuentes los trabajos sobre el sistema
cardiovascular.
ELIMINACIÓN DEL MODELO BIOLÓGICO
Muchas veces concluidos los experimentos son necesarios eliminar los animales, por lo general este
procedimiento se realiza mediante la administración endovenosa de aire o cloroformo.
En casos de gatos y conejos se acostumbra a administrar solución concentrada de barbitúrico (200
mg/ml de pentobarbital sódico). Pequeñas dosis del mismo (0.2 ml.) son requeridas para las ratas;
también se puede emplear uretano (7 g/kg).
Los ratones se exterminan rápidamente al encerrarlos en campanas saturadas de cloroformo.
PREPARACIÓN DE LOS FÁRMACOS PARA ENSAYO
La cantidad de droga necesaria para un experimento es por lo general pequeña, menor de 10 mg.;
aún si la muestra se ha pesado cuidadosamente, el error tiende a ser del 1%, por ello es preferible
pesar una mayor cantidad tal como 100 mg para tener una solución concentrada y luego diluirla
según requerimiento. Las soluciones deben ser preparadas pesando y completando el volumen
requerido. Las soluciones empleadas en farmacología son muy diluidas y conviene prepararlos en
varios pasos:
Primero se prepara una solución stock en agua estéril desionizada, y luego la solución de trabajo se
realiza diluyendo con suero fisiológico empleado en el baño para órganos aislados, a menos que el
volumen a añadir sea muy pequeño.
F-CV3-3B-2 Rev. Enero 2011
Determinación de la concentración de las soluciones de trabajo
Para conocer la concentración a la que deben prepararse las soluciones de trabajo deben
considerarse los siguientes parámetros:
Tipo de modelo experimental.
Vía de administración.
Volumen máximo recomendado por dicha vía de administración.
Volumen máximo para la administración de fármacos
ANIMAL VIA I.V. VIA I.P. VIA S.C. VIA I.M. VIA ORAL
Aguja Vol. Aguja Vol. Aguja Vol. Aguja Vol. Aguja Vol.
N° Máx. N° Máx. N° Máx. N° Máx. esp.N° Máx.
RATON 27 0.4 ml 25 0.5 ml 25 0.4 ml 25 0.4 ml 18 1.0 ml
RATA 27 0.5 ml 25 2.0 ml 25 0.5 ml 25 0.5 ml
GATO 25 21 5.0 ml 25 2.0 ml 25 2.0 ml
CONEJO 25 1.0 ml 21 5.0 ml 25 2.0 ml 25 2.0 ml
COBAYO 25 25 2.0 ml 25 1.0 ml 25 0.5 ml
Almacenamiento de los Fármacos
Algunos fármacos se conservan bien en solución, manteniéndolas en frascos tapados y refrigerados
para evitar la proliferación de microorganismos. Otras se descomponen rápidamente, así una
solución diluida de acetilcolina a pH 7, pierde totalmente su actividad en 1-2 h.; Las soluciones
diluidas de adrenalina, noradrenalina e isoprenalina pueden oxidarse y cambiar de color, por tanto
estas deben ser preparadas en el momento de usarse por dilución de la solución stock y a pH 4.
Preparación de las soluciones salinas fisiológicas
Deben prepararse a partir de sales químicamente puras, grado reactivo y agua destilada o
desionizada. En lugar de preparar las soluciones cada vez que se realice un ensayo, es mejor
preparar una solución stock concentrada y diluirla convenientemente el día que se va a realizar la
experiencia. Los errores de preparación no deben exceder jamás el 1%. Las soluciones fisiológicas
se mantienen bien hasta las 24 h., ya que son excelentes medios de cultivo de microorganismos,
debiendo guardarse en refrigeración.
Ejemplo:
Preparar una solución de trabajo de pentobarbital sódico para administrar vía intramuscular
(volumen máximo= 1 mL) una dosis de 50 mg/kg de peso a 100 ratones que pesan entre 40 y 50
g, a partir de una solución concentrada al 5%.
Si vamos a preparar una solución de trabajo para experiencias en farmacología es por dos motivos:
Porque los fármacos son muy potentes y por ello debemos administrar soluciones diluidas.
Porque con las jeringas que nos provee el mercado seria casi imposible medir milésimas de
mililitro.
Cuando preparamos soluciones diluidas o soluciones de trabajo a partir de soluciones concentradas,
inmediatamente debemos pensar en aplicar la siguiente fórmula:
C1 x V1 = C2 x V2
Donde C1 es la concentración de la solución concentrada y V1 es el volumen a medir de la solución
concentrada, para preparar un V2 que es el volumen de la solución de trabajo y C2 será su
concentración.
Datos:
Dosis = 50 mg/kg de peso.
Nº de ratones = 100
Peso de ratones= entre 40 y 50 g
Vía de administración= intramuscular (volumen máximo= 1 mL)
C1 = 5%
V1 = incógnita
F-CV3-3B-2 Rev. Enero 2011
C2 = incógnita
V2 = Nº de ratones x volumen máximo
Los pasos a seguir para preparar la solución son:
Paso 1: Calcular la cantidad de fármaco (necesitamos la dosis y peso del ratón)
50 mg ---------- 1kg peso ratón
X ---------- 50 g de peso ratón
Calculando obtenemos: X = 2.5 mg
Hemos considerado el peso mayor de ratón para que la solución a preparar nos pueda ser útil para
todos los ratones cuyo peso es menor de 50 g.
Paso 2: Determinar la concentración de la solución (necesitamos cantidad de fármaco y el
volumen en el que estará contenido esa cantidad, como referencia tenemos el volumen máximo = 1
mL, pero nunca debemos trabajar con los valores extremos, ni máximo, ni mínimo.
Entonces, se sugiere considerar el término medio, es decir 0.5 mL)
2.5 mg ---------- 0.5 mL, esto quiere decir que la solución tendrá una concentración de 2.5 mg por
cada 0.5 mL, pero nosotros debemos llevarlo a una concentración porcentual es decir g/ 100
mL.
Luego decimos, si:
2.5 mg ---------- 0.5 mL
X ---------- 100 mL X= 500 mg/100 mL = 0.5 %
Por tanto la C2 = 0.5%
Paso 3: Determinar el volumen a medir de la concentrada para preparar la solución de trabajo:
Utilizaremos la fórmula señalada antes: C1 x V1 = C2 x V2
Reemplazamos los datos :
5% x V1 = 0.5% x (Vol. Máx. x Nº ratones)
5% x V1 = 0.5% x 100 mL
V1 = 10 mL
Paso 4: Preparación de la solución de trabajo
Medir 10 mL de la solución concentrada de pentobarbital sódico y colocarla en una fiola de 100 mL,
luego aforar o enrasar con agua destilada capacidad suficiente para 100 mL.
CALCULO DEL VOLUMEN PARA ADMINISTRACION
Las dosis* que se emplearán en el desarrollo de las prácticas, ya se encuentran determinadas,
por lo que en este apéndice desarrollaremos las pautas que debe seguir el
estudiante a fin de realizar correctamente el cálculo del volumen a administrar al
modelo experimental.
Se presentan los siguientes datos:
Dosis en mg/kg de peso.
Peso en gramos del modelo animal.
Concentración del fármaco a ensayar o “solución de trabajo” (generalmente se encuentra en
porcentaje, es decir gramos/100 mL de solución)
F-CV3-3B-2 Rev. Enero 2011
Pasos a seguir:
1. Calcular la cantidad de fármaco en miligramos para la administración (está en
relación a la dosis señalada y al peso del modelo animal).
2. Calcular el volumen del fármaco en mililitros, que contiene la cantidad de fármaco
calculado anteriormente. Para obtener este dato, realizamos una simple regla de tres simple
(convirtiendo previamente los gramos de la concentración a miligramos o los miligramos de
fármaco a administrar en gramos, para uniformizar las unidades).
Caso Práctico
Determinar el volumen necesario, para administrar por vía intraperitoneal (i.p.), una dosis de 35
mg/kg de pentobarbital sódico 3.5%, a una rata de 200 g de peso.
1. Cálculo de la cantidad de fármaco (pentobarbital sódico):
35 mg ............ kg (1000 g) X= (200) (35) / 1000
X mg .……… 200 g
X = 7 mg
2. Cálculo del volumen del pentobarbital sódico 3.5%:
3.5 g (3 500 mg) ....... 100 mL X = (7) (100) / 3 500
7 mg …… X mL
X = 0.2 mL
*El cálculo de la dosis se realiza mediante la medición o cuantificación del efecto farmacológico o
respuesta biológica, consecutiva a la interacción fármaco-receptor. Las respuestas son por lo
general graduales, es decir, existe una relación sistemática y continua entre la dosis aplicada y la
magnitud o intensidad del efecto que dicha dosis produce.
Las dosis medias se obtienen a partir de las denominadas Curvas dosis-respuestas. Este tipo de
curvas, además son de importancia para determinar el índice terapéutico o seguridad de un fármaco
a partir de la DE50, DL50 , DE20, DL20
1.5. RESULTADOS
Los alumnos presentarán en clase los resultados de los problemas planteados por el
profesor.
1.6. CUESTIONARIO
a) Fundamente ¿porqué es muy importante que los animales de laboratorio, sean manipulados
con mucho cuidado y siempre con actitud amable, y nunca se les deba maltratar?
b) ¿Cuáles serían las opciones recomendables para eliminar a u modelo biológico, después de
una experiencia en farmacología?
c) Señale tres ejemplos de cada tipo de experimentación en farmacología:
d) Prepare soluciones de trabajo a partir de una solución concentrada de pentobarbital sódico
al 10%, para administrar a:
50 Ratones cuyo peso oscila entre 30 y 40 g.
50 Ratas cuyo peso oscila entre 250 y 300 g.
Tenga en consideración que la dosis a emplear, tanto en ratones, como en ratas es 30
mg/kg, y se administrará por vía intraperitoneal (volumen máximo= 1 mL)
e) De la solución anteriormente preparada, determine los volúmenes para administrar 25
mg/kg por vía s.c. a 10 ratones que pesan 21, 22, 25, 27, 28, 31, 34, 38, 39 y 40 g
F-CV3-3B-2 Rev. Enero 2011
1.7. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 02 (SEMANA 02)
LINEAMIENTOS DE INVESTIGACIÓN CIENTÍFICA
2.1. LINEAMIENTOS DE INVESTIGACIÓN CIENTÍFICA
2.1.1. MARCO TEÓRICO
La investigación científica no debe ser considerada como una actividad exclusiva de algunas
personas que trabajan en sofisticados laboratorios, utilizando instrumentos muy
complicados. Se puede investigar también en una comunidad carente de recursos básicos,
utilizando una entrevista muy simple como instrumento. Lo importante es investigar
siguiendo un método, es decir un procedimiento para tratar el problema. Un problema
particular requiere un conjunto de métodos o técnicas especiales.
El método científico es la estrategia de la investigación científica: afecta a todo el ciclo completo
de a investigación y es independiente del tema de estudio.
Una investigación se hace científica sólo en la medida en que los procedimientos que utiliza se
conforman a ciertos modelos lógicos que aseguran la validez de las conclusiones.
La investigación ya sea pura, básica o aplicada es una necesidad fundamental del hombre.
Precisamente los pueblos que investigan, tienen poderío y jerarquía y son cultos.
INVESTIGACIÓN CIENTÍFICA
Es la búsqueda sistematizada y objetiva de hechos o explicaciones de fenómenos. En pocas
palabras, es la búsquedas de nuevos conocimientos.
Etapas de la investigación
La investiación debe desarrollarse sistemáticamente y comprende las siguientes etapas:
planificación, ejecución y evaluación.
a) Planificación: en esta etapa se considera la totalidad de la investigación, tanto lo
precedente a la obtención de la información, como las etapas posteriores a ésta;
proponiéndose por escrito en un documento llamado protocolo o proyecto de investigación,
el desarrollo de todas las actividades planificadas.
b) Ejecución: debe realizarse todo lo planificado en la etapa anterior.
c) Evaluación: es la etapa, en la que debe establecerse en que medida se lograron los
objetivos propuestos
TIPOS DE INVESTIGACIÓN
El tipo de investigación se elige en función de los objetivos que se pretende alcanzar, de los
recursos disponibles y del tipo específico de problema que se quiere tratar.
Existen diversos criterios para agrupar a los tipos de investigación:
a) De acuerdo con el periodo en que se capta la información:
Retrospectivo - Prospectivo
Retrospectivo: utiliza la información captada anteriormente a su planeación con fines ajenos al
trabajo de investigación que se pretende realizar.
Prospectivo: utilizará la información que se recogerá, de acuerdo con los criterios del
investigador y para los fines específicos de la investigación a realizar.
b) De acuerdo a la evolución del fenómeno:
Longitudinal - Transversal
F-CV3-3B-2 Rev. Enero 2011
Longitudinal: en este tipo de estudio se mide en dos o más ocasiones las variables involucradas.
Implica el seguimiento, para estudiar la evolución de las unidades en el tiempo.
Transversal: estudio en el cual se mide una sola vez la o las variables y de inmediato se procede
a su descripción o análisis.
c) De acuerdo a la comparación de las poblaciones:
Descriptivo - Comparativo
Descriptivo: el estudio sólo cuenta con una población, la cual se pretende describir en función
de un grupo de variables y respecto de la cual no existen hipótesis centrales.
Comparativo: en el estudio existen dos o más poblaciones y donde se quiere comparar algunas
variables para contrastar una o varias hipótesis centrales. Un estudio de este tipo, puede tener
como antecedente a uno o varios estudios descriptivos.
En la investigación comparativa se destacan las consecuencias derivadas de la contrastación de
la o las hipótesis centrales. Adicionalmente, los objetivos de la investigación pueden referirse a
la determinación de diferencias significativas entre conjuntos de datos y se encuentran
resultados de contrastes de análisis estadístico aplicados a la información. En las investigaciones
de este tipo se busca establecer el tipo de relaciones entre los elementos de un fenómeno.
Los estudios comparativos, de acuerdo a como se abordan el fenómeno, se dividen en:
- Prospectivos de causa a efecto (estudios de cohortes o prospectivos concurrentes): se
relacionan dos o más grupos de sujetos que se diferencian en cuanto al grado de exposición al
factor causal (por ejemplo, expuestos y no expuestos a mucho, regular o nada), luego se
efectúa el seguimiento de estos grupos para conocer, evaluar y analizar la aparición del efecto,
así como la frecuencia con que éste se presenta dentro de cada grupo.
- Retrospectivos de causa a efecto (estudios no concurrentes): en estos estudios los
expuestos y los no expuestos son seleccionados de los archivos y se observa el efecto en
cada grupo. Se usa mayormente en estudios de contaminación ambiental.
- De efecto a causa (estudios retrospectivos o de casos y controles): se seleccionan grupos de
sujetos que tienen el efecto (pueden ser en varias modalidades) y los que no tienen y se
investiga el grado de exposición a factor causal en el pasado.
MEDIDAS DE ASOCIACIÓN
En los estudios epidemiológicos orientados a la búsqueda de factores etiológicos, se deben
establecer mediciones que expresen el grado o la fuerza de asociación entre los factores de
riesgo y la enfermedad en cuestión.
Se tienen dos tipos básicos de mediciones para medir la fuerza de asociación:
- Riesgo relativo (RR).
- Odds Ratio (OR).
La forma de obtener estos valores depende del tipo de estudio que se tenga:
- Comparativo, prospectivo, de causa a efecto: Cohortes.
- Comparativo, retrospectivo, de efecto a causa: Casos y Controles.
DETERMINACIÓN DEL RR:
ENFERMEDAD
FACTOR DE PRESENCIA AUSENCIA TOTAL
EXPOSICIÓN (+) (-)
PRESENTE A B A+B
AUSENTE C D C+D
TOTAL A+C B+D A+B+C+D
Donde:
A + B: Cantidad de personas con el factor presente.
A + C: Cantidad de personas que presentaron la enfermedad en el periodo
especificado.
F-CV3-3B-2 Rev. Enero 2011
Para cuantificar la fuerza de asociación entre el factor y la enfermedad, utilizamos la razón de
riesgos de hacer la enfermedad para aquellos que poseen o no el factor. Se tiene:
A / A+B : es el riesgo de hacer la enfermedad en aquellos que tienen el factor.
C / C+D: es el riesgo de hacer la enfermedad en aquellos que no tienen el
factor.
Entonces, la razón de riesgos será:
Razón de riesgo = A / A+B
C / C+D
Esta razón de riesgos, muchos investigadores le denominan RIESGO RELATIVO (RR).
DETERMINACIÓN DEL OR
ENFERMEDAD
FACTOR DE PRESENCIA AUSENCIA TOTAL
EXPOSICIÓN (+) (-)
PRESENTE A B A+B
AUSENTE C D C+D
TOTAL A+C B+D A+B+C+D
El OR es la razón de A / B a C / D, y estas cantidades son consideradas como las ODDS a favor de
los que tienen la enfermedad.
El ODDS es una medida de riesgo de experimentar la enfermedad en estudio cuando el factor está
presente.
OR = A/B = AxD
C/D BxC
d) De acuerdo a la interferencia del investigador:
De observación - Experimental
De observación: cuando el investigador, solo describe lo que sucede con la variable de una sola
población, no manipula dicha variable.
Experimental: Si el investigador manipula la variable en dos o más poblaciones.
2.1.2. COMPETENCIAS
Diseña y ejecuta protocolos para realizar investigación en farmacología clínica.
2.1.3. MATERIALES Y EQUIPOS
Proyector multimedia
Ficha de modelo de proyecto de investigación
2.1.4. PROCEDIMIENTO
Diseñar un protocolo de investigación de acuerdo al modelo siguiente:
F-CV3-3B-2 Rev. Enero 2011
PROTOCOLO DE INVESTIGACIÓN
Se denomina de esta manera al documento que contiene todo el procedimiento a seguirse para
efectuar el trabajo de investigación, es decir es un plan prospectivo de un proceso sistemático,
ordenado y coherente que busca verificar una hipótesis y/o alcanzar un objetivo.
Partes de un protocolo de investigación
Depende fundamentalmente del tipo de estudio que se planea realizar.
A) Definición del problema
Título
Antecedentes
Objetivos
Hipótesis
B) Tipo de estudio
C) Definición de la(s) población (es) de estudio
Características generales
Ubicación espacio – temporal
D) Diseño estadístico del muestreo
E) Descripción de las variables y escalas de medición
F) Proceso de captación de la información
G) Procesamiento, análisis estadístico e interpretación de la información
H) Recursos necesarios
I) Cronograma de actividades
J) Ética de la investigación
K) Referencias bibliográficas
DEFINICIÓN DEL PROBLEMA
Todo trabajo de investigación comienza con la percepción de un problema; es decir al observar un
estado de insatisfacción entre personas o grupos, o encontrar alguna laguna en el saber o
incoherencia en el saber.
El problema quedará definido, si consideramos los siguientes puntos:
Título
Un título debe ser un enunciado informativo y conciso, debe indicar el objetivo del estudio, puede
incluir lugar y tiempo en el que se efectuará el estudio. No se debe utilizar expresiones
como “un estudio o una investigación sobre .....”.
Antecedentes
Viene a ser el marco de referencia del trabajo. Debe incluir una buena revisión bibliográfica
actualizada, debe contener en lo posible, resultados o hallazgos de estudios pre-liminares a
nivel local, nacional o internacional.
De los antecedentes debe desprenderse lógicamente los objetivos y justificación del estudio.
Cuando se refiere a justificación se acostumbra a enunciar tres rubros:
a) La significación de un estudio: es significante, si el estudio reúne criterios de importancia y
pertinencia.
F-CV3-3B-2 Rev. Enero 2011
b) Trascendencia: si los resultados peden extenderse a otras áreas de interés, grupos sociales o
a efectos económicos.
c) Viabilidad: se refiere no sólo a la factibilidad, que es la capacidad técnica para realizar el
proyecto, sino fundamentalmente a la aceptación social que permita la subsistencia del
proyecto.
Objetivos
El objetivo de una investigación es un enunciado de un logro observable y evaluable al cabo de
dicha actividad. Los objetivos constituyen la meta hacia el cual está orientada la
investigación. Si es posible hay que jerarquizar los objetivos de acuerdo a su importancia.
Hipótesis
Es un supuesto, una proposición, una explicación probable que trata de explicar ciertos hechos; y
como tal debe ser contrastada.
Para poder contrastar o verificar una hipótesis es necesario estar en las posibilidades de medir las
variables.
Es conveniente distinguir dos clases de hipótesis: una científica y otra estadística.
Una hipótesis científica es una sugerencia de solución a un problema; la hipótesis estadística, es
solamente un enunciado respecto a un parámetro poblacional desconocido.
DEFINICIÓN DE LA POBLACIÓN EN ESTUDIO
Para ello es indispensable definir las características generales y la ubicación temporal y espacial de
la o las poblaciones.
Características generales
a) Criterios de inclusión: se refiere a las características que hacen que una unidad (individuo,
familia u otro) sea parte de la población.
b) Criterios de exclusión: señala a las características cuya presencia hace que una unidad no
sea parte de la población de estudio; por ejemplo, la existencia de una característica, una
enfermedad o un tratamiento que pueda modificar los resultados del estudio.
Ubicación en el tiempo y espacio
DISEÑO ESTADÍSTICO DEL MUESTREO
Sólo se realizará cuando la población antes definida es muy numerosa, y por lo tanto será necesario
seleccionar una muestra.
Unidad de análisis
Es la unidad para la que deseamos obtener la información estadística. En ciertos estudios existen
dos o más unidades de análisis; ejemplo: madre e hijo menor de 5 años.
Unidad de muestreo
Es una unidad del marco de muestreo. En algunos estudios es igual a la unidad de análisis. Por
ejemplo si se quiere estudiar en una comunidad desnutrición de niños menores de 5 años, y sólo se
dispone de un plano dividido en manzanas y viviendas (lotes) y se va a muestrear estas para llegar a
los niños menores de 5 años, la unidad de muestreo es una vivienda y la unidad de análisis es el niño
menor de 5 años.
Marco de muestreo
Es la relación completa de las unidades de muestreo. Ejemplo: Una lista de nombres, un plano, un
archivo clínico. En algunos estudios no se dispone de marco muestral, en tales casos se procederá a
su confección.
Tamaño de muestra
Para calcular el tamaño de una muestra se requiere habitualmente: una medida del grado de
variabilidad de los elementos poblacionales (desviación estándar), magnitud de los posible errores y
sus probabilidades de ocurrencia, tamaño de la población, entre otros.
Se pueden utilizar las siguientes fórmulas:
F-CV3-3B-2 Rev. Enero 2011
Para estudios con una población
1) n = Z2αSe2 / E2
2) n = Z2α pe qe / E2
Para estudios con dos poblaciones:
3) n = (Zα + Zβ)2 2(Se)2 / (x1 – x2)2
4) n = (Zα + Zβ)2 (p1q1 + p2q2) / (p1 – p2)2
donde :
n = tamaño de la muestra.
Zα = coeficiente de confiabilidad, cuando se usa un nivel de confianza del 95%, le corresponde 1.96.
Se y pe = desviación estándar estimada y proporción estimada, estas se pueden obtener de la
bibliografía o estudios pilotos.
E = es el error absoluto o precisión, este valor se debe asumir. Básicamente es la diferencia que
quisiéramos que exista entre la media poblacional que vamos a estimar y el promedio que
calcularemos con la muestra.
x1, x2 = son las medias aritméticas estimadas de las dos poblaciones.
p1, p2= son las proporciones estimadas de las dos poblaciones.
Métodos de selección
En el protocolo deberá especificarse el procedimiento que se seguirá para seleccionar los n
elementos de la población que conformarán la muestra, es decir las n unidades de muestreo.
Existen diversos métodos para seleccionar la muestra, entre ellos se encuentran: los empíricos y los
probabilísticos. Los estudios que utilizan este último método permitirán realizar inferencias.
DESCRIPCIÓN DE VARIABLES Y ESCALAS DE MEDICIÓN
Una de las etapas más importantes del proceso de investigación científica es la cuantificación de los
hechos o eventos observados; es decir, transformar en cifras el producto de nuestras percepciones.
Para ello, es necesario identificar con toda exactitud la característica o atributo a ser medido en los
elementos de estudio; luego hacer uso de un procedimiento objetivo, así como de un instrumento
sensible y confiable. Solo así la información obtenida permitirá llegar a conclusiones válidas.
En todo protocolo de investigación se debe especificar cada una de las variables que se estudiará,
así como la escala de medición utilizada.
Una variable es cualquier característica de objetos, animales y personas (es decir de una unidad de
análisis) que puede tomar diferentes valores.
Tipos de variables
a) Categóricas: que pueden expresarse cualitativamente. Ej. sexo.
b) Numéricas: que se expresan cuantitativamente. Ej. edad
Las variables en estudio deben seleccionarse en función de los objetivos de la investigación.
En los estudios experimentales habrá que especificar además las siguientes variables:
- Variable independiente: es la que manipula el investigador.
F-CV3-3B-2 Rev. Enero 2011
- Variable dependiente: es la que se observa con el fin de ver, que sucede como resultado de
la manipulación. Es la variable que se espera que cambie, o sea la que refleja el efecto del
experimento.
- Variable interviniente: son aquellas que no peden medirse directamente y aparecen en el
proceso del experimento entre el factor causal y el efecto. Estas variables pueden causar
problemas al experimento.
Escalas de medición
En cualquier estudio de investigación es necesario definir en qué escala se hará la medición de las
variables propuestas. Existen fundamentalmente cuatro tipos de escalas:
a) Nominal: son mutuamente excluyentes y exhaustivas. Ej. Estado civil, sexo, procedencia,
otros.
b) Ordinal: existe un grado de intensidad de la propiedad medida, por lo que las categorías
guardan un orden. Ej. Nivel de estudios: primaria, secundaria, superior.
c) De intervalo: se le asignan números para indicar la intensidad de una característica, con una
medida y origen arbitrarios, que se elige con base en conveniencias prácticas. Ej. Variables
temperatura.
d) De razón: se asignan números para señalar la intensidad de una característica con unidades
de medida arbitraria, pero de origen fijo, lo que mantiene la igualdad de las relaciones o
proporciones. Ejemplo: peso, talla.
En el protocolo de investigación, en este punto, es recomendable confeccionar el siguiente esquema
de tabla, que debe contener todas las variables estudiadas. Ej.
VARIABLE TIPO ESCALA DE MEDICIÓN
Edad Numérica-continua De razón
Sexo Categórica Nominal
N° de hijos Numérica-discreta De razón
PROCESO DE CAPTACIÓN DE LA INFORMACIÓN
En este punto se describirá con detalle, el procedimiento que se seguirá para obtener la
información necesaria para el contraste de la hipótesis y/o alcanzar el objetivo del estudio.
Los datos pueden ser obtenidos de dos maneras:
De registros de información: historias clínicas, censos de población y vivienda, anuarios, entre otros
registros. En estos casos reciben el nombre de datos secundarios.
Pero también se podrán obtener directamente de las unidades de observación, siguiendo ciertos
procedimientos, es decir por medio de cuestionarios, observaciones, entrevistas.
RECURSOS NECESARIOS Y CRONOGRAMA DE ACTIVIDADES
Para llevar a cabo una investigación, se debe disponer de los recursos necesarios, los mismos que
deben incluir los humanos, materiales y financieros. Se realizará un presupuesto de todos los gastos.
La investigación científica es un proceso que debe realizarse sistemáticamente, es decir paso a
paso. Una investigación puede durar meses y hasta años, según la naturaleza del estudio, por ello es
necesario elaborar un cronograma que incluya el tiempo que durará el estudio completo y las
secuencias que se realizarán en las diferentes actividades, la misma que deberá ser de
conocimiento de todo el equipo investigador. Existen muchos tipos de cronogramas, pero el que se
recomienda es el gráfico de Gant, que desglosa cada una de las actividades (o al menos las
principales) en función del tiempo.
F-CV3-3B-2 Rev. Enero 2011
CRONOGRAMA DE ACTIVIDADES
1
2 Actividades
3
1. Revisión bibliográfica
4 2. Elaboración del protocolo
5 3. Captación de datos
4. Procesamiento y análisis
6 0 1 2 3 4 5 6 7 8 9 5. Elaboración del informe
10 final
6. Publicación.
2.1.5. RESULTADOS
Diseña y ejecuta un protocolo de investigación.
2.1.6. CUESTIONARIO
a) Indique el objetivo que se busca al realizar una investigación científica:
b) Complete las siguientes expresiones en relación a la investigación científica:
La etapa en la cual se considera todo lo necesario para la realización de la
investigación científica, se conoce con el nombre
de ...........................................
.................................................... es la etapa de la investigación científica
en la cal se determina, en que porcentaje se cumplieron los objetivos propuestos.
c) Señale un título de investigación para cada estudio tipo: de casos control, cohortes y
experimental, señalando:
El objetivo principal.
La hipótesis central.
Las variables: independiente, dependiente e interviniente
Realice un cuadro de medición para las variables empleadas.
2.1.7. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed.
México: Editorial Mc Graw-Hill – Interamericana; 2011.
c) Hernandez S., Roberto. Metodología de la Investigación, 5ta Ed. (2002) Caracas.
Editorial McGrawHill
d) MENDEZ C., Metodología: Diseño y Desarrollo del Proceso de Investigación. 3ra Ed
(2001) Quebecor world Bogotá. Colombia.
e) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
f) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
g) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición
9. Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
2.2 METODOLOGÍA DE RESOLUCION DE CASOS CLINICOS
2.2.1 MARCO TEÓRICO
El seguimiento farmacoterapéutico es la práctica profesional en la que el Químico Farmacéutico se
responsabiliza de las necesidades del paciente relacionadas con los medicamentos, se realiza
mediante la detección, prevención y resolución de problemas relacionados a medicamentos (PRM).
Un problema relacionado con la farmacoterapia se define como: "un suceso indeseable, una
experiencia del paciente que implica, o se sospecha que implica, una terapia con medicamentos, y
que interfiere, real o potencialmente, con un resultado deseado para el paciente”. (Cipolle et al.,
1998)
2.2.2 COMPETENCIA
Resuelve casos clínicos utilizando el Método de Aproximación Orientado al Problema, que considera
tres fases: Evaluación, Plan y Seguimiento Farmacoterapéutico.
A. Evaluación
Breve descripción del paciente (edad, sexo, apariencia)
Razón principal para la entrevista con el paciente o visita.
Antecedentes demográficos del paciente.
La experiencia de la medicación según lo informado por el paciente (necesidades,
expectativas, preocupaciones, comprensión, preferencias, actitudes y creencias que
determinan el comportamiento del paciente que toma la medicación)
Historia exhaustiva de la medicación.
(Alergias, las alertas, el uso de drogas sociales y el estado de vacunación)
Registro de medicamentos actuales: descripción de todas las condiciones médicas que
se logró con farmacoterapia con las siguientes asociaciones realizadas:
Indicación – Medicamento – Régimen de dosificación - Resultados a la fecha
Antecedentes médicos relevantes: resultados del uso de medicamentos pasado.
Revisión de sistemas.
Identificación de problemas relacionados a los medicamentos: descripción del PRM,
medicamentos involucrados, y relaciones de causalidad.
Priorización de los múltiples PRM.
Resumen de la evaluación.
B. Plan de Atención (para cada PRM)
Objetivos de la terapia
Parámetros clínicos y de laboratorio utilizados para definir el objetivo de la terapia.
Valor observable, medible y tiempo para cada uno.
¿Cómo va a resolver los PRM del paciente?
Enfoques terapéuticos alternativos considerados.
Justificación de su producto y selección de la dosis.
¿Cómo va a lograr los objetivos de la terapia?
Intervenciones no farmacológicas.
Prevención de PRM.
Programa para la evaluación de seguimiento.
F-CV3-3B-2 Rev. Enero 2011
C. Evaluación del Seguimiento
Evidencia clínica y/o de laboratorio de la efectividad de la farmacoterapia para cada
indicación.
Evidencia clínica y/o de laboratorio de la seguridad de cada régimen de medicamentos.
Evidencia de cumplimiento.
Evaluación del estado de resultados.
Cambios necesarios en las terapias con medicamentos.
Programar las evaluaciones futuras.
Resumen del caso.
Proceso de seguimiento farmacoterapéutico
1. Establecer prioridades en la selección de pacientes: según su enfermedad o su medicación.
2. Establecer parámetros de seguimiento:
Parámetros objetivos: Signos o condiciones que pueden ser cuantificados, o constatados
mediante observación profesional o instrumentos.
Parámetros subjetivos: Percepciones o situaciones que relata el paciente, generalmente no
se pueden cuantificar y su valor depende de la credibilidad que el profesional le asigne.
3. Las fuentes utilizadas son la historia clínica, el kardex de enfermería, la entrevista con el
paciente o con miembros del equipo de salud.
Elaboración de la Presentación del Paciente
Realizar la entrevista al paciente o familiares.
Interpretar condiciones socioculturales y socioeconómicas.
Identificar situaciones fisiopatológicas que puedan modificar la cinética de los fármacos.
Interpretar valores de exámenes de laboratorio.
Tratamientos (farmacológicos y no farmacológicos).
Datos generales Antecedentes Signos y Síntomas Exámenes de
Mórbidos Laboratorio
Nombre (iniciales) Síntomas Síntomas generales: lo Hemograma
Edad Signos que refiere el paciente: Hemoglobina
Sexo Enfermedades Malestar general Glucosa
Raza congénitas Fiebre
Domicilio Enfermedades de la Pérdida de peso Perfil renal:
Procedencia infancia Debilidad Ácido úrico
Estado civil Quirúrgicos Fatiga Creatinina
Grado instrucción Traumatismos Insomnio
Ocupación Alergias: Prurito Perfil hepático:
Idioma Alimentarias Transaminasas (TGO,
Religión Medicamentos Signos vitales: TGP)
Vivienda Intoxicaciones Fosfatasa alcalina
Temperatura
Alimentación Bilirrubina
Presión arterial
Vestimenta Antecedentes Albúmina
Pulso
Higiene familiares:
Deporte y ejercicio Investigar etiología y Frecuencia respiratoria Perfil lipídico:
Hábitos nocivos: edades de morbi- Colesterol total
Somatometría:
Fumar mortalidad en la LDLc
Peso
Alcohol familia HDLc
Estatura
Café, té Triglicéridos
Tratamientos IMC
Tóxicos
Situación alternativos:
Exámenes especiales: Análisis de gases
socioeconómica Fitoterapia arteriales y electrolitos
RMN. TAC, ecografías
Otros
F-CV3-3B-2 Rev. Enero 2011
Elaboración de la Anamnesis Farmacológica
Realizar la entrevista al paciente o familiares, preguntando por el:
Nombre del Medicamento
Dosis, vía e intervalo
Fechas de inicio, fin o reinicio
Motivo de uso
Aceptación
Administración
Otros
Medicamentos antes Medicamentos actual
Antes de la hospitalización Considerar los fármacos administrados en el
Antes del PRM momento del evento
Automedicación o prescritos
Elaboración de la Clasificación de PRM según Minnesota (ver Anexo 01)
Indicación Medicamento Dosificación Resultados
Síntoma Nombre genérico o Dosis, Frecuencia, Vía y Valora seguridad
Signo Denominación Duración Valora efectividad
Síndrome Común todos los fármacos
Enfermedad Internacional (DCI) Relacionar: usados en una sola
Dosificación del indicación
Revisar: Relacionar: medicamento con el
Diagnósticos con Datos alterados estado fisiológico Evaluar:
tratamientos del paciente con (edad, gestación) o Con datos clínicos y
establecidos en GPC información del fisiopatológico analíticos si el
u otras fuentes medicamento: (insuficiencia renal o medicamento es
RAM, eficacia hepática) efectivo o seguro
comparativa, etc. para la indicación
dada.
F-CV3-3B-2 Rev. Enero 2011
Desarrollo de un plan de seguimiento Farmacoterapéutico
Una vez identificados los problemas que pueden ser concernientes al paciente, al profesional de
salud o a ambos, se procede a su ordenamiento según prioridades, lo cual dependerá de la
perspectiva de cada profesional de salud, colocando el problema más serio en primer lugar y así
sucesivamente. El término triaje designa un sistema por el que se clasifican un grupo de bajas u
otros pacientes según la gravedad de sus lesiones o enfermedades, para poder asignar prioridades
de tratamiento entre ellas.
Tipo de PRM Descripción de PRM Prioridad
Indicación Indicar el PRM identificado Alta
Efectividad con los datos del paciente Media
Seguridad Baja
Cumplimiento
Elaboración del Formato de Evolución SOAP:
La información obtenida en las fuentes debe organizarse en el formato SOAP, por lo que para cada
problema identificado y priorizado en la Lista de Problemas, los datos subjetivos y objetivos son
almacenados, evaluados e interpretados para desarrollar un plan, que puede ser para reunir más
información o para solucionar el problema.
(1) Organización de la Información:
S Subjetivo: Los datos subjetivos incluyen:
Síntomas o quejas del paciente
Observaciones de los profesionales de la salud.
La principal fuente de información es la entrevista con el paciente y con los profesionales de
la salud.
O Objetivo: Los datos objetivos incluyen:
Signos vitales
Resultados de Pruebas de Laboratorio
Hallazgos del examen físico
Resultados de procedimientos diagnósticos (Rx, ECG, TAC, etc.)
La principal fuente de información es la Historia Clínica.
A (2) Evaluación y Análisis de la Información:
Asesoría o Evaluación: Las actividades que realiza el químico farmacéutico son:
Interpretar los datos subjetivos y objetivos para cada problema.
Buscar explicaciones alternativas o factores contribuyentes.
Características fisiopatológicas del paciente.
Características relevantes del medicamento.
Desarrollar una propuesta o plan sugerido.
Monitorizar la respuesta a la terapia.
Decidir si la respuesta es la adecuada.
Documentar los problemas que se presentan con los medicamentos.
Evaluar el cumplimiento del paciente.
F-CV3-3B-2 Rev. Enero 2011
P (3) Formulación del Plan Sugerido:
Plan: Luego del proceso de evaluación y análisis de toda la información disponible
debidamente organizada, el profesional de salud, desarrolla una propuesta, o plan sugerido,
el cual será puesto a consideración del profesional responsable de la terapia del paciente,
para su aplicación, seguimiento y evaluación.
El plan sugerido puede abarcar varios aspectos como son:
1. Tratamiento: Sugerencias para resolver o prevenir problemas de salud, reales o
potenciales, relacionados con la nutrición, los cuales ya se encuentran previamente
identificados.
2. Monitorización de Parámetros:
a. Selección de parámetros subjetivos y objetivos que deberán ser monitorizados para
evaluar la respuesta a la terapia (generalmente los mismos que fueron usados para
el diagnostico)
b. Selección de los intervalos de tiempo para realizar estas mediciones.
c. Selección de acciones a tomar si ocurren RAM. (fármacos, disminución de dosis,
disminución de frecuencia, descontinuación, medidas alternativas como
administrar con alimentos, etc.).
3. Estudios adicionales para evaluar el problema: Cuando el problema persiste a pesar
de haber cumplido todos los procesos previos, y sugerencias sobre pruebas o estudios
que proporcionen mayor información que sirva para resolver el problema.
4. Educación al Paciente: Es primordial que el paciente conozca algunos datos
específicos de cada, medicamento que recibe como nombres, dosis, indicación, horario
de administración, precauciones, IM, RAM, almacenamiento, pautas adecuadas de
administración y cualquier otro dato necesario para el uso seguro de los fármacos.
Elaboración del Seguimiento
Objetivos Acciones propuestas Resultados Revisión del plan
terapéuticos
Utilizar los términos: De acuerdo al PRM se De acuerdo a la En función del
Revertir puede sugerir: evolución del tiempo se evalúa el
Minimizar Tratamiento paciente puede ser: objetivo terapéutico,
Resolver específico Favorable indicando:
Otros Modificación de la Mejoría Problema no
En relación a la dosis No mejora resuelto
clínica o analítica Suspensión del Remisión del
alterada del paciente fármaco problema
Otros Paciente de ALTA
F-CV3-3B-2 Rev. Enero 2011
PROBLEMAS RELACIONADOS CON MEDICAMENTOS Anexo 01 Clasificación de PRM según Minnesota
PROBLEMAS MÉDICOS Y FARMACOTERAPIA RELACIONADA INDICACIÓN
Medicamento innecesario
__Sin indicación apropiada
__Terapia duplicada
__Indicación de terapia no farmacológica
__Tratamiento de una RAM evitable
__Uso adictivo/recreacional
Necesita Medicamento Adicional
__Problema no tratado
__Preventivo/profiláctico
__Sinérgico/potenciar
PROBLEMA MÉDICO Y FARMACOTERAPIA RELACIONADA EFECTIVIDAD
Necesita un Medicamento Diferente
__Medicamento más efectivo disponible
__Problema refractario al medicamento
__Forma farmacéutica inapropiada
__No es efectiva para el problema médico
Dosis muy Baja
__Dosis incorrecta
__Frecuencia inapropiada
__Interacción medicamentosa
__Duración inapropiada
PROBLEMA MÉDICO Y FARMACOTERAPIA RELACIONADA SEGURIDAD
Reacción Adversa al Medicamento
__Efecto indeseable
__Medicamento no seguro para el paciente
__Interacción medicamentosa
__Dosis administrada o cambio muy rápido
__Reacción alérgica
__Contraindicaciones
Dosis muy Alta
__Dosis incorrecta
__Frecuencia inapropiada
__Duración inapropiada
__Interacción medicamentosa
__Administración incorrecta
PROBLEMA MÉDICO Y FARMACOTERAPIA RELACIONADA CUMPLIMIENTO/ ADHERENCIA
Incumplimiento
__No entendió las instrucciones
__Paciente prefiere no tomar
__Paciente olvida tomar
__El paciente no puede costear el medicamento
__No la puede tragar/administrar
__Medicamento no disponible
__No hay Problema(s) Relacionados con Medicamento(s)
Fuente: Cipolle RJ, Strand LM, Morley PC. Pharmaceutical Care Practice: The Clinician’s Guide, McGraw Hill,
2004
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 03 (SEMANA 03)
FÁRMACOS EN ASMA BRONQUIAL INDUCIDA
CASO CLÍNICO: FÁRMACOS EN ASMA
3.1. MARCO TEÓRICO: ASMA EXPERIMENTAL
Las enfermedades respiratorias globalmente consideradas constituyen el principal motivo de
primeras consultas en medicina primaria, así mismo, los estudios sobre utilización de medicamentos
demuestran que los agentes activos sobre el sistema respiratorio ocupan uno de los primeros
puestos, en cuanto a consumo.
Entre los fármacos que actúan sobre el Sistema Respiratorio, se encuentran:
Los broncodilatadores y otros agentes que actúan previniendo y controlando el asma bronquial.
Antitusígenos, estos fármacos actúan de tal manera que disminuyen la sensibilidad de “los
receptores de la tos” a sustancias, tales como irritantes químicos y autacoides, que
activan los receptores. Existen agentes que disminuyen la sensibilidad del “centro de la
tos”, entre estos se encuentran los opiáceos, morfina, codeína, dextrometorfano
(dextroisómero del éter metílico del levorfanol). Es tan eficaz como la codeína como
inhibidor de la tos, y a dosis muy elevadas puede producir efectos sobre el SNC.
Expectorantes, aquellos que incrementan la secreción por una acción directa sobre la mucosa
bronquial y/o a través de un mecanismo reflejo resultante de la irritación gastroduodenal. En este
grupo se encuentran: los aceites esenciales del grupo de los terpenos (eucaliptol), bálsamos (tolú),
compuestos de amonio (cloruro de amonio), guaifenesina, citrato de sodio o potasio. Y
Mucolíticos, fármacos que fluidifican las secreciones. Entre la diversidad de productos existentes,
aunque cuestionables se encuentran: los tioles (acetilcisteína y carbocisteína), la bromexina y
ambroxol. Los primeros rompen los puentes disulfuro de las mucoproteínas y reducen la viscosidad
de las secreciones
Asma Bronquial
Es un síndrome caracterizado por:
Obstrucción generalizada reversible de las vías aéreas.
Hiperreactividad bronquial.
Inflamación de la submucosa de las vías aéreas.
Tendencia incrementada a la broncoconstricción.
Clasificación del Asma Bronquial
Según su origen pueden ser:
Asma extrínseca
- Se caracteriza porque es provocada por alergenos externos conocidos.
- Las pruebas dérmicas inmediatas son positivas.
- Existe un aumento de la IgE en 50% a 60% de los sujetos.
- Su inicio por lo regular se produce en la infancia o vida adulta temprana.
- El asma generalmente es intermitente.
- Generalmente existen otras alergias asociadas (fiebre de heno y eccema).
- Son comunes los antecedentes familiares de alergias múltiples (asma, fiebre de heno,
eccema) hasta 50%
Asma intrínseca
- Se caracteriza porque no hay alergenos externos conocidos.
- Las pruebas dérmicas son negativas.
- Los niveles de IgE son normales o están disminuidas.
- El inicio por lo general (pero no invariablemente) se produce en adultos de mayor edad.
- El asma se presenta de una manera continua.
F-CV3-3B-2 Rev. Enero 2011
- La presentación de otras alergias asociadas es poco frecuente (7%).
- Son menos comunes los antecedentes familiares de alergias múltiples (20%).
Según la severidad del asma
Asma leve
- Se presenta en forma intermitente y los síntomas son breves (< 1-2 veces por semana).
- Los síntomas nocturnos del asma son menores de 2 veces por mes.
- Se presenta asintomático entre exacerbaciones.
El tratamiento es sólo agonista β2-adrenérgico de corta duración a condición.
Asma moderada
- Se presenta con exacerbaciones mayores a 1-2 veces por semana.
- Los síntomas de asma nocturna son menores de 2 veces al mes.
- Los síntomas requieren β2 agonistas adrenérgicos inhalados casi a diario.
El tratamiento requiere un agente antiinflamarorio inhalado diariamente, además de un
broncodilatador de larga duración a diario especialmente para los síntomas nocturnos.
Asma severa
- Las exacerbaciones son frecuentes y los síntomas continuos.
- Se presentan síntomas frecuentes de asma nocturna.
- La actividad física está limitada por el asma.
- Existen antecedentes de hospitalización por asma en el año anterior.
- Existe antecedentes de exacerbación previa en la que se puso en riesgo la vida del paciente.
El tratamiento consiste en inhalación diaria de agente antiinflamatorio, a dosis más altas,
utilización de broncodilatadores de larga duración a diario, especialmente para los síntomas
nocturnos y se usa frecuentemente los corticoides sistémicos.
En la mayoría de casos la crisis asmática está integrada por dos fases principales:
1. La fase inicial o respuesta inmediata, que se instaura inmediatamente y se caracteriza sobre
todo por la existencia de broncoespasmo. Las células implicadas son fundamentalmente los
mastocitos, aunque también podrían participar los macrófagos alveolares y plaquetas.
Las células activadas y otras células liberan una variedad de células biológicamente activas con
propiedades espasmogénicas y vasoactivas (histamina, factor activado de plaquetas,
leucotrienos -LTC4, LTD4, LTE4- tromboxano A2, prostaglandinas F2 alfa, y D2, bradicinina,
acetilcolina, y quimiotácticas (factor activador de las plaquetas, leucotrieno B 4, factor
quimiotáctico de eosinófilos, factor quimiotáctico de neutrófilos.Los factores quimiotácticos
atraen a las células inflamatorias poniendo en marcha a la …
2. Fase Inflamatoria Tardía, que se caracteriza por broncoespasmo acompañado de
vasodilatación, edema de la mucosa e hipersecreción de mucus, y a la larga hipertrofia de la
musculatura lisa.
En esta fase se produce la infiltración y activación de eosinófilos, y en menor grado de neutrófilos,
macrófagos, linfocitos y plaquetas. Estas células inflamatorias, a su vez, liberan mediadores
espasmogénicos, vasoactivos y quimiotácticos que perpetúan el proceso.
ANTIASMÁTICOS
Son fármacos activos en el control y/o prevención del asma bronquial.
CLASIFICACIÓN
I. Broncodilatadores
Son fármacos capaces de relajar el músculo liso de las vías aéreas.
a. Fármacos Beta-adrenérgicos
No selectivos : Adrenalina, efedrina, isoprenalina.
F-CV3-3B-2 Rev. Enero 2011
Selectivos : Catecolaminas: isoetarina, rimiterol.
No catecolaminas: salbutamol, fenoterol, orciprenalina, salmeterol,
clembuterol.
b. Metilxantinas
Teofilina, aminofilina (teofilina-etilendiamina), diprofilina, etamifilina, proxifilina.
c. Anticolinérgicos (Antimuscarínicos)
Bromuro de ipratropio.
II. Antiinflamatorios esteroideos
a. Sistémicos
Prednisona, hidrocortisona, triamcinolona.
b. Inhalatorios
Beclometasona dipropionato, budesonide, flunisolide, fluticasona.
III. Preventivos asmáticos
a. Bloqueadores de la liberación de Mediadores.
Cromonas: Cromoglicato sódico, Nedocromilo sódico.
b. Antihistamínicos
Ketotifeno, azelastina, Cetirizina.
c. Antileucotrienos
Zileuton, Montelukast, Zafirlukast.
IV. Otros antiasmáticos
a. Inmunosupresores: Ciclosporina.
b. Tromboxanos A2
c. Prostaglandina E2
HISTAMINA
La histamina es una amina sintetizada en 1907, que posteriormente fue aislada de los tejidos. Esta
compuesto por u anillo imidazólico y una cadena lateral etilamino.
Se encuentra almacenada principalmente en los mastocitos del tejido conjuntivo y en las células
basófilas de la sangre. En el organismo humano la histamina se puede encontrar en forma libre en
la piel, sistema gastro-intestinal, SNC y otros; en forma de recambio lento, en las células cebadas
de los tejidos perivasculares de muchos órganos, especialmente pulmón e hígado; como histamina
circulante en los basófilos sanguíneos, que vienen a ser los mastocitos circulantes.
Las acciones de la histamina están mediadas por tres tipos de receptores: H1, H2 y H3.
Los receptores H1, entre otras acciones participan en la contracción de la fibra muscular lisa
bronquial, produciendo broncoconstricción.
ANTIHISTAMÍNICOS
Son fármacos que antagonizan competitivamente las acciones de la histamina sobre los receptores
H1
Clasificación
Según su acción sedante:
I. Con acción sedante
Clorofeniramina, azatadina, tripolidina, dimenhidrinato, entre otros.
II. Sin acción sedante
Terfenadina, astemizol, loratadina, entre otros.
Según su grupo químico:
I. Derivados de la Etanolamina
Clemastina, dimenhidrinato, doxilamina, carbinoxamina, entre otros.
II. Derivados de la Etilendiamina
Mepiramina, tripelamina.
III. Derivados de las Alquilaminas
Clorofeniramina, bromofeniramina, tripolidina, entre otros.
IV. Derivados de las Piperidinas
Terfenadina, astemizol, loratadina, entre otros.
F-CV3-3B-2 Rev. Enero 2011
V. Derivados de la Piperazinas
Cetirizina, entre otros.
VI. Derivados de Fenotiazinas
Prometazina, isopentidilo, entre otros.
VII. Otros
Cinarizina, ciproheptadina, entre otros.
Experiencia
3.2. Competencia
Diseña y ejecuta una experiencia utilizando medicamentos que modifican la disnea inducida
por histamina y su prevención por clorofeniramina; asimismo interpreta los efectos
observados en el cobayo.
3.3. Material y Métodos
Modelo experimental : Cobayo (02)
Fármacos : Histamina clorhidrato 1%
Clorofeniramina 1%
Adrenalina 0.005% ó Salbutamol o fenoterol sol. 0.5%
Equipos : Polígrafo digital
Equipo para nebulización
3.4. Procedimiento:
a) Identificar y pesar a dos cobayos.
b) Prepara las jeringas conteniendo, una clorfeniramina, y la otra adrenalina.
c) A uno de ellos administrar 50 mg/kg de peso de clorfeniramina.
d) Luego de 10 minutos introducir a los dos cobayos en una campana de nebulización
herméticamente cerrada, observando el comportamiento del animal.
e) Luego saturar la atmósfera del recipiente, nebulizando con una solución de VIII
gotas de histamina 1% + 4 ml de suero fisiológico, controlar el tiempo en que se
produce la sintomatología característica del broncoespasmo. Observar.
f) Retirar al cobayo con disnea y administrar rápidamente adrenalina 0.04 mg/kg, vía
i.p., o colocar al cobayo en otra campana y nebulizar con III gotas de salbutamol o
fenoterol + 3 mL de suero fisiológico. Observar.
3.5. Resultados:
Medir los efectos (amplitud respiratoria, frecuencia respiratoria, frecuencia cardiaca)
Fármacos Efectos Clorfeni- Efectos Histamina Efectos Adrenali- Efectos
basales ramina (FR y AR) (FR y AR) na (FR y AR)
(FR y AR)
Cobayos
Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
CASO CLÍNICO: FARMACOTERAPIA DEL ASMA BRONQUIAL
La niña Q.C de 5 años, 18 kg de peso es conducida a la emergencia porque desde hace dos días
presenta disnea y tos, que progresivamente empeora. Estos síntomas fueron precedidos por tres días
de síntomas de infección viral de vías respiratorias altas (dolor de garganta, rinorrea y tos).
Ella ha experimentado varios ataques de bronquitis en los dos últimos años y fue hospitalizada por
neumonía tres meses antes. La niña no está siendo tratada con ninguna medicación en este
momento.
El examen físico revela aparente ansiedad, en moderada dificultad respiratoria con sibilancias,
ocasional tos, prolongada fase espiratoria, hiperinflación torácica y retracción supraesternal,
supraclavicular e intercosal. Inspiración bilateral y sibilancia con disminución de los sonidos
respiratorios sobre el lado izquierdo.
Los signos vitales son: frecuencia respiratoria (FR): 30 por minuto, presión arterial (PA): 110/83 mm
Hg, frecuencia cardiaca (FC): 130 latidos por minuto, temperatura: 37.8 ºC.
Se le administra 2.5 mg de salbutamol (ventolín) es decir 0.5 mL de una solución 0.5% en 2.5 mL de
solución salina mediante nebulización con aire comprimido por 10 minutos. Luego del tratamiento,
la niña presenta un mejoramiento subjetivo y se siente más confortable. Sin embargo a la
auscultación se escuchan ruidos.
Preguntas a responder:
a) ¿Qué signos y síntomas son consistentes con obstrucción bronquial aguda?
b) ¿Qué exámenes auxiliares adicionales pueden ayudar a evaluar la extensión de la
obstrucción bronquial en la niña?
c) ¿Qué signos y síntomas o mediciones de laboratorio pueden predecir mejor, si la niña
requiere hospitalización o puede recaer y retornar a la emergencia?
d) ¿Porqué fue seleccionado un β2-agonista como el broncodilatador de primera elección, en
preferencia a otros broncodilatadores como la aminofilina o atropina?
e) ¿Por qué el β2-agonista salbutamol fue administrado por nebulización, y no por vía oral o
por vía parenteral?
f) ¿Habría sido otro β2-agonista más efectivo en la terapia inicial?
g) Debido a que los síntomas no fueron resueltos completamente con la primera dosis de
nebulización con salbutamol. Los análisis de gases arteriales obtenidos fueron: pH 7.45, Pa
O2 60 mm Hg y Pa CO2 28 mm Hg; los signos vitales indicaron: FC: 140 latidos/min, FR:
27/min, PA: 110/74 mm Hg. Después de 20 minutos, se administró 2.5 mg de salbutamol
cada 20 minutos, en un periodo de dos horas. Después de tres tratamientos, la niña
presento sonidos respiratorios claramente despejados, su frecuencia cardiaca y presión
arterial disminuyeron a 100 latidos/min y 100/65 mm Hg, respectivamente. ¿Fue la dosis y
el intervalo de administración de salbutamol apropiados?
h) La niña incrementó su frecuencia cardiaca de 130 lat/min (al momento de su ingreso a
emergencia) a 140 lat/min después de su primera nebulización y su presión diastólica
disminuyó de 83 a 74 mm Hg. ¿Explique porqué se producen estos cambios?
F-CV3-3B-2 Rev. Enero 2011
3.6. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 04 (SEMANA 04)
FÁRMACOS EN HIPERTENSIÓN ARTERIAL: DIURESIS EXPERIMENTAL
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
4.1. MARCO TEÓRICO: HIPERTENSIÓN ARTERIAL
Se define como la elevación crónica de la presión arterial sistólica (máxima) a 140 mmHg. o más,
y/o de la presión arterial diastólica (mínima) a 90 mmHg o más. Los principales elementos que
contribuyen a la hipertensión son: el volumen de sangre, gasto cardiaco y la resistencia vascular
periférica.
Clasificación de la Hipertensión Arterial
Según su etiología
HTA esencial, primaria o idiomática (90% a 95%) de etiopatogenia
desconocida.
Hipertensión arterial secundaria (5% a 10%), puede deberse a:
Hiperaldosterismo (síndrome de Conn)
Hipersecreción de otros mineralcorticoides.
Hipersecreción de glucocorticoides (síndrome de Cushing)
Fecocromocitoma (tumor de origen medular suprarrenal)
Tumor de células yuxtaglomerulares
Hipertensión renal (estrechamiento de una o ambas arterias renales)
Enfermedad renal: glomeruronefritis, pielonefritis, enfermedad poliquística.
Estenosis aórtica.
Policitemia grave.
Medicamentos: AINES, glucocorticoides y otros.
Según su severidad:
HIPERTENSIÓN PAS (mm Hg) PAD (mm Hg)
Normal < 130 < 85
Normal alta 130 – 139 85 - 89
Estadío I (ligera) 140 - 159 90 – 99
Estadío II (moderada) 160 - 179 100 – 109
Estadío III (severa) ≥ 180 ≥ 110
Estadío IV (muy grave) ≥ 210 ≥ 120
ESTADIO I: No se aprecian signos objetivos de alteración orgánica
ESTADIO II: Aparecen por lo menos uno de los siguientes signos de afección orgánica:
hipertrofia ventricular (detectada por rayos x, electrocardiograma y ecografía), proteinuria y
ligero aumento de la concentración de creatinina.
ESTADIO III. Aparecen signos de lesión de algunos órganos (a causa de HTA). A nivel de corazón
se observa insuficiencia ventricular izquierda, a nivel de encéfalo hemorragia cerebral
(encefalopatía hipertensiva), y en el fondo de ojo hemorragia y exudados retinianos con o sin
edema papilar.
HTA ESENCIAL, PRIMARIA O IDIOMÁTICA (90% A 95%)
Pacientes con HTA sin causa definible. Existe dificultad para descubrir los mecanismos responsables
de la HTA en estos pacientes, se ele atribuye a una variedad de sistemas implicados en la regulación
de la PA (adrenérgicos, periféricos o centrales, renales, hormonales y vasculares) y a la complejidad
de las interrelaciones entre estos sistemas. Existen otros factores probablemente involucrados,
como los genéticos, alimentarios (sensibilidad a la sal), ambientales, psicosociales síndrome de
estrés, sedentarismo y/o tabaquismo.
F-CV3-3B-2 Rev. Enero 2011
También existen factores que modifican la evolución de la HTA, entre los que se encuentran la
edad, raza, sexo, tabaco, consumo de alcohol, colesterol sérico, intolerancia a loa glucosa y peso
corporal.
Factores de riesgo
Sexo: la HTA predomina en varones hasta los 50-55 años, a partir de esta
edad la predominancia es en mujeres.
Edad, Raza, Herencia.
Sal, Grasas saturadas y alcohol.
Sobrepeso, tabaco, café y té.
Calcio, potasio, magnesio: datos epidemiológicos indican que suplementos
cálcicos, potásicos y de magnesio se asocian a una menor incidencia de hipertensión
arterial.
Sedentarismo y ejercicio físico.
El sueño y la relajación
Factores psicosociales: al parecer el estrés produce elevación de la
presión arterial.
Sintomatología
La mayoría de los pacientes no sufren molestias, la enfermedad suele progresar en forma
silenciosa hasta que ocurren algunas graves complicaciones: a nivel del corazón, cerebro o
riñón.
La HTA puede provocar los siguientes signos y síntomas:
Dolor de cabeza persistente (especialmente en la región frontal y por
la mañana), siendo este síntoma propio de presiones diastólicas mayores de 100 mm Hg.
Dolor en la nuca, sangrado nasal espontáneo, transtornos de la visión
(por alteraciones en la retina).
Zumbido en los oídos, palpitaciones, fatiga muscular.
Dolor de pecho, (debido a angina de pecho o estrés músculo
esquelético).
Perdida de la conciencia, y dificultad para respirar (ocasionada por
cierto grado de insuficiencia cardiaca).
Los mareos, el nerviosismo y el insomnio también pueden presentarse,
pero aparecen por causas muy diversas.
Complicaciones
Corazón: hipertrofia ventricular izquierda (HVI), insuficiencia
coronaria.
Riñón: la prevalencia de insuficiencia renal atribuible a
hipertensión arterial esencial oscila entre el 4 y 10% (82).
Sistema nervioso central: ataque isquemico transitorio (TIA), Infarto
cerebral, demencia multiinfarto (demencia vascular)
Arteriopatia periférica.
Hipertensión en situaciones especiales
En los diferentes grupos étnicos y raciales:
La prevalencia de HTA entre los grupos étnicos y raciales difiere de los de la población en
general:
Los hindúes tienen mayor prevalencia que el resto de la población.
Los hispánicos y latinos, es similar o algo menor que los blancos no hispánicos, a pesar de la
alta tasa de obesidad y diabetes tipo 2 que existe en esta población.
Los asiáticos responden mejor a algunos medicamentos antihipertensivos que los blancos.
La incidencia de HTA en las personas de raza negra es una de las más elevadas del mundo,
comparada con la de los blancos, ésta se desarrolla a más temprana edad y la PA promedio
es mucho más elevada.
Los individuos de color a menudo no reciben tratamiento hasta que la presión arterial está
elevada durante largo tiempo y se ha dañado algún órgano. Este aspecto tiene que ver con
la alta incidencia de morbilidad y mortalidad asociada con la hipertensión en la población
de raza negra, incluida la enfermedad renal desarrollada en la última etapa.
F-CV3-3B-2 Rev. Enero 2011
Las evidencias muestran que los logros en el tratamiento y el control de la hipertensión en
algunos grupos, especialmente los de menor nivel socioeconómico, requieren una educación
y programas antihipertensivos más específicos.
En ancianos:
La HTA es el principal factor de riesgo de morbimortalidad cardiovascular en la población
mayor de 65 años. Los criterios para establecer los límites de normalidad en este grupo
poblacional difieren de unas clasificaciones a otras como sigue:
PAS PAD
Óptima OMS > 160 mm Hg > 95 mm Hg
JNC-V > 140 mm Hg > 90 mm Hg
Consenso español en el > 140 mm Hg > 90mm Hg
control de la HTA
En la
Infancia
y Adolescencia
Se estima una prevalencia del 1,5-3%.
En el embarazo
La HTA constituye la complicación más frecuente durante el embarazo y es una de las
principales causas de prematuridad, morbilidad perinatal y mortalidad materna.
Con el uso de Anticonceptivos Orales
Experimentan un pequeño y, a veces casi imperceptible aumento de la presión arterial,
aunque dentro de los niveles normales.
En diabetes mellitus
En dislipidemias y colesterol
En gota
En asma bronquial
En pacientes quirúrgicos
Normas generales para una farmacoterapia en HTA
a) Medidas no farmacológicas:
Modificaciones de estilo de vida:
Reducción de peso
Ingestión moderada de alcohol
Actividad física regular
Reducción de ingestión de sal
Cesar de fumar
RESPUESTA INADECUADA
F-CV3-3B-2 Rev. Enero 2011
b) Medidas farmacológicas
Continuar con:
Los cambios de estilo de vida
Primera selección farmacológica
Diuréticos y beta bloqueadores son preferidos por que se ha demostrado
reducción en la morbimortalidad
Inhibidores de la ECA, antagonistas del calcio, bloqueadores de receptores alfa 1
y bloqueadores alfa y beta.
RESPUESTA INADECUADA
Incremento dosis, sustituir o agregar un agente de diferente clase
RESPUESTA INADECUADA
Agregar un segundo o tercer agente
FÁRMACOS ANTIHIPERTENSIVOS
Concepto
Son aquellos agentes utilizados en control de la hipertensión arterial con la finalidad de evitar la
morbi-mortalidad cardiovascular.
Clasificación de los Fármacos Antihipertensivos
a) Diuréticos
- Tiazídicos: hidroclorotiazida, clorotazida, ciclopentiazida.
- De Asa: furosemida, bumetanida, ácido etacrínico
- Ahorradores de potasio: amilorida, espironolactona, triamtereno
b) Betabloqueadores
- Cardioselectivos: atenolol, acebutolol,
esmolol, metoprolol, entre otros.
- No selectivos: propranolol, sotalol, pindolol,
timolol, nadolol, alprenolol y otros
c) Antagonistas de los canales de calcio
- Dihidropiridinas: nifedipino, amlodipino,
isradipino, felodipino, lacidipino, lercadinipino, manidipino, nilvadipino, nisoldipino,
nitrendipino y otros.
- Fenilaquilaminas: verapamilo.
- Benzotiazepinas: diltiazem
d) Inhibidores de la enzima convertidora de angiotensina II: captopril,
enalapril, lisinopril, fosinopril, trandolapril, moexipril, perindopril, quinapril, ramipril,
espirapril, zofenopril, cilazapril, alacepril, delapril y otros.
F-CV3-3B-2 Rev. Enero 2011
e) Bloqueadores de los receptores de angiotensina: losartan, valsartan,
candesartan, eprosartan, irbesartan, tasosartan, telmisartan.
f) Bloqueadores -1 adrenérgicos: prazocina, terazocina, alfuzocino,
tamsulocino, doxazocino, bunazocino, trimazocino y otros.
g) Bloqueantes y - bloqueadores adrenérgicos: labetalol, carvedilol,
bucindolol.
h) Agonistas -2 adrenérgicos centrales: metildopa, clonidina
i) Vasodilatadores directos:
Arteriales: hidralazina, diazóxido, minoxidil.
Venosos: nitroglicerina, dinitrato de isosorbide, 5-mononitrato
de isososrbide.
Arteriales y venosos: nitroprusiato.
j) Bloqueantes ganglionares: trimetafán
FARMACOLOGÍA DE LOS AGENTES ANTIHIPERTENSIVOS
DIURÉTICOS
Son fármacos que estimulan la excreción renal de agua y electrolitos, como consecuencia de su
acción sobre el transporte iónico a lo largo de la nefrona. La interferencia de los diuréticos se
puede llevar en uno o varios sitios del recorrido tubular.
Su objetivo principal es conseguir un balance negativo de agua, pero los diuréticos no actúan
directamente sobre el agua, si no a través del sodio (diuréticos natriuréticos) o de la osmolaridad
(diuréticos osmóticos), pero directa o indirectamente pueden modificar los niveles de otros iones y
alterar otras funciones.
Clasificación
Diuréticos de máxima eficacia: actúan en los segmentos diluyentes entre estos mencionamos a la
furosemida, bumetanida, piretanida, torasemida, ácido etacrínico, etozolina y otros.
Diuréticos de eficacia mediana: actúan en la porción final diluyente cortical y en el primer
segmento del túbulo distal, entre estos se encuentran la hidroclorotiazida, clorotiazida,
ciclopentazida, altizida, bendroflumetiazida, mebutizida, indapamida, xipamidda y quinetazona y
otros.
Diuréticos de eficacia ligera: su sitio de acción es variable, entre estos encontramos: a)
Ahorradores de potasio: actúan en el último segmento del túbulo distal por inhibición de la
aldosterona: espironolactona y canrenoato de potasio, o con independencia de la aldosterona como
el amiloride y triamtereno. b) Los inhibidores de la anhidrasa carbónica: acetazolamida y
diclorfenamida. c) Los agentes osmóticos: actúan en el túbulo proxial, tales como el manito e
isosorbide.
Mecanismos de acción
Diuréticos de asa
Estos Se fijan a la proteina cotransportadora Na+-K+-2Cl- situada en la membrana luminar del
segmento grueso de la rama ascendente del asa de Henle y la inhiben, en consecuencia impiden
este importante transporte de iones (Na*, K+ y 2 Cl-). Estos fármacos también inhiben la
reabsorción de Ca+2 y Mg+2 en la rama gruesa ascendente, con lo que incrementan su eliminación
Diuréticos tiazídicos
Se fijan selectivamente al cotransportador de Na+-Cl- de ala membrana luminar del túbulo
contorneado distal, interfiriendo de esta manera en la corriente iónica de Na+ y de Cl-.
Diuréticos ahorradores de potasio
F-CV3-3B-2 Rev. Enero 2011
Son diuréticos que inhiben la reabsorción de Na+ en el túbulo contorneado distal y la porción inicial
del túbulo colector, reducen su intercambio con el K+. La acción diurética es escasa, ya que el
aumento de la fracción de eliminación de Na+ que provocan no supera el 5%, pero esta acción
diurética puede ser mayor cuando existe hiperactividad del túbulo distal por hiperaldosteronismo
primario, o secundario a la acción de los diuréticos de asa. Su valor reside, sobre todo, en su
capacidad de interferir en los procesos de pérdida de K+.
Existen dos clases de ahorradores de potasio: a) los inhibidores de la aldosterona y los inhibidores
directos del transporte de Na+.
a) Inhibidores de la aldosterona
La espironolactona tiene una estructura similar a la aldosterona, y actúa inhibiendo de
manera competitiva, esteroespecífica y reversible la acción de la aldosterona al unirse al
receptor específico que se encuentra en las células epiteliales del túbulo distal. En
consecuencia, impiden que la aldosterona promueva la síntesis de proteínas necesarias para
facilitar la reabsorción de sodio.
b) Triamtereno y amiloride
Actúan a nivel del tubo contorneado distal y comienzo del conducto colector desde la
superficie luminar. Bloquean a los canales de Na+ que se encuentran en la membrana
luminar de las células principales, por donde penetra el ión a favor de gradiente
electroquímico creado por la bomba de Na+ situada en la membrana basolateral. El bloqueo
del canal hace que la membrana luminar pierda su potencial transmembrana y se
hiperpolarice; en consecuenciia se pierde la carga negativa intraluminal que hacía salir a los
cationes K+, H+, Ca+2, y Mg+2. De este modo, estos diuréticos inhiben la reabsorción de Na+
en grado muy moderado y reducen la secreción de K+.
BETABLOQUEADORES
Mecanismo de acción
Son capaces de bloquear a los receptores -1 y -2 adrenérgicos.
Las acciones producidas por los betabloqueadores son:
a) Disminuyen la fuerza de contracción (gasto cardiaco).
b) Disminuyen la frecuencia cardiaca.
c) Disminuyen la velocidad de conducción del impulso cardiaco.
d) Disminuyen la producción de renina.
e) Reducen el tono simpático.
f) Reducen la resistencia vascular periférica.
Existen dos entidades fisiopatológicas, que requieren el concurso de fármacos con acción
predominantemente renal. Estas son el edema y la diabetes insípida.
Edema
Consiste en la hinchazón de los tejidos blandos debida a expansión anormal del volumen de líquido
intersticial. El líquido de edema es un trasudado de plasma que se acumula cuando está
facilitado el movimiento de líquido desde el espacio vascular al intersticial. Para que
aparezca edema es necesaria la retención renal de sal y agua. La distribución del edema
puede ser una clave importante de su causa.
Edema localizado, limitado a un órgano o lecho vascular, fácilmente distinguible del edema
generalizado. El edema unilateral de una extremidad suele ser debido a obstrucción
venosa o linfática, también puede producirse por estasis de una extremidad inferior
paralizada.
Edema generalizado, hinchazón de los tejidos blandos de todas o la mayor parte de las regiones
corporales. La hinchazón bilateral de las extremidades inferiores, más pronunciada después de
permanecer varias horas de pie, y el edema pulmonar suelen ser de origen cardiaco.
F-CV3-3B-2 Rev. Enero 2011
El tratamiento esta orientado inicialmente a identificar la causa subyacente del edema, luego la
restricción de sal y el uso de diuréticos.
Diabetes insípida
Es un trastorno debido a una alteración de la secreción de hormona antidiurética, la función de esta
secreción es concentrar la orina y conservar de esta forma el agua. En la diabetes insípida central se
libera una cantidad insuficiente de vasopresina en respuesta a los estímulos fisiológicos.
El tratamiento esta orientado a la reposición hormonal, administrando vasopresina.
Diuréticos
Son fármacos que actúan sobre los túbulos renales y son utilizados en una diversidad de situaciones
clínicas, relacionadas con el metabolismo anormal de electrolitos y agua. Casi todos los diuréticos
ejercen sus efectos en la superficie luminal de las células del túbulo renal. Sus mecanismos de
acción incluyen las interacciones estereoselectivas con proteínas de transporte específicas de
membrana.
Existen diversos grupos de diuréticos, entre ellos tenemos:
Los inhibidores de la anhidrasa carbónica: acetazolamida.
La anhidrasa carbónica se encuentra en muchos sitios de la nefrona, incluyendo el citoplasma y las
membranas luminal o basolateral, y en los eritrocitos que se encuentran en los capilares periféricos.
El sitio en que predomina la anhidrasa carbónica es en la membrana luminal del túbulo proximal, en
donde esta enzima cataliza las reacciones de hidratación/deshidratación del CO 2 que intervienen en
la resorción del bicarbonato.
Los inhibidores de la anhidrasa carbónica producen diuresis por bicarbonato de sodio y una
reducción en las reservas totales del bicarbonato de sodio.
Los diuréticos de asa: furosemida, bumetanida, piretanida.
Estos agentes de corta acción inhiben la resorción de cloruro de sodio en la rama ascendente gruesa
del asa de Henle. Debido a la gran capacidad absortiva de cloruro de sodio de este segmento, los
agentes que actúan en este sitio, producen un efecto diurético mucho mayor que el observado con
cualquier otro grupo diurético.
Las tiazidas: hidroclorotiazida, benztiazida, bendroflumetiazida, otros.
Inhiben la reabsorción tubular de sodio y cloro, a nivel del túbulo contorneado distal aumentando de
esta manera la excreción de agua y sodio a este nivel.
Diuréticos ahorradores de potasio
Actúan a nivel del túbulo colector (donde se lleva a cabo el intercambio de iones sodio por los iones
potasio e hidrógeno por un intercambiador regulado por la aldosterona).
Experiencia
4.2. Competencia
Diseña y ejecuta una experiencia sobre medicamentos antihipertensivos que modifican el
volumen de diuresis actuando a nivel renal, e interpreta los efectos observados con el uso
de diversos diuréticos y antidiuréticos.
4.3. Material y Métodos
Modelo experimental : Rata (6)
Fármacos : Furosemida, 3 %
Acetazolamida, sol. 3%
Espironolactona, sol. 1.5%
Hidroclorotiazida 1.5%
Vasopresina, 1 U.I./mL
4.4. Procedimiento:
a) Dejar a 6 ratas en ayuno durante 12 horas previa a la prueba, sin privarles de agua.
b) Marcar y pesar a las ratas, luego realizar la administración de 50 ml/kg de agua tibia y
colocarlas en sus correspondientes jaulas de diuresis.
F-CV3-3B-2 Rev. Enero 2011
c) Luego de 20 minutos de la hidratación, administrar vía intraperitoneal a las ratas Nº 2,
3 y 4, los siguientes fármacos: furosemida 20 mg/kg, Hidroclorotiazida 10 mg/kg,
acetazolamida 20 mg/kg, espironolactona 12.5 mg/kg, y Vasopresina 1 U.I./kg
respectivamente.
d) Controlar cada 20 minutos el volumen de orina eliminado por cada rata.
e) Al final de la prueba pesar nuevamente cada rata.
4.5. Resultados:
Fármacos Peso (g) Diuresis (mL)
Basal Final 20’ 40’ 60’
Blanco
Furosemida
Hidroclorotiazida
Acetazolamida
Espironolactona
Vasopresina
4.6. Interpretación de los resultados observados:
F-CV3-3B-2 Rev. Enero 2011
CASO CLÍNICO: FÁRMACOS EN HTA
D.C. es un varón negro de 50 años es evaluado por el servicio de cardiología, le miden de rutina la
PA. D.C presenta una molestia tipo pesadez a nivel occipital, cefalea en la mañana´; con
diagnóstico de HTA desde hace 6 años y tratado con disminución de peso y dieta baja en sal. El
paciente tomó medicación por dos años, pero la suspendió por su voluntad. En los últimos 12 meses
aumentó aproximadamente 7 kg de peso. Presenta antecedentes de apendicectomía hace 30 años y
úlcera hace 10 años. Tiene antecedentes familiares, su padre tuvo HTA y falleció de infarto al
miocardio (IMA) a los 54 años de edad; su madre tuvo diabetes mellitus e HTA y fallecio de
accidente cerebro vascular (ACV) a los 65 años de edad. D.C. fuma cigarrillos desde hace 35 años y
piensa que su presión arterial se ha elevado por el estrés de su trabajo. Durante la semana pasada
ha tenido descanso médico (no asistió a su trabajo).
El examen físico revela un buen desarrollo, sobrepeso. Mide 5’9’’ y pesa 108 kg. Sus presiones
arteriales son las siguientes, sentado: 164/98 mm Hg (brazo izquierdo), 168/98 mm Hg (brazo
derecho); Parado: 162/98 mm Hg (brazo izquierdo) y 166/98 mm Hg (brazo derecho). Su pulso: 84
lat/min y regular. El examen fundoscópico revela moderado estrechamiento arterial, no
hemorragias o exudados. Los demás exámenes no son remarcables.
Los exámenes de laboratorio son: BUN: 24 mg/dL, creatinina séria: 1.7 mg/dL, glucosa 95 mg/dL,
K+: 4.0 mEq/L, ácido úrico 8.0 mg/dL, hematocrito: 42%, colesterol toral: 224 mg/dL, HDL: 37
mg/dL. Urianálisis: proteinuria: 1+, no glucosuria. Electrocardiograma y placa rayos X de tórax con
moderada hipertrofia ventricular.
Cuestionario
a) ¿Qué estado de HTA demuestra el paciente D.C.?
b) La historia del D.C. demuestra que tiene conceptos errados sobre HTA y mala interpretación
de su enfermedad. ¿Debería ser educado acerca de la etiología de la HTA? ¿Porqué?
c) ¿Qué adicional información sobre el estilo de vida debiera adquirir D.C?
d) ¿Qué evidencia de daño a órgano blanco manifiesta D.C. y éstos pueden ser reversibles con
el control de HTA?
e) ¿Qué factores de riesgo presenta tanto para HTA, como para ACV?
f) ¿Qué información acerca de su HTA, tratamiento y métodos que promuevan su cumplimiento
debe proporcionarse a D.C.
g) ¿Qué riesgos y complicaciones pueden surgir de la HTA no tratada, las que pueden
prevenirse con una terapia apropiada?
h) ¿Cuál es el objetivo del tratamiento de la HTA del D.C.?
i) ¿Sería mas apropiado reducir la presión diastólica a 80 mm Hg?
j) ¿Qué medidas no farmacológicas pueden implementarse para controlar la HTA?
k) ¿Cuáles son los principios importantes para el tratamiento de la HTA?
l) ¿Cuáles son los pasos individualizados de cuidado y que podrían ser utilizados en el manejo
de la HTA de D.C.?
m) ¿Qué categorías de fármacos antihipertensivos debe ser usado en el tratamiento de la HTA
de D.C. y cómo deben ser seleccionados?
n) ¿Qué diurético debe ser seleccionado para D.C. y que reducción de la HTA se podría
esperar?
o) ¿Cómo podría D.C. ser aconsejado acerca de su terapia diurética?
F-CV3-3B-2 Rev. Enero 2011
Después de tres semanas de tratamiento con hidroclorotiazida 25 mg QD (una vez al día), D.C.
regresa a la evaluación clínica, no presenta molestias, su cefalea ha desaparecido. Su PA: 152/94
mm Hg sin ortostasis. Su peso es de 106 kg, K+: 3.8 mEq/L, ácido úrico: 9.0 mg/ dL y los otros
valores de laboratorios son los mismos.
a) ¿Qué datos subjetivos y objetivos deben ser considerados para evaluar la eficacia y
seguridad de los diuréticos tiazídicos? ¿Cuál es su concepto acerca de los datos señalados
anteriormente?
b) ¿Cuál es el significado de hipokalemia inducida por diuréticos y son observados éstos en
D.C.?
c) Si se requiere suplemento de potasio para manejar hipokalemia inducida por diurético, ¿qué
opciones terapéuticas pueden ser utilizadas en forma ambulatoria?
d) ¿Cuál es el significado clínico de hieruricemia e hiperglicemia inducida por diuréticos?
¿Podrían estos efectos adversos (que fueron evidentes la última semana) ser controlados?
e) ¿Cuál es el significado de alteraciones de lípidos séricos inducidos por diuréticos, deberían
ser tratados?
f) ¿Qué otras anormalidades metabólicas deben ser monitoreadas, cuando se utilizan terapia
con diuréticos?
4.7. Cuestionario:
a) Interpretar los resultados observados con los medicamentos empleados en la
experiencia de diuresis y antidiuresis experimental.
b) Interprete las diferencias en acción diurética entre furosemida e hidroclorotiazida.
4.8. Fuentes de Información
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA Nº 05 (SEMANA 05)
INSUFICIENCIA CARDIACA EXPERIMENTAL
RESOLUCIÓN DE CASO CLÍNICO
5.1. MARCO TEÓRICO
Insuficiencia cardiaca
Es la situación clínica en la que el corazón es incapaz de mantener un volumen minuto adecuado en
relación al retorno venoso y a las necesidades tisulares.
En términos generales, la insuficiencia cardiaca es un síndrome complejo cuyas manifestaciones
clínicas son el resultado de las alteraciones de la regulación de la función ventricular y de la puesta
en marcha de los mecanismos de compensación del deterioro primario de la función cardiaca.
Es necesario tener conocimiento que la función ventricular depende de la interacción de cuatro
factores que regulan el volumen de sangre expulsado por el corazón (volumen minuto). Tres de ellos
(pre-carga, post-carga y contractilidad) modifican el volumen que expulsa el corazón en cada latido
(volumen de eyección), mientras que el cuarto, la frecuencia cardiaca, actúa directamente sobre el
volumen minuto.
La pre-carga o fuerza que distiende el miocardio antes de contraerse está representada por la
tensión de la pared ventricular al final de la diástole. La pre-carga depende de la volemia, del tono
venoso, de la distensibilidad ventricular y de la contribución de la aurícula al llenado ventricular.
La post-carga es la fuerza contra la que se contrae el músculo cardiaco, es decir, la fuerza que
debe desarrollar el ventrículo para abrir las válvulas sigmoideas y enviar la sangre a las arterias
aorta y pulmonar.
La contractilidad es la fuerza que desarrolla el corazón para contraerse. Este parámetro está
determinado por la concentración de calcio intracelular, el tono simpático o la angiotensina II.
La frecuencia cardiaca está determinada por el tono vegetativo, en el miocardio insuficiente
predomina la acción del simpático, produciéndose una taquicardia compensadora.
La insuficiencia cardiaca se puede tratar:
1. Mediante fármacos que aumentan la contractilidad (Fármacos inotrópicos positivos).
2. Fármacos que mejoran el rendimiento hemodinámico cardiaco por reducir la pre-carga
(diuréticos, vasodilatadores venosos) y/o la post-carga (vasodilatadores arteriales o
arteriovenosos), IECA
1. Fármacos Inotrópicos
a. Glucósidos digitálicos (cardiotónicos)
b. Inotrópicos no digitálicos.
Agentes adrenérgicos: Dobutamina, dopamina, adrenalina
Estimulantes de la adenilciclasa no adrenérgicos.
Nucleótidos cíclicos: Dibutiril-AMPc
Inhibidores de la fosfodiesterasa: Metilxantinas, anrinona.
2. Fármacos Vasodilatadores
3. Diuréticos
4. Inhibidores de la enzima convertidora de angiotensina
CARDIOTÓNICOS
Son un grupo de agentes farmacológicos utilizados en el control de la insuficiencia cardiaca;
también se les conoce como, Glucósidos Cardiotónicos. En el corazón insufiiente, éstos permiten
F-CV3-3B-2 Rev. Enero 2011
realizar el mismo trabajo con menor consumo de oxígeno o gasto de energía, o bien, un mayor
trabajo con el mismo consumo de oxígeno o gasto de energía.
Estos glucósidos se encuentran en diversas plantas, especialmente en las hojas de la Digitalis lanata
o Digitalis purpúrea, por lo que en forma genérica se les denomina también digitálicos. También se
encuentran en el estrofanto, la escila o adelfa.
Estos agentes actúan de manera directa sobre el miocardio, donde incrementan la contracción
intrínseca de la fibra muscular (inotropismo positivo) y modifican el resto de propiedades
fisiológicas del corazón en un mismo sentido y son de utilidad en el tratamiento de la insuficiencia
cardiaca congestiva.
Los glucósidos están formados por una aglicona o genina (constituida por un anillo esteroide
(ciclopentanoperhidrofenantreno) al que se une en la posición 17 un anillo lactónico no saturado
y una fracción glucídica (compuesta por una cadena de varios azúcares o desoxiazúcares. El enlace
glucosídico está situado en el carbono 3 del anillo esteroide.
Las geninas son las que poseen la actividad farmacológica básica, pero la fracción glucídica
contribuye a modificar la liposolubilidad, las características farmacocinéticas y potencia
farmacológica.
Efectos Farmacológicos y Tóxicos de los Digitálicos sobre el corazón
1. Aumento de la contractilidad y reducción de la frecuencia cardiaca.
2. Prolongación del periodo refractario del Sistema de Conducción aurículo ventricular.
3. Acortamiento del periodo refractario de la aurícula y del ventrículo.
4. Depresión temprana de la excitabilidad de la aurícula y tardía de la del ventrículo.
5. Exaltación del automatismo de los tejidos de la aurícula, del nodo A-V y del ventrículo.
6. Depresión temprana de la velocidad de conducción de la aurícula y tardía de la del ventrículo.
7. Depresión de la velocidad de conducción auriculoventricular.
Entre los glucósidos cardiotónicos tenemos: Digitoxina, digoxina, deslanósido, Ouabaína.
VASODILATADORES
Son fármacos que producen relajación de la musculatura lisa vascular.
Se ha señalado que la función ventricular depende de la actuación coordinada de cuatro factores:
precarga, postcarga, contractilidad y frecuencia cardiaca. Los vasodilatadores
constituyen otro enfoque en el tratamiento de la insuficiencia cardiaca, ya que
mejoran la función ventricular actuando sobre el componente vascular a través de la
dilatación venosa (reducción de la precarga) y/o arterial (reducción de la postcarga)
que producen.
Los vasodilatadores no modifican por sí mismos la contractilidad cardiaca: sin embargo al reducir el
trabajo y las demandas miocárdicas de oxígeno pueden indirectamente aumentar la contractilidad
miocárdica.
Los vasodilatadores venosos producen una acumulación de sangre en el territorio venoso,
reduciendo el volumen y la presión diastólica ventricular, la presión de la aurícula derecha y la
presión capilar pulmonar; como consecuencia mejoran los signos de congestión pulmonar y
sistémica y disminuyen la tensión de la pared ventricular durante la diástole, lo que a su vez reduce
el trabajo cardiaco, las demandas de oxígeno y la isquemia cardiaca.
Los vasodilatadores arteriales disminuyen la postcarga, al reducir las resistencias vasculares
periféricas; como consecuencia aumentan el volumen sistólico y el volumen minuto y disminuyen el
consumo miocárdico de oxígeno. Además al aumentar la eyección del ventrículo izquierdo pueden
disminuir la presión diastólica ventricular y el tamaño del ventrículo.
Experiencia
5.2. Competencia
F-CV3-3B-2 Rev. Enero 2011
Diseña y ejecuta experiencias con el uso de digitálicos y estimulantes cardiacos e interpreta
los efectos observados sobre las propiedades electrofisiológicas del corazón sano y con
insuficiencia inducida en sapo.
F-CV3-3B-2 Rev. Enero 2011
5.3. Material y Métodos
Modelo experimental : Sapo
Fármacos : Deslanósido 0.02%
Pentobarbital sódico sol. 1%
Equipos : Equipo para disección
Miógrafo
Quimógrafo
5.4. Procedimiento
a) Inmovilizar a un sapo por destrucción medular y colocarlo en un soporte apropiado, en
posición de cúbito dorsal, fijando sus extremidades con alfileres en forma divergente.
b) Con una pinza se levanta la piel sobre el esternón, cortar el pliegue longitudinal
cutáneo, seccionar transversalmente el xifoesternón y luego a todo el largo, evitando
lesionar la vena abdominal.
c) Liberar al corazón del pericardio que lo recubre.
d) Aislar la vena abdominal e inyectar en ella 0.1 mg del deslanósido, observar los
resultados por 15 minutos, luego inyectar por igual vía 3 mg de pentobarbital sódico y
observar por 5 minutos, a continuación administrar por la misma vía 0.1 mg de
deslanósido. Observar.
Observar y comparar los resultados obtenidos.
5.5. Resultados:
Efectos (Fuerza de contracción, frecuencia cardiaca y tamaño cardiaco)
Efectos Deslanó Efectos Pentobar Efectos Deslanó Efectos Adrena- Efectos
Sapos basales sido bital sido lina
1
-- --
2
-- -- -- --
5.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
5.7. Cuestionario:
a) Interpretar los efectos observados con el uso del pentobarbital, deslanósido, y
adrenalina en la experiencia señalada.
b) Evalúa los efectos observados con deslanósido y adrenalina en la experiencia y
compárelos con los teóricos; justifique sus usos en la insuficiencia cardiaca congestiva.
c) Evalúa los efectos de acumulación del deslanósido y sus consecuencias.
5.8. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 06 (SEMANA 06)
FÁRMACOS EN ANGINA DE PECHO
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
6.1. Marco Teórico: ANGINA DE PECHO
Uno de los principales síntomas que se puede originar en el aparato cardiovascular es el
dolor coronario. Las evidencias sostienen la idea que este dolor se debe a una isquemia
relativa del miocardio (un menor aporte de oxígeno en relación a las demandas); además de
la isquemia relativa, se presume que las terminaciones nerviosas aferentes sean activadas
por sustancias derivadas de esta isquemia.
Habitualmente el dolor se presenta en individuos mayores de 40 años, preferentemente en
hombres.
El carácter clínico típico o clásico fue insuperablemente descrito en 1768 por Williams
Heberden, quien lo denomino angina pectoris, considerando la sensación de opresión que
experimenta el que lo padece.
La angina de pecho se caracteriza por:
1. Dolor fundamentalmente central y
retroesternal, no muy bien delimitado.
2. Con tendencia a irradiarse hacia los lados,
cuello o mandíbula; hacia el hombro o miembro cubital del miembro superior izquierdo
o a otras localizaciones.
3. Uniformemente opresivo, más rara vez
quemante.
4. Duración de algunos minutos (2 a 5 minutos, si
el factor precipitante es eliminado).
5. El dolor está asociado al esfuerzo, emoción, o
ambos.
6. Entre los factores que alivian el dolor, se
encuentran: la quietud, el alcohol y la trinitrina. También se ha señalado que la
compresión del seno carotídeo, al reducir la frecuencia cardiaca, produce rápido alivio.
Algo similar ocurre con la maniobra de Valsalva.
7. Otros síntomas que acompañan son: angustia,
debilidad, leve dificultad para respirar, palidez, sudor, eructos.
CLASIFICACIÓN
La angina de pecho puede clasificarse, según la forma de presentación en tres grupos:
a) Angina de esfuerzo: el dolor se desencadena por ejercicios físicos, emociones u otras
circunstancias que aumentan la demanda de oxígeno por el miocardio. Existen cuatro
grados (del I al IV) de acuerdo a la gravedad.
b) Angina de reposo: ocurre en forma espontánea, sin relación con esfuerzos;
aparentemente se debe a un vasoespasmo coronario que reduce el aporte de oxígeno al
miocardio (ej. la angina variante o de Prinzmetal).
c) Angina mixta: coexisten las dos anteriores sin predominio claro de ninguna de ellas.
Y según su forma evolutiva en:
a) Angina estable: cuyas características clínicas no han variado en el último mes; suele
tratarse de una angina de esfuerzo de larga evolución.
b) La angina inestable: es a que ha aparecido o agravado en los últimos 30 días; por lo
general se debe a un agravamiento agudo de la irrigación cardiaca por vasoespasmo,
trombosis coronaria incompleta u otra causa. El término inestable señala que la
evolución del paciente es imprevisible.
F-CV3-3B-2 Rev. Enero 2011
MECANISMOS DE LA PRODUCCIÓN DE LA ANGINA DE PECHO
1) En condiciones basales el corazón extrae gran parte del oxígeno (65%-75%)
contenido en la sangre coronaria que lo irriga. Cuando existe un aumento del trabajo
cardiaco, se incrementan los requerimientos miocárdicos de oxígeno; estos mayores
requerimientos no pueden satisfacerse exclusivamente con una extracción adicional del
oxígeno sanguíneo, por lo que es preciso aumentar el riego coronario.
2) En un individuo normal el flujo sanguíneo coronario puede incrementarse de 4 a 6
veces si es necesario; por ello tanto en condiciones basales, como cuando hay aumento de
trabajo cardiaco, existe un perfecto equilibrio entre la demanda de oxígeno por el
miocardio y el aporte de éste por la circulación coronaria.
3) En los individuos normales el riego sanguíneo de las distintas regiones cardiacas es
heterogéneo, y comparativamente existe una menor irrigación de la región subendocárdica
que de la subepicárdica; esto se debe a que durante la sístole todo el músculo cardiaco se
contrae hacia el centro del ventrículo, lo que genera un gradiente de presión
intramiocárdica, y así, la presión en el área subendocárdica es mucho mayor que en la
región subepicárdica., y el flujo sanguíneo coronario en los vasos transmurales y
subendocárdicos es mínimo.
4) Para compensar esta relativa isquemia subendocárdica causada por la contracción
cardiaca, durante la diástole se pone en marcha un mecanismo autorregulador, que
favorece una vasodilatación coronaria subendocárdica y genera un mayor aporte sanguíneo a
esta zona que a la subepicárdica.
5) En cualquier caso, a pesar de este mecanismo compensador, los aumentos de la
demanda o las disminuciones de la oferta de oxígeno al corazón podrán causar alteraciones
isquémicas, más fácilmente y en mayor medida en la zona subendocárdica.
6) En el ataque anginoso se produce una isquemia miocárdica transitoria, como
consecuencia de un desequilibrio entre el aporte y la demanda de oxígeno cardiacos; este
desequilibrio se debe fundamentalmente a una disminución patológica de la oferta, como
consecuencia de alteraciones graves en la circulación coronaria, siendo la causa más
frecuente (de disminución de riego sanguíneo coronario) la aterosclerosis.
7) Las placas ateromatosas, al obstruir la circulación, impiden que se produzca un
aumento del riego coronario suficiente para compensar los mayores requerimientos
ocasionados por situaciones de esfuerzo.
8) Raramente el riego sanguíneo se reduce por vasoespasmos coronarios que pueden
provocar ataques anginosos en situaciones de reposo.
9) En determinados individuos la aterosclerosis y el vasoespasmo pueden coexistir en
la génesis del ataque anginoso.
MECANISMOS ANTIANGINOSOS DE LOS FÁRMACOS
1) Los fármacos antianginosos carecen de actividad analgésica propiamente dicha,
pero suprimen el dolor anginoso ya establecido y previenen las crisis anginosas porque
restablecen el equilibrio entre la demanda y la oferta de oxígeno en el miocardio , debido a
la capacidad que tienen estos agentes para controlar alguno o varios factores que controlan
dicho equilibrio.
2) La demanda de oxígeno miocárdica es directamente proporcional a la frecuencia
cardiaca, la contractilidad del miocardio y la tensión de la pared ventricular durante la
sístole. A su vez los valores de estas variables dependen de factores neurohumorales
(principalmente tono simpático cardiaco) y la cuantía del retorno venoso y de la presión
arterial.
3) Entonces, los fármacos ANTIANGINOSOS que reduzcan los valores de la frecuencia,
contractilidad cardiaca, retorno venoso y la presión arterial podrán disminuir la demanda
de oxígeno por el miocardio y ejercer un efecto antianginoso.
4) La oferta de oxígeno al miocardio depende del contenido arterial de oxígeno, de su
capacidad para disociarse de la hemoglobina y del flujo sanguíneo coronario. Este último
está determinado principalmente por el calibre coronario, la duración de la diástole (ya que
la compresión de los vasos intramurales y del plexo subendocárdico durante la sístole
reduce el flujo transmural coronario) y el gradiente de perfusión coronario (determinado
por la diferencia entre la presión telediastólica del ventrículo y la presión diastólica
aórtica).
F-CV3-3B-2 Rev. Enero 2011
5) Los fármacos ANTIANGINOSOS podrán aumentar la oferta de oxígeno al miocardio al
inhibir el vasoespasmo coronario, incrementar la duración de la diástole (y, por tanto, la
distribución transmural de flujo coronario) y/o reducir la presión telediastólica
ventricular, con el consiguiente aumento del gradiente de perfusión.
CLASIFICACION DE LOS ANTIANGINOSOS
1. Los vasodilatadores (nitratos y nitritos): nitroglicerina, dinitrato de
isosorbide, 5-mononitrato de isosorbide, nitrito de amilo y otros.
2. β-Bloqueadores adrenérgicos.
3. Antagonistas del calcio.
4. Otros antianginosos: molsidomina, amiodarona.
EXPERIENCIA
6.2. COMPETENCIA:
Diseña y ejecuta una experiencia sobre angina de pecho inducida, e interpreta los efectos
observados en el modelo biológico.
6.3. MATERIALES Y MÉTODOS
6.4. PROCEDIMIENTO
6.5. RESULTADOS
6.6. INTERPRETACIÓN DE LOS RESULTADOS
6.7. FUENTES DE INFORMACIÓN RECOMENDADA
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 07 (SEMANA 07)
FÁRMACOS EN INFARTO AGUDO DEL MIOCARDIO
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
g.1. Marco Teórico
El infarto agudo de miocardio (IAM) es la situación en la que existe necrosis de las células del
miocardio como consecuencia de una isquemia prolongada Supone el 36% de los casos ingresados
con la sospecha diagnóstica de síndrome coronario agudo (SCA) 1, cuadro clínico ocasionado por la
enfermedad arterial coronaria en situación de inestabilidad, que se define desde diferentes
perspectivas relacionadas con aspectos clínicos, electrocardiográficos, bioquímicos y características
patológicas2,3. El IAM y la angina inestable son las categorías diagnósticas más importantes del
mismo.
Cuadro clínico
El síntoma isquémico característico es el dolor en el centro del tórax que se describe como algo que
aprieta o pesa, de intensidad severa, con una duración mínima de 20 minutos, que no se modifica
con los movimientos musculares, respiratorios ni con la postura, al que se pueden unir otro tipo de
síntomas como malestar, incomodidad, dolor en epigastrio, brazo, muñeca, mandíbula, espalda u
hombro, así como disnea, sudoración, náuseas, vómitos, mareo o una combinación de todos ellos 3,
aparece en reposo o en ejercicio, rara vez es punzante o muy localizado. Hay necrosis miocárdica
sin síntomas o con presentación atípica, como ocurre en diabéticos o ancianos. En ocasiones los
síntomas no son reconocidos y se confunden con otras entidades como indigestión o síndrome viral.
Cuando el dolor se refiere al abdomen se asocia con más frecuencia a nausea y vómito y es más fácil
confundirlo con enfermedad abdominal 2. El IAM puede ser causa de edema agudo de pulmón y de
muerte súbita.
Diagnóstico
Se debe hacer una valoración clínica cuidadosa y un electrocardiograma (ECG). El diagnóstico de
sospecha se realizará en presencia del cuadro clínico descrito, en ocasiones asociado a una historia
previa de cardiopatía isquémica, sexo masculino, edad avanzada y existencia de factores de riesgo
cardiovascular conocidos. Se valorará la situación como de alto riesgo en presencia de angina
progresiva, dolor prolongado ≥20 minutos, edema pulmonar, hipotensión y arritmias 1,3. El
diagnóstico del infarto de miocardio debe realizarse sin demora, la terapia precoz mejora de
manera decisiva el pronóstico.
El daño en el miocardio se puede estimar a través de los síntomas y de las pruebas completarías
como: ECG, marcadores de daño miocárdico, ecocardiograma, imágenes de perfusión miocárdica y
ventriculografía de contraste2.
Marcadores de daño miocárdico
Como resultado de la necrosis miocárdica aparecen en el torrente circulatorio las proteínas:
Myoglobina, Troponina T, Troponina I, Creatin Fosfo Kinasa (CPK) y Lactato deshidrogenasa (LDH).
Se realiza el diagnóstico de IAM cuando se elevan en sangre los marcadores más sensibles y
específicos de daño miocárdico: troponinas cardíacas y CPK-MB, que reflejan el daño en el
miocardio pero no indican su mecanismo de aparición, de tal manera que un valor elevado sin
evidencia clínica de isquemia nos obliga a buscar otras causas de lesión 2 .
F-CV3-3B-2 Rev. Enero 2011
Clasificación
Según la presentación clínica
← Síndrome coronario agudo sin elevación de ST (SCASET)
← Angina inestable
← Infarto de miocardio sin elevación de ST (NSTEMI)
La mayor parte de los casos de NSTEMI será un infarto de miocardio no Q
(NQMI)
Una proporción pequeña será un infarto con onda Q (QMI)
← Síndrome coronario agudo con elevación de ST (STEMI)
← La mayor parte de los casos de STEMI será un infarto de miocardio con onda Q (QMI)
← Una proporción pequeña será un infarto sin onda Q (NQMI)
Según el tamaño
← Microscópico: Necrosis focal
← Pequeño: afecta a una superficie inferior al 10% del tamaño del ventrículo izdo
← Medio: entre el 20% y 30% del ventrículo izdo
← Grande: superficie mayor del 30% del ventrículo izdo
Según la localización
← Anterior, lateral, inferior, posterior, antero septal.
← Puede estar afectada más de una zona.
Tratamiento
En todo paciente con dolor torácico se hará una historia clínica, un examen físico y un ECG
buscando el diagnóstico de un SCA. El diagnóstico temprano y el traslado urgente son claves para la
supervivencia. La terapia precoz mejora de manera decisiva el pronóstico.
Fase inicial extrahospitalaria
Monitorización siempre que sea posible. En las primeras horas más del 80% de los IAM presentan
arritmia, generalmente grave como la fibrilación ventricular o la taquicardia ventricular sin pulso,
causa principal de muerte en estas situaciones. La rápida realización de una cardioversión con un
desfibrilador contribuye a salvar vidas. Así pues, la monitorización y la preparación del desfibrilador
debe realizarse tan pronto se reciba al paciente 3[D]. Avisar al Centro Coordinador de Urgencias
(Teléfonos 061 y 112) solicitando una ambulancia medicalizada que traslade al paciente
monitorizado al centro hospitalario más próximo1[B].
Ácido acetilsalicílico 250-300 mgr. masticado (preferiblemente sin protección gástrica para mejorar
la absorción). Administrar de forma inmediata siempre que no existan contraidicaciones (úlcera
activa, alergia a la aspirina o anticoagulación)1,2,3,7 [A].
Nitroglicerina sublingual a dosis de 0,4-0,8 mgrs. que puede repetirse 3 ó 4 veces con intervalos de
5´. Es adecuado para la angina y la hipertensión no tiene un efecto significativo en la mortalidad 8
[D]. Contraindicado si existe hipotensión (TAS< 90 mmHg).
F-CV3-3B-2 Rev. Enero 2011
Cloruro mórfico con una dosis inicial de 2,5-5 mgrs. IV (o SC si no es posible la IV), puede repetirse
el tratamiento hasta 3 veces usando 2,5-5 mgrs. por dosis 4. Para su administración puede diluirse
una ampolla de 10 mgrs. (1 cc.) con 9 cc de suero fisiológico.
Oxígeno al 35% en pacientes con hipoxia (saturación de oxígeno <90%) o edema pulmonar [D]. No
existe evidencia de que la administración rutinaria de oxígeno a todos los pacientes con SCA mejore
los resultados clínicos y reduzca el tamaño del infarto. En los animales de experimentación se ha
demostrado que la oxigenoterapia puede limitar el daño miocárdico y reducir la elevación del ST 3.
Tratamiento hospitalario9
Ácido acetilsalicílico y Clopidogrel: Los pacientes con IAM se benefician de la asociación de 300 mg
de ácido acetil salicílico con 75 mg clopidogrel diariamente. Es más efectivo que la aspirina sola
usada en las 12 primeras horas tras el IAM [A] El tratamiento con aspirina debe ser mantenido a
largo plazo en todos los pacientes con SCA1,3[A].
Antagonistas de los receptores de la glucoproteina IIB/IIA: Administrados por vía intravenosa han
demostrado su utilidad en el tratamiento de los pacientes con SCA de alto riesgo, sobre todo si se
realiza intervención coronaria percutánea1,3[B].
Heparina de bajo peso molecular usada en las primeras 48 horas reduce las tasas de reinfarto en los
casos de SCA con cambios electrocardiográficos y elevación de marcadores cardíacos 3[A].
Betabloqueantes: Son los antianginosos de primera línea en el tratamiento del dolor en los
pacientes con SCA sin elevación del ST (SCASET) y en la prevención secundaria. Aunque en el STEMI
han demostrado que se produce una reducción de la mortalidad existe el riesgo del shock
cardiogénico. Son útiles en pacientes con hipertensión y taquicardia y en ausencia de bradicardia,
hipotensión o insuficiencia cardíaca. En los pacientes con SCA se valorará la utilización inmediata de
betabloqueantes por vía oral o intravenosa 3 [B]. Los pacientes con IAM deben recibir tratamiento a
largo plazo con beta bloqueantes3 [A].
Inhibidores de la enzima conversora de la angiotensia (IECA): Diferentes estudios han demostrado
su efecto beneficioso en pacientes con IAM independientemente de que tengan disfunción
ventricular o insuficiencia cardíaca, por estos motivos se recomiendan a todos los pacientes con IAM
de forma continuada [B]. En pacientes de alto riesgo se ha observado el beneficio que se obtiene al
introducirlos en las primeras 36 horas tras el infarto, por lo que se recomienda su utilización en
dicho período3[A].
Antagonistas de los inhibidores de la angiotensina: (ARA II) indicados en los pacientes que no
toleren los IECA por sus efectos secundarios (ocurre en el 30% de los casos). Los pacientes con IAM
complicado y disfunción ventricular izquierda o fallo cardíaco deben de iniciar el tratamiento a
largo plazo con ARA II si no toleran los IECA3[A].
Antialdosterónicos: Los pacientes con IAM y disfunción ventricular (fracción de eyección <40%) en
presencia de signos de insuficiencia cardíaca o diabetes deben iniciar tratamiento a largo plazo con
espironolactona3 [B].
Estatinas: Los estudios confirman que el inicio precoz del tratamiento con estatinas a dosis altas, es
seguro y beneficioso a corto plazo sobre la prevención de la isquemia recurrente y la
mortalidad10,11. Los pacientes con SCA antes de ser dados de alta en el hospital deben haber
iniciado tratamiento con estatinas. [B].
Nitratos: No han demostrado influencia en la reducción de la mortalidad. Su indicación actual es
para el tratamiento de los síntomas en relación con la isquemia y con la insuficiencia cardíaca en
fase aguda3.
Antagonistas del calcio: No han demostrado beneficio en los pacientes con IAM, por ello no se
recomienda su uso rutinario3.
Control de glucemia, los pacientes diabéticos con infarto de miocardio e hiperglucemia marcada
recibirán tratamiento intensivo para el control adecuado de la glucemia sobre todo en las primeras
24 horas1,3[B].
Intervención psicológica precoz
F-CV3-3B-2 Rev. Enero 2011
g.2. COMPETENCIA:
Diseña y ejecuta una experiencia en infarto agudo del miocardio (IMA) inducida, e
interpreta los efectos observados en el modelo biológico.
g.3. MATERIALES Y MÉTODOS
g.4. PROCEDIMIENTO
g.5. RESULTADOS
g.6. INTERPRETACIÓN DE LOS RESULTADOS
F-CV3-3B-2 Rev. Enero 2011
g.7. FUENTES DE INFORMACIÓN RECOMENDADA
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA Nº 8 (SEMANA 09)
COAGULACIÓN Y ANTICOAGULACIÓN EXPERIMENTAL
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
8.1. MARCO TEÓRICO
La hemostasia constituye el mecanismo fundamental de defensa que tiene el organismo para
impedir la pérdida de sangre después de la lesión de un vaso. La activación de este proceso
depende de la compleja interacción entre factores muy diversos:
a) La dinámica del flujo sanguíneo. b) Los componentes de la pared vascular, c) Las plaquetas.
Y d) Ciertas proteínas del plasma y de los tejidos.
El resultado fisiológico de esta interacción es la formación del tapón hemostático y del coágulo
sanguíneo, constituidos por una acumulación inicial de plaquetas y por la formación de una malla de
proteínas insolubles, la fibrina, que engloba a otros elementos formes de la sangre
La formación de fibrina se debe a la acción de una enzima proteolítica que alcanza un papel
esencial, la trombina.
Se requiere al mismo tiempo, mecanismos que controlen o equilibren la formación de fibrina. Para
ello el organismo dispone de dos líneas fundamentales de defensa:
La inactivación o inhabilitación de la trombina en el propio plasma por una serie de factores
endoteliales y plasmáticos, y
El proceso de la fibrinólisis que evita el desarrollo indefinido del trombo, como consecuencia de
la activación de una enzima fibrinolítica, la plasmina.
La pérdida de equilibrio entre estos dos mecanismos significa la aparición de cuadros patológicos:
La Diátesis Trombótica, arterial o venosa, según los condicionantes vásculo-sanguíneos que
entren en juego, y
La diátesis Hemorrágica.
La Coagulación de la sangre es un proceso caracterizado por una cascada de reacciones
proteolíticas, que terminan por convertir el fibrinógeno (proteína soluble del plasma), en fibrina
insoluble. Para ello, es preciso que actúe la enzima crítica, la trombina (factor II).
La iniciación del proceso requiere de un factor desencadenante, que puede ser variado. La ruptura
de la continuidad de la superficie endotelial estimula, por una parte la actividad plaquetaria, y son
las mismas plaquetas, las que liberan factores de la coagulación, que la inician en el ambiente
periplaquetario. Por
otra parte, el contacto del plasma con el colágeno de la pared vascular o con otra superficie no
natural provoca la activación de un conjunto de factores relacionados entre sí, como la calicreína,
el factor XII o factor Hageman, el cininógeno y el factor XI. El resultado final de este proceso inicial
ligado al contacto con una superficie es la formación del factor XI activado, que ya está
directamente implicado con el proceso de la coagulación en su vía intrínseca o propiamente
vascular.
Pero, además, la coagulación puede tener un inicio extravascular mediante la activación de factores
tisulares, que con el concurso de algunos factores de contacto, terminan por activar el factor VII, es
la llamada Vía Extrínseca.
F-CV3-3B-2 Rev. Enero 2011
ESQUEMA DE LA COAGULACIÓN SANGUÍNEA
Precalicreina
Cininógeno
Contacto
Calicreína
Cininógeno
Contacto
Factores tisulares
XII XIIa
Cininógeno
Contacto
XI XIa XIIa
XIa
IXa
IX IXa VIIa VII
Xa Xa
Plaquetas FL FL tisular
IIa Ca++ Ca++
VIII VIIIa Proteina tisular
X Xa
Tis
FL
Plaquetas
Ca++
IIa
Va
V XIII
TROMBINA Ca++
PROTROMBINA
XIIIa
FIBRINOGENO Fibrina Fibrina
soluble insoluble
F-CV3-3B-2 Rev. Enero 2011
Los modificadores de la coagulación sanguínea se dividen en:
1. Agentes Procoagulantes o Hemostáticos
a. Agentes utilizados por su acción vascular
Que actúan por taponamiento hemostático: esponjas de gelatina o de fibrina, trombina
de plasma bovino.
Que actúan produciendo vasoconstricción :adrenalina, serotonina.
De acción inespecífica :etamsilato, dobesilato, monosemicarbazona de
adrenocromo.
b. Agentes utilizados por su acción plaquetaria
desmopresina.
c. Agentes utilizados por su acción sobre la coagulación
Déficit de factores concretos: factor VIII
Vitamina K
d. Agentes inhibidores de la fibrinólisis
Aprotinina, ácido aminocaproico, ácido p-aminobenzoico, ácido tranexámico.
2. Agentes Trombolíticos
a. Inespecíficos: Estreptoquinasa, uroquinasa.
b. Específicos : Activador tisular del plasminógeno, complejo activador acilado SK-
plasminógeno, prouroquinasa.
3. Fármacos Anticoagulantes
a. Heparinas
Heparina clásica o no fraccionada.
Heparinas de bajo peso molecular.
Heparinoides.
b. Anticoagulantes orales
Warfarina
Fenindiona.
4. Antiagregantes Plaquetarios
a. Que intervienen la vía del Fosfoinositol/tromboxano
Aspirina, triflusal, ridogrel.
b. Que estimulan la vía del AMPc
Epoprostenol, dipiridamol
c. Otros
Ticlopidina, pentoxifilina, antioxidantes.
F-CV3-3B-2 Rev. Enero 2011
Experiencia 1
8.2. Competencias
Diseña y ejecuta una experiencia “in vivo” sobre fármacos que modifican el tiempo de
coagulación, interpretando adecuadamente los correspondientes efectos observados.
8.3. Material y Métodos
Modelo experimental : Conejo (2)
Fármacos : Heparina 2%
Protamina 2%
8.4. Procedimiento
a) Seleccionar, marcar y pesar dos conejos (de aproximadamente 2 kg), y determinar en
condiciones basales su tiempo de coagulación por el método de Lee-White.
b) Luego al conejo Nº 2, administrar heparina 5 mg/kg, vía i.v. y luego determinar el tiempo
de coagulación a los 5’ y 10’. El conejo Nro. 01 es el control.
c) Después, administrar protamina 5 mg/kg, vía i.v., luego determinar el tiempo de
coagulación a los 5’ y 10’
8.5. Resultados
Conejo Fármacos Tiempo de coagulación
BASAL 1’ 2’ 5’ 10´ 20’ 30’
1 --
2 Heparina --
+ Protamina -- --
8.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
Experiencia 2
8.7. Competencias
Diseña y ejecuta una experiencia “in vitro” sobre fármacos que modifican el tiempo de
coagulación, interpretando adecuadamente los correspondientes efectos observados.
8.8. Material y Métodos
Modelo biológico : hombre
Fármacos : Heparina, sol. 5%
Warfarina, sol. 1%
Citrato de sodio, sol. 20%
Oxalato de sodio, sol. 2%
Cloruro de calcio, sol. 10%
8.9. Procedimiento
Determinación del tiempo de coagulación por el método de Lee-White.
a) Seleccionar y numerar 06 tubos de prueba, luego colocar a los Nº 2 al 6 las siguientes
sustancias: heparina (0.05 mL), warfarina (0.1 mL), citrato de sodio (0.1 mL), citrato de sodio
(0.1 mL), oxalato de sodio (0.1 mL).
b) Extraer sangre (realizando la técnica correspondiente) de la vena basílica de un voluntario
colocando a todos los tubos 1 mL de sangre. Y al tubo Nº 5 agregar cloruro de calcio (0.1 mL).
c) Medir el tiempo de coagulación al 1’, 3’, 5’, 10’, 15’, 20’, 25’ y 30’.
8.10. Resultados:
Tubo Fármacos Tiempo de coagulación
1’ 3’ 5’ 10’ 15’ 20’ 25’ 30’
1
2 Heparina
3 Warfarina
4 Citrato sodio
5 Citrato sodio
+ CaCl2
6 Oxalato sodio
8.11. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
8.12. Cuestionario:
Interpretar lo siguiente:
a) Participación de calcio en el mecanismo de coagulación.
b) La importancia de los mecanismos de activación del factor X y del factor II.
c) La modificación de la coagulación sanguínea con el uso de heparina, warfarina,
protamina, vitamina K y las sales de calcio in vitro.
8.13. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 09 (SEMANA 10)
INVESTIGACIÓN DE FÁRMACOS EN ANEMIAS
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
9.1. Marco Teórico: ANEMIAS
Anemias son trastornos caracterizados por la producción disminuida de eritrocitos (o hemoglobina),
es prematura la destrucción de eritrocitos o a sido excesiva la pérdida de sangre generalmente con
el resultado de que una o más de las medidas cuantitativas de los eritrocitos (hemoglobina,
hematocrito, número de eritrocitos) son inferiores a lo normal.
Clasificación
Anemias por pérdida excesiva de sangre
Anemia post hemorrágica aguda.
Anemia post hemorrágica crónica.
Anemias por producción deficiente de eritrocitos
Deficiencia de los factores relacionados con la eritropoyesis.
Deficiencia de hierro.
Deficiencia de cobre.Deficienca de vitamina B12 y ácido fólico (anemia
perniciosa y anemia megalobásticas relacionadas).
Deficiencia por ácido ascórbico.
Anemias por insuficiencia de la médula ósea
Anemia hipoplásica y aplásica.
Anemias sideroblásticas.
Anemias por destrucción excesiva de los eritrocitos (anemias hemolíticas)
Anemias debidas a defectos eritrocíticos intrínsecos.
Anemias debidas a factores eritrocíticos extrínsecos.
Anemias por producción disminuída y destrucción aumentada de eritrocitos
Síntesis defectuosa de hemoglobina (Hb)
Hemoglobinopatías (anemias de células falciformes y trastornos
relacionados).
Talasemias.
Anemia asociadas a enfermedades crónicas (infección, cáncer, artritis reumatoide)
Anemia por nefropatías.
Anemia por hepatopatías.
Anemia del mixedema.
Anemia por invasión de la médula ósea (anemias mieloptísicas)
Síntomas Generales
Las manifestaciones clínicas de las anemias están relacionadas directamente con su gravedad y
agudeza, porque son causadas por hipoxia tisular y representan las respuestas cardiovasculares
compensatorias.
Los síntomas subjetivos que están relacionados con la anemia grave son:
Debilidad, vértigo, dolor de cabeza, tinnitus, sensación visual de moscas
volantes.
Fatigabilidad fácil, somnolencia, irritabilidad y conducta psicótica.
Ocasionalmente amenorrea, pérdida de la líbido o fiebre ligera.
Pueden presentarse síntomas gastrointestinales o insuficiencia cardiaca
congestiva.
En algunas anemias hay ictericia y esplenomegalia.
Consideraciones terapéuticas generales
El tratamiento de la anemia debe ser específico. La respuesta a la terapia
específica es parte de la evaluación diagnóstica.
Después de haber conseguido valores de laboratorio normales y haber
corregido la causa subyacente, puede ser necesario continuar la terapia durante algunas
semanas (deficiencia de ácido fólico) o meses (deficiencia de hierro) para reponer las reservas.
F-CV3-3B-2 Rev. Enero 2011
En algunos casos, la causa de la deficiencia no es reversible (anemia perniciosa, telangiectasia
hemorrágica hereditaria) y la terapia de sustitución dura toda la vida.
La transfusión de sangre se reserva para pacientes con hemorragia activa,
con hemorragia reciente y que se espera que continúe, o cuando el enfermo tiene signos y
síntomas de hipoxemia.
Anemia por deficiencia de hierro
Anemia por pérdida crónica de sangre, anemia microcítica hipocrómica; clorosis, anemia
hipocrómica del embarazo, la infancia y la niñez.
Se caracteriza por eritrocitos pequeños, pálidos y depleción de las reservas de hierro.
Anemia por deficiencia de vitamina B12 y ácido fólico
La deficiencia de vitamina B12 o de ácido fólico pueden ocasionar una
síntesis defectuosa de nucleoproteína.
Para que las células se dividan, tiene que haber una duplicación del ADN, la
nucleoproteína de los cromosomas. La coenzima B12 y el ácido fólico son necesarias para la
síntesis del ADN. Si una de estas dos sustancias está deficiente, se altera la síntesis de la
nucleoproteína, teniendo por resultado una anemia caracterizada por hematopoyesis
megaloblástica con producción de eritrocitos aumentados de tamaño (macrocitos), ovales, con
un tiempo de vida anormalmente corto.
Los estudios sobre el ciclo de hierro indican una actividad aumentada de la
médula ósea, signo de dispoyesis en la que muchas células son destruidas antes de que puedan
circular.
Anemia por deficiencia de vitamina B12
La vitamina B12 se encuentra en la carne y en otros alimentos proteínicos
animales. La absorción tiene lugar en el ìleon terminal y exige la presencia intacta del “factor
intrínseco”, sustancia específica secretada por las células parietales gástricas en el fundus y en
el cuerpo del estómago, para transportar la vitamina a través de la mucosa intestinal. La
vitamina B12 se almacena en el hígado en cantidades suficientes para mantener necesidades
fisiológicas durante 3 a 5 años.
El principal mecanismo fisiopatológico es la absorción disminuída de
vitamina B12.
En la anemia perniciosa que es la causa más común de deficiencia de
vitamina B12, la mucosa gástrica atrófica deja de secretar factor intrínseco.
Síntomas
En la mayoría de pacientes se desarrolla de manera insidiosa y progresiva
conforme las grandes reservas hepáticas de B12 se deplecionan.
Ocasionalmente pueden observarse esplenomegalia y hepatomegalia.
Pueden presentar diversas manifestaciones gastrointestinales: anorexia,
estreñimiento y diarrea intermitentes y dolor abdominal mal localizado.
La glositis descrita corrientemente como “quemazón de la lengua” es un
síntoma precoz.
Es común la pérdida de peso.
Puede haber compromiso neurológico: parestesias transitorias de
extremidades superiores, neuropatía periférica, irritabilidad, ligera depresión, delirio,
paranoia.
Alteración de la médula espinal comienza en la columna dorsal, con pérdida
de la sensación de vibración en las extremidades inferiores y del sentido de posición y ataxia;
sigue la participación de la columna lateral, con espasticidad, reflejos hiperactivos y signo de
Babinski.
Puede haber deficiencias endocrinas, especialmente hipotiroidismo e
insuficiencia adrenal.
Tratamiento
La cantidad de vitamina B12 presenta relación con la cantidad administrada.
La terapia tiene relación con la restauración de las reservas hepáticas,
normalmente de 3,000 μg a 10,000 μg, y la retención de vitamina B12 disminuye conforme se
consigue la restauración de las reservas.
F-CV3-3B-2 Rev. Enero 2011
La dosis recomendada es de 1000 μg IM, 2-4 veces por semana.
La corrección se consigue generalmente a las 6 semanas; la mejoría neural
estable puede demorar 18 meses.
La terapia de mantenimiento con vitamina B12 (100 μg/mes IM) debe
administrarse toda la vida, excepto si se corrige en mecanismo fisiopatológico de la deficiencia.
Anemia por deficiencia de ácido fólico
El ácido fólico abunda especialmente en las verduras, levadura, hígado y las
setas (aparato esporífero de los hongos).
Se absorbe en el duodeno y en la parte alta del yeyuno. El depósito hepático
de folato es limitado proporcionando una reserva para sólo 2-4 meses en ausencia de aporte.
El ácido ascórbico es esencial para la reducción del ácido fólico a su forma
metabólicamente activa: el ácido tetrahidrofólico.
El alcohol interfiere con el metabolismo intermediario del ácido fólico; es
por ello que los alcohólicos crónicos tienden a desarrollar tienden a desarrollar anemia
macrocítica.
Los niños pueden tener deficiencia en vitamina C, y pueden presentar
anemia megalobástica de la infancia.
Síntomas
Hay pocos síntomas y signos físicos además de anemia, palidez, fatiga,
glositis.
No hay anormalidades neurológicas.
Los exámenes de sangre periférica y de la médula ósea muestran dispoyesis
megaloblástica característica.
Tratamiento
Administración de ácido fólico vía oral 1 mg/día
HIERRO
(Las sales de hierro: fumarato ferroso, gluconato ferroso, sulfato ferroso, ferrodextrán)
Mecanismo de acción
El hierro es un componente esencial en la formación fisiológica de
hemoglobina, y es necesario en cantidades adecuadas para una efectiva eritropoyesis y la
capacidad resultante para transportar oxígeno de la sangre.
El hierro tiene una función similar en la producción de la mioglobina;
también participa como cofactor de varias enzimas esenciales.
El hierro administrado por vía oral (en alimentos o como suplemento) pasa a
través de las células mucosa en estado ferroso y se une a la proteína transferrina; en esta forma
el hierro es transportado en el organismo a la médula ósea para la producción de glóbulos rojos.
El ferrodextrán se absorbe desde el lugar de inyección a los capilares y al
sistema linfático, se elimina del plasma mediante células del sistema retículoendotelial y se
disocia en hierro y en dextrán. El hierro liberado se une inmediatamente a subunidades
proteicas para formar hemosiderina o ferritina o, en un menor grado transferrina.
El hierro unido a proteínas rellena eventualmente los depósitos de hierro
vacíos y se incorpora a la hemoglobina.
Efectos adversos
Sólo para uso oral
Frecuentemente: dolor, calambres o inflamación abdominal o gástrica.
Infrecuentemente: dolor de garganta o pecho, heces con sangre fresca o digerida (posiblemente
irritación por contacto o contacto con zonas ulcerosas o concentración elevada de hierro en una
zona), estreñimiento, orina oscurecida, pirosis, coloración de los dientes (con formas líquidas).
Indicaciones
Anemia por deficiencia de hierro (profilaxis y tratamiento); pueden
recomendarse en dieta inadecuada, mala absorción, embarazo , perdida de sangre, infancia.
F-CV3-3B-2 Rev. Enero 2011
VITAMINA B12
La vitamina B12 es un término genérico con el que se designa a un grupo de compuestos
conteniendo cobalto, denominados cobalaminas los cuales presentan un grupo macrocítico
tetrapirrólico unido al dimetilbenzimidazolil nucleótido. Un grupo R variable unido al átomo de
cobalto central determina el tipo de vitamina B12 congénere (grupo ciano en cianocobalamina;
hidroxi en hidroxocobalamina; metilo en metilcobalamina, entre otros).
Tanto la vitamina B12 y ácido fólico son importantes para la síntesis de nucleótidos de purina y
metabolismo de algunos aminoácidos. Son esenciales para el crecimiento y replicación.
Una deficiencia de vitamina B12 o folatos produce un defecto en la síntesis de ADN y anormalidades
de la maduración celular.
La cianocobalamina e hidroxocobalamina son formas farmacéuticas de vitamina B12 usados
clínicamente para tratar la deficiencia de vitamina B12. Las dos formas activas de coenzima
intracelular de vitamina B12 son la metilcobalamina y deoxiadenosil cobalamina, los cuales son
sintetizados in vivo de hidroxocobalamina o cianocobalamina. La cobalamina presente en el plasma
es la metilcobalamina.
Mecanismo de acción
La vitamina B12 actúa como coenzima en varias funciones metabólicas,
incluyendo metabolismo de grasas y carbohidratos y síntesis de proteínas.
Es necesaria en el crecimiento, replicación celular, hematopoyesis y síntesis
de nucleoproteínas y mielina; debido en gran parte a sus efectos sobre el metabolismo de
metionina, ácido fólico y ácido malónico.
Efectos adversos
Diarrea, prurito; rash cutáneo, sibilancias (reacción anafiláctica después de
la administración parenteral).
Indicaciones
Anemia perniciosa (por falta o inhibición del factor intrínseco), anemia
megaloblástica o macrocítica.
Profilaxis y tratamiento por deficiencia de vitamina B12.
Dietas no habituales (para adelgazamiento)
ACIDO FOLICO
El ácido fólico (ácido pteroilglutámico) después de su absorción es reducida a ácido tetrahidrofólico
el cual actúa como aceptor de unidades de un carbón. Estos se unen a diferentes posiciones a 6
formas de principales congéneres y cada uno de ellos presenta un rol principal en el metabolismo
intracelular.
Las coenzimas formadas del ácido fólico son instrumentos en los siguientes metabolismos
intracelulares: conversión de homocisteína a metionina; conversión de serina a glicina; síntesis de
timidilato, metabolismo de histidina, síntesis de purinas y utilización o generación de formiato.
Mecanismo de acción
El ácido fólico después de convertirse en ácido tetrahidrofólico es necesario para la eritropoyesis
normal y para la síntesis de nucleoproteínas.
Efectos adversos
Raramente: fiebre, rash cutáneo (reacción alérgica).
Indicaciones
Profilaxis y tratamiento de la deficiencia vitamínica.
En anemia megaloblástica y macrocítica, y glositis.
Dietas no habituales (para adelgazamiento)
F-CV3-3B-2 Rev. Enero 2011
F-CV3-3B-2 Rev. Enero 2011
EXPERIENCIA
9.2. COMPETENCIA:
Diseña y ejecuta una experiencia con fármacos que mejoran los niveles de hemoglobina,
interpretando los resultados observados.
9.3. MATERIALES Y MÉTODOS
9.4. PROCEDIMIENTO
9.5. RESULTADOS
9.6. INTERPRETACIÓN DE LOS RESULTADOS
9.7. CUESTIONARIO
Interpretar los efectos observados en los niveles de hemoglobina, hematocrito y/o
recuento de hematíes con el uso de sales ferrosas, ácido ascórbico, ácido fólico y
vitamina B12
F-CV3-3B-2 Rev. Enero 2011
9.8. FUENTES DE INFORMACIÓN RECOMENDADA
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed.
Científicas y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 10 (SEMANA 11)
ACTIVIDAD ANTIBACTERIANA EXPERIMENTAL
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
10.1. MARCO TEÓRICO
El aumento progresivo en el número de antibacterianos disponibles implica con frecuencia, una
mayor dificultad de su empleo, ya que exige conocer con detalle sus diversos aspectos: actividad
antibacteriana, características farmacocinéticas, toxicidad, entre otros factores. Es por ello, que
muchas veces se utilizan en forma incorrecta, y como consecuencia, disminuye su eficacia
terapéutica, se favorece la aparición de resistencias bacterianas, aumenta la incidencia de
reacciones adversas medicamentosas (RAM), sobre todo las sobreinfecciones, y se incrementa los
costos de los tratamientos, al emplear muchas veces en forma innecesaria y al amparo de una
intensa promoción por parte del marketing de las industrias farmacéuticas.
Los antibacterianos son medicamentos útiles en el control y tratamiento de las infecciones
provocadas por bacterias.
CLASIFICACIÓN DE LOS FÁRMACOS ANTIBACTERIANOS
Según su actividad antiinfecciosa
a) Bactericidas: Producen la muerte de los agentes infecciosos. Entre estos se encuentran: los -
lactámicos, aminoglucósidos, rifampicina, vancomicina, polimixinas, fosfomicina, quinolonas,
bacitracina y nitrofurantoínas.
b) Bacteriostáticos: Inhiben el crecimiento bacteriano, aunque el microorganismo permanece
viable, de tal modo que si el antibiótico se suspende puede recuperarse y volver a multiplicarse.
Por ello, es necesario la participación de los mecanismos de defensa del huésped. Entre estos se
encuentran: Cloranfenicol, lincosaminas, eritromicinas, sulfamidas, trimetoprim y tetraciclinas.
Según su espectro de actividad antiinfecciosa
a) De espectro reducido: son aquellos que actúan contra un escaso grupo de gérmenes. Por
ejemplo: penicilinas, cefalosporinas, rifampicina, vancomicina, aminoglucósidos y otros.
b) De espectro ampliado: son aquellos que además de ser eficaces contra gram positivos,
también presentan actividad contra un grupo significativo de gérmenes gram negativos. Por
ejemplo: ampicilina, amoxicilina.
c) De amplio espectro: son activos contra múltiples grupos de gérmenes (gram positivos y gram
negativos, ricketsias, espiroquetas) abarcando un gran número de especies de los mismos.
Ejemplo: tetraciclinas, fenicoles, macrólidos, lincosaminas, entre otros.
Según su mecanismo de acción antibacteriana
a) Inhibición de la síntesis de la pared celular, en fases diversas de la síntesis: beta-
lactámicos (penicilinas, cefalosporinas, imipenem, aztreonam), fosfomicina, cicloserina,
vancomicina, bacitracina.
b) Desorganización de la membrana citoplasmática, lo que conduce a la
desintegración celular: polimixinas, amfotericina B, nistatina.
c) Inhibición de la síntesis de proteínas, por actuar sobre los ribosomas, en la
iniciación (subunidad 30S): tetraciclinas; en la elongación (subunidad 50S): cloranfenicol,
eritromicina, lincosaminas; en ambas con muerte bacteriana: aminoglucósidos.
d) Interferencia en la síntesis y/o el metabolismo de los ácidos nucléicos: rifampicina
(ARN-polimerasa ADN-dependiente), quinolonas (ADN-epimerasas), metronidazol, actinomicina.
e) Antimetabolitos que bloquean la síntesis de ácido fólico: sulfamidas, pirimetamina,
trimetoprim.
f) Análogos de ácidos nucleicos que interfieren en su metabolismo, particularmente
en los virus: aciclovir, zidovudina, ribavirina, entre otros.
SELECCIÓN DEL ANTIBIÓTICO
Al seleccionar un antibiótico es necesario:
a) Identificación etiológica
Asegurar el origen de la fiebre, ya que esta no necesariamente es signo de infección, y
aunque esta exista, puede ser de etiología no tratable con antibióticos (infecciones víricas).
F-CV3-3B-2 Rev. Enero 2011
Es necesario investigar el microorganismo responsable por los tos clínicos y, siempre que sea
posible por estudios bacteriológicos.
En las infecciones graves, una vez establecido el diagnóstico presuntivo (de aproximación),
se iniciará el tratamiento empírico con el antibiótico más eficaz y menos tóxico, valorando
la posibilidad de utilizar una asociación de antibióticos.
Ante los resultados del estudio bacteriológico se valorará la posibilidad de cambiar el
tratamiento, teniendo en consideración que dicho cambio sólo debe realizarse cuando la
evolución clínica del paciente no sea favorable.
Conocer con detalle los diversos aspectos farmacológicos del antimicrobiano a emplear:
actividad antibacteriana, características farmacocinéticas, toxicidad, entre otros.
Es necesario analizar factores que dependerán del paciente infectado.
b) Sitio de la infección
Es un factor muy importante, ya que condiciona no sólo el antimicrobiano a emplearse,
sino la dosis y la vía de administración.
El antimicrobiano debe alcanzar como mínimo la CIM para el germen infectante. Se debe
conocer l irrigación del tejido, la capacidad de difusión del antimicrobiano y la inactivación
debida a la presencia de pus o fibrina. Por ejemplo la mala penetración por la barrera
hematoencefálica (beta-lactámicos, aminoglucósidos, eritromicina, vancomicina y
anfotericina B); cuando existe meningitis la permeabilidad aumenta y se puede alcanzar
concentraciones terapéuticas con algunos de ellos (penicilina G, cefalosporinas de tercera
generación), mientras que con otros es necesario recurrir a la administración intratecal o
intraventricular (aminoglucósidos, vancomicina).
c) Edad
d) Embarazo y lactancia
e) Función renal y hepática
f) Peculiaridades idiosincráticas: genéticas o metabólicas que influye en el
comportamiento terapéutico o tóxico del antibiótico. Ej. pacientes con déficit de glucosa-6-
fosfatodeshidrogenasa, en los que pueden ocasionar hemólisis las sulfamidas, nitrofurantoína,
furazolidona, cloranfenicol. En acetiladores lentos la isoniazida muestra una mayor tendencia
a producir neurotoxicidad. Por causas no bien conocidas, la administración i.m. de antibióticos
en los enfermos diabéticos presenta una menor Biodisponibilidad.
g) Otros factores:
Presencia de pus.
Existencia de procesos obstructivos (litiasis renal o biliar): favorecen la éxtasis y el
crecimiento bacteriano, dificultando la llegada del antibiótico al sitio de la infección.
La presencia de cuerpos extraños (material de sutura, prótesis, catéteres, sondas) que
contribuyen a mantener la infección.
Presencia de microorganismos anaerobios (pueden reducir la actividad de algunos
antibióticos, ej. aminoglucósidos)
F-CV3-3B-2 Rev. Enero 2011
ASOCIACIONES DE ANTIBIÓTICOS
Al igual que otros fármacos es preferible utilizar un único antibiótico para el tratamiento de una
infección. Las ventajas son:
Evitar riesgos tóxicos innecesarios.
Reducción del costo.
Disminuye la posibilidad de aparición de resistencias (en casos de resistencia por un solo
escalón, puede ocurrir lo contrario (tratamiento de la tuberculosis)
Cuando se asocian antibióticos sobre un cultivo in vitro pueden aparecer las siguientes respuestas:
a) Sinergismo: cuando el efecto observado es igual o mayor a la suma de los efectos de ambos
antibióticos .
b) Antagonismo: cuando el efecto observado es menor al antimicrobiano más eficaz cuando se
administra sólo. Ej. β-lactámicos y antibióticos bacteriostáticos (tetraciclinas). En general debe
evitarse la asociación bactericida-bacteriostático.
c) Indiferencia: La acción combinada no es más potente que la del producto más eficaz cuando
se emplea sólo.
La asociación se justifica:
a) Para impedir la aparición de resistencias a antibióticos (tratamiento de micobacterias).
b) Como terapéutica inicial (en pacientes inmunosuprimidos e infecciones graves).
c) En infecciones mixtas: sobre todo en infecciones peritoneales, pélvicas, accesos cerebraes
en inmunosuprimidos.
d) Para reducir la toxicidad.
e) Producción de sinergias
Infecciones por enterococos (endocarditis, las penicilinas facilitan la penetración de
los aminoglucósidos en as bacterias).
Infecciones por Staphylococcus aureus (la asociación de Rifampicina con vancomicina
aumenta la acción bactericida, evitando desarrollo de resistencias a la Rifampicina
sola).
Infecciones por Pseudomona aeruginosa ( los aminoglucósidos muestran sinergia con la
carbenicilina, ticarcilina y ureidopenicilinas).
PROFILAXIS CON ANTIBIÓTICOS
Una de las principales causas de consumo exagerado de antibióticos, en todo el mundo es su
utilización con fines profilácticos. Si el uso es excesivo resulta peligroso por los problemas de
creación de resistencias y toxicidad.
Se aplica la profilaxis en las siguientes situaciones:
a) Para evitar la adquisición de microorganismos exógenos.
b) Para evitar el acceso a zonas estériles del organismo de gérmenes situados en otras zonas.
Ej. infecciones de las vías urinarias por bacterias de la vagina o intestino.
c) Para evitar o disminuir la gravedad de procesos agudos en pacientes crónicos.
d) Disminuir la aparición de infecciones en pacientes de alto riesgo: inmunosuprimidos.
e) Impedir recaídas en infecciones graves previas. Endocarditis bacteriana.
f) Para prevenir aparición de infecciones como consecuencia de intervenciones quirúrgicas.
F-CV3-3B-2 Rev. Enero 2011
Experiencia N° 1
10.2. Competencia
Diseña y ejecuta una experiencia sobre la variación del diámetro de inhibición del
crecimiento bacteriano por el uso de diversos medicamentos (discos de sensibilidad),
interpretando adecuadamente los resultados observados.
10.3. Material y Métodos
Modelo experimental : Suspensión de Bacillus subtilis o St. Aureus
Suspensión de E. coli
Materiales : Discos de sensibilidad de antimicrobianos:
Penicilina G, Cefalotina, Cefuroxima, Ceftriaxona
Vancomicina, Gentamicina, Imipenem, Ciprofloxacino
Cotrimoxazol, Cloranfenicol, Aztreonam, Eritromicina.
Patrón para suspensiones de microorganismos.
10.4. Procedimiento
a) Preparar 08 placas con agar.
b) Realizar una dilución de las dos suspensiones de microorganismos, gram (+) y gram (-),
comparando con los respectivos patrones.
c) Sembrar en 4 placas con la suspensión de microorganismos gram (+) y en las otras con los
microorganismos gram (-).
d) Luego, colocar con una pinza estéril los discos de sensibilidad a una distancia aproximada de
3 cm (una de otra).
e) Incubar las placas por 18 a 48 horas.
f) Entonces examinar la inhibición del crecimiento y calificar de acuerdo al tamaño del
diámetro en:
10.5. Resultados
Lectura:
ATB ACTIV. C/St. aureus ACTIV. C/E. coli
CIM SENSIBIL DIB SENSIBIL CIM SENSIBIL DIB SENSIBIL
1
2
3
4
5
6
7
8
9
10
Muy sensible = MS
Sensible = S
Resistente = R
Muy resistente = MR
Concentración inhibitoria mínima = CIM
Diametro de inhibición bacteriana = DIB
10.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
10.7. Cuestionario:
a) Interpretar los diámetros de inhibición bacteriana observados con los diferentes discos
de sensibilidad ATB.
b) Interpretar la relación existente entre CIM-90 y diámetros de inhibición bacteriana de
los diversos medicamentos empleados en la experiencia.
10.8. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed. Científicas
y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica Panamericana,
Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 11 (SEMANA 12)
FÁRMACOS EN INFECCIONES POR VIH
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
11.1. MARCO TEÓRICO
Cuando se descubrió que el VIH era la causa del SIDA, detener o disminuir la reproducción del virus
se convirtió en uno de los principales objetivos científicos. Se ha alcanzado un progreso significativo
a pesar de la incertidumbre que todavía existe sobre cuándo empezar, cambiar o combinar terapias
antiretrovirales.
Durante los años más recientes, la llegada de nuevos medicamentos y la combinación de terapias ha
permitido por primera vez, desarrollar estrategias del manejo antiviral del VIH a largo plazo.
Los objetivos de la terapia antiviral:
Extender y mejorar la calidad de vida a largo plazo;
Contener el virus a limites inferiores de detección, o tan bajo como sea posible, por el
mayor tiempo posible;
Optimizar y ampliar la efectividad de las terapias disponibles;
Disminuir la toxicidad de los medicamentos y controlar los efectos secundarios y la
interacción entre los medicamentos.
Estructura de un virus
Los virus son los agentes infecciosos más pequeños (20 a 300 nm. De diámetro), que contienen
como genoma sólo una clase de ácido nucleico (RNA O DNA) . El ácido nucleico se
encuentra encerrado en una cubierta proteínica, la cual puede estar rodeada por una
membrana que contiene lípidos
Las proteínas de la envoltura se ensamblan para construir la cápside, la cual encapsula y estabiliza
al ácido nucleico viral contra el medio extracelular y facilita la adhesión y quizá la penetración del
virus al ponerse en contacto con las nuevas células sensibles.
La cápside es la envoltura proteínica que envuelve al ácido nucleico del genoma. Las cápsides
vacías pueden ser subproductos del ciclo de replicación de los virus con simetría ecosaédrica.
El Nucleocápside, es la cápside junto con el ácido nucleico encapsulado.
Los capsómeros son unidades morfológicas que se observan en el microscopio electrónico sobre la
superficie de las partículas virales icosaédricas. Los capsómeros representan grupos de polipétidos,
pero las unidades morfológicas no comprenden necesariamente a unidades estructurales definidas
desde el punto de vista químico.
La cubierta, membrana que contiene lípidos y que circunda a ciertas partículas virales. Se adquiere
durante la maduración del virus por un proceso de gemación a través de una membrana celular. En
la superficie de la cubierta quedan expuestas las glucoproteínas codificadas por el virus
Múltiples virus contienen envolturas de lípidos como parte de su estructura. El lípido se adquiere
cuando la nucleocápside viral experimenta gemación a través de una membrana celular durante la
F-CV3-3B-2 Rev. Enero 2011
maduración. Ocurre gemación solo en los sitios en que se han insertado proteínas virales
específicas en la membrana de la célula huésped
Las cubiertas virales contiene glucoproteínas, son las que fijan la partícula viral a una célula blanco
por interacción con un receptor celular. Las glucoproteínas son además importantes antígenos
virales.
Quimioprofilaxis
Quimioprofiláxis, es el tratamiento de una persona ya infectada por el virus (VIH) con fármacos
antivirales para evitar que se desarrolle la enfermedad (SIDA).
Las razones por las cuales se deben utilizar Terapias Antivirales son bastante claras, a pesar de las
dudas y frustraciones ocasionadas por la incapacidad de algunas tratamiento de un solo
medicamento en producir beneficios a largo plazo.
Cuando una personas ha sido infectada por primera vez con el VIH se desarrollan elevados niveles
del virus, los cuales normalmente vienen acompañados de síntomas y una disminución de las células
CD4+. El sistema inmunologico, sin la ayuda de terapias antivirales, logra contener de una manera
impresionante el virus, aunque no por completo.
En La mayoría de los casos, los recuentos de células CD4+ vuelven parcialmente a sus niveles
normales y, por lo general las personas recuperan un buen estado de salud clínica por muchos años.
Nuevos estudios han demostrado que, aún durante ese periodo de aparente estado de buena salud,
el organismo está permanentemente librando una agresiva batalla entre el VIH. Además al
funcionamiento errático del sistema inmunológico ocasionado por el VIH, con el tiempo este es
consumido por la constante y rápida actividad del virus.
Con base en lo anterior, tiene mucho sentido tratar de disminuir o detener al máximo y por el
mayor tiempo posible la reproducción del VIH. Un número importante de medicamentos han
demostrado disminuir considerablemente los niveles del virus encontrados en la sangre (Carga
Viral), y los mismos, casi siempre logran incrementar los recuentos de células CD4+ (indicador
común de la salud inmunológica) lo que nos indica algún grado de respuesta del sistema
inmunológico. De otra parte, los medicamentos antiretroviales que no reducen la Carga Viral,
generalmente también fallan en mejorar las mediciones de la salud inmunológica, tales como los
recuentos de CD4+.
Existe una clara relación entre los altos niveles de VIH en la sangre (Carga Viral) y los niveles más
avanzados de la enfermedad e incremento del riesgo de desarrollo de la misma. Como regla
general, la enfermedad se desarrolla más rápida en la medida que se producen más virus en el
organismo. También, en la medida que se producen menos virus, existe menos oportunidad
de “mutación” del virus, lo que lo vuelve más peligroso. Diferentes estudios han demostrado
que cuando la carga viral se reduce y se logran incrementar los recuentos de CD4+ por 24
semanas o más, se está logrando demorar el desarrollo de la enfermedad y la muerte.
El reto para los fabricantes de medicamentos antiretrovirales es desarrollar drogas que generen
reducciones en la carga viral a largo plazo, tanto en la sangre como en los tejidos del organismo
donde se acumula el virus. Sin embargo, las terapias no deben tener altos niveles de toxicidad ni
afectar la calidad de vida de las personas. Muchos investigadores están de acuerdo en que, a menos
que se logre controlar la reproducción del virus, cualquier otro esfuerzo por reconstruir la salud
inmunologica fallará.
Aunque las terapias antiretrovirales deterioran la capacidad de reproducción del VIH, estas no son
una cura, pues ninguna de ellas ha demostrado erradicar el virus del organismo. Con el tiempo, el
virus se transforma y cambia a tal punto que ya no lo afectan los medicamentos. Este proceso
denominado “resistencia viral” es bastante probable que se presente con casi todos los
medicamentos antiretrovirales. Muchos investigadores temen que nunca será posible erradicar el
virus del organismo sin importar que tan buenos sean los medicamentos o que tan pronto se inicie el
tratamiento. De otra parte, también es claro que al contener el virus se gana mayor tiempo de vida
y al tomar una terapia efectiva se puede llevar una vida normal a pesar de la infección del VIH.
F-CV3-3B-2 Rev. Enero 2011
CICLO VITAL DEL VIH-1
Características que deben señalar que un antiviral es eficaz
Los antivirales son sustancias químicas que inhiben con eficacia la replicación virica, sin afectar
apenas el metabolismo celular, lo cual es posible gracias a la selectividad especifica de estas
sustancias hacia la síntesis o la función de los ácidos nucleicos o de las enzimas viricas.
Un antiviral eficaz debe ser una sustancia con capacidad para penetrar en la célula infectada y
frenar selectivamente la multiplicación del virus, pero sin ser tóxica para la célula huésped, ni
pera el resto de las células no infectadas.
También teóricamente un antiviral seria una sustancia que impediría la penetración del virus en
la célula
F-CV3-3B-2 Rev. Enero 2011
CLASIFICACIÓN DE ANTIVIRALES
Inhibidores de la Proteasa
- Saquinavir, Ritonavir, Indinavir, Nelfinavir y otros.
Inhibidores de Transcriptasa Inversa Análogos de los
Nucleósidos
- Zidovudine, Estavudina, Lamivudina y otros.
- Stavudine y Zerit
- Laivudine y Epivir
Inhibidores de Transcriptasa Inversa Análogos de los
Nucleótidos
Tenofo
vir, Adefovir y otros
Inhibidores de Transcriptasa Inversa No Nucleosidos
- Nevirapina, Delavirdina, Efavirenz y otros.
Inhibidores de la Integrasa
- Ralteg
ravir, Elvitegravir y otros.
Inhibidores de la Fusión
- Enfuvi
rtida, maraviroc, vicriviroc (discontinuado).
Interferones
Son productos naturales que liberan las células normales solo
cuando son infectadas por un virus, y cuya reacción de acción
no se conoce del todo, pero altera la "replicación" del virus sin
alterar las funciones de las células normales. Hay muchos
tipos. El llamado interferon- se emplea en diversas viriasis,
generalmente en pacientes inmunodeprimidos (pacientes con
defensas alteradas)
F-CV3-3B-2 Rev. Enero 2011
Experiencia N° 1
11.2. Competencia
Diseña y ejecuta una experiencia sobre VIH inducida, y evalúa los efectos observados sobre el
recuento de células CD4 o carga viral con el uso de algunos medicamentos.
11.3. Material y Métodos
Modelo experimental :
Materiales :
11.4. Procedimiento
a)
b)
c)
d)
e)
f)
11.5. Resultados
11.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
11.7. Cuestionario:
Interpretar los efectos que se observan sobre la carga viral y/o recuento de células CD4 con
el uso de antirretrovirales: inhibidores de la transcriptasa inversa, inhibidores de las
proteasas, inhibidores de la fusión e inhibidores de la integrasa.
11.8. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed. Científicas
y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica Panamericana,
Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 12 (SEMANA 13)
FÁRMACOS ANTIHELMÍNTICOS
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
12.1. Marco Teórico
F-CV3-3B-2 Rev. Enero 2011
Huevo fértil de Ascaris lumbricoides Huevo fértil de Ascaris lumbricoides
Huevo infértil de A. lumbricoides con campo oscuro
Huevo infértil de Ascaris con corteza parcialmente
desintegrada, probablemente por estar el
paciente con tratamiento
Taenia solium
F-CV3-3B-2 Rev. Enero 2011
Escólex de Taenia solium
Estado de conservación
Clasificación científica
Reino: Animalia
Filo: Platelmintos
Clase: Cestoda
Orden: Cyclophyllidea
Familia: Taeniidae
Género: Taenia
Especie: T. solium
Nombre binomial
Taenia solium
Linnaeus, 1758
Taenia solium
F-CV3-3B-2 Rev. Enero 2011
CLASIFICACIÓN DE HELMINTOS
HELMINTOS:
Del griego “helmins” gusano sinónimo de gusano. Son
animales pluricelulares que se clasifican en
platelmintos, comúnmente conocidos como gusanos
planos y redondos.
Los helmintos se dividen en:
-Nemaltelmintos: nemátodos
-Platelmintos: tremátodos y cestodos
NEMATODOS: Son organismos que en corte
transversal se ven redondos. Se encuentran en
cualquier parte donde los busquemos, debido a su
gran adaptabilidad al medio ambiente. La mayoría de
ellos son de vida libre, aunque algunos de ellos
se encuentran en el hombre, presentan
simetría bilateral, cavidad corporal no revestida por endotelio. Están cubiertos por una cutícula
fisiológicamente activa, es de quitina que puede en ocasiones ser una superficie para obtener
nutrientes, a pesar de tener tubo digestivo bien definido. Son gonocoricos (hay machos y hembras) a
excepción de algunas de vida libre que no lo son. Tubo digestivo bien definido como boca, ano y
cloaca, algunos ovíparos y muy pocos vivíparos. Sistema nervioso completo, aunque sencillo de
fuera hacia dentro, de corte transversal tiene: cutícula hipodermis, capa muscular, canal excretor
longitudinal, por los extremos, sistema nervioso también longitudinal, cavidad bucal armada, con
labios y papilas dentro de cada labio. Ejemplo:
1. Ascaris lumbricoides
2. Enterobius vermicularis
3. Trichiuris trichiura
En su ciclo vital presentan las fases de:
1ª. Fase- huevo
2ª. Fase- larva de primero, segundo y tercer estadío
3ª. Fase- adulto
Sus huéspedes pueden ser monogenéticos o di genéticos. Su mecanismo de transmisión es pasiva
(inoculativa y vía oral. Se reproducen por sinogamia.
PLATELMINTOS: Son gusanos planos, acelomados, cuyo cuerpo está constituido por un parénquima,
en donde se hallan embebidos los aparatos o sistemas. Pueden o no presentar un cuerpo
segmentado, además pueden tener tubo digestivo rudimentario o carecer totalmente de él. La
mayoría de los hermafroditas (monoicos) y poseen genitales complejos. Están provistos de órganos
de fijación.
F-CV3-3B-2 Rev. Enero 2011
TREMATODOS: También llamados dístomas o duelas: presentan forma foliar o de hoja. Son
organismos no segmentados (monozoicos. Pueden presentar una o dos ventosas con las cuales se
fijan a su huésped. Las fases de su ciclo vital son:
1ª. Fase: huevo
2ª. Fase: miracidio
3ª. Fase: esporocito
4ª. Fase: redia
5ª. Fase: cercaria
6ª. Fase: metacercaria
7ª. Fase: adulto
Necesitan dos huéspedes: intermediario y definitivo. Su mecanismo de transmisión es pasivo vía
oral.
CESTODOS: También llamados taenias; tienen forma de cinta, la mayoría pero no todos, son
segmentados (polizoicos), con un órgano de fijación pequeño y globoso, el escolex, el cual
presenta ventosas circulares o botrías alargadas y puede haber o no un rostelo formado por
numerosos ganchos.
Su ciclo presenta las siguientes fases:
1ª. Fase: huevo
2ª. Fase: larva (cisticerco, cisticercoide, hidatideo o cenuria)
Pueden realizar su ciclo de vida en un solo huésped monogénico. Su mecanismo de transmisión es
pasivo de vía oral. Se reproducen por sinogamia.
Aspectos clínicos de la ascariasis:
La clínica de la ascaríasis es variada. A veces la infección es asintomática, o de escasa o
atenuada signo sintomatología. Otras veces se presenta bajo la forma de un cuadro clínico
atípico o complejo, dependiendo siempre su gravedad de: a) la carga parasitaria infectante b)
las características del huésped: edad, competencia inmunológica, enfermedad de base.
Podemos hablar de formas asintomáticas o sintomáticas. Las primeras se dan generalmente en
adultos. Las formas sintomáticas ocurren principalmente en niños, en los que suele observarse:
disminución de peso, anorexia, retardo del crecimiento, dolores de tipo cólico, diarreas que
alternan con períodos de constipación, nerviosismo e irritabilidad, prurito nasal y/o anal,
urticaria, vómica de Áscaris o salida del parásito por vía bucal o por el ano.
La invasión pulmonar puede producir un cuadro de bronquitis asmatiforme, descripta por
Loeffler en 1932. El síndrome de Loeffler cursa con: fiebre, disnea, cianosis, hemoptisis y
patrón radiográfico de condensación.
F-CV3-3B-2 Rev. Enero 2011
Las complicaciones varían de acuerdo con los órganos afectados; la obstrucción intestinal por
masas de Ascaris o perforación de la pared intestinal, darán un cuadro de abdomen agudo. La
obstrucción del apéndice o divertículo podrá manifestarse corno apendicitis o diverticulitis. La
invasión de la vía biliar y pancreática puede originar pancreatitis, colecistitis, colangitis y
abscesos hepáticos.
Las manifestaciones clínicas varían en severidad, según el número de parásitos en el sistema
biliar y de si permanecen en los conductos o regresan al intestino. Todos los individuos que se
evaluaron en el presente estudio eran sintomáticos en el momento del diagnóstico, excepto
una mujer que pasó a cirugía por sospecha de colecistitis crónica. Se obtuvo historia de dolor
abdominal en todos los pacientes, en su mayoría cólico, localizado en el cuadrante superior
derecho. El dolor severo, que puede ser agudo, ocurre con la migración de parásitos al árbol
biliar. Es de comienzo súbito, tipo cólico, en el epigastrio, el cuadrante superior derecho o
justo bajo el apéndice xifoides, se irradia al hombro, la espalda o el hipogastrio, y se calma
poco con analgésicos. Se ha descrito que dolor, anorexia, náuseas y vómito son comunes y
pueden ser persistentes y severos12,15. La historia de parásitos en el vómito ocurre con
frecuencia (48%) y es una ayuda para el diagnóstico. Entonces, el paciente que se presenta con
dolor en el cuadrante superior derecho y que ha eliminado parásitos por vía bucal, puede tener
helmintos en la vía biliar.
Aspectos clínicos de la teniasis:
El Peligro y los Síntomas
La “Teniasis” en si no conlleva gran peligro, la tenia como huésped no es especialmente
molesto, pueden observarse síntomas gastrointestinales leves, como náusea, dolor abdominal o
diarrea, nerviosismo, problemas para conciliar el sueño, falta de apetito, perdida de peso.
Muchos casos cursan sin síntomas y algunos expulsan segmentos de tenias en las evacuaciones.
La Teniasis se suele contraer al ingerir carne cruda o poco cocinada con una larva enquistada,
actualmente las medidas higiénicas y normas específicas para erradicar este parásito hace
improbable “contaminarse” de este modo.
El problema más grave se suele dar cuando la infección se da directamente por huevos de la
tenia, de este modo una persona que padezca teniasis puede autoinfectarse o infectar a los
demás con sus huevos.
Los síntomas generalmente, la infestación por tenia no presenta síntomas y la infección se
reconoce cuando la persona infectada expulsa segmentos de proglótides en las heces,
especialmente si el segmento se mueve.
Muchos infectados no presentan síntomas, cuando llegan a presentarse los más comunes
son:
- Náuseas.
- Dolor abdominal.
- Trastornos del apetito.
- Malestar general
- Diarrea.
Hay personas que al defecar expulsan segmentos de las tenias.
Antihelminticos
Una de las más importantes causas mundiales de morbilidad está dada por las infecciones por
parásitos (protozoarios y helmintos). Estas enfermedades muchas veces se consideran triviales pero
un vistazo a su estadística global exterioriza su verdadera relevancia, habida cuenta que afectan a
alrededor de la mitad de la población mundial (¡más de tres mil millones de personas!), muy
especialmente en cuanto a helmintiasis se refiere, de las cuales se ha llegado a reportar una
prevalencia tal que alcanza al menos la cuarta parte de la población mundial.
Farmacoterapia
De manera análoga a la terapia antibacteriana, la farmacoterapia intenta afectar al agente causal
sin causar daño al huésped; contemplándose los siguientes blancos:
A. Funciones propias del parásito, que no se presentan en el huésped.
F-CV3-3B-2 Rev. Enero 2011
B. Funciones comunes al parásito y al huésped, pero que son indispensables sólo para la
supervivencia del primero.
C. Funciones comunes al parásito y al huésped, necesarias a ambos, pero diferenciables desde el
punto de vista farmacológico. En la tabla 1 se muestran algunos ejemplos de cada uno de los
casos planteados.
Blancos de la farmacoterapia antiparasitaria
BLANCO PARÁSITO FÁRMACO
FUNCIONES PROPIAS DEL PARÁSITO
Enzimas para la síntesis de esteroles Tripanosomas Azoles
Oxidorreductasa Piruvato-Ferrodoxina Protozoarios Nitroimidazoles
anaeróbicos
FUNCIONES INDISPENSABLES AL PARÁSITO
Ornitina descarboxilasa Protozoarios -difluorometilornitina
FUNCIONES COMUNES, DIFERENCIABLES FARMACOLÓGICAMENTE
Microtúbulos Helmintos Benzimidazoles
Transmisión Sináptica Helmintos Piperazina
Benzimidazoles
Grupo de fármacos químicamente relacionados, que comparten los siguientes mecanismos de
acción:
Inhibición de la polimerización microtubular del parásito (unión a la -tubulina)
Disminución de la captación de glucosa (larvas/adultos)
Otros: inhibición de la rodoquinol fumarato reductasa, desacoplamiento de la fosforilación
oxidativa
Entre sus representantes están el albendazol, el mebendazol y el tiabendazol, en preparados orales,
lo que es frecuente para este tipo de fármacos.
Espectro: Amplio, útil contra Ascaris, Ancylostoma, Necator, Trichuris, Strongyloides.
Neurocisticercosis.
Piperazina
Es una amina cíclica secundaria, cuyos mecanismos de acción propuestos incluyen:
Bloqueo de la respuesta muscular parasitaria ante la acetilcolina. Esto conlleva una
hiperpolarización de la célula muscular, la cual entonces aumenta su umbral de respuesta,
causando una parálisis flácida del parásito, el cual, entre otros efectos, pierde sus medios de
sujeción y es eliminado
Disminución de la captación de glucosa (larvas/adultos)
Todos los preparados son orales (jarabes, tabletas).
Espectro: Principalmente contra Ascaris.
Pamoato de Oxantel / Pirantel
Sustancias químicamente relacionadas, cuyo mecanismo de acción es el siguiente:
Son bloqueantes despolarizantes de la respuesta muscular, conllevando a una despolarización
persistente, que se manifiesta como parálisis espástica del parásito, el cual entonces se
F-CV3-3B-2 Rev. Enero 2011
elimina. Por la contraposición de sus mecanismos de acción, se produce una interacción de
antagonismo con la piperazina.
Los preparados son orales (jarabes, tabletas).
Espectro: principalmente contra especies de Ascaris y Trichuris. También tienen acción contra las
uncinarias (Ancylostoma, Necator). La combinación se utiliza porque el pirantel, a diferencia del
oxantel, es ineficaz contra Trichuris trichiura.
Praziquantel
Es una pirazinoisoquinolina, cuyo mecanismo de acción es el que sigue:
Aumento de la permeabilidad de la membrana celular al ión calcio, lo que lleva a una
contracción muscular muy marcada, manifestada de manera semejante a la explicada para el
pamoato de oxantel/pirantel (Parálisis muscular espástica)
Vacuolización y desintegración del tegumento (envoltura parasitaria), lo que deja inerme al
parásito
Los preparados son orales.
Espectro: Contra especies de platelmintos (tenias, esquistosomas)
Esquemas de tratamiento de helmintiasis frecuentes
Parasitosis Fármacos de elección
Ascariasis Mebendazol: 100 mg BID por 3 días o 500 mg una sola vez
Albendazol: 400 mg una sola vez
Pamoato de Pirantel: Dosis única de 10 mg/Kg (máximo à 1 g)
Piperazina: 75 mg/Kg (máximo: 3,5 g) VO OD por 2 días (ó 50 mg/Kg, por 5 días)
Tricuriasis Mebendazol: 100 mg BID por 3 días o 500 mg una sola vez
Albendazol: 400 mg una sola vez
Pamoato de Oxantel: Dosis única de 10 mg/Kg (máximo à 1 g)
Flubendazol: 100 mg BID por 3 días
Oxiuriasis Pamoato de Pirantel: Dosis única de 10 mg/Kg (máximo à 1 g)
Mebendazol: 100 mg BID por 3 días o 500 mg una sola vez
Albendazol: 400 mg una sola vez
Piperazina: 50 mg/Kg, en dos tomas, por 5 - 7 días
Anquilostomiasis Pamoato de Pirantel: 10-20 mg/Kg (máximo à 1 g) por 3 días
Albendazol: 400 mg / día por 3 días
Mebendazol: 100 mg BID por 3 días
Flubendazol: 300 mg/día por 2 días
Teniasis Praziquantel: 10 mg/Kg en dosis única
Mebendazol: 200 mg BID VO por 4 días
F-CV3-3B-2 Rev. Enero 2011
Experiencia
12.2. Competencia
Diseña y ejecuta una experiencia sobre la modificación de la actividad de la motilidad del
Ascaris lumbricoides o lombriz de tierra con el uso de algunos medicamentos, e interpreta
adecuadamente los efectos observados.
12.3. Material y Métodos
Modelo experimental : Tenia, ascaris o lombriz de tierra.
Fármacos : Extracto de pepas de zapallo
Extracto de Menta piperita
Extracto de pepas de papaya
Extracto de calabaza
Praziquantel
Piperazina
Niclosamida
Mebendazol
Albendazol
Pamoato de pirantelo
Preparación de extractos:
Preparación del extracto de pepas de zapallo
a) Obtener aproximadamente, 50 g de pepas de zapallo, dejar secar y pulverizarlas.
b) Luego hervir en unos 300 mL de agua, filtrar y envasarlo en un frasco debidamente
rotulado, señalando la fecha de producción.
Preparación del extracto de Menta piperita
Obtener aproximadamente, 50 g de hojas de menta y hervirlos en unos 300 ml de agua. Filtrar y
envasarlo en un frasco debidamente rotulado, señalando la fecha de producción.
Preparación del extracto de pepas de papaya y de calabaza
Realizar el mismo procedimiento utilizado para preparar los extractos de pepas de zapallo.
12.4. Procedimiento
a) Seleccionar y enumerar 9 tubos.
b) Colocar en dichos tubos, 5 ml de las siguientes soluciones: suero fisiológico, extracto de
pepas de zapallo, extracto de menta piperita, extracto de pepas de calabaza, extracto
de pepas de papaya, pamoato de pirantelo, piperazina, praziquantel, niclosamida,
mebendazol y albendazol.
c) Colocar en cada uno de los tubos una tenia, ascaris o lombriz de tierra.
d) Observar el estado de los helmintos cada 5’ hasta los 30’.
F-CV3-3B-2 Rev. Enero 2011
12.5. Resultados:
Tubo Fármacos Parálisis observada
Nº 5’ 10’ 15’ 20’ 25’ 30’
1 Suero fisiológico
2 E. pepas Zapallo
3 E. Menta piperita
4 Pamoato pirantelo
5 E. pepas Papaya
6 Calabaza
7 Praziquantel
8 Niclosamida
9 Albendazol
10 Mebendazol
11 Piperazina
12.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
12.7. Cuestionario:
Interpretar los efectos observados sobre la motilidad del Ascaris lumbricoides con el uso de
los fármacos.
12.8. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed. Científicas
y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica Panamericana,
Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 13 (SEMANA 14)
FÁRMACOS EN DIABETES MELLITUS INDUCIDA
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
13.1. Marco teórico
Diabetes mellitus
La diabetes mellitus es la enfermedad endocrina más frecuente, se caracteriza por alteraciones
metabólicas y complicaciones a largo plazo, que afectan a los ojos, riñones, nervios y vasos
sanguíneos. No es una entidad homogénea, y se han descrito varios síndromes diabéticos distintos.
Criterios de diagnóstico de la diabetes mellitus
El diagnóstico de la diabetes mellitus es posible por cualquiera de los siguientes procedimientos:
1) Una glicemia en ayunas igual o mayor de 126 mg/dL, especialmente
asociada a síntomas: astenia, somnolencia, prurito vulvar y susceptibilidad a infecciones.
2) Una glicemia al azar igual o mayor a 200 mg/dL asociado a síntomas
clásicos: poliuria, polidipsia, pérdida de peso, visión borrosa.
3) Una glicemia igual o mayor de 200 mg/dL, dos horas después de una
sobrecarga de 75 g de glucosa por vía oral
Clasificación de la diabetes mellitus
I. Diabetes mellitus tipo 1: Destrucción de las células beta, que conducen a una deficiencia
absoluta de insulina. Puede ser: a) autoinmune o b) idiopática (HLA y anticuerpos negativos)
II. Diabetes mellitus tipo 2: Participación de factores genéticos y ambientales. Varía desde
estados donde predomina la resistencia a la insulina con relativa deficiencia de insulina a estados
donde la deficiencia secretoria predomina sobre la resistencia.
III. Diabetes de etiologías identificables:
a) Defectos genéticos de la función de la célula beta: cromosoma 12, HNF-1
alfa.
b) Defectos genéticos en a acción de la insulina: resistencia a la insulina tipo
Acantosis nigricans.
c) Enfermedades del páncreas exocrino: pancreatitis, neoplasia.
d) Endocrinopatía: acromegalia, síndrome de Cushing.
e) Inducida por fármacos o sustancias químicas: pentamidina,
glucocorticoides
f) Infecciones: rubéola congénita
g) Formas infrecuentes de Diabetes Inmuno-mediadas: síndrome de hombre
tieso.
h) Otros síndromes genéticos asociados algunas veces a diabetes: síndrome
de Down, síndrome de Klinefelter.
IV. Diabetes mellitus gestacional:
F-CV3-3B-2 Rev. Enero 2011
Manifestaciones clínicas
La sintomatología de la diabetes mellitus clínicamente manifiesta varía de un paciente a otro. La
mayoría de veces, los síntomas se deben a la hiperglicemia (poliura, polidipsia, polifagia), pero el
primer acontecimiento pede ser una descompensación metabólica aguda, seguida de un coma
diabético. En ocasiones la primera manifestación es una complicación degenerativa, como una
neuropatía, sin que la hiperglicemia haya causado síntomas.
Objetivos del tratamiento de la diabetes mellitus
a) Mantener un buen control metabólico y garantizar una buena calidad de vida al
paciente diabético.
b) Educar al paciente y su familia en el manejo de la diabetes mellitus (compliaciones
agudas y crónicas, nutrición y ejercicio).
c) Entrenar al paciente en técnicas de autocontrol y monitoreo y lograr
autosuficiencia.
d) Mantener la glicemia lo más cerca de lo normal durante todo el día.
e) Controlar los síntomas.
f) Conseguir un peso adecuado.
g) Prevenir las complicaciones agudas y crónicas.
h) Reducir la mortalidad
i) Evitar el tabaco y sedenterismo.
Un protocolo completo para estudiar el efecto hipoglicemiante de una sustancia debe incluir
las siguientes experiencias:
Experiencia N° 1
13.2. Competencias
Diseña y ejecuta una experiencia sobre la modificación de los niveles de glicemia e
interpreta los efectos observados con el uso de algunos medicamentos en diabetes mellitus
inducido por aloxano
13.3. Material y Métodos
Modelo experimental: Ratones albinos machos (15)
Materiales: Jeringas 1 mL
Capilares de microhematocrito
Tiras reactivas
Cánula para administración oral para ratones.
Fármacos: Aloxano
Glibenclamida
Insulina
13.4. Procedimiento
a) Los animales deben ser llevados al laboratorio con tres días de anticipación, mantenerlos
con temperatura controlada y con libre acceso al agua y alimentos.
b) Antes de proceder a la administración del fármaco y del agua destilada, tomar una
muestra de sangre con los microcapilares. Estas muestras serán los valores de glicemia a
tiempo cero.
c) Cuarenta y ocho horas antes del experimento, tratar los animales (12 ratones, del N° 4 al
15) con una dosis de aloxano (100 mg/kg), vía intraperitoneal.
d) A un grupo de tres ratones (N° 1 al 3), se le administra suero fisiológico por vía oral
(grupo control negativo).
e) Tomar muestras de sangre con los microcapilares y determinar las glicemias a todos los
ratones.
F-CV3-3B-2 Rev. Enero 2011
f) Doce horas antes del experimento, los alimentos deben ser retirados, permitiendo al
animal agua a libre voluntad.
g) Antes de proceder a la administración del fármaco hipoglicemiante y del agua destilada,
tomar una muestra de sangre con los microcapilares. Anotar.
h) Seguidamente se administra los fármacos antidiabéticos a los grupos experimentales:
glibenclamida por vía oral a cuatro ratones (N° 8 al 11) e insulina a los otros cuatro (N°
12 al 15).
i) Los ratones de los grupos control negativo (tres que recibieron suero fisiológico) y control
positivo (cuatro que recibieron aloxano), sólo reciben agua por la misma vía.
j) Tomar muestras adicionales de sangre a los 30’, 60’ y 90’.
k) Analizar las muestras de sangre. Anotar.
13.5. Resultados
Ratones Glicemia Aloxano Glicemia Glibencla- Insulina Glicemia
Basal mida
1 - - -
2 - - -
3 - - -
4 - -
5 - -
6 - -
7 - -
8 -
9 -
10 -
11 -
12 -
13 -
14 -
15 -
13.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
13.7. Cuestionario:
a) Interpretar la modificación de los niveles de glicemia con el uso de insulina,
glibenclamida y metformin en pacientes con DM I y DM II
13.8. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed. Científicas
y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica Panamericana,
Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
PRÁCTICA N° 14 (SEMANA 15)
FÁRMACOS EN INTOXICACIONES INDUCIDAS
RESOLUCIÓN DE CASO CLÍNICO FARMACOLÓGICO
14.1. Marco teórico
AGENTES TÓXICOS: Antídotos y Antagonistas
Tóxico o veneno es toda sustancia que incorporada al organismo vivo produce por su naturaleza y en
determinadas condiciones alteraciones de la fisiología celular transitorias o definitivas incompatibles
con la salud o la vida. Sin embargo, como lo indicara Paracelso: "toda sustancia es veneno, solo la
dosis hace que esta no sea venenosa", así por ejemplo, el exceso de agua puede producir una
intoxicación hídrica; una pequeña cantidad de dióxido de carbono actúa como estimulante, pero un
exceso es mortal.
Existe una extraordinaria variabilidad en los cuadros clínicos y formas de presentación de las
intoxicaciones; y dos tipos generales de tratamiento, uno inespecífico, en el cual se adoptan medidas
para el mantenimiento de las funciones vitales y disminución de los niveles sanguíneos (por reducción
de la absorción o incremento de la eliminación) de la sustancia en sobredosis, y otro específico, en el
cual se utilizan productos que tienen la propiedad de actuar directamente sobre los medicamentos u
otros que están produciendo intoxicaciones.
Un número muy reducido de intoxicaciones tienen un tratamiento con antídotos específicos y aún en
estos casos, ello no exime de la necesidad de usar otras medidas no específicas (Vomitivos, lavado
gástrico, purgantes drásticos, mantenimiento de una ventilación adecuada, entre otras), pero quizá,
tanto o más importantes que las primeras. Estos tratamientos terapéuticos inespecíficos son en
muchas oportunidades los únicos que se pueden ofrecer al intoxicado.
El profesor E. Astolfi ha sintetizado el enfoque que debe tenerse en consideración en el tratamiento
de una intoxicación aguda, señalando una serie de medidas concomitantes contra el veneno y a favor
del paciente, las mismas que señalamos a continuación:
A favor del enfermo
Inmediatas
Reanimación cardiorrespiratoria y medidas de apoyo a las funciones vitales (vía respiratoria libre,
ventilación y oxigenación o soporte cardiovascular y renal), en casos de: "Shock", Apnea, fibrilación
ventricular, cianosis, coma profundo, deshidratación severa, entre otras manifestaciones clínicas.
Mediatas
Búsqueda de posibles complicaciones, profilaxis integral, protección anticipada, según la acción
conocida del tóxico (hepatotóxico o nefrotóxico) y abstención de iatrogenia "antitóxica" y tratamiento
sintomático.
Tardías
Rehabilitación, psicoterapia (especialmente en casos de pacientes que llevan a cabo actos suicidas) y
clínica general.
Contra el veneno
Entre de los procedimientos dirigidos contra el tóxico, el rescate del mismo es de singular
importancia.
Rescate (eliminación) del tóxico
Consiste en prevenir una mayor absorción del tóxico, ya que la gravedad y el riesgo de complicaciones
dependen de la cantidad de sustancia ingerida; o incremento de la eliminación del tóxico
1) Descontaminación digestiva: a) mediante la administración de eméticos o vomitivos (jarabe de
ipeca, apomorfina, entre otros procedimientos); no se recomienda cuando el paciente está en
estado de somnolencia o coma, en ingestión de hidrocarburos o sustancias que dañan la mucosa,
F-CV3-3B-2 Rev. Enero 2011
insuficiencia cardiovascular severa, shock, convulsiones, gran tamaño del producto. b) Purgantes
drásticos y/o c) Lavado gástrico.
2) Descontaminación respiratoria: a) Ventilación adecuada. b) Asistencia respiratoria (ej.
Oxigenoterapia).
3) Descontaminación cutáneo-mucosa: a) Lavados prolongados. b) Cambio total de ropas. c)
Administración de antídotos locales.
4) Depuración renal: diuresis forzada para aumentar la eliminación urinaria del tóxico.
5) Transfusión sanguínea, diálisis peritoneal o Hemodialisis: se recomiendan cuando la sustancia
no reconoce un tratamiento específico y es muy tóxica, o el enfermo se agrava (hemólisis
intravascular, hipercalemia, uremia, cianosis) y además el tóxico es dializable.
6) Tratamiento con antídotos (sustancias que antagonizan o neutralizan específicamente por
diferentes mecanismos la acción tóxica de otra sustancia), estos pueden ser: a) Por competición
(dimercaprol, D-penicilamina, entre otros). b) Por quelación (formación de compuestos no
disociables de fácil eliminación renal, tal es el caso del E.D.T.A).
7) Eliminación del tóxico mediante el empleo de: a) Quelantes (señalados antes) o b) Variación del
pH urinario, ya sea, por alcalinización o acidificación del medio interno (ej. Alcalinización del
medio con la administración parenteral de bicarbonato de sodio para incrementar la eliminación
urinaria de sobredosis de barbitúricos o salicilatos; o la acidificación del medio con cloruro de
amonio para la mayor excreción de anfetaminas o alcaloides).
F-CV3-3B-2 Rev. Enero 2011
Experiencia N° 1
14.2. Competencias
Diseña y ejecuta una experiencia con fármacos antídotosútiles en intoxicaciones inducidas
en ratones.
14.3. Materiales y Métodos
Modelo experimental : Ratón (4)
Fármaco : Cianuro de sodio, sol. 0.2%
Nitrito de sodio, sol. 0.3%
Tiosulfato de sodio sol. 20%
14.4. Procedimiento
a) Seleccionar, marcar y pesar 3 ratones.
b) Observar la capacidad de caminata, respiratoria y fuerza de la cabeza.
c) Administrar a los ratones Nº 2, 3 y 4 cianuro de potasio, 10 mg/kg vía s.c., observar y anotar
el tiempo de latencia.
d) Al ratón Nº 3, inmediatamente después de la administración de cianuro, administrar el
fármaco antídoto nitrito de sodio, 30 mg/kg, vía i.p. Observar.
e) Al ratón Nº 4, inmediatamente después de la administración de cianuro, administrar vía i.p.
los fármacos antídotos nitrito de sodio, 30 mg/kg, y tiosultafo de sodio 1g/kg vía i.p. Observar.
14.5. Resultados
Fármaco Tiempo de Efectos
Ratón latencia
1 Suero
2 Cianuro sodio
3 Cianuro sodio +
Nitrito sodio
4 Cianuro sodio +
Nitrito sodio +
Tiosulfato de sodio
14.6. Interpretación de los resultados:
F-CV3-3B-2 Rev. Enero 2011
14.7. Cuestionario
a) Interprete el envenenamiento producido con el cianuro de potasio, así como la actividad
antitóxica del nitrito de sodio y tiosulfato de sodio.
b) Indique la diferencia que existe entre antídoto y antagonista.
c) Señale cinco ejemplos de antídoto y antagonista indicando sus mecanismos de acción y
respectivas aplicaciones clínicas.
14.8. FUENTES DE INFORMACIÓN
a) Florez J, Armijo J. Farmacología Humana. Farmacología Humana. Edición 6. Ed. Científicas
y Técnicas. España, 2013.
b) Goodman and Gilman. Las Bases Farmacológicas de la Terapéutica. 12va. Ed. México:
Editorial Mc Graw-Hill – Interamericana; 2011.
c) Velazquez P, Lorenzo. Farmacología Básica y Clínica. Edición 18. Ed. Médica Panamericana,
Madrid 2011
d) Rang H, Dale M. Farmacología. Edición 7. España: Ed. Harcourt Brace; 2012.
e) Yee Y., Koda-Kimble. Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009.
F-CV3-3B-2 Rev. Enero 2011
FUENTES BIBLIOGRÁFICAS
LIBROS
CYTED Manual de Técnicas de Investigación. Programa Iberoamericano de
Ciencia y Tecnología para Desarrollo. 1993
Florez J., Armijo J. Farmacología Humana. Edición 6. Ed. Científicas y Técnicas.
España, 2013
Ganong, William Fisiología Médica. Edición 17. Ed. El Manual Moderno. U.S.A., 1999
Goodman and Gilman Las Bases Farmacológicas de la Terapéutica. Edición 12. McGraw-
Hill Interamericana. México, 2011
Katzung, Bertram G. Farmacología Básica y Clínica. Edición 12. Editorial El Manual
Moderno. México, 2012
Navarro M., Bacigalupo R. y col. Formulario Nacional de Medicamentos Esenciales. MINSA 2000
Aguilar C., Cervantes L. y col Manual de Terapéutica Médica. Cuarta Edición. McGraw-Hill
Interamericana. 2000
Bevilacqua-Bensoussan y col. Fisiopatología clínica. 2 edición, 1996. Editorial “El Ateneo”
Carey Ch., Lee H. y col. Manual Washington de terapéutica médica. 10 edición, 1999. Serie
manuales espiral.
Comité Join Formulary Formulario Nacional Británico. British Medical Association, 1998
Dreisbach, Robert Manual de Toxicología Clínica. Edición 5. USA. 2003
Ellenhorn, Matthew Ellenhorn’s Medical Toxicology: Diagnosis and treatment of Human
Poisoning. Edición 2. USA, 1992.
Fauci A., Braunwald E. y col. Principios de Medicina Interna de Harrison. Edición 14. 1998.
Mc Graw Hill
Foye, Willian O. Principios de Química Farmacéutica. Edición 2. Ed. Revertè.
España, 1991
Gilbert J, Villanueva E Medicina y Química Legal. Ed. 6. Editorial Elsevier Masson, España;
2004.
Jáuregui P Luis Antimicrobianos: Uso terapéutico en infectología clínica. USA 2005
Kalant , Roschlau W Principios de la Farmacología Médica. Edición 6. Oxford University
Press. México, 2002
Lorenzo P, Moreno A y otros Velázquez Farmacología Básica y Clínica. Edición 18. Ed. Médica
Panamericana, Madrid 2011
McPhee S., Ganong W. y col. Fisiopatología médica. Edición 5. 2005. Editorial El manual
moderno.
Opie, Lionel H. Fármacos en Cardiología. Edición 6. Interam. McGraw-Hill. México,
2004
Rang H, Dale M. Farmacología. Edición 7. Ed. Harcourt Brace, España,2012.
Rothlin R., Tessler R. Farmacología. Edición 1ra.- Gráfica Jorda. Argentina, 1995
Tierney L, Saint S y otros Manual de Diagn y tratamiento. 2ª Ed. 2006. Editorial El Manual
Moderno, Mexico
USP, Convention Inc USP DI Información de Medicamentos. Edición 30. USA, 2010
Yee Y., Koda-Kimble Terapéutica Aplicada: El uso clínico de los Fármacos. Edición 9.
Lippincott Williams & Wilkins. U.S.A., 2009
F-CV3-3B-2 Rev. Enero 2011
REVISTAS
New England Journal of medicine
Lancet
JAMA
MEDLINE US National Library
American Journal of Health System Pharmacist
British Medical Journal
FUENTES INFORMATIZADAS DE ACCESO DIRECTO (ON LINE)
MartinDale Extrapharmacopeia 2011
Physician Desk Reference (PDR) 2011
Drug and Pharmacology
Drug Evaluation 2011
Poisindex 2011
Tomes plus
Medline
F-CV3-3B-2 Rev. Enero 2011
También podría gustarte
- Guia de Practicas Farmacologia Ii 2020Documento107 páginasGuia de Practicas Farmacologia Ii 2020Shirley UlloaAún no hay calificaciones
- Practica 2....Documento4 páginasPractica 2....Nei Marllori Davila CaisaraAún no hay calificaciones
- Guía de prácticas de Farmacología IIDocumento110 páginasGuía de prácticas de Farmacología IIAnonymous iuy4yz40% (1)
- Problemas Relacionados Con Los Medicamentos (PRM) y Resultados Negativos Asociados A La Medicación (RNM)Documento1 páginaProblemas Relacionados Con Los Medicamentos (PRM) y Resultados Negativos Asociados A La Medicación (RNM)Doris DTAún no hay calificaciones
- Laboratorio 1Documento6 páginasLaboratorio 1Deysi OlivaresAún no hay calificaciones
- Guia de Practica Farmacologia General y Especial - 2017-IIDocumento58 páginasGuia de Practica Farmacologia General y Especial - 2017-IITorricelli Carrasco Slater100% (1)
- ANTIASMÁTICOSDocumento44 páginasANTIASMÁTICOSYanet Velasquez QuintanaAún no hay calificaciones
- Causas de PRMDocumento21 páginasCausas de PRMGleMn Enriquez AncoAún no hay calificaciones
- Conf.7-FARMACOS ANTIPARKINSONIANOS, ANTICONVULSIVOS Y SPICOFARMACOS.Documento7 páginasConf.7-FARMACOS ANTIPARKINSONIANOS, ANTICONVULSIVOS Y SPICOFARMACOS.José Carlos Rosas CarhuanchoAún no hay calificaciones
- Primer Consenso de Granada Sobre PRMDocumento5 páginasPrimer Consenso de Granada Sobre PRMAlexander ValderramaAún no hay calificaciones
- Mendeley 20200915004226Documento17 páginasMendeley 20200915004226Karla HuamancajaAún no hay calificaciones
- Intoxicación Por Marihuana y OtrosDocumento33 páginasIntoxicación Por Marihuana y OtrosKike Leal100% (2)
- Receptores FarmacologicosDocumento3 páginasReceptores FarmacologicosangiejzAún no hay calificaciones
- FarmacoDocumento16 páginasFarmacodavis luis mera atalayaAún no hay calificaciones
- Factores que influyen en la absorción de fármacosDocumento17 páginasFactores que influyen en la absorción de fármacosDiego AAún no hay calificaciones
- PRM 2 - Grupo 5Documento40 páginasPRM 2 - Grupo 5Jorge DdcAún no hay calificaciones
- Regulacion Plantas Medicinales en LA y Peru Diplomatura UNMSM 2015Documento43 páginasRegulacion Plantas Medicinales en LA y Peru Diplomatura UNMSM 2015Karmen UriarteAún no hay calificaciones
- 011 Tesis Farmacia Merino & Machaca, Rev - LB, FinalizadaDocumento97 páginas011 Tesis Farmacia Merino & Machaca, Rev - LB, FinalizadaAlexander Davis Galarza LandaAún no hay calificaciones
- Guia de Practicas Farmacoquímica IIDocumento80 páginasGuia de Practicas Farmacoquímica IIcriss payanoAún no hay calificaciones
- 12-09-19 NORMAS APLICABLES OF Mary Rodriguez-1Documento80 páginas12-09-19 NORMAS APLICABLES OF Mary Rodriguez-1YsabelRodriguezCerna0% (1)
- No. 6 Sinergismo y AntagonismoDocumento4 páginasNo. 6 Sinergismo y AntagonismoDaniel Valtierra GuerraAún no hay calificaciones
- Informe N°5 HipoglicemiantesDocumento9 páginasInforme N°5 HipoglicemiantesJessica Benavides Bermudez100% (3)
- Hipnóticos y SedantesDocumento12 páginasHipnóticos y SedantesJoselyn Ramirez VargasAún no hay calificaciones
- Farmacia Clinica - S1 IntroducciónDocumento24 páginasFarmacia Clinica - S1 IntroducciónjanssenAún no hay calificaciones
- Avancede Tesis 17 Junio 2021Documento63 páginasAvancede Tesis 17 Junio 2021RAQUELAún no hay calificaciones
- Clase 2 2019-1 Farmacología Reacciones Adversas UNMSM - SERUMS PDFDocumento11 páginasClase 2 2019-1 Farmacología Reacciones Adversas UNMSM - SERUMS PDFVictor AlvaradoAún no hay calificaciones
- Seminario 01 - Farmacología en Gestantes.-1Documento21 páginasSeminario 01 - Farmacología en Gestantes.-1Beanella BarriosAún no hay calificaciones
- AntiasmäticosDocumento45 páginasAntiasmäticosArmany PytterAún no hay calificaciones
- Alprazolam PowerDocumento10 páginasAlprazolam PowereduardoAún no hay calificaciones
- Farmacodinamia Receptores OkDocumento33 páginasFarmacodinamia Receptores OkIng Joyce David Sedano Mendoza100% (1)
- Antibioticos Betalactamicos y Otros Agentes Activos en La Pared Celular - Saul Condori Galindo - Grupo 1SDocumento14 páginasAntibioticos Betalactamicos y Otros Agentes Activos en La Pared Celular - Saul Condori Galindo - Grupo 1SSaul CondoriAún no hay calificaciones
- XXX1Documento45 páginasXXX1Miguel Angel Copa CAún no hay calificaciones
- Notificación RAM farmacovigilanciaDocumento56 páginasNotificación RAM farmacovigilanciawilmerAún no hay calificaciones
- PRM Roosevelt 2021Documento32 páginasPRM Roosevelt 2021JAIME CESAR SANTI LEÓNAún no hay calificaciones
- PRACTICA N1 - Farmacologia IDocumento19 páginasPRACTICA N1 - Farmacologia IHaydee Cabeza Rojas100% (6)
- AntiparkinsonianosDocumento14 páginasAntiparkinsonianosDario Ángel BazanAún no hay calificaciones
- Informe 2 Farmaco FinalDocumento10 páginasInforme 2 Farmaco FinalJose ReyesAún no hay calificaciones
- Efectos TetratogenosDocumento6 páginasEfectos TetratogenosKelly Zagaceta AranibarAún no hay calificaciones
- Farmacoterapia-Examen de Final-2Documento3 páginasFarmacoterapia-Examen de Final-2David Vásquez DíazAún no hay calificaciones
- FarmacoepidemiologiaDocumento34 páginasFarmacoepidemiologiasindyd_44100% (1)
- 002 Correlaciones Estructura Actividad BioisosterismoDocumento36 páginas002 Correlaciones Estructura Actividad BioisosterismoJhons Mejía EspejoAún no hay calificaciones
- Determinación de proteínas hepáticasDocumento16 páginasDeterminación de proteínas hepáticasDilcerCerna0% (1)
- Proyecto Efectos Adversos y Farmacovigilancia Version 1Documento56 páginasProyecto Efectos Adversos y Farmacovigilancia Version 1Bioquimica Upla0% (1)
- Comunicacion Eficaz en FarmaciaDocumento5 páginasComunicacion Eficaz en FarmaciaCarlos Bobadilla PoquiomaAún no hay calificaciones
- Clase 06-Antiepilépticos y AntiparkinsonianosDocumento26 páginasClase 06-Antiepilépticos y AntiparkinsonianosDavid Vasquez50% (2)
- ReceptoresDocumento14 páginasReceptoresMauricio Espinoza MaechelAún no hay calificaciones
- Practica 5 de FarmacologiaDocumento14 páginasPractica 5 de FarmacologiaRoyserAún no hay calificaciones
- Antidiabéticos orales sulfonilureas y meglitinidasDocumento22 páginasAntidiabéticos orales sulfonilureas y meglitinidasSamuel CruzAún no hay calificaciones
- TESIS Ricci Yissela - Condori DianaDocumento112 páginasTESIS Ricci Yissela - Condori DianaCorporacion DigitalAún no hay calificaciones
- Propiedades y usos terapéuticos del Tilo de hoja grandeDocumento32 páginasPropiedades y usos terapéuticos del Tilo de hoja grandeNancy BetzaAún no hay calificaciones
- Practica de Antagonismo y SinergismoDocumento7 páginasPractica de Antagonismo y SinergismoJose Carlos Torres EsquivelAún no hay calificaciones
- Diseño de Fármacos Asistido Por OrdenadorDocumento28 páginasDiseño de Fármacos Asistido Por Ordenadoroligoelemento100% (1)
- Intoxicación por benzodiacepinasDocumento24 páginasIntoxicación por benzodiacepinasLuliana Cusicahua HuamanAún no hay calificaciones
- 1 Farmacia - Hospitalaria - IDocumento43 páginas1 Farmacia - Hospitalaria - ILupe Ccorahua RetamozoAún no hay calificaciones
- Guía Práctica de FarmacologíaDocumento42 páginasGuía Práctica de FarmacologíaDaniel Navarrete HilarioAún no hay calificaciones
- 21.guia de Practicas Farmacologia Ii 2020Documento107 páginas21.guia de Practicas Farmacologia Ii 2020thalia troncosAún no hay calificaciones
- Guia de Practicas Farmacologia Ii 2019-2 20ago2019Documento110 páginasGuia de Practicas Farmacologia Ii 2019-2 20ago2019luis Jhobel toribio arteagaAún no hay calificaciones
- Guia de Practicas Farmacologia Ii 2021-IiDocumento114 páginasGuia de Practicas Farmacologia Ii 2021-IiMarco Mamani HuamanculiAún no hay calificaciones
- Guia de Practicas Farmacologia Ii 2022-IDocumento114 páginasGuia de Practicas Farmacologia Ii 2022-IRosa Maria Torres CárdenasAún no hay calificaciones
- GUIA - DE - PRACTICAS - FARMACOLOGIA - II - 2019-1 - Actualizado - 2 (1) .docIMPORTANTE VALEDocumento108 páginasGUIA - DE - PRACTICAS - FARMACOLOGIA - II - 2019-1 - Actualizado - 2 (1) .docIMPORTANTE VALETeresa Saavedra100% (1)
- Capacidad amortiguadora de fluidos biológicosDocumento12 páginasCapacidad amortiguadora de fluidos biológicosAnonymous q3hUTAAún no hay calificaciones
- Informe 1 BioqDocumento12 páginasInforme 1 BioqAnonymous q3hUTAAún no hay calificaciones
- Muestreo HechoDocumento10 páginasMuestreo HechoAnonymous q3hUTAAún no hay calificaciones
- Farmacologia-Clase5 203 0Documento22 páginasFarmacologia-Clase5 203 0Anonymous q3hUTAAún no hay calificaciones
- BPM OmsDocumento48 páginasBPM OmsguillermoAún no hay calificaciones
- Muestreo Hecho BioestadisiticaDocumento4 páginasMuestreo Hecho BioestadisiticaAnonymous q3hUTAAún no hay calificaciones
- Farmacologia-Clase5 203 0Documento22 páginasFarmacologia-Clase5 203 0Anonymous q3hUTAAún no hay calificaciones
- GP Fco I 2017 - I 203 0Documento51 páginasGP Fco I 2017 - I 203 0Anonymous q3hUTAAún no hay calificaciones
- Evaluación RAM causasDocumento25 páginasEvaluación RAM causasAnonymous q3hUTAAún no hay calificaciones
- Receptores B2adrenergicos en Enfermedad CardiovascularDocumento8 páginasReceptores B2adrenergicos en Enfermedad CardiovascularFe LipeAún no hay calificaciones
- Guia de Practicas 2016 I 33 0Documento9 páginasGuia de Practicas 2016 I 33 0Anonymous q3hUTAAún no hay calificaciones
- Que Es PudmedDocumento15 páginasQue Es PudmedAnonymous q3hUTAAún no hay calificaciones
- Receptores farmacológicos Farmacología IDocumento3 páginasReceptores farmacológicos Farmacología IAnonymous q3hUTAAún no hay calificaciones
- Capacidad amortiguadora de fluidos biológicosDocumento12 páginasCapacidad amortiguadora de fluidos biológicosAnonymous q3hUTAAún no hay calificaciones
- Guia de Practicas Control Microbioogico de Medicamentos Farmac 2016 I 33 0Documento45 páginasGuia de Practicas Control Microbioogico de Medicamentos Farmac 2016 I 33 0analiAún no hay calificaciones
- Fundamento MicrobiologiaDocumento3 páginasFundamento MicrobiologiaAnonymous q3hUTAAún no hay calificaciones
- Interpretación de análisis clínicosDocumento78 páginasInterpretación de análisis clínicosAnonymous q3hUTA0% (1)
- Guia de Bioquimica - 1-200 0Documento11 páginasGuia de Bioquimica - 1-200 0Anonymous q3hUTAAún no hay calificaciones
- Anemia Sideroblastica BEADocumento19 páginasAnemia Sideroblastica BEAAnonymous q3hUTAAún no hay calificaciones
- Proced PastaDocumento5 páginasProced PastaAnonymous q3hUTAAún no hay calificaciones
- Receptores farmacológicos Farmacología IDocumento3 páginasReceptores farmacológicos Farmacología IAnonymous q3hUTAAún no hay calificaciones
- Guía práctica Bioquímica Farmacia 2017Documento40 páginasGuía práctica Bioquímica Farmacia 2017LILIANA0% (1)
- Cuest FarmacoDocumento2 páginasCuest FarmacoAnonymous q3hUTAAún no hay calificaciones
- Fundamento MicrobiologiaDocumento3 páginasFundamento MicrobiologiaAnonymous q3hUTAAún no hay calificaciones
- Atenolol 2Documento15 páginasAtenolol 2Anonymous q3hUTA100% (1)
- Muestreo Hecho BioestadisiticaDocumento4 páginasMuestreo Hecho BioestadisiticaAnonymous q3hUTAAún no hay calificaciones
- Mecanismos de acción farmacológicaDocumento3 páginasMecanismos de acción farmacológicaAnonymous q3hUTAAún no hay calificaciones
- Tarea Intervalo de Confianza 200 0Documento4 páginasTarea Intervalo de Confianza 200 0Anonymous q3hUTAAún no hay calificaciones
- HospitalDocumento14 páginasHospitalAnonymous q3hUTAAún no hay calificaciones
- BIODISPONIBILIDADDocumento2 páginasBIODISPONIBILIDADAnonymous QIfBPavAún no hay calificaciones
- TextoDocumento188 páginasTextoAbdiel BlancoAún no hay calificaciones
- Inmuno Clase 12Documento10 páginasInmuno Clase 12Martina CortesAún no hay calificaciones
- Errores de Medicación en Formulas Magistrales PDFDocumento7 páginasErrores de Medicación en Formulas Magistrales PDFsarimarAún no hay calificaciones
- Padrón Nominal Hta DM Nucleo ViñasDocumento6 páginasPadrón Nominal Hta DM Nucleo Viñaskarolina.villafuerteAún no hay calificaciones
- Pno de AspectoDocumento7 páginasPno de AspectoJacqueline RosalesAún no hay calificaciones
- Combinación de Lamotrigina y Ácido ValproicoDocumento2 páginasCombinación de Lamotrigina y Ácido ValproicoDavid DiazAún no hay calificaciones
- Formulario Nacional de MedicamentosDocumento26 páginasFormulario Nacional de MedicamentosManuel Alejandro Merino Salamanca100% (1)
- TEMP-001-ED.01 Control de Temperatura y Humedad AmbienteDocumento11 páginasTEMP-001-ED.01 Control de Temperatura y Humedad AmbienteNati Martin100% (7)
- 14.historia de La AntibioticoterapiaDocumento66 páginas14.historia de La Antibioticoterapiafsilvaf93Aún no hay calificaciones
- 1683 DioxadolDocumento5 páginas1683 Dioxadolmcwillgo100% (1)
- Trabajo 2º Parcial FarmacologiaDocumento7 páginasTrabajo 2º Parcial FarmacologiaMauricio De assis CanoAún no hay calificaciones
- 0106 Desarrollo Farmacéutico PDFDocumento4 páginas0106 Desarrollo Farmacéutico PDFPosada DosAún no hay calificaciones
- Unidad 1 Tarea 2 Principios Generales Farmacologia Laura Marcela ZambranoDocumento9 páginasUnidad 1 Tarea 2 Principios Generales Farmacologia Laura Marcela Zambranolaura zambranoAún no hay calificaciones
- Que Es DrogaDocumento12 páginasQue Es DrogaBoris Milton Mamani IchutaAún no hay calificaciones
- Farmacología - QuinolonasDocumento2 páginasFarmacología - QuinolonasRoger Alejandro MontoyaAún no hay calificaciones
- Vía de Administración IntravascularDocumento4 páginasVía de Administración IntravascularIsabel MartínezAún no hay calificaciones
- CSF Reglamento de Control de Dopaje Edición 2009Documento27 páginasCSF Reglamento de Control de Dopaje Edición 2009Daniel Andrés Salvador EspinosaAún no hay calificaciones
- Monografia de Intramuscular 2Documento7 páginasMonografia de Intramuscular 2022200587kAún no hay calificaciones
- Vademecum PediatricoDocumento5 páginasVademecum PediatricoLescar ArguelloAún no hay calificaciones
- Adquisición y manejo de medicamentos controladosDocumento30 páginasAdquisición y manejo de medicamentos controladosLeslyAnguloAún no hay calificaciones
- Clase 8. Farmacología Endocrinometabólica IIIDocumento43 páginasClase 8. Farmacología Endocrinometabólica IIIElizabeth Amaya 2Aún no hay calificaciones
- Fórmula médica para pañales y medicamentosDocumento7 páginasFórmula médica para pañales y medicamentosEsthefaniaAngelAún no hay calificaciones
- Ketamine - Drug Information - UpToDateDocumento39 páginasKetamine - Drug Information - UpToDateRenzo Vasquez VarillasAún no hay calificaciones
- Anestesicos LocalesDocumento5 páginasAnestesicos Localesjhony_prieto92Aún no hay calificaciones
- Inadecuada Administración de MedicamentosDocumento26 páginasInadecuada Administración de Medicamentosshareligamer28Aún no hay calificaciones
- Tema 12 PPT TRATAMIENTO DE URGENCIAS Y EMERGENCIAS HIPERTENSIVAS Eva AlfaroDocumento18 páginasTema 12 PPT TRATAMIENTO DE URGENCIAS Y EMERGENCIAS HIPERTENSIVAS Eva AlfarojernsssAún no hay calificaciones
- KasaDocumento6 páginasKasaGloria Velez MaciasAún no hay calificaciones
- Arsenal Farmacologico Terapeutico HPHDocumento39 páginasArsenal Farmacologico Terapeutico HPHBelén Hernández Díaz100% (1)
- Anti Helm Into SDocumento15 páginasAnti Helm Into SNico Andres CastroAún no hay calificaciones