Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Estadosdelamateria 140724161407 Phpapp01
Cargado por
wendy vargas0 calificaciones0% encontró este documento útil (0 votos)
11 vistas27 páginasnmbbmbmb
Título original
estadosdelamateria-140724161407-phpapp01
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentonmbbmbmb
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
11 vistas27 páginasEstadosdelamateria 140724161407 Phpapp01
Cargado por
wendy vargasnmbbmbmb
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 27
ESTADOS DE LA MATERIA
En ciencia, se entiende por materia. Este
concepto está asociado con todo aquello que
nos rodea y que podemos percibir por los
sentidos. Es de lo que está hecho
el Universo: el aire, las rocas, los mares,
las plantas, los animales, etc. Todo. Y
además sabemos que la materia se presenta
con distintas formas. Que no siempre son
distinguibles y diferenciables a simple vista.
En ciencia, a estas formas se las
denominan estados físicos o estados de
agregación, porque nos dan una idea de
¿Cuántos estados de la materia existen?
En concreto son seis los estados físicos
de la materia admitidos a día de hoy. No
hay ningún error en su número. En la
actualidad el hombre admite la existencia
de, por ahora, seis (6) estados para la
materia:
Sólido
Líquido
Gas
Plasma
Condensado de Bose-Einstein
Condensado fermiónico (de Fermi).
Estado Sólido
Un cuerpo sólido es uno de los Un cubo de
cuatro estados de agregación de hielo es un
la materia (siendo los otros gas, estado solido
líquido, plasma y el Bose-
Einstein), se caracteriza porque
opone resistencia a cambios de
forma y de volumen. Sus
partículas se encuentran juntas y
correctamente ordenadas. Las
moléculas de un sólido tienen
una gran cohesión y adoptan
Manteniendo constante la presión a baja
temperatura los cuerpos se presentan en
forma sólida y encontrándose entrelazados
formando generalmente estructuras cristalinas.
Esto confiere al cuerpo la capacidad de
soportar fuerzas sin deformación aparente.
El sólido más ligero conocido es un material
artificial el Aero gel con una densidad de 3
mg/cm3 o 3 kg/m3, el vidrio, que tiene una
densidad de 1,9 g/cm³, mientras que el más
denso es un metal, el osmio (Os), que tiene
Propiedades de los sólidos
Elasticidad: Un sólido no recupera su forma original
cuando es deformado. Un resorte es un objeto en que
podemos observar esta propiedad ya que vuelve a su
forma original.
Fragilidad: Un sólido puede romperse en muchos
fragmentos (quebradizo).
Dureza: hay sólidos que no pueden ser rayados por
otros más blandos. El diamante es un sólido con
dureza elevada.
Forma definida: Tienen forma definida, son relativamente
rígidos y no fluyen como lo hacen los gases y los
líquidos, excepto bajo presiones extremas del medio.
Alta densidad: Los sólidos tienen densidades
relativamente altas debido a la cercanía de sus
Inercia: es la dificultad o resistencia que opone un
sistema físico o un sistema social a posibles cambios,
en el caso de los sólidos pone resistencia a cambiar
su estado de reposo.
Tenacidad: En ciencia de los Materiales la tenacidad
es la resistencia que opone un material a que se
propaguen fisuras o grietas.
Maleabilidad: Es la propiedad de la materia, que
presentan los cuerpos a ser labrados por deformación.
La maleabilidad permite la obtención de delgadas
láminas de material sin que éste se rompa, teniendo
en común que no existe ningún método para
cuantificarlas.
Ductilidad: La ductilidad se refiere a la propiedad de
Estado Liquido
El estado líquido es un estado Agua
de agregación de la materia
intermedio entre el estado sólido
y el estado gaseoso. Las
moléculas de los líquidos no
están tan próximas como las de
los sólidos, pero están menos
separadas Su forma es esférica
si sobre él no actúa ninguna
fuerza externa. Por ejemplo, una
gota de agua en caída libre
Como fluido sujeto a la fuerza de la gravedad,
la forma de un líquido queda definida por su
contenedor. En un líquido en reposo sujeto a
la gravedad en cualquier punto de su seno
existe una presión de igual magnitud hacia
todos los lados, tal como establece el principio
de Pascal. Si un líquido se encuentra en
reposo, la presión hidrostática en cualquier
punto del mismo viene dada por:
Estado Gaseoso
Los gases, igual que los Gas
líquidos, no tienen forma fija pero,
a diferencia de éstos, su
volumen tampoco es fijo. También
son fluidos, como los líquidos.
En los gases, las fuerzas que
mantienen unidas las partículas
son muy pequeñas. En un gas
el número de partículas por
unidad de volumen es también
muy pequeño.
Las partículas se mueven de forma
desordenada, con choques entre ellas y con las
paredes del recipiente que los contiene. Esto
explica las propiedades de expansibilidad y
compresibilidad que presentan los gases: sus
partículas se mueven libremente, de modo que
ocupan todo el espacio disponible. La
compresibilidad tiene un límite, si se reduce
mucho el volumen en que se encuentra
confinado un gas éste pasará a estado líquido.
Al aumentar la temperatura las partículas se
mueven más deprisa y chocan con más energía
Si calentamos un líquido, se transforma en gas.
Este proceso recibe el nombre de vaporización.
Cuando la vaporización tiene lugar en toda la
masa de líquido, formándose burbujas de vapor
en su interior, se denomina ebullición. También
la temperatura de ebullición es característica de
cada sustancia y se denomina punto de
ebullición. El punto de ebullición del agua es
100 °C a la presión atmosférica normal.
Plasma
En física y química, se
Lámpara de
denomina plasma al cuarto Plasma
estado de agregación de la
materia, un estado fluido similar
al estado gaseoso pero en el
que determinada proporción de
sus partículas están cargadas
eléctricamente y no poseen
equilibrio electromagnético, por
eso son buenos conductores
eléctricos y sus partículas
Formas comunes de plasma
Producidos Plasmas espaciales
Plasmas terrestres
artificialmente y astrofísicos:
•En los televisores •Los rayos durante •Las estrellas (por
o monitores una tormenta. ejemplo, el Sol).
con pantalla de •La ionosfera. •Los vientos solares.
plasma. •La aurora boreal. •El medio
•En el interior de interplanetario (la
los tubos materia entre
fluorescentes (ilumina los planetas
ción de bajo del Sistema Solar.
consumo).8
•En soldaduras de
arco eléctrico bajo
protección por gas
(TIG, MIG/MAG,
Condensado de Bose-
Einstein Distribución de momentos
que confirma la
En física, el condensado de existencia de un nuevo
estado de agregación de
Bose-Einstein es el estado de la materia, el condensado
de Bose-Einstein.
agregación de la materia que
se da en ciertos materiales a
muy bajas temperaturas. La
propiedad que lo caracteriza es
que una cantidad macroscópica
de las partículas del material
pasan al nivel de mínima
energía, denominado estado
fundamental.
El condensado es una propiedad
cuántica que no tiene análogo clásico.
Debido al principio de exclusión de
Pauli, sólo las partículas bosónicas
pueden tener este estado de
agregación: si las partículas que se
han enfriado son fermiones, lo que se
encuentra es un líquido de Fermi.
Eric Cornell y Carl Wieman lograron
en 1995 por primera vez, enfriar
átomos al más bajo nivel de energía,
menos de una millonésima
de Kelvin por encima del cero
absoluto, una temperatura muy inferior
a la mínima temperatura encontrada
en el espacio exterior. Utilizaron el
método de enfriamiento por láser,
haciendo que la luz rebote en los
Cuando los fotones rebotan en el
átomo, el electrón en el átomo que
absorbe el fotón salta a un nivel
superior de energía y rápidamente
salta de regreso a su nivel original,
expulsando el fotón de nuevo,
logrando el descenso de su
temperatura.
Condensado fermiónico
El condensado fermiónico es un
estado de agregación de la
materia en el que la materia
adquiere superfluidez. Se
produce a temperaturas muy
bajas, cercanas al cero absoluto.
Fue creado en la Universidad
de Colorado por primera vez en
1999; el primer condensado de
Fermi formado por átomos fue
creado en 2003.
El principio de exclusión de Pauli
establece que es imposible que dos
fermiones ocupen el mismo lugar. Esto
con el tiempo se ha alterado puesto
que los electrones estabilizan a la
onda dándole una forma estable.
Deborah S. Jin, Markus Greiner y
Cindy Regal han dado un paso más
y también, gracias a la ultra
congelación de partículas, han
el gas fermiónico está completamente
integrado por fermiones. Éstos, a
diferencia de los bosones, son poco
sociables y por definición nunca dos
de ellos pueden ocupar el mismo
estado de movimiento. Un par de
fermiones idénticos no pueden ocupar
el mismo estado cuántico. A altas
temperaturas, las conductas de estas
partículas elementales son casi
es en este instante cuando se
acentúa el carácter antagónico de
bosones y fermiones.
¿Pero cómo se comportan los
fermiones ultra congelados?
Para resolver el enigma, los físicos de
Boulder usaron rayos láser para
atrapar una pequeña nube de 500.000
átomos de potasio. Limitando su
movimiento natural, enfriaron los
átomos a 50.000 millonésimas de
grados por encima del cero absoluto.
Por su carácter arisco, los fermiones
de esos átomos deberían repelerse,
pero no fue así. Al aplicar un campo
crearon un maravilloso condensado.
Según los padres del nuevo estado,
este hallazgo podría dar pie a una
amplia gama de aplicaciones prácticas.
Por ejemplo, el gas fermiónico ofrece
una nueva línea de investigación en
el campo de la superconductividad, el
fenómeno por el que la electricidad
discurre sin resistencia alguna, y con
esto controlar a los fermiones con
Otros posibles estados de la materia
Existen otros posibles estados de la materia;
algunos de estos sólo existen bajo condiciones
extremas, como en el interior de estrellas muertas,
o en el comienzo del universo después del Big
Bang o gran explosión:
Superfluido
Materia degenerada
Materia fuertemente simétrica
Materia débilmente simétrica
Materia extraña o materia de quarks
Superfluido polaritón
Materia fotónica
También podría gustarte
- AnalisiDocumento4 páginasAnalisiwendy vargasAún no hay calificaciones
- AnalisisjajDocumento1 páginaAnalisisjajwendy vargasAún no hay calificaciones
- Analisis PDFDocumento1 páginaAnalisis PDFwendy vargasAún no hay calificaciones
- Producción Pintura VinílicaDocumento11 páginasProducción Pintura VinílicaPtar SlpAún no hay calificaciones
- Es Manual de PinturasDocumento17 páginasEs Manual de PinturasAlan Eric SanguinettiAún no hay calificaciones
- AnalisisjajDocumento1 páginaAnalisisjajwendy vargasAún no hay calificaciones
- Analisis PDFDocumento1 páginaAnalisis PDFwendy vargasAún no hay calificaciones
- La Pirólisis de Los Residuos Plásticos Implica La Descomposición Térmica en El Ausencia de OxígenoDocumento1 páginaLa Pirólisis de Los Residuos Plásticos Implica La Descomposición Térmica en El Ausencia de Oxígenowendy vargasAún no hay calificaciones
- Technical Background Wetting and Dispersing AdditivesDocumento12 páginasTechnical Background Wetting and Dispersing AdditivesJose L CamaAún no hay calificaciones
- La Pirólisis de Los Residuos Plásticos Implica La Descomposición Térmica en El Ausencia de OxígenoDocumento1 páginaLa Pirólisis de Los Residuos Plásticos Implica La Descomposición Térmica en El Ausencia de Oxígenowendy vargasAún no hay calificaciones
- Pinturas Okokok PDFDocumento76 páginasPinturas Okokok PDFSarah ClarkAún no hay calificaciones
- LatexDocumento11 páginasLatexJavier Ceja PerezAún no hay calificaciones
- Método de BroydenDocumento2 páginasMétodo de Broydenwendy vargasAún no hay calificaciones
- Tema 4 Operaciones UnitariasDocumento29 páginasTema 4 Operaciones UnitariassinforossoAún no hay calificaciones
- ProcesoLixiviaciónRecuperaMineralesValiososDocumento2 páginasProcesoLixiviaciónRecuperaMineralesValiososFIDELOSWALDOAún no hay calificaciones
- Ecuaciones diferenciales resueltasDocumento265 páginasEcuaciones diferenciales resueltasJ Deep AguirreAún no hay calificaciones
- IMPRIMIRDocumento2 páginasIMPRIMIRwendy vargasAún no hay calificaciones
- IMPRIMIRDocumento2 páginasIMPRIMIRwendy vargasAún no hay calificaciones
- Instrumentos de Medicion de Presión PDFDocumento1 páginaInstrumentos de Medicion de Presión PDFwendy vargasAún no hay calificaciones
- 1Documento6 páginas1wendy vargasAún no hay calificaciones
- Ex PosicionDocumento5 páginasEx Posicionwendy vargasAún no hay calificaciones
- Cúal Es La Diferencia Entre La Velocidad Corriente Arriba y La Velocidad Corriente LibreDocumento1 páginaCúal Es La Diferencia Entre La Velocidad Corriente Arriba y La Velocidad Corriente Librewendy vargasAún no hay calificaciones
- Ana GabrielaDocumento25 páginasAna Gabrielawendy vargasAún no hay calificaciones
- La Pirólisis de Los Residuos Plásticos Implica La Descomposición Térmica en El Ausencia de OxígenoDocumento1 páginaLa Pirólisis de Los Residuos Plásticos Implica La Descomposición Térmica en El Ausencia de Oxígenowendy vargasAún no hay calificaciones
- Nombre SDocumento1 páginaNombre Swendy vargasAún no hay calificaciones
- 6 - Caida LibreDocumento17 páginas6 - Caida LibreJ Luis TupiaAún no hay calificaciones
- 1Documento6 páginas1wendy vargasAún no hay calificaciones
- FiltracionDocumento9 páginasFiltracionpaolatenjohAún no hay calificaciones
- SustanciaDocumento1 páginaSustanciawendy vargasAún no hay calificaciones
- Cuchara Trituradora Marca MontabertDocumento4 páginasCuchara Trituradora Marca MontabertOthoniel CastillaAún no hay calificaciones
- Componente Práctico Autónomo EsfuerzosDocumento21 páginasComponente Práctico Autónomo EsfuerzosIsmael MedinaAún no hay calificaciones
- Abreviaturas de Comandos de Autocad en InglesDocumento8 páginasAbreviaturas de Comandos de Autocad en InglesJeorge Esrom ChambiAún no hay calificaciones
- Sistema de CristalizacionDocumento5 páginasSistema de CristalizacionFabiola CalderonAún no hay calificaciones
- PVCDocumento12 páginasPVCyeimy cruz farcequeAún no hay calificaciones
- Tanques de Lavado: Separación de Agua y PetróleoDocumento2 páginasTanques de Lavado: Separación de Agua y PetróleoPablo TapiaAún no hay calificaciones
- ISCO Catalog vm2022 - 3Documento1 páginaISCO Catalog vm2022 - 3nestorAún no hay calificaciones
- 1 Tema I Mec 101Documento19 páginas1 Tema I Mec 101Milton Arriaga MenachoAún no hay calificaciones
- Pets-Vyf.006 Movimiento de Tierras y Demoliciones Seijj CicDocumento3 páginasPets-Vyf.006 Movimiento de Tierras y Demoliciones Seijj CicAlexander Tamayo VidalAún no hay calificaciones
- Sistema Hidráulico de Un AvionDocumento14 páginasSistema Hidráulico de Un AvionRamses RodriguezAún no hay calificaciones
- Presentacion Formaleta Metalica AndescolDocumento12 páginasPresentacion Formaleta Metalica Andescolandres_hernandez_30Aún no hay calificaciones
- Analicen Las Fuentes de Poder A Disposición de Caruso para Dirigir A Los DecoradoresDocumento3 páginasAnalicen Las Fuentes de Poder A Disposición de Caruso para Dirigir A Los DecoradoresMagnolia CarreñoAún no hay calificaciones
- Lab. de Accionamiento Nro4 2011Documento11 páginasLab. de Accionamiento Nro4 2011Juan Orihuela EnriquezAún no hay calificaciones
- Práctica 4 Distribuidor Vertical de LadrillosDocumento6 páginasPráctica 4 Distribuidor Vertical de LadrillosJuanCruzZamoraAún no hay calificaciones
- Practica No. 1 Laboratorio (I)Documento10 páginasPractica No. 1 Laboratorio (I)Juan-Carlos OrtizAún no hay calificaciones
- Tutorial de Visual Basic ScriptingDocumento162 páginasTutorial de Visual Basic ScriptingManolo Josè Pajaro BorrasAún no hay calificaciones
- Cálculo iluminación oficinas SENADocumento3 páginasCálculo iluminación oficinas SENAPeru Divino PeruAún no hay calificaciones
- Variables UrbanasDocumento6 páginasVariables UrbanasVeronica RodriguezAún no hay calificaciones
- v30 TraducidoDocumento66 páginasv30 TraducidoKaren Estefani Monge HerreraAún no hay calificaciones
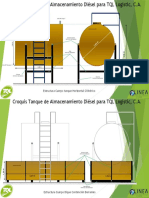
- Croquis Tanque Gasoil TQL Logistic C.A.Documento2 páginasCroquis Tanque Gasoil TQL Logistic C.A.Efrain HernandezAún no hay calificaciones
- Manual Mindjet Mindmanager6 1233189050922765 3Documento22 páginasManual Mindjet Mindmanager6 1233189050922765 3Juan Carlos Hernandez CriadoAún no hay calificaciones
- Composición y Propiedades Del Gas Natural en La GuajiraDocumento9 páginasComposición y Propiedades Del Gas Natural en La GuajiraAlexander Illidge AraujoAún no hay calificaciones
- Parametros de Mapeo Geotecnico DisertacionDocumento22 páginasParametros de Mapeo Geotecnico DisertacionCristhiam Bladimir Huallanca Sosa0% (1)
- Modem Router Wifi CBX 1511 Adsl Aba Cantv PDFDocumento2 páginasModem Router Wifi CBX 1511 Adsl Aba Cantv PDFFrancisco AlvarezAún no hay calificaciones
- CatalogoNewtek Dientes AcrilicoDocumento6 páginasCatalogoNewtek Dientes AcrilicoKarina OjedaAún no hay calificaciones
- Memoria de Cálculo Compuertas-Molienda CrovisaDocumento21 páginasMemoria de Cálculo Compuertas-Molienda CrovisaDeibyd Ramos SulloAún no hay calificaciones
- Cuestionario Metodología de OyMDocumento3 páginasCuestionario Metodología de OyMSantanecoAún no hay calificaciones
- Hard FillDocumento487 páginasHard Filltin gomez rosasAún no hay calificaciones
- Mantenimiento de PararrayosDocumento4 páginasMantenimiento de PararrayosluisalidaAún no hay calificaciones
- Mapetex Sel SP PDFDocumento2 páginasMapetex Sel SP PDFYatsen Jepthe Maldonado SotoAún no hay calificaciones