Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Determinacion de Orden de Reaccion
Cargado por
marielaDerechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Determinacion de Orden de Reaccion
Cargado por
marielaCopyright:
Formatos disponibles
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE
ACTIVACIN
OBJETIVO: Comprobacin de la influencia de la concentracin de los reactivos sobre la
velocidad de reaccin. Obtencin experimental de la velocidad media de reaccin y de
los rdenes parciales de cada reactivo en una reaccin qumica.
FUNDAMENTO
La velocidad de una reaccin qumica aumenta con la concentracin de los reactivos,
con la temperatura y con la presencia de un catalizador. Vamos a comprobar estos
efectos sobre la reaccin redox entre los iones yodato, IO3, y los iones hidrgeno sulfito,
HSO3 en disolucin acuosa. La reaccin ajustada es:
IO3(ac) + 3 HSO3(ac) 3 SO42(ac) + 3 H +(ac) + I(ac)
Para observar el final de la reaccin, se pone un exceso de yodato y se aade un poco
de almidn. As, cuando se agotan los iones hidrgeno sulfito, tiene lugar la reaccin
redox siguiente:
5 I(ac) + IO3(ac) + 6H+ (ac) 3 H2O(l) + 3 I2 (ac)
El yodo, I2, liberado en este proceso produce inmediatamente con el almidn un intenso
color azul, que indicar el final de la reaccin principal.
Factores que afectan a la velocidad de las reacciones. Existen varios factores que
afectan la rapidez de una reaccin qumica: la concentracin de los reactivos, la
temperatura, la existencia de catalizadores y la superficie de contacto tanto de los
reactivos como del catalizador. Los catalizadores pueden aumentar o disminuir la
velocidad de reaccin
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
INTRODUCCION
En dicha prctica comprobaremos como en la velocidad de reaccin qumica influyen la
composicin de los reactivos, la temperatura y por ltimo el efecto que produce introducir
un catalizador a la reaccin. Para esta prctica utilizaremos iones yodato IO3- y iones
hidrogeno sulfito
HSO3IO3-(ac) + 3HSO3-(ac) 3SO42-(ac) + 3H+(ac) + I-(ac)
Tambin se aborda algunos aspectos cuantitativos de la velocidad de las reacciones
qumicas. En particular, nos interesa conocer y controlar la influencia cintica de la
concentracin y de la temperatura, y su reflejo cuantitativo en forma de ecuaciones o
leyes cinticas empricas. Para conseguir un mejor aprovechamiento de las experiencias
a realizar, es necesario que domines los fundamentos y significado de los conceptos ms
bsicos que se definen en Cintica Qumica. En primer lugar, debemos definir una
magnitud que nos mida la velocidad de reaccin de modo objetivo. Para una reaccin
genrica:
aA + bB +.....pP + qQ
MATERIAL Y REACTIVOS
Material Reactivos
3 recipientes de vidrio Yodato de potasio 0.150 M, KIO3(ac)
1 matraz Erlenmeyer de 50 mL tapn Hidrogeno de sulfito de sodio 0.1 M,
NaHSO3(ac)
1 perilla 1 pipeta graduada de 1, mL Disolucin de almidn
1 vaso de pp de 100 mL o menor Nitrato de cobre (II) 0.02 M
1 cronometro 1 termmetro Agua
MTODO EXPERIMENTAL
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
1.-EFECTO DE LA CONCENTRACIN SOBRE LA VELOCIDAD DE REACCIN.
1.1.- Experimentos a temperatura ambiente
Realizaremos una serie de ensayos, a temperatura ambiente, trabajando con exceso de
ion yodato para observar el final de la reaccin. En estas experiencias, modificaremos la
cantidad de IO3y estudiaremos cmo afecta esta variacin al tiempo de reaccin.
Experiencia 1(repetir tres veces):
-Preparar dos matraces Erlenmeyer limpios y aadir las siguientes cantidades:
[e1]: 2mLde una disolucin de yodato 0,150 M y, a continuacin, 5mL de agua. Agitar.
[e2]: 2mL de la disolucin de hidrgeno sulfito 0,020 M y 1mL de la disolucin de almidn
al 2%.Agitar.
-Medir la temperatura de ambas disoluciones, antes de mezclarlas, y
Anotar el resultado.
-Verter, rpidamente, la disolucin con HSO3sobre el Erlenmeyer que contiene la
disolucin de IO3 y
conectar el cronmetro. Agitar, con una varilla y observar atentamente la disolucin hasta
que aparezca el color azul.
-Detener el cronmetro cuando el contenido del matraz se vuelva azul muy oscuro.
Anotar el tiempo de reaccin transcurrido.
-Lavar el material y repetir, dos veces ms, la misma experiencia. Anotar en cada caso
el tiempo de reaccin.
Experiencia 2 (repetir tres veces):
En dos matraces erlenmeyer aadir las cantidades que se indican a continuacin y
repetir, tres veces, la operacin anterior:
[e1]: 1,5 mL de una disolucin de yodato 0,150 M y, a continuacin, 5,5 mL de agua.
Agitar.
[e2]: 2mL de la disolucin de hidrgeno sulfito 0,020 M y 1mL de la disolucin de almidn
al 2%.Agitar.
Anotar el tiempo de reaccin transcurrido
Experiencia 3 (repetir tres veces):
En dos matraces Erlenmeyer aadir las cantidades que se indican a continuacin
y repetir, tres veces, la operacin anterior:
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
[e1]: 1mL de una disolucin de yodato 0,150 M y, a continuacin, 6mL de agua. Agitar.
[e2]: 2mL de la disolucin de hidrgeno sulfito 0,020 M y 1mL de la disolucin de almidn
al 2%.Agitar.
2.-EFECTO DE LA TEMPERATURA SOBRE LA VELOCIDAD DE REACCIN.
Experiencia 4:
-Preparar dos matraces Erlenmeyer limpios y aadir las siguientes cantidades:
[e1]: 2mL de una disolucin de yodato 0,150 M y, a continuacin, 5 mL de agua. Agitar.
[e2]: 2mL de la disolucin de hidrgeno sulfito 0,020 M y 1mL de La disolucin de almidn
al 2%. Agitar.
-Preparar un bao de hielo picado e introducir los dos Erlenmeyer.
-Cuando la temperatura de ambas disoluciones se encuentre entre 5 y 10 C, anotar la
temperatura exacta que marca el termmetro. Verter, rpidamente, la disolucin con
HSO3sobre el Erlenmeyer que contiene la disolucin de IO3y conectar el cronmetro.
-Agitar y observar atentamente la disolucin hasta que aparezca el color azul. Detener
el cronmetro cuando el contenido del matraz se vuelva azul muy oscuro.
3.-EFECTO DE LOS CATALIZADORES
Experiencia 5:
Repetir el ensayo de la experiencia 1 mezclando las disoluciones a temperatura ambiente
y aadiendo 6 gotas de disolucin de nitrato de cobre (II) 0,02 M. Anotar el tiempo de
reaccin transcurrido en la experiencia.
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
TECNICA EXPERIENCIA 1.-EFECTO DE LA CONCENTRACIN SOBRE LA
VELOCIDAD DE REACCIN.
Segundo matraz:2mL
Primer matraz:2mLde
Preparar dos matraces de la disolucin de
una disolucin de
Erlenmeyer y aadir hidrgeno sulfito 0,020
yodato 0,150 M y, a
las siguientes M y 1mL de la
continuacin, 5mL de
cantidades: disolucin de almidn
agua. Agitar
al 2%.Agitar.
Anotar el resultVerter,
conectar el
rpidamente, la
Medir la temperatura cronmetro. Agitar, con
disolucin con
de ambas disoluciones, una varilla y observar
HSO3sobre el
antes de mezclarlas, y atentamente la
Erlenmeyer que
anotar el resultado disolucin hasta que
contiene la disolucin
aparezca el color azul.
de IO3ado
Detener el cronmetro
cuando el contenido
del matraz se vuelva
azul muy oscuro.
Anotar el tiempo de
reaccin transcurrido.
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
Experiencia 2 (repetir tres veces):
En dos
Segundo
matraces Primer
matraz: 2mL
erlenmeyer matraz: 1,5
de la
aadir las mL de una
disolucin de Anotar el
cantidades disolucin de
hidrgeno tiempo de
que se indican yodato 0,150
sulfito 0,020 reaccin
a continuacin M y, a
M y 1mL de la transcurrido
y repetir, tres continuacin,
disolucin de
veces, la 5,5 mL de
almidn al
operacin agua. Agitar
2%.Agitar
anterior:
Experiencia 3 (repetir tres veces):
En dos
matraces
Erlenmeyer 2mL de la
1mL de una
aadir las disolucin de
disolucin de
cantidades hidrgeno Anotar el
yodato 0,150
que se sulfito 0,020 tiempo de
M y, a
indican a M y 1mL de reaccin
continuacin,
continuacin la disolucin transcurrido
6mL de
y repetir, de almidn
agua. Agitar.
tres veces, la al 2%.Agitar.
operacin
anterior:
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
TECNICA 2.-EFECTO DE LA TEMPERATURA SOBRE LA VELOCIDAD DE
REACCIN. Experiencia 4:
[e1]: 2mL de una [e2]: 2mL de la
Preparar dos matraces
disolucin de yodato disolucin de hidrgeno
Erlenmeyer limpios y
0,150 M y, a sulfito 0,020 M y 1mL de
aadir las siguientes
continuacin, 5 mL de La disolucin de almidn
cantidades:
agua. Agitar. al 2%. Agitar.
-Cuando la temperatura Verter, rpidamente, la
de ambas disoluciones disolucin con
Preparar un bao de
se encuentre entre 5 y HSO3sobre el
hielo picado e introducir
10 C, anotar la Erlenmeyer que contiene
los dos Erlenmeyer.
temperatura exacta que la disolucin de IO3y
marca el termmetro conectar el cronmetro.
Agitar y observar
atentamente la disolucin
hasta que aparezca el
color azul. Detener el
cronmetro cuando el
contenido del matraz se
vuelva azul muy oscuro.
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
3.-EFECTO DE LOS CATALIZADORES
Experiencia 5:
Repetir el
ensayo de la Aadir 6 gotas Anotar el
experiencia 1 de disolucin tiempo de
mezclando las de nitrato de reaccin
disoluciones a cobre (II) 0,02 transcurrido en
temperatura M. la experiencia
ambiente
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
1.- Efecto de la concentracin sobre la velocidad de reaccin.
a.- Escribir la reaccin qumica ajustada y completar el
Vtotal =
[IO3], [HSO3],
mol/L: mol/L:
t4(s) t5(s) t6(s) t7(s) t8(s [IO3] 1[HSO
) T , ]
Exp 3
t1 (s) t2 (s) t3(s) (C mol/ vo
.
) L mol/L.s
3 t
1h 4 min 1h 2 50 58 1h
1 47.3 18 50.3 min min min 10
5 min min 2 seg min
1h 8 min 54mi 1h 52mi
35 38 59se n 10seg n
2 18
min min g 26se 38se
min
g g
1h 4 min 44mi 1h 50mi
29 48 n 0.1se n
3 19
min min 27se g 19se
min
g g
23 24 55 27
10 57.4 23 min min min min
4
seg 0 min min 18seg 42
seg
6.25 30 28min 8 min
47.9 15
5 min min 0.3 17
0 min min
seg seg
siguiente cuadro:
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
B.- Haciendo uso de los tiempos de reaccin y suponiendo una cintica de la forma v
k[IO3 ]m[HSO3 ]3 determinar el orden parcial de reaccin para el yodato.
Relacin de
Clculos para determinar el orden de reaccin
velocidades
v1
v2
v1
v3
Ley cintica y orden
global de reaccin
2.- Efecto de la temperatura sobre la velocidad de reaccin.
A.- Complete el siguiente cuadro con los datos obtenidos en la experiencia 4 y
comprelos con los de la prueba 1 realizada previamente.
1[HSO ]
T [IO3] 3
Exp. t1 (s) vo mol/L.s
(C) [HSO3]
3 t
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
B.- Explicar que influencia tiene la temperatura sobre la velocidad de reaccin. Razone
la respuesta.
C.- Calcular la energa de activacin utilizando los datos cinticos de las experiencias 1
y 4. Detalle todos los pasos necesarios.
El cambio de temperatura en la reaccin provoca un
Ecuacin general de incremento de la velocidad de las partculas, ya que la
Arrhenius velocidad de reaccin se duplica por cada 10 C de aumento
de la temperatura. K=AE-EA/RT
Ec. que relaciona la Ecuacin general de Arrhenius Ec. que relaciona la Ea con
Ea con dos dos temperaturas Ln(k1/k2)=(Ea/R)x(1/T2 1/T1)
temperaturas
Expresin que
relaciona k1/k2 con
K1 x t1 = k2 x t2 (k1/k2)=(t2/t1)
los tiempos de
reaccin
Ln(t2/t1)=(Ea/R)x(1/T2 1/T1); Ln(115/60)=(Ea/8,314)x(1/280
Clculos para 1/294,6); 0,65=(Ea/8,314)x 1,77 x10-4;
obtener Ea Ea= 30531,64 J/mol 30,53164 kJ/mol
3.- Efecto de los catalizadores.
A.- Complete el siguiente cuadro:
1[HSO ]
[IO3] 3
Exp. Catalizador t1 (s) vo mol/L.s
[HSO3]
3 t
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
OBSERVACIONES
Se prepararon las 5 experiencias con las cantidades de reactivos que se solicitaron en
cada tecnica de acuerdo a un orden, se realizaron las tres experiencias donde se queria
comprobar mediante el experimento el efecto de la concentracion sobre la velocidad de
reaccion, se realizaron una serie de ensayos a temperatura ambiente, se trabaj con un
exceso de ion yodato y observar la reaccin, se modific as mismo la cantidad de IO 3- .
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
En la experiencia 4 y 5 donde se debi observar el efecto de la temperatura sobre la
velocidad de reaccin, se modific la temperatura a 10 C, se conoci la rapidez o
velocidad de una reaccin s se ve afectada por la variacin de la temperatura ya que en
esta parte de la prctica se poda observar que la velocidad de reaccin de la muestra
fra fu excesivamente lenta con unos tiempos grandes mostrados en el cronometro.
Y en la experiencia 5, el ion cobre (II), actu como catalizador en la reaccin, lo que
provoca un incremento de velocidad de la reaccin pero sin consumirse sobre dicha
reaccin, ya que el catalizador facilita que los reactivos se transformen en productos. La
Ea es menor que en una reaccin sin catalizar.
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
UNIVERSIDAD VERACRUZANA
FACULTAD DE CIENCIAS QUMICAS
LABORATORIO DE EQUILIBRIO Y CINTICA QUMICA
PRACTICA 8. DETERMINACIN DEL ORDEN DE REACCIN Y ENERGA DE ACTIVACIN
CONCLUSION
La prctica no pudo realizarse con xito de acuerdo a lo comprendido dentro de la teora
ya que la reaccin HSO3IO3-(ac) + 3HSO3-(ac) 3SO42-(ac) + 3H+(ac) + I-(ac) no se
llev a cabo, las razones pudieron haber sido que alguno de los reactivos empleados
para esta prctica estaban descompuestos ya que no se obtuvieron las coloraciones
azules esperadas. Por lo cual procedimos a realizar una investigacin para conocer
tericamente que se pretenda aprender en esta prctica y la conclusin fue la siguiente.
En esta prctica se tuvo que observar que dependiendo de qu cantidad utilicemos de
ion yodato y de hidrogeno sulfito, la velocidad de reaccin podr variar pero a cantidades
muy pequeas, mientras que si se utiliza un catalizador como en esta prctica el nitrato
de cobre (II), la disolucin no cambiara pero la velocidad de reaccin se ver afectada
considerablemente incrementando su velocidad hasta el doble de la inicial sin el
catalizador.
Y se tuvo que visualizar que la velocidad de reaccin de la muestra fra (de 5C a 10C)
fue excesivamente lenta. Mientras que la rapidez de reaccin de las otras soluciones (a
temperatura ambiente) debieron ser mucho ms rpidas.
As mismo en esta prctica se debi comprender cmo se ve afectada la velocidad de
una reaccin a travs de diferentes temperaturas y concentraciones.
BIBLIOGRAFIA
Raymond, CHANG. Qumica. 10a Edicin, Editorial Mc. Graw Hill. Mxico D.F
2010.
Chang, Raymond (2002). Qumica. 7 edicin. Mc Graw Hill.
ELABORADO POR: REVIS: APROB:
Mara Guadalupe Cosme Reyes
Ma. Guadalupe Barquet Barquet
FECHA: Mayo 2017 FECHA: FECHA:
REVISIN No. 1 PGINA No. 1 FECHA DE LTIMA REVISIN:
También podría gustarte
- LAB 1 - Factores Que Afectan La Velocidad de La ReaccionDocumento16 páginasLAB 1 - Factores Que Afectan La Velocidad de La ReaccionAlejandra CarlosamaAún no hay calificaciones
- Practica N °2Documento6 páginasPractica N °2mijaheel ferrufinoAún no hay calificaciones
- Efectos de La TemperaturaDocumento11 páginasEfectos de La TemperaturaSinaí VictoriaAún no hay calificaciones
- Informe 2Documento7 páginasInforme 2JeanAún no hay calificaciones
- Manual Equilibrio ViejitoDocumento30 páginasManual Equilibrio ViejitojesusAún no hay calificaciones
- Previo-5-Efecto de La Temperatura en La Rapidez de Una ReaccionDocumento9 páginasPrevio-5-Efecto de La Temperatura en La Rapidez de Una ReaccionDavid Ramirez Torres100% (4)
- Cinética química: efecto de la concentración en la velocidad de reacciónDocumento10 páginasCinética química: efecto de la concentración en la velocidad de reacciónChrystian Richard Llancuani RojasAún no hay calificaciones
- Cinetica QuimicaDocumento17 páginasCinetica QuimicaLesly CórdovaAún no hay calificaciones
- Subtema 2.3 Practica de Metodos de Velocidad de Reaccion 2Documento9 páginasSubtema 2.3 Practica de Metodos de Velocidad de Reaccion 2Adán Fonseca HernandezAún no hay calificaciones
- Guía N°2 Cinética Química PDFDocumento11 páginasGuía N°2 Cinética Química PDFFernando Samame DelgadoAún no hay calificaciones
- Guia de LaboratorioDocumento5 páginasGuia de Laboratoriotatiana barbosaAún no hay calificaciones
- Velocidad Reacción QuímicaDocumento8 páginasVelocidad Reacción QuímicaAPPY T.N.TAún no hay calificaciones
- Informe de QuimicaDocumento15 páginasInforme de QuimicaYENNY AMANDAAún no hay calificaciones
- Practica de Laboratorio - Cinetica QuimicaDocumento3 páginasPractica de Laboratorio - Cinetica Quimicali100% (1)
- Factores que afectan el equilibrio químicoDocumento10 páginasFactores que afectan el equilibrio químicoLuisYupaAún no hay calificaciones
- Informe N°1 - CoordinacionDocumento11 páginasInforme N°1 - CoordinacionJose AdrianAún no hay calificaciones
- Guia 4 - 5Documento5 páginasGuia 4 - 5MARIA JOSE TRIANA RANGELAún no hay calificaciones
- Informe N 3 Velocidad de ReacciónDocumento7 páginasInforme N 3 Velocidad de ReacciónTalia BarraganAún no hay calificaciones
- Practica Lab-Cinetica QuimicaDocumento4 páginasPractica Lab-Cinetica QuimicaPaul UsquianoAún no hay calificaciones
- MANUAL DE FISICOQUIMICA II AlumnosDocumento19 páginasMANUAL DE FISICOQUIMICA II AlumnosIsabelaEstradaRodriguezAún no hay calificaciones
- Informe 9-Cinetica QuímicaDocumento6 páginasInforme 9-Cinetica QuímicaMari NarvaezAún no hay calificaciones
- G8 - Cinética QuímicaDocumento9 páginasG8 - Cinética QuímicaNeeiVidarteEspinoAún no hay calificaciones
- Guía N°2 Cinética Química-1 PDFDocumento11 páginasGuía N°2 Cinética Química-1 PDFPatricia Angelica ChuraAún no hay calificaciones
- Informe 3 de Laboratorio de Quimica InorganicaDocumento7 páginasInforme 3 de Laboratorio de Quimica InorganicaMauricio Medrano MaciasAún no hay calificaciones
- Relación entre concentración de KI y tiempo en una reacción químicaDocumento12 páginasRelación entre concentración de KI y tiempo en una reacción químicaLuciaAún no hay calificaciones
- PRACTICA #1 QII Influencia de La Naturaleza de Las Sustancias en La VelocidadDocumento4 páginasPRACTICA #1 QII Influencia de La Naturaleza de Las Sustancias en La VelocidadCamila RodriguezAún no hay calificaciones
- Informe de Laboratorio #01 Equilibrio QuimicoDocumento18 páginasInforme de Laboratorio #01 Equilibrio Quimicojhordy hizo jamancaAún no hay calificaciones
- Practica 2 Velocidad de Reacción-EQ.11Documento11 páginasPractica 2 Velocidad de Reacción-EQ.11Astrid AVAún no hay calificaciones
- Informe de Laboratorio N°6Documento28 páginasInforme de Laboratorio N°6Cristian Suarez0% (1)
- Cinética QuímicaDocumento10 páginasCinética QuímicaShalAún no hay calificaciones
- Fisico Quimica Informe 3Documento10 páginasFisico Quimica Informe 3heydeee hinostroza obregonAún no hay calificaciones
- LABO-4-Q MNDocumento17 páginasLABO-4-Q MNNavarro ValeriaAún no hay calificaciones
- Reacciones Quimicas y Ley de Conservacion de La MasaDocumento3 páginasReacciones Quimicas y Ley de Conservacion de La Masaalex0% (1)
- Quimica Inorganica. Reacciones QuimicasDocumento13 páginasQuimica Inorganica. Reacciones QuimicasCristhian Yaranga ÑañaAún no hay calificaciones
- Reporte Practica 12 MaraDocumento6 páginasReporte Practica 12 MaraAndrea Cisneros100% (1)
- Practica de Velocidad de ReaccionDocumento12 páginasPractica de Velocidad de ReaccionJose Maria Quintas GironAún no hay calificaciones
- Practica 5 Laboratorio Integral IIDocumento11 páginasPractica 5 Laboratorio Integral IIIan Mar0% (1)
- Reporte P1 FQ MartesDocumento6 páginasReporte P1 FQ MartesJose MaresAún no hay calificaciones
- Práctica No. 2Documento10 páginasPráctica No. 2angelesAún no hay calificaciones
- Ley de CosenosDocumento12 páginasLey de CosenosPaola QuizhpeAún no hay calificaciones
- Guia de Laboratorio Cinetica Quimica 1 para 3° MedioDocumento4 páginasGuia de Laboratorio Cinetica Quimica 1 para 3° MedioEsteban Junox Belial CortesAún no hay calificaciones
- Practica 10,11,12Documento13 páginasPractica 10,11,12Rosi GonzalezAún no hay calificaciones
- Cinetica CorregidoDocumento9 páginasCinetica CorregidoRosa CordovaAún no hay calificaciones
- Practica 8. PRINCIPIO DE LA CONSERVACIÓN DE LA MATERIA-1Documento4 páginasPractica 8. PRINCIPIO DE LA CONSERVACIÓN DE LA MATERIA-1lyfaAún no hay calificaciones
- Trabajo de Labo #8Documento12 páginasTrabajo de Labo #8Rosmery GonzalesAún no hay calificaciones
- Reaccion de VelocidadDocumento7 páginasReaccion de Velocidadpatricia leonAún no hay calificaciones
- Practicas 2bach QuimicaDocumento36 páginasPracticas 2bach QuimicaMontserrat GarcíaAún no hay calificaciones
- Practica N° 12Documento12 páginasPractica N° 12Wilfredo Gutierrez AllpaccaAún no hay calificaciones
- Práctica 4 - Cinética QuímicaDocumento9 páginasPráctica 4 - Cinética QuímicaGerardo Escamilla PerezAún no hay calificaciones
- Informe - Cinética QuímicaDocumento12 páginasInforme - Cinética QuímicaKatherine Esmeralda Correa MachareAún no hay calificaciones
- Informe Nº2Documento8 páginasInforme Nº227 Luis Enrique RomeroAún no hay calificaciones
- Factores que influyen en la velocidad de reacción químicaDocumento13 páginasFactores que influyen en la velocidad de reacción químicaCESAR AUGUSTO CHAMPI PALOMINOAún no hay calificaciones
- Mol y estequiometria en la reacción de MgCO3 con H2SO4Documento7 páginasMol y estequiometria en la reacción de MgCO3 con H2SO4CRISTAL GONZALEZAún no hay calificaciones
- Reporte 4 LabQuiDocumento12 páginasReporte 4 LabQuiPablo Andres Salazar SabillonAún no hay calificaciones
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadDe EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadAún no hay calificaciones
- Termodinámica clásica. Protocolos experimentales sobre primera y segunda leyes, y sobre potenciales selectosDe EverandTermodinámica clásica. Protocolos experimentales sobre primera y segunda leyes, y sobre potenciales selectosAún no hay calificaciones
- Fermentacion Lactica YogurtDocumento4 páginasFermentacion Lactica YogurtYris100% (1)
- 458 2013 07 24 Cap 5 Proteinas PDFDocumento4 páginas458 2013 07 24 Cap 5 Proteinas PDFElizabeth AguilarAún no hay calificaciones
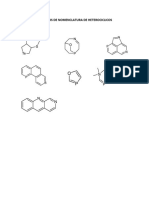
- Ejercicios de Nomenclatura de HeterociclicosDocumento1 páginaEjercicios de Nomenclatura de HeterociclicosmarielaAún no hay calificaciones
- HeterociclicaDocumento2 páginasHeterociclicamarielaAún no hay calificaciones
- Artículo de InvestigaciónDocumento6 páginasArtículo de InvestigaciónmarielaAún no hay calificaciones
- Sintesis Del 3Documento1 páginaSintesis Del 3marielaAún no hay calificaciones
- Producción de MetanoDocumento5 páginasProducción de MetanomarielaAún no hay calificaciones
- Propiedades Fisicas y Toxicologicas Del ZincDocumento1 páginaPropiedades Fisicas y Toxicologicas Del ZincmarielaAún no hay calificaciones
- Producción de MetanoDocumento5 páginasProducción de MetanomarielaAún no hay calificaciones
- Síntesis 2-fenil-bencimidazol microondasDocumento1 páginaSíntesis 2-fenil-bencimidazol microondasmarielaAún no hay calificaciones
- DocumentoDocumento13 páginasDocumentomarielaAún no hay calificaciones
- Optimizing Culturing Conditions For Bacillus SubtilisDocumento8 páginasOptimizing Culturing Conditions For Bacillus SubtilismarielaAún no hay calificaciones
- FermentacionesDocumento3 páginasFermentacionesmarielaAún no hay calificaciones
- Síntesis de Ácido BarbitúricoDocumento1 páginaSíntesis de Ácido BarbitúricomarielaAún no hay calificaciones
- Práctica 13Documento1 páginaPráctica 13marielaAún no hay calificaciones
- Practica 8 Naranja II (Diazo Compuestos)Documento14 páginasPractica 8 Naranja II (Diazo Compuestos)mariela100% (1)
- YogurtDocumento2 páginasYogurtmarielaAún no hay calificaciones
- Alimentos ProcesadosDocumento2 páginasAlimentos ProcesadosmarielaAún no hay calificaciones
- YogurtDocumento1 páginaYogurtmarielaAún no hay calificaciones
- YogurtDocumento1 páginaYogurtmarielaAún no hay calificaciones
- Optimizing Culturing Conditions For Bacillus SubtilisDocumento8 páginasOptimizing Culturing Conditions For Bacillus SubtilismarielaAún no hay calificaciones
- Fermentacion Lactica YogurtDocumento4 páginasFermentacion Lactica YogurtYris100% (1)
- Elaboración de Yogurt en 4 PasosDocumento3 páginasElaboración de Yogurt en 4 PasosDennysSucAún no hay calificaciones
- Organica 3 Practica 1Documento7 páginasOrganica 3 Practica 1marielaAún no hay calificaciones
- Definición de Un Ciclo Económico GermanDocumento5 páginasDefinición de Un Ciclo Económico GermanmarielaAún no hay calificaciones
- Alimentos ProcesadosDocumento2 páginasAlimentos ProcesadosmarielaAún no hay calificaciones
- Determinacion de Orden de ReaccionDocumento14 páginasDeterminacion de Orden de Reaccionmariela0% (1)
- Alimentos ProcesadosDocumento2 páginasAlimentos ProcesadosmarielaAún no hay calificaciones
- Alimentos ProcesadosDocumento2 páginasAlimentos ProcesadosmarielaAún no hay calificaciones
- Determinacion de Orden de ReaccionDocumento14 páginasDeterminacion de Orden de Reaccionmariela0% (1)
- Manual Z50Documento21 páginasManual Z50Sabri DuceAún no hay calificaciones
- Grupo 1 - Principios de Flotacion y Tipos PDFDocumento12 páginasGrupo 1 - Principios de Flotacion y Tipos PDFCarlos Chura AlanguiaAún no hay calificaciones
- LeyesKirchhoffDocumento7 páginasLeyesKirchhoffvicksenteAún no hay calificaciones
- Informe Química AnaliticaDocumento11 páginasInforme Química AnaliticaJuan David Muñoz PasquelAún no hay calificaciones
- CabreraLD Tarea2 Modulo2Documento21 páginasCabreraLD Tarea2 Modulo2julian martinezAún no hay calificaciones
- Anaya Haritza Batx 2 SoluzioakDocumento115 páginasAnaya Haritza Batx 2 SoluzioakSaioa AsuaAún no hay calificaciones
- Trabajo Adolescente y Desercion Escolar en El PeruDocumento49 páginasTrabajo Adolescente y Desercion Escolar en El PeruCIES: Consorcio de Investigación Econimica y Social100% (1)
- Cálculo diferencial aplicacionesDocumento2 páginasCálculo diferencial aplicacionesMelissadiaz26Aún no hay calificaciones
- Guia de EjercciosDocumento4 páginasGuia de EjercciosDavid RiveraAún no hay calificaciones
- Código calculadora C# con operaciones básicasDocumento7 páginasCódigo calculadora C# con operaciones básicasHiciano GarciaAún no hay calificaciones
- Guía práctica de vectores en física aplicadaDocumento45 páginasGuía práctica de vectores en física aplicadaDiego Liza Garcia0% (2)
- Ecuaciones Reducibles A Primer OrdenDocumento7 páginasEcuaciones Reducibles A Primer OrdenMarvinJosephDeLaCruzAntaurcoAún no hay calificaciones
- Guias DecimalesDocumento7 páginasGuias DecimalesYamile Arriega MontenegroAún no hay calificaciones
- Especificaciones Técnicas de PavimentoDocumento48 páginasEspecificaciones Técnicas de PavimentoKONNOR CIA SACAún no hay calificaciones
- Plan de Estudios Laboratorio de Física Básica IDocumento3 páginasPlan de Estudios Laboratorio de Física Básica ILaura AAún no hay calificaciones
- Aplicación de la derivada en ingeniería ambientalDocumento3 páginasAplicación de la derivada en ingeniería ambientalYeico AlvarezAún no hay calificaciones
- CuestionarioDocumento10 páginasCuestionarioANDER EDUARDO CASTILLO VALLEJOSAún no hay calificaciones
- LG X/R: 3 - El Módulo de Análisis de Malla Dimensionamiento de Los ElectrodosDocumento1 páginaLG X/R: 3 - El Módulo de Análisis de Malla Dimensionamiento de Los ElectrodosangelicaAún no hay calificaciones
- Algebra FasorialDocumento17 páginasAlgebra FasorialMiguel RodasAún no hay calificaciones
- Clases Grado 8Documento2 páginasClases Grado 8Angela SteerAún no hay calificaciones
- Adc y TacometroDocumento7 páginasAdc y TacometroluizAún no hay calificaciones
- FS5340213Documento2 páginasFS5340213Clareth Antonio Rodriguez LopezAún no hay calificaciones
- Control de Un Tanque de Agua Con 3 NivelesDocumento8 páginasControl de Un Tanque de Agua Con 3 NivelesRafaelAún no hay calificaciones
- FormularioDocumento1 páginaFormularioBenja Ramos BarrosAún no hay calificaciones
- Mec 3330 - Sem 2-2019-Res AuxDocumento4 páginasMec 3330 - Sem 2-2019-Res AuxRonald V. Nina VelizAún no hay calificaciones
- Conservación de energía explica por qué la pelota regresa más lentaDocumento5 páginasConservación de energía explica por qué la pelota regresa más lentaJill Martínez Velásquez75% (4)
- STP TeoriaDocumento12 páginasSTP TeoriarodrigoAún no hay calificaciones
- Documento Sin TítuloDocumento2 páginasDocumento Sin TítuloJairo Ortiz MorenoAún no hay calificaciones
- Anexo 1 Ejercicios y Formato Pre TareaDocumento8 páginasAnexo 1 Ejercicios y Formato Pre TareaMayerly Yiceth SiachoqueAún no hay calificaciones
- A. Esquemas de SintaxisDocumento2 páginasA. Esquemas de Sintaxisparvy90Aún no hay calificaciones