Documentos de Académico
Documentos de Profesional
Documentos de Cultura
24-Articulo 2 PDF
Cargado por
Qf Jhon DonadoTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
24-Articulo 2 PDF
Cargado por
Qf Jhon DonadoCopyright:
Formatos disponibles
Revista de Ciencias Biolgicas y de la Salud Universidad de Sonora
El saber de mis hijos har
www.biotecnia.uson.mx mi grandeza
PERSPECTIVAS ACTUALES DEL USO DE PROTENAS RECOMBINANTES
Y SU IMPORTANCIA EN LA INVESTIGACIN CIENTFICA E INDUSTRIAL
CURRENT PERSPECTIVES ON THE USE OF RECOMBINANT PROTEINS AND THEIR IMPORTANCE
IN SCIENTIFIC AND INDUSTRIAL RESEARCH
Guevara-Hernndez E1, Lpez-Zavala AA1, Jimnez-Gutirrez LR1 y Sotelo-Mundo RR1,2,*
1
Centro de Investigacin en Alimentacin y Desarrollo, A.C. Carretera a Ejido La Victoria Km 0.6. PO Box. 1735. Hermosillo,
Sonora, 83304, Mxico. | 2Departamento de Investigacin en Polmeros y Materiales. Universidad de Sonora. Blvd. Rosales
y Blvd. Luis Encinas. Hermosillo, Sonora 83000, Mxico.
RESUMEN used. Usually, PR may have similar structural and functional
El descubrimiento de la estructura y el mecanismo properties as the natural protein, and they are produced in
de replicacin del ADN han permitido el desarrollo de tc- high yield. However, some PR is difficult to obtain due to the
nicas biomoleculares para su manipulacin, gracias a estos formation and accumulation of aggregates (inclusion bo-
avances es posible sintetizar protenas en organismos en los dies). The chaperone co-expression and the use of modified
que no se encuentran de manera natural (sobreexpresin host strains are some strategies used to solve some of these
heterloga). A las protenas producidas de esta manera se les problems. Despite these limitations, PR technology has been
conoce como protenas recombinantes (PR). widely used in different industries such as pharmaceuticals,
Las PR se pueden producir en una gran variedad de food, among others. On the other hand, the use of PR has
sistemas biolgicos, como bacterias, levaduras y hasta clu- enabled major advances in the understanding of diverse
las eucariontes. Comercialmente estn disponibles un gran cellular processes in scientific research.
numero de sistemas de expresin y uno de los ms utilizados Keywords: Recombinant proteins, plasmids, heterologous
es el sistema basado en la ARN polimerasa del fago T7. Las expression, protein expression
PR pueden tener caractersticas estructurales y funcionales
muy similares a las protenas naturales y por lo general se INTRODUCCIN
producen con alta eficiencia. Sin embargo, algunas PR no El cido desoxiribonucleico (ADN) contiene la
son funcionales o sufren problemas de plegamiento cuando informacin necesaria para la sntesis de protenas. El de-
se expresan en clulas procariontes, formando agregados scubrimiento del cdigo gentico abri la posibilidad de
moleculares que se conocen como cuerpos de inclusin. La obtener pptidos y/o protenas a gran escala a partir de
coexpresin con otras protenas, como las chaperonas o el diversos organismos en los cuales no se producen de manera
uso de cepas modificadas para la sobreexpresin, son algu- natural. A las protenas obtenidas de esta manera se les con-
nas de las estrategias utilizadas para evitar la formacin de oce como PR. stas se pueden producir en microorganismos
agregados. A pesar de estas limitantes, la tecnologa de PR como bacterias, hongos, virus y levaduras, as como en lneas
es ampliamente utilizada en investigacin y en la industria celulares cultivables de insectos, plantas y de mamferos
farmacutica y alimentaria. Esta revisin tratar sobre los (Jonasson et al., 2002; Palomares et al., 2004), sistemas de
principales aspectos del proceso de produccin de PR y sus expresin de protenas sin clulas y tambin en animales y
aplicaciones. plantas trangnicas (Farrokhi et al., 2009).
Palabras claves: Protenas recombinantes, sobreexpresin La sobreexpresin de PR ofrece la ventaja de producir
heterloga, plsmidos, biofrmacos, sobreexpresin de pro- grandes cantidades de la protena de inters con caractersti-
tenas. cas similares a la protena natural y de manera relativamente
fcil y rpida. Esta tecnologa cuenta con al menos 35 aos
ABSTRACT y por su aplicacin tanto en la industria farmacutica y ali-
The discovery of DNAs structure has allowed the mentaria, como en la investigacin cientfica, se encuentra
development of molecular techniques for its manipulation. entre los desarrollos ms importantes del siglo XX (Porro et
With these advances it is possible to synthesize proteins in al., 2005).
organisms that are not found naturally (called protein hete- El procedimiento para producir una PR consiste en
rologous over expression). A protein produced in this way is introducir el ADN que codifica para la protena de inters en
known as recombinant proteins (PR), since it is the product un vector de sobreexpresin (plsmidos, virus, csmidos).
of recombinant DNA. The PR can be produced in a variety of El vector contiene un origen de replicacin que le permite
systems, like bacteria, yeast and eukaryotic cells. Likewise, copiarse dentro de la clula hospedera, una regin promo-
there are several expression systems available; being the tora que permite la produccin de la protena de inters, un
system based on phage T7 RNA polymerase one of the most sitio de clonacin mltiple (SCM), que es una regin que con-
Autor para correspondencia: Dr. Rogerio R. Sotelo-Mundo
Volumen XV, Nmero 3
8 Correo electrnico: rrs@ciad.mx; rsotelo@polimeros.uson.mx
Recibido: 31 de octubre de 2012
Aceptado: 12 de marzo de 2013
Guevara-Hernndez et al: Perspectivas Actuales del Uso de Protenas / XV (3): 8-17 (2013)
tiene diversos sitios de restriccin que permiten la insercin electrnicas disponibles para la comunidad cientfica, orga-
de ADN entre ellos y en algunos casos, genes de resistencia nizadas en libreras que contienen los genomas completos,
a antibiticos y genes reporteros, que facilitan la seleccin por ejemplo, la Librera Mayor de Genomas Microbianos
de las colonias de bacterias que tendran el vector con la (EMGLib, por sus siglas en ingls, http://pbil.univ-lyon1.fr/
informacin gentica insertada. emglib/emglib.html) contiene todos los genomas de bacte-
Por ejemplo, para crear un plsmido recombinante, rias secuenciados a la fecha (Perrire et al., 1999).
se lleva a cabo un procedimiento de ligacin que permite Existe un gran nmero de pginas electrnicas con
insertar dentro del SCM del vector, un segmento de ADN bases de datos de genes, difieren bsicamente en la infor-
que corresponde al marco de lectura funcional, que con- macin proporcionada, ya sea por el tipo de organismo
tiene la informacin para la generacin de la protena de de estudio o por la aplicacin y estudios en los que se han
inters. Al producto de este vector, ms el fragmento de ADN enfocado. Una de las bases de datos ms utilizada por la
codificante (inserto), se denomina construccin. El siguiente comunidad cientfica es la del Centro Nacional para la In-
paso es la transformacin, sta se realiza al insertar la con- formacin en Biotecnologa (NCBI, por sus siglas en ingls,
struccin dentro de la clula hospedera y sta se convierte http://www.ncbi.nlm.nih.gov/). Esta base de datos almacena
en una fbrica celular de la protena de inters (Palomares et la informacin referente a secuencias genmicas en el Banco
al., 2004). La bacteria Escherichia coli es uno de los sistemas de Genes (GenBank). Adems, contiene un ndice de artculos
de sobreexpresin ms utilizados para la produccin de PR. cientficos y una recopilacin de enfermedades genticas
Algunas ventajas que ofrece son su rpida reproduccin, humanas (Perrire et al., 1999).
utiliza medios de cultivo relativamente baratos, buen mane- Otras bases de datos disponibles y de libre acceso son:
jo en fermentaciones de alta densidad y fcil escalamiento. El banco de datos de protenas (PDB, por sus siglas en ingls;
Adems, ha sido uno de los organismos ms utilizados como http://www.pdb.org/pdb/home/home.do), la iniciativa de
modelo de estudio, debido a esto se ha sido caracterizado Estructura de Protenas del Instituto Nacional de Salud de
ampliamente y se han desarrollado numerosas herramientas Estados Unidos (NHI por sus siglas en ingls, http://www.
que han facilitado su clonacin y expresin gentica (Baneyx nigms.nih.gov/Initiatives/PSI/) y la base de datos SPINE del
y Mujacic, 2004). Instituto Europeo de Bioinformtica (EBI, por sus siglas en
Otra ventaja del uso de las PR es que se puede hacer ingls, http://www.ebi.ac.uk/euprojects/index.html). Estas
mutagnesis dirigida para modificar su secuencia de ami- bases de datos proporcionan la informacin de los genes que
nocidos, algunos ejemplos de estas tcnicas son: la PCR de codifican para la protena de inters.
extensin por sobreposicionamiento (OE-PCR por sus siglas En algunos casos la informacin de la regin codifi-
en ingls), mutagnesis de casete, el mtodo de Kunkel entre cante est completa, pero en otros, se pueden encontrar eti-
otras. Esto permite cambiar la secuencia de aminocidos y quetas de fragmentos expresados (conocidas como EST, por
conferir o suprimir caractersticas especficas que se deseen sus siglas en ingls). Estas regiones son de gran utilidad para
estudiar, como la estabilidad trmica, la inmunogenicidad, completar la regin codificante de la protena que se desea
propiedades estructurales o alguna otra de inters industrial, estudiar y a partir de all iniciar con el proceso de produccin
mdico o farmacolgico (Palomares et al., 2004). de PR. Esta propiedad es muy importante, ya que se puede
Con los avances en el conocimiento de biologa mo- investigar una protena determinada de un organismo sin
lecular y biotecnologa, es relativamente sencillo producir que sea necesario conocer su genoma completo, por ejem-
PR. Muchas protenas pueden ser obtenidas con algn m- plo, se puede hacer una bsqueda de secuencias similares
todo que utilice la tecnologa de la PR. Sin embargo, antes conocidas de otros organismos en estas bases de datos y es
de iniciar un proceso de produccin, se debe establecer un posible encontrar el gen completo, o bien slo fragmentos,
protocolo adecuado en base a las caractersticas de la PR que que mediante el uso de primers degenerados (que son
se desea expresar y esto definir, por ejemplo: el sistema de formados a partir de secuencias conservadas en todos los
sobreexpresin, el vector de sobreexpresin, si se expresar organismos) se pueden obtener los fragmentos restantes del
la protena completa o algn dominio, las posibles dificulta- gen mediante la tcnica del PCR.
des que se puedan presentar en el proceso, las estrategias de
purificacin y almacenamiento de la PR. SNTESIS DE PROTENAS RECOMBINANTES
En este artculo se har una breve descripcin de las La ARN polimerasa (ARNpol) es una enzima que realiza
principales tcnicas de sobreexpresin de PR y se revisarn una de las funciones ms importantes de la clula: la tran-
sus campos de aplicacin en el mbito cientfico e industrial, scripcin del ADN. Este es el proceso por el cual se genera
as como sus tendencias y perspectivas. una copia de ARN mensajero (ARNm) a partir de un molde
de ADN. En eucariontes y procariontes este proceso se lleva a
BASES DE DATOS DE SECUENCIAS GENTICAS cabo por un sistema complejo de protenas que conforman la
En los ltimos aos los avances en la secuenciacin ARNpol, sin embargo, en organismos como los bacterifagos
de genes han culminado en la elucidacin de la secuencia (p.ej. fago T7), la ARNpol es menos compleja: se compone por
completa del genoma humano, as como de otros organis- una sola subunidad y es capaz de realizar todo el proceso de
mos. Esta informacin se ha depositado en bases de datos transcripcin, como su homloga en organismos superiores.
Volumen XV, Nmero 3
9
Guevara-Hernndez et al: Biotecnia / XV (3): 8-17 (2013)
Otra caracterstica importante de esta ARNpol es que pre- protena de inters no puede detectarse, tanto en la fraccin
senta una elevada velocidad de transcripcin y sus regiones soluble como en la insoluble. Sin embargo cuando el sistema
promotoras son altamente especficas (McAllister y Raskin, T7 funciona correctamente, se puede tener rendimientos
1993; Tunitskaya y Kochetkov, 2002). Estas caractersticas ha- de hasta el 50 % de la protena recombinante con respecto
cen a la ARNpol del fago T7 (T7-ARNpol) un excelente modelo a la protena total de la bacteria (Changchien et al., 2000;
para implementarse en sistemas de expresin de PR, ya que Studier et al., 1990). Por ello, se han desarrollado alternativas
en estos sistemas se requiere de una alta eficiencia de po- en el diseo de vectores de sobreexpresin, algunos de ellos
limerizacin de nucletidos y al mismo tiempo una elevada contienen diferentes secuencias cercanas al sitio de clon-
capacidad de regulacin sobre su funcin. acin que expresan diversas etiquetas de fusin (tags, en
Los sistemas de expresin basados en la T7-ARNpol, ingls), que facilitan la purificacin, solubilidad o transporte
fueron creados para la produccin de PR en E. coli. El sistema al periplasma de las protenas que se desea expresar, por
de sobreexpresin pET que utiliza esta enzima es el ms con- ejemplo, los vectores pET14-16 que contienen una etiqueta
ocido comercialmente para la sobreexpresin de PR (Studier de fusin de histidinas que facilita la purificacin por medio
y Moffatt, 1986). Como se mencion anteriormente, esta po- de cromatografa de afinidad a metales (IMAC), los vectores
limerasa posee una alta especificidad por su regin promo- de sobreexpresin pET32 y pET41-42 contienen una etiqueta
tora, asimismo, tambin tiene una alta capacidad de proces- de fusin con tiorredoxina y GST (glutatin S-transferasa) que
amiento, de regulacin y funciona adecuadamente en E. coli facilita la solubilidad de algunas protenas y tambin su pu-
(Studier y Moffatt, 1986). En el sistema pET se usa una cepa rificacin. En el mercado existen un gran nmero de vectores
de E. coli llamada BL21, que contiene el gen de la T7-ARNpol. que ofrecen una alternativa al sistema pET, estos contienen
Para tener control de la sntesis de la PR y dado que es ms diferentes caractersticas que se adecan a casos particulares
eficiente este proceso durante la fase exponencial, la regin de sobrexpresin. Por mencionar algunos, se encuentran los
promotora del vector generalmente est bajo el control del vectores con diferentes promotores como el T5, ramnosa,
operador lac, el represor lacI se encuentra presente bloque- arabinosa, entre otros. El vector pCold que es usado para
ando la expresin de la T7-ARNpol y por lo tanto, tambin protenas que presentan problemas de solubilidad en siste-
la expresin de la protena de inters. Al aadir un inductor mas basados en el sistema T7 al disminuir la temperatura de
como el isopropilo de tiogalctsido (IPTG), el promotor deja sobreexpresin. Puede contener tambin secuencias para fa-
de estar reprimido y se inicia la sntesis de la PR. vorecer el rendimiento de la protena que se desea expresar,
El sistema T7 no es infalible, ya que se pueden pre- por ejemplo, una secuencia con protenas chaperonas, para
sentar bajos niveles de sobreexpresin de la protena de mejorar el rendimiento y plegado, o bien con lisozima, para
inters. Si la protena es txica para la bacteria, sta sufre ofrecer estabilidad a algunas protenas y facilitar la lisis de
lisis y el cultivo no crece adecuadamente. En otros casos, la clulas, vectores con diferentes inductores que permiten la
Figura 1. Diagrama general de produccin y obtencin de PR.
Figure 1. General diagram for recombinant proteins production.
Volumen XV, Nmero 3
10
Guevara-Hernndez et al: Perspectivas Actuales del Uso de Protenas / XV (3): 8-17 (2013)
expresin de protenas txicas, como el sistema Rhamex de a menudo requieren interaccionar con otras molculas para
DNA 2.0. El proceso general para la produccin de protenas su correcto plegamiento. En ocasiones, algunas protenas no
recombinantes se describe grficamente en la figura 1. se pueden obtener en su forma funcional mediante procesos
Primero, se puede obtener el ADN complementario clsicos de PR.
(ADNc) mediante la transcripcin reversa del ARN mensajero Actualmente, es posible mejorar el plegado de la PR
de inters y su posterior secuenciacin para confirmar la al co-expresarse con otras protenas con las que interacta
identidad. Posteriormente se utilizan enzimas de restriccin (Grslund et al., 2008). Adems, se ha demostrado que la
para clonar el ADNc (o fragmento de inters) en un vector co-expresin de chaperonas facilitan el plegamiento de la
de expresin basado T7-ARNpol (sistema pET). En caso de PR de inters (Deuerling y Bukau, 2004). Por ejemplo, se ha
ser necesario, esos sitios nicos de restriccin se pueden reportado que el vector pG-Tf2 (Takara Bio Inc.) favorece la
introducir mediante PCR con iniciadores que se extiendan produccin y el correcto plegado de PR que no haba sido
corriente arriba y abajo de la regin codificante de inters posible producirlas por tcnicas de sobreexpresin clsicas,
(Barron et al., 2007; Geisse y Fux, 2009; Palomares et al., 2004). como es el caso de la lisozima y otras. Este vector contiene
Algunos de los vectores de expresin contienen una una combinacin de las chaperonas tipo GroEL-GroES y Tig.
etiqueta en el amino o en el carboxilo terminal. Generalmente Si bien se ha demostrado su efectividad a nivel laboratorio,
se utilizan etiquetas de histidinas, argininas o protenas de aun hacen falta ms estudios para evaluar su uso a escala
fusin, como la GST o la tiorredoxina, lo que facilita en gran industrial (Grslund et al., 2008).
medida la purificacin de la PR mediante cromatografa de En nuestro grupo de investigacin se han producido
afinidad o de intercambio inico para el caso de la etiqueta protenas recombinantes en su forma soluble y funcional,
de argininas (Terpe, 2003). Para algunas aplicaciones como utilizando este sistema de expresin, como la lisozima del
la cristalografa de protenas o la generacin de anticuerpos, camarn (gamba) blanco Litopenaeus vannamei (de-la-Re-
esta insercin debe ser eliminada y esto se logra incluyen- Vega et al., 2004), la timidilato sintasa del WSSV (White Spot
do un sitio de corte para una proteasa especfica. Algunos Syndrome Virus, por sus siglas en ingls) (Arvizu-Flores et
ejemplos son la enterocinasa que reconoce una secuencia al., 2009), la glutatin-S-transferasa (Salazar-Medina et al.,
de 5 aminoacidos (DDDDK), la proteasa TEV (ENLYFGS) y la 2010), la nucletido cinasa (Quintero-Reyes et al., 2012), la
proteasa PreScission (LEVLFQ/GP). timidina monofosfato cinasa del WSSV (Guevara-Hernandez
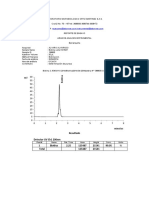
Lo siguiente es Transformar una cepa de E. coli, como et al., 2012), entre otras. Para el caso de la lisozima, que con-
la BL21, que sea compatible con el plsmido recombinante, tiene enlaces disulfuros en su estructura, se establecieron las
formado por el vector de expresin pET u otro utilizado, que condiciones de sobreexpresin (Figura 2) y replegamiento
contenga la regin codificante de inters y seleccionar la ce- in vitro para obtener protena soluble a partir de cuerpos de
pas de acuerdo a los criterios de seleccin de antibiticos del inclusin.
vector (resistencia a ampicilina, kanamicina, etc.). Las bacte-
rias se inoculan en caldo LB o algn otro medio previamente FBRICAS BIOLGICAS PARA LA PRODUCCION
optimizado para E. coli BL21 transformadas con el constructo.
DE PROTENAS RECOMBINANTES
Al llegar a la fase exponencial (cuando la densidad ptica del
Se han desarrollado una gran variedad de sistemas
cultivo est entre 0,4-0,8 a 600 nm) se aade el inductor. Se
de expresin, tanto procariontes como eucariontes para
contina con el crecimiento del cultivo proveyendo aireacin
la produccin de PR. Los organismos ms utilizados son:
suficiente para mantener una adecuada oxigenacin en el
bacterias, levaduras, insectos, plantas y clulas de mamferos
medio y se determina el tiempo ms adecuado de expresin,
(Basile y Peticca, 2009). En algunos de ellos se utiliza el micro-
mediante anlisis de electroforesis en condiciones desnatu-
organismo completo (p.ej. E. coli) y en otros se utilizan clulas
ralizantes y reductoras SDS-PAGE (Lesley y Wilson, 2005). Para
derivadas del organismo (p.ej. cultivos vegetales, clulas
finalizar, se recupera la biomasa y se purifica la PR mediante
de insecto o de mamfero) o bien, se puede implementar la
lisis celular y tcnicas cromatogrficas. En algunos casos se
expresin de protenas libre de clulas.
puede secretar la PR al medio de cultivo mediante el uso de
Los sistemas ms utilizados para la produccin de
vectores especialmente diseados para ello.
protenas recombinantes en EUA y Europa son los microor-
Las protenas que mejor se expresan en bacterias y en
ganismos, con un 55 % (del cual 39 % corresponde a E. coli y
particular en el sistema pET son las citoplasmticas, es decir,
un 15 % a levaduras ) y clulas de mamfero, especficamente
aqullas que llevan a cabo su funcin en el citosol. Protenas
clulas de ovario de hmster (CHO), con un 35 % (Rader,
de membrana, secretadas o que contengan modificaciones
2008).
post-traduccionales, como glicosilaciones, fosforilaciones
La bacteria E. coli, es uno de los sistemas ms utilizados
amidaciones, formacin de puentes disulfuro, etc. son prob-
para la produccin de PR. Esta bacteria tiene la capacidad de
lemticas al sobreexpresarse en E. coli.
crecer rpidamente y con alta densidad en medios de cultivo
La produccin de PR es un proceso relativamente
de bajo costo. Adems, en el mercado hay una gran disponib-
sencillo y ofrece muchas ventajas. Sin embargo, uno de los
ilidad de cepas mutantes, un ejemplo es el sistema BL21 de
principales obstculos es obtener la PR en su forma soluble y
Invitrogen que carece de las proteasas lon y ompT, esto re-
funcional. Muchas protenas son complejos multi-proteicos y
Volumen XV, Nmero 3
11
Guevara-Hernndez et al: Biotecnia / XV (3): 8-17 (2013)
polimerasa T7 y que permite disminuir la sobreexpresin
basal, haciendo ms estable la expresin de la PR.
Algunos insertos que codifican para protenas eucari-
ontes contienen codones (codones raros) cuyos tripletes no
se presentan naturalmente en E. coli, por lo que es necesario
modificar la secuencia del inserto para incluir los codones
que si se presentan en la bacteria. Una alternativa es usar las
cepas de Novagen, Rosetta, Rosetta-Blue y Rosetta-Ga-
mi, que contiene los tripletes para los codones raros (AGG,
AGA, AUA, CUA, CCC, GGA). Otras lneas celulares, como
Origami y OrigamiB presentan una mutacin en los genes
trxB y gor que favorecen la formacin de puentes disulfuro en
el citoplasma (http://goo.gl/oRJkl). Algunos ejemplos de PR
producidas en esta bacteria son protenas para usos industri-
ales, como renina, amilasas, proteasas y celulasas, protenas
Figura 2. Cintica tpica de sobre expresin de lisozima
teraputicas, como insulina, hormonas de crecimiento e in-
de camarn (Litopenaeus vannamei) en E. coli. La figura
terferones, entre muchas otras (Lesley y Wilson, 2005). Otras
representa un gel de poliacrilamida donde las protenas se
bacterias que tambin han sido utilizadas como modelo para
separan en condiciones desnaturalizantes y reductoras y
la produccin de PR son: Lactococcus lactis y Bacillus subtilis,
migran de acuerdo a su masa molecular. STD corresponde
pero en menor grado (Morello et al., 2008; Nijland y Kuipers,
al estndar de masa molecular, el carril 1 corresponde al
2008).
cultivo sin inducir, los carriles 2-10 corresponden a muestras
Otro de los organismos utilizados para producir PR
colectadas de biomasa cada hora despus de la induccin.
son las levaduras. Las ms usadas son Pichia pastoris y Sac-
El carril HEL corresponde a una muestra de lisozima de clara
charomyces cerevisiae, en las cuales se han expresado cientos
de huevo con una masa de 14 kDa.
de protenas diferentes (Cregg et al., 2000; Mattanovich et al.,
Figure 2. Expression pattern of recombinant shrimp lyso-
2004; Porro et al., 2005). Generalmente las levaduras, al igual
zyme (Litopenaeus vannamei) expressed as a recombinant
que las lneas celulares de insectos y mamferos se utilizan
form in E. coli. The figure shows a polyacrylamide gel under
para sobreexpresar protenas que son txicas o que no se
denaturing and reducing conditions, where all bacterial pro-
pueden plegar correctamente en E. coli (Kost et al., 2005;
teins are separated. The proteins migrate according to their
Oker-Blom y Vuento, 2003). Adems, estos sistemas pueden
molecular weight. STD corresponds to the molecular weight
realizar modificaciones post-traduccionales, excretar la PR al
marker, lane 2 corresponds to uninduced bacteria, and lanes
medio de cultivo y tambin se obtienen rendimientos may-
2-10 correspond to samples taken each hour post induction.
ores al 50 % (Grslund et al., 2008)
Lane labeled with HEL contains hen egg white lysozyme,
La expresin transitoria del gen (por sus siglas en
which has a molecular weight of 14 kDa.
ingls: TGE) en clulas de mamfero es una importante tec-
nologa para la generacin de PR. La TGE, cumple todos los
duce la degradacin de las protenas heterlogas expresadas requisitos en materia de cantidad y calidad de los productos.
en estas clulas y de vectores de expresin compatibles con Para las lneas celulares CHO y HEK293 se han optimizado
E. coli. protocolos que permiten la produccin de protenas con
E. coli no es capaz de realizar modificaciones post-tra- un alto rendimiento (Geisse y Fux, 2009). Por otro lado, en
duccionales, necesarias para la mayora de las protenas de el 2009, Basile y Peticca utilizaron al parsito Leishmania
eucariontes. Sin embargo, existen algunos vectores que tarentolae como modelo para la expresin de genes het-
ayudan a realizar estas modificaciones. Por ejemplo, el vector erlogos. La familia Tripanosomatidaea a la que pertenece
pET12a contiene una etiqueta de sealizacin que permite este protozoo se caracteriza por ser ricos en glicoprotenas.
que la PR se acumule en el periplasma de la bacteria (EMD Se ha reportado que las protenas sobreexpresadas en este
Chemical/Novagen, USA). parsito presentan las glicosilaciones en la misma posicin
Aunque no todas las PR pueden ser sintetizadas en E. que las estructuras de las protenas nativas. Si bien, su uso en
coli, se ha logrado mejorar el rendimiento y la versatilidad de la tecnologa de PR es reciente, ya se han producido varias
este microorganismo (Baneyx, 1999; Shokri et al., 2003), cada enzimas y receptores de membrana citoplasmtica y adems
lnea celular puede presentarse de diferentes formas modifi- se pueden producir a nivel intracelular o pueden ser secreta-
cando algunas caractersticas de su genoma, por ejemplo, la das al medio de cultivo.
designacin DE3 en las bacterias, indica que estn basados Entre los diferentes sistemas basados en tejidos
en la RNA polimerasa del fago T7 y por lo tanto, se encuen- vegetales, la produccin de PR en semillas es la plataforma
tran bajo el control del promotor LacUV5, la designacin ms utilizada. Este sistema ofrece varias ventajas, tales como:
pLysS, indica que la bacteria hospedera contiene el gen que mnimo costo de produccin, no propaga virus y patgenos
codifica la lisozima T7, que es un inhibidor natural de la RNA de mamferos, confiere un almacenamiento estable de la PR
Volumen XV, Nmero 3
12
Guevara-Hernndez et al: Perspectivas Actuales del Uso de Protenas / XV (3): 8-17 (2013)
y adems, es capaz de realizar modificaciones post-traduc- sin en bacterias, promoviendo un correcto plegado en estos
cionales en las protenas (Jamal et al., 2009; Lau y Sun, 2009; casos. Los sistemas de expresin libres de clulas ms usados
Ahmad et al., 2010). son los basados en extractos de E. coli, germen de trigo y
El primer producto biofarmacutico producido en sistemas derivados de clulas de mamfero (Farrokhi, 2009).
clulas de plantas fue la hormona del crecimiento humana,
producida en tabaco transgnico en 1986 (Barta et al., 1986). LIMITACIONES EN LA PRODUCCIN DE PR
Desde entonces, diversas especies de plantas, como cereales, A pesar de la importancia y al amplio uso de la tec-
legumbres, frutas y vegetales han sido utilizados para la pro- nologa de PR tanto en la industria farmacutica como en la
duccin de biofrmacos, anticuerpos y vacunas (Miao et al., investigacin, an no se cuenta con una estrategia infalible
2008; He et al., 2008). para la obtencin de PR.
No obstante, el principal obstculo para la produccin Se han analizado una gran cantidad de variables y fac-
de PR en tejidos vegetales ha sido su bajo nivel de acumu- tores en el proceso de produccin (temperatura, pH, oxgeno,
lacin. Para solventar esta situacin, se han implementado cepas hospederas etc.) que se sabe estn estrechamente re-
estrategias de transformacin de los cloroplastos, expresin lacionados con el rendimiento e integridad de la PR. Tambin
transitoria y fusin de protenas (Ahmad et al., 2010). Sin se ha evaluado la importancia de la composicin del medio
embargo, se ha reportado que los tejidos de plantas son de cultivo (concentracin, tipo y consumo de nutrientes,
altamente influenciados por factores ambientales, como la etc.) (Holmes et al., 2009), por lo que es necesario establecer
temperatura, la luz, la salinidad, la sequa, la nutricin, los experimentalmente las condiciones ptimas para cada PR.
insectos y plagas (Jamal et al., 2009). A continuacin se mencionan algunas de las dificultades y
Una alternativa es la produccin de PR en clulas limitaciones que suelen presentarse en los protocolos de
de plantas en biorreactores, ya que se pueden controlar sntesis y purificacin de estas protenas:
las condiciones de produccin, aumentar la consistencia 1- La recombinacin de un plsmido recombinante
y homogeneidad del producto, simplifica la purificacin que codifica la PR en el genoma del hospedero. Esto puede
(especialmente de protenas secretadas extracelularmente), tener como consecuencia la interrupcin de genes impor-
reduce la contaminacin potencial de endotoxinas y mico- tantes en el genoma del hospedero y dar origen a genotipos
toxinas derivadas de las plantas y del suelo y minimiza el desconocidos que son incapaces de sintetizar la PR. En el
silenciamiento post-transcripcional de genes (PTGS) (Huang mejor de los casos se puede producir la PR, pero con bajo
y McDonald, 2009). rendimiento (Barron et al., 2007).
El principal compartimento de almacenamiento de 2.- Deterioro de la fisiologa celular del hospedero.
protenas recombinantes de clulas de plantas generadas en El estrs por manejo es uno de los principales factores
bioreactores son las vacuolas (almacenamiento de protenas que afectan el desarrollo y crecimiento del hospedero
en vacuolas, PVS por sus siglas en ingls). sta a su vez se divi- (Sevastsyanovich et al., 2010). Otro factor importante es el
de en tres compartimentos morfolgica y bioqumicamente estrs nutricional al que estn sujetos los microorganismos
diferentes: La matriz, la estructura globoide y la cristaloide. hospederos. En conjunto, estos factores pueden ocasionar
La matriz es el reservorio principal de protenas solubles, la errores de transcripcin que repercuten en la integridad de
estructura globoide presenta un ambiente cido que contie- la PR. Estos errores aleatorios son difciles de detectar, ya que
ne cido ftico o cristales de oxalato y la estructura cristaloide producen una mezcla heterognea de polipptidos. Las pro-
que puede estar conformada por protenas de almacena- tenas alteradas pueden estar presentes en cantidades muy
miento. Para que las protenas recombinantes puedan alcan- pequeas, pero el nmero total de molculas defectuosas
zar estos depsitos se pueden agregar seales especficas podra ser sustancial en el rendimiento de la PR (Barron et al.,
que se encuentran en las protenas naturales, esto permite 2007; Mattanovich et al., 2004).
a su vez seleccionar el compartimento de almacenamiento 3- Una inadecuada aireacin del cultivo puede pro-
para la protena recombinante (Miao et al., 2008). vocar limitaciones en la produccin de aminocidos y la
Los cuerpos grasos de las semillas (OB por sus siglas estabilidad del plsmido (Holmes et al., 2009).
en ingls), tambin son utilizados para la produccin de PR Se han empleado varias estrategias para minimizar
en bioreactores. Algunas de las ventajas de este organelo, estas limitaciones. Barron y Piskavera (2007), desarrollaron
es que existen en diversos tejidos vegetales, como semillas, alternativas a los protocolos estndar para minimizar el error
polen, frutas y oleaginosas. Adems se pueden generar pro- durante la sntesis de las PR. Estos protocolos se basan en
tenas de fusin con oleosinas, que pueden ser purificadas la insercin directa del material gentico en el hospedero.
fcilmente por centrifugacin (Miao et al., 2008). Adems incluyeron marcadores de seleccin negativa en
En la tcnica de la expresin libre de clulas todos los combinacin con los marcadores tradicionales.
componentes necesarios para la replicacin de ADN son ais- Los procesos de automatizacin son de gran ayuda
lados y usados con un templado, que puede ser ADN o RNA para establecer los mtodos de control y calidad, adecuados
para generar la protena. Una de las principales ventajas de durante la sntesis de la PR. Esto permite hacer reproducibles
este sistema es que se puede evitar la toxicidad que presen- los protocolos de produccin de PR y ejecutarlos con mayor
tan algunas protenas heterlogas en los sistemas de expre- facilidad (Acton et al., 2005; Genomics:-GTL-Roadmap., 2005).
Volumen XV, Nmero 3
13
Guevara-Hernndez et al: Biotecnia / XV (3): 8-17 (2013)
Asmismo, se han desarrollado nuevas cepas de E. coli, ms textil, alimentaria y energtica (Tabla 1).
resistentes al manejo y al estrs producido por la sobreex- La industria farmacutica ha sido una de las ms
presin. Estas cepas incluyen mejores marcadores de selec- beneficiadas con la tecnologa de produccin de PR (Geisse
cin o modificaciones en el metabolismo (baja produccin de y Fux, 2009). La insulina fue el primer biofrmaco comer-
acetato) (Eiteman y Altman, 2006). Para mejorar el problema cializado que se obtuvo mediante esta tecnologa. Esta
de plegamiento se han probado diferentes estrategias, como molcula ha sido valorada entre los 10 medicamentos ms
modificaciones en la fuerza del promotor, la temperatura de comercializados en el mundo en cuanto a produccin y a las
cultivo, optimizacin de codones raros (tARN) en la cepa Ro- altas ganancias econmicas que se derivan de su comerciali-
setta-Gami de E. coli; as como la co-expresin de chaperonas zacin. Este biofrmaco se produce bajo diferentes nombres
en cualquier tipo de cepa E. coli BL21(DE3) (Martinez-Alonso comerciales, como humulina, InsulR, Lantus y Arasnep,
et al., 2010). Sin embargo, es posible que la co-expresin de entre otros.
chaperonas pueda reflejarse en un bajo rendimiento de la PR Desde mediados de la dcada pasada cientos de fr-
(Martinez-Alonso et al., 2010). macos haban sido probados para el tratamiento de diversas
Con respecto a la recuperacin de la PR, las protenas enfermedades y actualmente ms de 100 frmacos han sido
de fusin y la adicin de etiquetas de afinidad a metales han aprobados desde el ao 2000 a lo que va del presente ao
facilitado en gran de medida los procesos de purificacin de (http://www.biopharma.com/approvals.html) y se estima
la PR (Jonasson et al., 2002). que para los prximos aos los biofrmacos representarn el
En la actualidad existe gran inters en producir PR 12 % del total de las ventas mundiales de medicamentos de
para el uso de aplicaciones farmacuticas, industriales o para prescripcin (Tabla 2).
el desarrollo de la investigacin cientfica. Si bien, se han im- En Mxico tambin se producen PR de inters far-
plementado un gran nmero de metodologas exitosas para macolgico. Laboratorios Silanes S.A. de C.V. es unos de los
la produccin de PR, a menudo se presentan dificultades pioneros a nivel mundial en la produccin de anti-venenos
en las diferentes etapas de su proceso de produccin. Por lo (http://www.silanes.com.mx/html/bioclon.html), en colab-
que es necesario determinar las condiciones ideales para la oracin con el Instituto Bioclon, comercializan varios fabo-
produccin y recuperacin de la PR que se est generando. terpicos para tratar picaduras de insectos y otros animales
venenosos para el humano (Boyer et al., 2009, Casasola et al.,
CAMPOS DE APLICACIN Y COMERCIALIZA- 2009), aunque los faboterpicos no son PR, este laboratorio
utiliza esta tecnologa durante su desarrollo. Algunos de sus
CIN DE PROTENAS RECOMBINANTES productos, como el Alacramyn y el Antivipmyn han sido
Desde sus inicios en la dcada de los 70, la industria
aprobados por la FDA y son distribuidos en varios pases.
biotecnolgica del ADN recombinante ha crecido continua-
Las industrias relacionadas con la produccin de
mente. Sus campos de aplicacin se han expandido a dife-
PR se han establecido prcticamente en todas las regiones
rentes ramas industriales, como la farmacutica, ambiental,
Tabla 1. Aplicaciones y beneficios Industriales de protenas recombinantes. Tomado de: BIO-Report 2008.
Table 1. Applications and industrial benefits of recombinant proteins. Source: BIO-Report 2008.
Campo de aplicacin Usos Beneficios
Industria farmacutica Produccin de compuestos activos, Disminuye costos y tiempo de
intermediarios terapias. produccin, frmacos ms especficos,
disminuye reacciones inmunolgicas e
infecciones
Aplicaciones ambientales Deteccin de contaminantes Ms baratos y rpidos que las pruebas
mediante anticuerpos monoclonales convencionales. Se pueden aplicar en
campo
Industria papelera Mejora el proceso de manufactura Disminuye la toxicidad de los residuos
mediante el uso de enzimas del procesamiento de la pulpa
Industria textil Aplicaciones en la fabricacin secado Disminuye la toxicidad de residuos de
y terminacin de productos, adicin produccin, detergentes ms efectivos
de enzimas en detergentes
Industrias de los alimentos Procesos de produccin, generacin Mejora de procesos, calidad de
de aditivos y conservadores productos, tcnicas de anlisis
Industria energtica Uso de enzimas en procesos de Generacin de biocombustibles
produccin de biocombustibles ms limpios y a partir de desechos
industriales o agrcolas
Volumen XV, Nmero 3
14
Guevara-Hernndez et al: Perspectivas Actuales del Uso de Protenas / XV (3): 8-17 (2013)
Tabla 2. Frmacos recombinantes aprobados en el mercado. mos celulares (Mathews, 1999; Smithies et al., 1985). Una
Tomado de Drago-Serrano, 2006. de las principales ventajas es que las PR se pueden obtener
Table 2. Recombinant drugs approved for market. rpidamente y en abundancia. Esto permite tener acceso
Source: Drago-Serrano, 2006. prcticamente ilimitado a la PR para realizar cualquier tipo de
estudio relacionado con su funcin. Adems, se pueden gen-
Frmaco Compaa Ao de aprobacin erar variantes a la protena de inters mediante tcnicas de
mutacin de ADN. En la mayora de los casos, el costo de pro-
Kogenate Bayer 1993
duccin de PR es relativamente bajo respecto a la obtencin
Nutropin Genetech 1994 de la protena a partir de su fuente natural. Debido a esto, la
tecnologa de PR se ha convertido en una de las tcnicas ms
Norditropin Novo Nordisk 1995 utilizadas en diversos campos de la investigacin cientfica.
Puregon N.V. Organon 1996 (Genomics:-GTL-Roadmap., 2005).
Benefix Genetics Institute 1997 CONCLUSIN
Insuman Hoechst AG 1997 Existe una gran variedad en sistemas de expresin y
organismos hospederos para la produccin de PR. Adems,
Apidra Aventis 2004 la complejidad y diversidad de las caractersticas fsico-
qumicas de las protenas, hace que sea necesario plantear
Advate Factor VIII Baxter AG 2004
una estrategia adecuada para tener una solucin a los
problemas que puedan surgir durante la sntesis de PR. Por
del mundo con ganancias de miles de millones de dlares lo tanto, los protocolos de purificacin y estrategias deben
(Tabla 3). Tan solo en EUA, entre el 2009-2010 se registr un ser elaborados para cada caso en particular. Los avances
incremento record de 4,5 billones de dlares en este sector. tecnolgicos y cientficos han permitido que la sntesis de PR
Adems, Se espera que este sector tenga un crecimiento del sea una herramienta disponible para diversas necesidades.
1,5 % para el ao 2018. Por esta razn se considera que este Cada vez son ms las aplicaciones en las que las PR han sido
sector tendr uno de los crecimientos ms importantes de la utilizadas, siendo la industria farmacutica y la alimentaria
industria privada para los EUA. las ms beneficiadas. Asmismo, en el mbito cientfico el
Por otro lado, la tecnologa de la PR se ha utilizado uso de las PR ha permitido entender y elucidar rutas meta-
para el estudio y comprensin de los diferentes mecanis- blicas y mecanismos celulares que son importantes para
el desarrollo de la vida. La mayora de las estructuras de
protenas depositadas en el PDB, han sido obtenidas a partir
Tabla 3. Ventas de productos biotecnolgicos 2008. Toma- de PR. Diversas ramas del conocimiento cientfico hacen uso
da de Biotech Guide 2008. constante de la tecnologa del ADN recombinante, ya que
Table 3. Gross sales of biotechnology products during permite obtener una protena de inters de manera rpida
2008. Source: Biotech Guide 2008. y abundante. La aplicacin de enzimas recombinantes a
tratamientos ambientales depende del costo del proceso,
Ventas
adems de no ser recomendable liberar al medio ambiente
Segmento (x109 Ejemplos
dlares) material gentico recombinante conteniendo plsmidos con
resistencia a antibiticos. Su aplicacin como catalizador en
Bioenergtica 26 Etanol, diesel procesos qumicos es mas factible, en particular catalizando
reacciones estereoselectivas sobre sustratos racmicos. Esta
Hidrocoloides (gomas, almidones y cualquier otra aplicacin debe considerar que el costo de
Ext. vegetales 24 industriales)
aceites esenciales produccin y purificacin de la PR compense la aplicacin a
realizar.
Productos biocatalticos, antibiticos,
farmacuticos 12
protenas teraputicas AGRADECIMIENTOS
Se agradece el financiamiento otorgado por el CO-
Polmeros 12 Hule natural, PLA, polioles
NACYT (Consejo Nacional de Ciencia y Tecnologa) de Mxico
(proyecto CB-2009-131859) y por las becas para estudios
Alimenticio 9 Acido ctrico, lisina, acido glutmico,
doctorales otorgadas a los primeros tres autores. Agradece-
Vit. B12, cidos grasos poliinsaturados
mos a la Dra. Ana Mara Caldern de la Barca su apoyo en la
Olequmico 9 Surfactantes, alcoholes y glicerol
revisin del presente manuscrito.
Enzimas en detergentes, procesamiento REFERENCIAS
Enzimtico 2.5 de textiles,
procesamiento de granos
Volumen XV, Nmero 3
15
Guevara-Hernndez et al: Biotecnia / XV (3): 8-17 (2013)
Acton, T. B., Gunsalus, K. C., Xiao, R., Ma, L. C., Aramini, J., Baran, transient gene transfer into Mammalian cells. Methods En-
M. C., Chiang, Y. W., Climent, T., Cooper, B. y Denissova, N. G. zymol, 463, 223-38.
2005. Robotic cloning and protein production platform of Genomics:-Gtl-Roadmap. 2005. Protein production and
the Northeast Structural Genomics Consortium. Methods in characterization. Revew of the Department of Energy
Enzymology. 394:210-243. Genomics:GTL Program. Washington D.C.
Ahmad, A., Pereira, E. O., Conley, A. J., Richman, A. S. y Menassa, Grslund, S., Nordlund, P., Weigelt, J., Bray, J., Gileadi, O., Knapp,
R. 2010. Green Biofactories: Recombinant Protein Produc- S., Oppermann, U., Arrowsmith, C., Hui, R. y Ming, J. 2008.
tion in Plants. Recent Patents on Biotechnology 4:242-259. Protein production and purification. Nature Methods.
Arvizu-Flores, A. A., Aispuro-Hernandez, E., Garcia-Orozco, K. D., 5:135-146.
Varela-Romero, A., Valenzuela-Soto, E., Velazquez-Contreras, Guevara-Hernandez, E., Garcia-Orozco, K. D. y Sotelo-Mundo,
E. F., Rojo-Dominguez, A., Yepiz-Plascencia, G., Maley, F. y R. R. 2012. Biochemical Characterization of Thymidine
Sotelo-Mundo, R. R. 2009. Functional identity of the active Monophosphate Kinase from white Spot Syndrome Virus:
sites of crustacean and viral thymidylate synthases. Compa- A Functional Domain from the Viral ORF454. Protein and
rative Biochemistry and Physiology Part C 150:406-13. Peptide Letters. 19:1220-1224.
Baneyx, F. 1999. Recombinant protein expression in Escherichia He, Z. M., Jiang, X. L., Qi, Y. y Luo, D. Q. 2008. Assessment of the
coli. Current Opinion in Biotechnology. 10:411-21. utility of the tomato fruit-specific E8 promoter for driving
Baneyx, F. y Mujacic, M. 2004. Recombinant protein folding vaccine antigen expression. Genetica. 133:207-214.
and misfolding in Escherichia coli. Nature Biotechnology. Holmes, W. J., Darby, R. A., Wilks, M. D., Smith, R. y Bill, R. M. 2009.
22:1399-408. Developing a scalable model of recombinant protein yield
Barron, N., Piskareva, O. y Muniyappa, M. 2007. Targeted genetic from Pichia pastoris: the influence of culture conditions,
modification of cell lines for recombinant protein produc- biomass and induction regime. Microbial Cell Factory. 8-35.
tion. Cytotechnology. 53:65-73. Huang , T. K. y Mcdonald, K. A. 2009. Bioreactor Engineering for
Barta A., Sommergruber, K., Thompson, D., Hartmuth, K., M.A., Recombinant Protein Production in Plant Cell Suspension
M. y Matzke, A. J. M. 1986. The expression of a nopaline Cultures. Biochemical Engineering Journal. 45:168-184.
synthase-human growth hormone chimaeric gene in trans- Jamal, A., Ko, K., Kim, H. S., Choo, Y. K. y Joung, H. 2009. Role of ge-
formed tobacco and sunflower callus tissue. Plant Molecular netic factors and environmental conditions in recombinant
Biology. 6;347-357. protein production for molecular farming. Biotechnology
Basile, G. y Peticca, M. 2009. Recombinant protein expression in Advances. 27:914-923.
Leishmania tarentolae. Molecular Biotechnoloogy. 43:273-8. Jonasson, P., Liljeqvist, S., Nygren, P. A. y Stahl, S. 2002. Genetic
Boyer, L. V., Theodorou, A. A., Berg, R. A., Mallie, J., Chavez- design for facilitated production and recovery of recombi-
Mendez, A., Garcia-Ubbelohde, W., Hardiman, S. y Alagon, A. nant proteins in Escherichia coli. Biotechnology and Applied
2009. Antivenom for critically ill children with neurotoxicity Biochemistry. 35:91-105.
from scorpion stings. New England Journal of Medicine. Kost, T. A., Condreay, J. P. y Jarvis, D. L. 2005. Baculovirus as versa-
360:2090-2098. tile vectors for protein expression in insect and mammalian
Casasola, A., Ramos-Cerrillo, B., De Roodt, A. R., Carbajal Saucedo, cells. Nature Biotechnology. 2:567-75.
A., Chippaux, J. P., Alagon, A. y Stock, R. P. 2009. Paraspecific Lau, O. S. y Sun, S. S. 2009. Plant seeds as bioreactors for recombi-
neutralization of the venom of African species of cobra by an nant protein production. Biotechnol Advances. 27:1015-22.
equine antiserum against Naja melanoleuca: a comparative Lesley, S. A. y Wilson, I. A. 2005. Protein production and crystalli-
study. Toxicon. 53:602-608. zation at the joint center for structural genomics. Journal of
Changchien, L. M., Garibian, A., Frasca, V., Lobo, A., Maley, G. F. y Structural and Functional Genomics. 6:71-79.
Maley, F. 2000. High-level expression of Escherichia coli and Martinez-Alonso, M., Garcia-Fruitos, E., Ferrer-Miralles, N., Rinas,
Bacillus subtilis thymidylate synthases. Protein Expression U. y Villaverde, A. 2010. Side effects of chaperone gene co-
and Purification. 19:265-270. expression in recombinant protein production. Microbial
Cregg, J. M., Cereghino, J. L., Shi, J. y Higgins, D. R. 2000. Re- Cell Factories. 9:64.
combinant protein expression in Pichia pastoris. Molecular Mathews, C. K. 1999. Biochemistry. Upper Saddle River, NJ, USA,
Biotechnology. 16:23-52. Prentice Hall.
De-La-Re-Vega, E., Garcia-Orozco, K. D., Calderon-Arredondo, S. Mattanovich, D., Gasser, B., Hohenblum, H. y Sauer, M. 2004.
A., Romo-Figueroa, M. G., Islas-Osuna, M. A., Yepiz-Plascencia, Stress in recombinant protein producing yeasts. Jorunal of
G. M. y Sotelo-Mundo, R. R. 2004. Recombinant expression Biotechnology. 113:121-135.
of marine shrimp lysozyme in Escherichia coli. Electronic Mcallister, W. T. y Raskin, C. A. 1993. The phage RNA polymerases
Journal of Biotechnology. 7:298-304. are related to DNA polymerases and reverse transcriptases.
Deuerling, E. y Bukau, B. 2004. Chaperone-assisted folding of Molecular Microbiology. 10:1-6.
newly synthesized proteins in the cytosol. Critical Reviews in Miao, Y., Ding, Y., Sun, Q. Y., Xu, Z. F. y Jiang, L. 2008. Plant bio-
Biochemistry and Molecular Biology. 39:261-277. reactors for pharmaceuticals. Biotechnology and Genetetic
Eiteman, M. A. &yAltman, E. 2006. Overcoming acetate in Esche- Engineering Reviews. 25:363-380.
richia coli recombinant protein fermentations. TRENDS in Morello, E., Bermudez-Humaran, L. G., Llull, D., Sole, V., Miraglio,
Biotechnology, 24, 530-536. N., Langella, P. y Poquet, I. 2008. Lactococcus lactis, an effi-
Farrokhi, N., Hrmova, M., Burton, R. A. & Fincher G. B. 2009. Hete- cient cell factory for recombinant protein production and
rologous and Cell Free Protein Expression Systems. Methods secretion. Journal of Molecular Microbiology and Biotech-
in Molecular Biology. 513:175-198. nology. 14:48-58.
Geisse, S. & Fux, C. 2009. Recombinant protein production by Nijland, R. y Kuipers, O. P. 2008. Optimization of protein secre-
Volumen XV, Nmero 3
16
Guevara-Hernndez et al: Perspectivas Actuales del Uso de Protenas / XV (3): 8-17 (2013)
tion by Bacillus subtilis. Recent Patents on Biotechnology.
2:79-87.
Oker-Blom, C. y Vuento, M. 2003. Reconstitution of recombinant
viral envelope proteins. Methods in Enzymology, 372, 418-
28.
Palomares, L. A., Estrada-Mondaca, S. y Ramrez, O. T. 2004. Pro-
duction of recombinant proteins: challenges and solutions.
Methods in Molecular Biology. 267:15-52.
Perrire, G., Bessires, P. y Labedan, B. 1999. The Enhanced Mi-
crobial Genomes Library. Nucleic Acids Research. 27:63.
Porro, D., Sauer, M., Branduardi, P. y Mattanovich, D. 2005. Re-
combinant protein production in yeasts. Molecular Biotech-
nology. 31:245-259.
Quintero-Reyes, I., Garcia-Orozco, K., Sugich-Miranda, R., Arvizu-
Flores, A., Velazquez-Contreras, E., Castillo-Yaez, F. y Sotelo-
Mundo, R. 2012. Shrimp oncoprotein nm23 is a functional
nucleoside diphosphate kinase. Journal of Bioenergetics
and Biomembranes. 44:325-331.
Rader, R. A. 2008. Expression Systems for Process and Product
Improvement: A Perspective on Opportunities for Innovator
and Follow-On Product Developers. BioProcess Internatio-
nal. 6:S4-S9.
Salazar-Medina, A. J., Garcia-Rico, L., Garcia-Orozco, K. D.,
Valenzuela-Soto, E., Contreras-Vergara, C. A., Arreola, R.,
Arvizu-Flores, A. y Sotelo-Mundo, R. R. 2010. Inhibition by
Cu2+ and Cd2+ of a mu-class glutathione S-transferase from
shrimp Litopenaeus vannamei. Journal of Biochemical and
Molecular Toxicology. 24:218-222.
Sevastsyanovich, Y. R., Alfasi, S. N. & Cole, J. A. 2010. Sense and
nonsense from a systems biology approach to microbial
recombinant protein production. Biotechnol Appl Biochem,
55, 9-28.
Shokri, A., Sanden, A. M. y Larsson, G. 2003. Cell and process
design for targeting of recombinant protein into the culture
medium of Escherichia coli. Applied Microbiology and Biote-
chnology. 60:654-64.
Smithies, O., Gregg, R. G., Boggs, S. S., Koralewski, M. A. y Ku-
cherlapati, R. S. 1985. Insertion of DNA sequences into the
human chromosomal beta-globin locus by homologous
recombination. Nature. 317:230-234.
Studier, F. W. y Moffatt, B. A. 1986. Use of bacteriophage T7 RNA
polymerase to direct selective high-level expression of clo-
ned genes. Journal of Molecular Biology. 189113-30.
Studier, F. W., Rosenberg, A. H., Dunn, J. J. y Dubendorff, J. W.
1990. Use of T7 RNA polymerase to direct expression of
cloned genes. Methods in Enzymology. 185:60-89.
Terpe, K. 2003. Overview of tag protein fusions: from molecular
and biochemical fundamentals to commercial systems.
Applied Microbiology and Biotechnology. 6:523-33.
Tunitskaya, V. L. y Kochetkov, S. N. 2002. Structural-functional
analysis of bacteriophage T7 RNA polymerase. Biochemistry
(Moscu). 67:1124-1135.
Volumen XV, Nmero 3
17
También podría gustarte
- Control de cambios en SGCDocumento4 páginasControl de cambios en SGCQf Jhon DonadoAún no hay calificaciones
- Gestión no conformidadesDocumento10 páginasGestión no conformidadesQf Jhon DonadoAún no hay calificaciones
- Admd-Df-007 - Jefe de Control de CalidadDocumento1 páginaAdmd-Df-007 - Jefe de Control de CalidadQf Jhon DonadoAún no hay calificaciones
- Admd-Df-010 - Analista de Control de CalidadDocumento1 páginaAdmd-Df-010 - Analista de Control de CalidadQf Jhon DonadoAún no hay calificaciones
- PCGC-NG-004 - Desarrollo de Auditorías y AutoinspeccionesDocumento4 páginasPCGC-NG-004 - Desarrollo de Auditorías y AutoinspeccionesQf Jhon DonadoAún no hay calificaciones
- El Culpable Escondido de La Feminización de Su PróstataDocumento5 páginasEl Culpable Escondido de La Feminización de Su PróstataQf Jhon DonadoAún no hay calificaciones
- PCGC-NG-013 - Flujo Del Proceso de ProducciónDocumento8 páginasPCGC-NG-013 - Flujo Del Proceso de ProducciónQf Jhon DonadoAún no hay calificaciones
- PCGC-NG-003 - Atención de Quejas y Reclamos, Sugerencias y FelicitacionesDocumento8 páginasPCGC-NG-003 - Atención de Quejas y Reclamos, Sugerencias y FelicitacionesQf Jhon DonadoAún no hay calificaciones
- TecnicA Chilena Pra Determinar Minerales Por AADocumento4 páginasTecnicA Chilena Pra Determinar Minerales Por AAElsa BurbanoAún no hay calificaciones
- PCGC-NG-011 - Gestión Del Riesgo para La CalidadDocumento9 páginasPCGC-NG-011 - Gestión Del Riesgo para La CalidadQf Jhon DonadoAún no hay calificaciones
- Fisiologia Del Aparto Reproductor Masculino PDFDocumento26 páginasFisiologia Del Aparto Reproductor Masculino PDFPepe Flores GarciaAún no hay calificaciones
- PCGC-NG-017 - Normas Técnicas y Legales Que Deben Cumplir Los Medicamentos Homeopáticos Magistrales y OficinalesDocumento9 páginasPCGC-NG-017 - Normas Técnicas y Legales Que Deben Cumplir Los Medicamentos Homeopáticos Magistrales y OficinalesQf Jhon DonadoAún no hay calificaciones
- Ptcc-Ne-D002 - Protocolo de Estabilidad de Algodón Absorbente2Documento11 páginasPtcc-Ne-D002 - Protocolo de Estabilidad de Algodón Absorbente2Qf Jhon DonadoAún no hay calificaciones
- Micro 2Documento8 páginasMicro 2Qf Jhon DonadoAún no hay calificaciones
- Micro 2Documento8 páginasMicro 2Qf Jhon DonadoAún no hay calificaciones
- Micro 2Documento8 páginasMicro 2Qf Jhon DonadoAún no hay calificaciones
- Cálculo de pérdida por secado de guaifenesinaDocumento2 páginasCálculo de pérdida por secado de guaifenesinaQf Jhon DonadoAún no hay calificaciones
- Micro 2Documento8 páginasMicro 2Qf Jhon DonadoAún no hay calificaciones
- F T GlucidexDocumento3 páginasF T GlucidexQf Jhon DonadoAún no hay calificaciones
- anexo20PIC PDFDocumento29 páginasanexo20PIC PDFLucia Rodriguez AguilarAún no hay calificaciones
- 32 Anexo-19 PDFDocumento6 páginas32 Anexo-19 PDFQf Jhon DonadoAún no hay calificaciones
- Valoracion HPLC Pureza CromatograficaDocumento3 páginasValoracion HPLC Pureza CromatograficaQf Jhon DonadoAún no hay calificaciones
- Residuo de incineración de dextrometorfanoDocumento2 páginasResiduo de incineración de dextrometorfanoQf Jhon DonadoAún no hay calificaciones
- Programa de Capaitacion en BPMDocumento3 páginasPrograma de Capaitacion en BPMQf Jhon DonadoAún no hay calificaciones
- CXS - 212s - Codex El Azzucar PDFDocumento5 páginasCXS - 212s - Codex El Azzucar PDFcariali12Aún no hay calificaciones
- Monografia GuaifenesinaDocumento3 páginasMonografia GuaifenesinaQf Jhon DonadoAún no hay calificaciones
- F T GlucidexDocumento3 páginasF T GlucidexQf Jhon DonadoAún no hay calificaciones
- Reporte análisis pureza BiotinaDocumento3 páginasReporte análisis pureza BiotinaQf Jhon DonadoAún no hay calificaciones
- Rotación EspecificaDocumento2 páginasRotación EspecificaQf Jhon DonadoAún no hay calificaciones
- Reportes MicrobiologicoDocumento2 páginasReportes MicrobiologicoQf Jhon DonadoAún no hay calificaciones
- Laboratorio Identificacion de BiomoleculasDocumento11 páginasLaboratorio Identificacion de BiomoleculasDiego Herrera EscobarAún no hay calificaciones
- 02 B2 U1 Planificacion Destreza 2Documento1 página02 B2 U1 Planificacion Destreza 2Denisse VélezAún no hay calificaciones
- Biologia Guia 3 Grado 8Documento6 páginasBiologia Guia 3 Grado 8Samuel VivasAún no hay calificaciones
- Semana 7Documento8 páginasSemana 7Emilie RossiAún no hay calificaciones
- Biologia 1391 Tarea 3 Gesella MendozaDocumento9 páginasBiologia 1391 Tarea 3 Gesella Mendozagissella Mendoza CarmonaAún no hay calificaciones
- Actividad 6 Aformato Proyecto Formativo Modelos Economicos - Economia PoliticaDocumento22 páginasActividad 6 Aformato Proyecto Formativo Modelos Economicos - Economia PoliticaJose Ignacio Encinas ArancibiaAún no hay calificaciones
- Bme U1 A1 KarfDocumento5 páginasBme U1 A1 KarfKaren Ruiz FloresAún no hay calificaciones
- Enzimas OxidorreductasasDocumento3 páginasEnzimas OxidorreductasasStherling Angulo0% (1)
- Autoevaluacion de BCDocumento13 páginasAutoevaluacion de BCMarianella PintoAún no hay calificaciones
- Biotecnologia de Proteinas Recombinates para La Aplicacion de La AcuaculturaDocumento23 páginasBiotecnologia de Proteinas Recombinates para La Aplicacion de La AcuaculturaGerman Maza0% (1)
- TP Metabolismo Aminoácidos y ProteínasDocumento5 páginasTP Metabolismo Aminoácidos y ProteínasRoo EsquivelAún no hay calificaciones
- Célula eucariota: estructura y componentesDocumento11 páginasCélula eucariota: estructura y componentesIsmael Cabello CarrilloAún no hay calificaciones
- Ficha de Ciencias 6toDocumento1 páginaFicha de Ciencias 6toJimmy joel Paredes mendietaAún no hay calificaciones
- CP450Documento2 páginasCP450Alejandra CardenasAún no hay calificaciones
- Aislamiento de AdnDocumento6 páginasAislamiento de AdnStephany GaleanoAún no hay calificaciones
- VACUNASDocumento23 páginasVACUNASJara MillioAún no hay calificaciones
- Biotecnología para jóvenesDocumento84 páginasBiotecnología para jóvenesLupita SotoAún no hay calificaciones
- Transporte a través de la membrana celular: difusión, ósmosis y endocitosisDocumento4 páginasTransporte a través de la membrana celular: difusión, ósmosis y endocitosisRenata RamírezAún no hay calificaciones
- Flashcards Vacunas Covid 19Documento16 páginasFlashcards Vacunas Covid 19La Loka JasmineAún no hay calificaciones
- Genética Bacteriana I 2016Documento53 páginasGenética Bacteriana I 2016Valeria Dos SantosAún no hay calificaciones
- Tema 4.1Documento79 páginasTema 4.1PeñuelaAún no hay calificaciones
- ACFrOgAcY9XdinwdtrvMnyPJi AvU5whvLI4qp4tSJewMiAixffo Kmuv4H76l0 DbdeUu5ADkI 8Hgm80KRoaPLrJeDgwTgaFt52Y4tTJ-Ga1gE-h2v5LVvLfHq OD9sEuKO QBeKTteg9Yu-r3Documento7 páginasACFrOgAcY9XdinwdtrvMnyPJi AvU5whvLI4qp4tSJewMiAixffo Kmuv4H76l0 DbdeUu5ADkI 8Hgm80KRoaPLrJeDgwTgaFt52Y4tTJ-Ga1gE-h2v5LVvLfHq OD9sEuKO QBeKTteg9Yu-r3Neiris Pallares CarreñoAún no hay calificaciones
- Celulas Madres PDFDocumento5 páginasCelulas Madres PDFRamon ColmenaresAún no hay calificaciones
- Biotecnologia PDFDocumento105 páginasBiotecnologia PDFCamila Gomez AldanaAún no hay calificaciones
- TP 02 Electroforesis en Geles de Agarosa - 1c23Documento7 páginasTP 02 Electroforesis en Geles de Agarosa - 1c23saaciarciancioAún no hay calificaciones
- Apuntes Sobre MitosisDocumento18 páginasApuntes Sobre Mitosiscarla gomezAún no hay calificaciones
- Acidos Nucleicos 17-18-170910104832 PDFDocumento17 páginasAcidos Nucleicos 17-18-170910104832 PDFAnonymous GS7buYAún no hay calificaciones
- Genetica ProgramaDocumento4 páginasGenetica ProgramaRhina RamirezAún no hay calificaciones
- Estudio del bombeo de protones por levaduraDocumento4 páginasEstudio del bombeo de protones por levaduraSharon Dayan Cubas100% (1)
- El Genoma HumanoDocumento2 páginasEl Genoma HumanoLunailed AdeurAún no hay calificaciones