Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Absorcion Atomica
Cargado por
jorge uribeTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Absorcion Atomica
Cargado por
jorge uribeCopyright:
Formatos disponibles
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
ANLISIS QUMICO POR ESPECTROFOTOMETRA DE ABSORCIN
ATMICA
PRESENTADO POR:
DUVAN STIVEN GOMEZ NAVARRO CDIGO: 2122430
LINA MARA SIERRA SERRANO CDIGO: 2102588
JORGE URIBE CDIGO: 2082274
GRUPO A
PRESENTADO A:
PROFESOR: JHON FREDDY PALACIOS
UNIVERSIDAD INDUSTRIAL DE SANTANDER
FACULTAD DE INGENIERAS FISICOQUMICAS
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
BUCARAMANGA
2016
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
1. INTRODUCCIN
En el presente informe se analizar la tcnica de espectrofotometra de absorcin
atmica para conocer la concentracin que tiene el cobre en un mineral de sulfuro de
cobre, para saber si es viable realizar la extraccin de este valioso metal por
lixiviacin, la aplicacin de esta tcnica es de gran importancia para el crecimiento
como ingenieros metalrgicos en la rama de la metalurgia extractiva, adems esta
tcnica nos ayuda a conocer la concentracin del metal que se desea en inters para
saber si la lixiviacin es buena o no.
En la industria se utiliza este mtodo para analizar la eficiencia de todo el circuito
cerrado de lixiviacin de minerales, extrayendo muestras en cada uno de los
procesos, ya sea en agitacin, espesadores, molienda y filtros, por esto es de gran
ayuda esta tcnica para conocer si el proceso de extraccin del metal en una planta
determinada est bien o hay que cambiar uno de estos procesos y hacerlo ms
eficiente.
2. OBJETIVOS
2.1 OBJETIVO GENERAL
Analizar y comprender el funcionamiento de la tcnica de espectrofotometra
de absorcin atmica y con ello determinar la disolucin de los metales en los
procesos de lixiviacin.
2.2 OBJETIVOS ESPECFICOS
Investigar y comprender el fundamento de la tcnica de espectrofotometra
de absorcin atmica y conocer sus diferentes aplicaciones.
Determinar la concentracin de cobre presente en soluciones provenientes
de un proceso de lixiviacin.
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
3. EQUIPOS, MATERIALES Y REACTIVOS
Figura1. Esquema de los principales implementos de laboratorio utilizados en las prcticas.
4. FUNDAMENTOS TERICOS
1. Fundamento conceptual de la tcnica.
Absorcin atmica
La espectroscopia de absorcin atmica (EAA), tiene como fundamento la
absorcin de radiacin de una longitud de onda determinada. Esta radiacin es
absorbida selectivamente por tomos que tengan niveles energticos cuya
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
diferencia en energa corresponda en valor a la energa de los fotones
incidentes. La cantidad de fotones absorbidos, est determinada por la ley de
Beer, que relaciona sta prdida de poder radiante, con la concentracin de la
especie absorbente y con el espesor de la celda o recipiente que contiene los
tomos absorbedores.
Tcnica analtica cuantitativa aplicable al anlisis de elementos metlicos, del
orden de las ppm o trazas ([<0.01%, ppm]) en minerales, muestras biolgicas,
metalrgicas, farmacuticas, aguas, alimentos, etc.
Las muestras analizar deben estar en estado lquido.
Se basa en la absorcin de radiacin electromagntica por las partculas atmicas,
ya que parte de la luz que pasa a travs de esas partculas atmicas es absorbida
por los tomos, y es utilizada para pasar a su nivel excitado, disminuyendo as la
intensidad de la misma.
Descripcin de la tcnica de EAA: la tcnica de absorcin atmica en flama en
una forma concisa consta de lo siguiente: la muestra en forma lquida es aspirada
a travs de un tubo capilar y conducida a un nebulizador donde sta se desintegra
y forma un roco o pequeas gotas de lquido. Las gotas formadas son conducidas
a una flama, donde se produce una serie de eventos que originan la formacin de
tomos. Estos tomos absorben cualitativamente la radiacin emitida por la
lmpara y la cantidad de radiacin absorbida est en funcin de su concentracin.
La seal de la lmpara una vez que pasa por la flama llega a un monocromador,
que tiene como finalidad el discriminar todas las seales que acompaan la lnea
de inters. Esta seal de radiacin electromagntica llega a un detector o
transductor y pasa a un amplificador y por ltimo a un sistema de lectura.
Ilustracin 1. Equipo de absorcin atmica, partes que lleva este equipo.
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
Fuentes de radiacin: una vez que han sido formados los tomos, la flama
tiene la misma funcin que una celda en espectroscopia visible o Ultravioleta.
Los tomos de la flama absorben radiacin de acuerdo a la Ley de Beer si esta
corresponde a la diferencia en energa entre los niveles energticos de algunos de
los tomos presentes, de los contrario, la radiacin pasa por la flama sin disminuir
la potencia de haz como efecto de los tomos contenidos en ella. El desarrollo de
un equipo comercial de absorcin atmica fue hasta principio de los cincuentas, ya
que aunque su potencial se vislumbra desde fines del siglo pasado, no se saba
an como tener una fuente de radiacin para este tipo de espectroscopia.
Niveles cunticos en tomos: como ya ha sido mencionado con anterioridad, los
tomos de los diferentes elementos tienen lneas bien definidas que corresponden
a transiciones entre diferentes niveles atmicos. Estas transiciones tienen anchos
espectrales de dcimas o hasta centsimas de nanmetro. Cada elemento va a
responder a la excitacin de una radiacin de longitud de onda muy especfica ya
que solo este elemento absorbe o emite tal tipo de radiacin, porque esta
corresponde a la diferencia en energa entre dos niveles particulares de ese
tomo.
Ilustracin 2.Diagrama de niveles de energa para el sodio y para el potasio.
Lmpara de ctodo hueco: Este tipo de fuente de radiacin es de las
ampliamente difundidas en la EAA. Las lmparas de ctodo hueco (LCH o HCL
[Hollow Cathode Lamp]) consisten de un cilindro de vidrio sellado al vaco y con un
gas inerte en su interior. Dentro de este mismo cilindro se encuentran dos
filamentos; uno de ellos es el ctodo y el otro el nodo. El nodo generalmente es
un alambre grueso hecho de nquel o tungsteno, el ctodo es en forma de un
cilindro hueco, en el interior del cual se encuentra depositado en forma de una
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
capa el elemento metlico que se va a excitar. Tambin regularmente y
cuando esto es posible el ctodo est enteramente hecho del metal a
analizar.
Ilustracin 3. Lmpara de ctodo hueco, con nodo de tungsteno, y el ctodo constituido
del metal que se desea analizar.
Proceso de atomizacin:
1. El lquido disolvente se evapora, y la muestra permanece seca.
2. Vaporizacin. La muestra slida se evapora a gas.
3. Atomizacin. Los compuestos que componen la muestra se dividen en tomos
libres.
Monocromador: Dispersa las distintas longitudes de onda de la radiacin emitida
por la fuente y separa la lnea particular que se desea medir.
2. Aplicaciones de esta tcnica.
En metalurgia, la absorcin atmica es una tcnica muy til ya que permite
determinar diversos elementos en un amplio rango de concentraciones. Las
mayores dificultades radican en la puesta en solucin de aleaciones o de los
mismos metales, las cuales se efectan por medio de ataques con cidos fuertes,
por ejemplo, el cido ntrico, clorhdrico, sulfrico y perclrico. Normalmente se
determina Fe, Pb, Ni, Cr, Mn, Co, Sb y Cu entre otros, en rangos que van desde
0.003 % hasta 30 % en aleaciones con base Cu, Zn, Al, Pb, Fe y Sn entre otras.
Esta tcnica de absorcin atmica es ampliamente utilizada en el estudio de
artefactos arqueolgicos, en el anlisis de materiales metlicos no ferrosos
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
(aleaciones de cobre), lo cual puede ayudar al entendimiento del desarrollo
de la metalurgia del cobre y bronce y de tcnicas de fundicin en pocas
pasadas. Tambin puede utilizarse para el anlisis elemental de artefactos de
pedernal.
Bioqumica: Anlisis de Cerio, determinacin de calcio, determinacin de
Magnesio, Sodio y Potasio entre otros.
Productos Alimenticios: Anlisis de pescado y productos martimos, anlisis de
leche, jugos de fruta entre otros.
Geoqumica: Anlisis de bauxita, rocas y slidos, silicatos, carbonatos.
Industrialmente: Anlisis de cemento, vidrio, fibra cermica, pinturas entre otros.
Petroqumica: Anlisis de aceites lubricantes, aditivos, gasolina.
Frmacos y Cosmticos: Anlisis de lociones, preparaciones farmacuticas.
Otras aplicaciones.
Determinar los orgenes de objetos de cermica que fueron adquiridos a
travs de comercio.
Encontrar diferencias qumicas entre objetos originales y copias de los
objetos
Fluidos biolgicos, sangre y orina.
Cuando se requiere la destruccin de la materia orgnica, mediante la
calcinacin en seco o por va hmeda.
Formacin de compuestos de asociacin con quelatos metlicos seguida de
la extraccin en fase orgnica y medida de la absorbancia atmica del
metal.
Conocer fuente y origen de las arcillas.
Determinacin de una amplia gama de elementos en: suelos, rocas,
productos petrolferos, productos farmacuticos, metales y aleaciones.
3. Limitaciones de esta tcnica, por tipo de muestra y por nivel de
concentracin.
Los metales se analizan individualmente y no simultneamente. Por lo general no
es aplicable a no metales
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
Tipo muestra
Esta tcnica presenta una notable desventaja y es que se solo puede ser aplicada
a metales solubles y que se encuentren es estado lquido. Adems, solo se puede
analizar los elementos de inters de una mezcla por separado, aumentando de
este modo el tiempo del anlisis.
Todos los elementos que se analizan por esta tcnica tienen un comportamiento
lineal. Un punto muy importante para el anlisis de las muestras es que esta debe
ser soluble y, estar muy bien filtrada sin ningn tipo de sedimentos.
Nivel de concentracin
El rango de concentracin ptimo para un elemento determinado en la solucin
usando espectroscopia de absorcin atmica es tpicamente 1-10 ppm (1 g/ml de
sol.), aunque finalmente depende del elemento que se desea a analizar. Tambin
es un factor importante que la concentracin lmite para el anlisis depender
principalmente de la cantidad de muestra disponible.
4. Anlisis cuantitativo de cobre en soluciones de lixiviacin
4.1 Preparacin de las muestras a analizar
Las muestras problemas fueron denominadas de mayor a menor concentracin
como 1, 2 y 3 respectivamente y la dilucin realizada a cada una se realiz de la
siguiente manera:
Muestra
1era Dilucin
2da Dilucin
Dilucin
1ml
100ml
1ml
100ml
10000 veces
1ml
100ml
1ml
50ml
5000 veces
0.1ml
100ml
-------
1000 veces
Tabla1. Tabla de las muestras a analizar en el mtodo anlisis
qumico por espectrofotometra de absorcin atmica
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
De esta
solucion tomar
nuevamente 1
ml y aforarla en
100 ml de
agua.
Pesar cierta cantidad de
sulfato pentahidratado.
Diluir en 100 ml de agua
Tomar 1 ml de solucion y
aforarla en 100 ml.
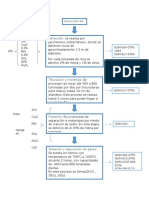
Imagen1. Diagrama del procedimiento para la preparacin de las muestras a analizar en el mtodo
anlisis qumico por espectrofotometra de absorcin atmica
4.2 Patrones utilizados
4.3 Condiciones operativas del espectrofotmetro para la lectura de las
muestras
Para analizar los constituyentes atmicos de una muestra es necesario atomizarla.
La muestra debe ser iluminada por la luz. Finalmente, la luz es transmitida y
medida por un detector, con el fin de reducir el efecto de emisin del atomizador o
del ambiente.
Es necesario optimizar el paso de banda espectral del monocromador empleado
para la seleccin de la longitud de onda, la velocidad de aspiracin de la solucin,
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
los parmetros del sistema de deteccin y lectura y en el caso de absorcin
atmica, la intensidad de corriente de la lmpara de ctodo hueco.
Se debe tener en cuenta factores como:
Muestras bien diluidas y baja concentracin.
Libre de sedimentos.
Seleccin adecuada de la lmpara.
La distribucin energtica de niveles excitados
Las probabilidades de transicin para emisin y absorcin
El coeficiente de absorcin atmica
Las caractersticas de la celda de atomizacin
5. PROCEDIMIENTO
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
Identificar las muestras
y tomar con una pipeta
aforada alcuotas
adecuadas de la
solucin.
Aadir las soluciones
en balones aforados.
Asegurarse que la
concentracin de cobre
quede entre los rangos
adecuados.
Aforar los balones con
agua destilada,taparlos
y agitar.
Ubicar el baln en el
equipo de
espectrofotometra
Leer la concentracin
del equipo, realizar los
clculos y anlisis
pertinentes para
conocer la
concentracin de cobre
en las muestras que
provienen de un
proceso de lixiviacin.
Imagen2. Diagrama del procedimiento para el mtodo anlisis qumico por espectrofotometra de
absorcin atmica
6. DATOS, CLCULOS Y ANLISIS DE RESULTADOS
Datos iniciales:
Pm CuSO4. 5H2O = 250 g/mol
Pm Cu = 64 g/mol
I Obtenemos la concentracin de las muestras
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
Concentracin de Cu en la muestra 1:
64
[Cu] = 7,85 x 250 x 50 ml x
1000 ml 1000 mg
x
=40192 mg/l
1L
1g
Concentracin de Cu en la muestra 2:
V 1 C 1=V 2 C 2
C 2=
v 1 c 1
V2
C 2=
0.10 40192
=8038.4 mg/ l
0.50
Concentracin de Cu en la muestra 3:
V 2C 2=V 3 C 3
C 3=
C 3=
v2c2
V3
0.10 8038.4
=1607.68 mg/l
0.50
II A partir de las concentraciones y el volumen al que debo llevar dicha
concentracin hallo los volmenes sabiendo que se necesita obtener 2 ppm de
cada muestra
Volumen inicial de la muestra 1 para llevarlo a un volumen de 500ml y
2 ppm.
Vi=
0,5 x 2
=2.49 x 10E-5 L= 24,9
40192
Volumen inicial de la muestra 2 para llevarlo a un volumen de 100ml y
2 ppm
0,1 x 2
V i= 8038 =2,49 x 10E-5 L= 24,9
Volumen inicial de la muestra 3 para llevarlo a un volumen de 100ml y
2 ppm
Vi=
0,1 x 2
=1,24 x 10E-4 L= 124
1608
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
III Cuando se realiza la dilucin y son llevadas las muestras al equipo de
espectrofotometra de absorcin atmica, se generan los siguientes resultados:
Muestra
Absorbancia
[Cu] ppm
0,1060
1,923
0,0999
1,807
0,1056
1,916
Tabla 1. Resultados de
absorbancia y
concentracin
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
Parametros iniciales
para la realizacion del
proceso.
Resultados de cada
una de las muestras
analizadas y
IV Se realiza el clculo de la concentracin real de las muestras estudiadas
Muestra 1:
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
V 1 C 1=V 2 C 2
[Cu]=
0.5 1,923
=38614,46 ppm
2.49 x 10E-5
Muestra 2:
V 1 C 1=V 2 C 2
[ Cu ] = 0.1 1,807 =7257,03 ppm
2.49 x 10E-5
Muestra 3:
V 1 C 1=V 2 C 2
[Cu]=
0.1 1,916
=1545,16 ppm
1,24 x 10E-4
La concentracin experimental es la cantidad de soluto que se tiene en la solucin
y se da por partes por milln; al realizar la prctica de laboratorio se encuentra que
las concentraciones de la solucin eran menores que las reales, debido a que no
se trabaj con mediciones exactas de la concentracin de la especie a analizar,
puesto que se requirieron volmenes muy pequeos y pueden existir errores en la
toma de dichos volmenes con el instrumento (micropipeta).
Para cada muestra se realiz una dilucin diferente debido a su concentracin, es
decir, a mayor concentracin se diluy ms la muestra para alcanzar una
concentracin de hasta dos ppm puesto que este valor se encontraba en el rango
de la curva de calibracin.
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
Grfica comparativa entre concentraciones encontradas
Absorbancia vs Concentracin
0.11
0.11
0.1
ABSORBANCIA
0.1
0.1
0.1
0.1
1,800
1,820
1,840
1,860
1,880
1,900
1,920
1,940
Concentracin [cU] PPM
Figura . Absorbancia Vs Concentracin.
Fuente: Autores
Al analizar la grfica obtenida del laboratorio de espectrofotometra de absorcin
atmica, es necesario establecer experimentalmente una curva que relacione la
seal analtica obtenida con la concentracin del elemento analito (Cu) en la
solucin a analizar (CuSO4), la cual es denominada curva de calibracin, siendo
esta una lnea recta. Esta grafica se obtendr con varios estndares denominados
patrones que debern tener una composicin qumica similar a la de muestra que
cubran el mbito de concentraciones requeridas (0 5 ppm).
En base a la grfica obtenida se puede evidenciar la relacin absorbanciaconcentracin de las muestras preparadas en laboratorio. Dado que guardan una
variacin lineal es claro que siguen la Ley de Lambert-Beer, pues en la medida en
que aumenta la concentracin del elemento a analizar, asimismo lo hace su
absorbancia; esto debido a que al existir mayor cantidad de iones de la especie
analizada, en la solucin, se podr absorber mucha ms energa dado que cada
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
ion absorbe cierta cantidad, pero en conjunto esto se magnifica y el valor
aumenta considerablemente.
7. CONCLUSIONES Y RECOMENDACIONES
Como se puede observar para la primera muestra se obtuvo una
concentracin real de 38614,46 [ppm] es decir que por cada litro de
solucin se tiene 38,61 [g] de Cu disueltos en un litro, lo que significa que
es muy bueno porque tericamente se deban disolver 40, 2[g] por litro
obtenindose una eficiencia del 96%, lo que significa que el mtodo de
lixiviacin utilizado es bueno.
Para la segunda y tercera muestra se obtuvieron 7257,0.3 [ppm] y 1545,16
[ppm] respectivamente donde tericamente para la segunda muestra se
deban disolver 80,4 [g] por litro de solucin y 16,1 [g] por litro de la tercera
muestra, demostrando as que el lixiviante utilizado (agua) es eficiente para
la obtencin de cobre a partir de sulfato de cobre, obtenindose una
eficiencia de disolucin del ms del 95%.
En conclusin, general el utilizar la tcnica de espectroscopia de absorcin
atmica es de gran ayuda para saber si el lixiviante utilizado es bueno o no
para la obtencin del metal de inters y si as saber la eficiencia que tiene
este lixivainte. Llegado el caso se llegue a presentar una baja concentracin
de sulfato de cobre en el agua, es porque posiblemente se est disolviendo
otro compuesto que disminuye la concentracin de cobre disuelto, por
tanto, se deben hacer otros estudios de la mena que se est utilizando.
Como una recomendacin, sera que nosotros mismos pudiramos realizar
la muestra patrn de la cual se sacaron las alcuotas para las posteriores
disoluciones, y saber con exactitud el peso de la muestra de CuSO4. 5H2O
que se utiliz porque se pudo haber suministrado un peso errneo.
ESCUELA DE INGENIERA METALRGICA Y CIENCIA DE MATERIALES
LABORATORIO DE HIDRO Y ELECTROMETALRGIA
8. BIBLIOGRAFA
Blago Razmilic. Merck Qumica Chilena Soc. Ltda. Espectroscopia de
absorcin. Atmica. [En lnea]. [Consultado: 20 de agosto del 2016].
Disponible en: http://www.fao.org/docrep/field/003/ab482s/ab482s04.htm
Equipos de Espectrofotmetro de absorcin atmica. [En lnea].
[Consultado:
20
de
agosto
del
2016].
Disponible
en:
http://pendientedemigracion.ucm.es/info/iqpapel/equipos/absorcionatomica.htm
LABORATORIO DE TECNICA INSTRUMENTAL UVA. Espectroscopia de
absorcin atmica. [En lnea]. [Consultado: 20 de agosto del 2016].
Disponible
en:
http://laboratoriotecnicasinstrumentales.es/analisisqumicos/espectroscopa-de-absorcin-atmica
Skoog, Holler. Principios de Anlisis Instrumental, Quinta edicin, Mc Graw
Hill, [ Consultado: 20 de agosto del 2016].
También podría gustarte
- Practica 9Documento6 páginasPractica 9Javier San Juan MercadoAún no hay calificaciones
- Práctica 1 ElectrometalurgiaDocumento6 páginasPráctica 1 ElectrometalurgiaJonathan BautistaAún no hay calificaciones
- Proceso de Manufactura, La Termodinámica en El Corte de Los MetalesDocumento12 páginasProceso de Manufactura, La Termodinámica en El Corte de Los MetalesAnnelysAún no hay calificaciones
- Extraccion Zinc y CupritaDocumento5 páginasExtraccion Zinc y Cupritacoreano63Aún no hay calificaciones
- Depositos de Estibina CuarzoDocumento19 páginasDepositos de Estibina CuarzoYaquelin HanccoAún no hay calificaciones
- Tema 2. Capitulo I. Introduccion A La Quimica de La Coordinacion.2014Documento15 páginasTema 2. Capitulo I. Introduccion A La Quimica de La Coordinacion.2014JorgeMartinAún no hay calificaciones
- Analisis de Au y Ag Por Via Seca 2Documento8 páginasAnalisis de Au y Ag Por Via Seca 2milagrosAún no hay calificaciones
- Presentación Hierro Nodular Procesos y Características Junio 2015Documento165 páginasPresentación Hierro Nodular Procesos y Características Junio 2015MARCOAún no hay calificaciones
- SKARNDocumento92 páginasSKARNOmar Rodriguez100% (1)
- Colegio Integrado Santa TeresitaDocumento2 páginasColegio Integrado Santa TeresitacolisanteAún no hay calificaciones
- Tarea 3 - Metales y MetalurgiaDocumento11 páginasTarea 3 - Metales y MetalurgiajohnAún no hay calificaciones
- Tabla de Pesos Especificos de Algunos MaterialesDocumento7 páginasTabla de Pesos Especificos de Algunos MaterialesGERARDO CORREA PORTILLOAún no hay calificaciones
- Cuaderno 2 Recuperacion Pendientes 2014 15 PDFDocumento9 páginasCuaderno 2 Recuperacion Pendientes 2014 15 PDFanasanchezvazAún no hay calificaciones
- Cubierta de Una ViviendaDocumento25 páginasCubierta de Una ViviendaManenita Terán GallardoAún no hay calificaciones
- Aluzinc MirominaDocumento5 páginasAluzinc MirominaKiro Irwing Alvarez JaraAún no hay calificaciones
- Clasificacion de La Mineria PeruanaDocumento17 páginasClasificacion de La Mineria PeruanaDiaz Velasquez EliasAún no hay calificaciones
- Catálogo Kubiteja TradicionalDocumento7 páginasCatálogo Kubiteja TradicionalLeonel CalvaAún no hay calificaciones
- Texturas de Rocas SedimentariasDocumento80 páginasTexturas de Rocas SedimentariasAníbalUrangoAlcántara75% (4)
- Geología Regional y LocalDocumento2 páginasGeología Regional y LocalKeny Alvarado CalderonAún no hay calificaciones
- Discontinuidades en El Metal Base y de La Soldadura FinalDocumento8 páginasDiscontinuidades en El Metal Base y de La Soldadura FinalFrank Merello PortocarreroAún no hay calificaciones
- Terminologia IngenierilDocumento6 páginasTerminologia IngenierilErickChávezAún no hay calificaciones
- Presentacion de Clasificacion de Aceros Anibal Moran 1Documento27 páginasPresentacion de Clasificacion de Aceros Anibal Moran 1Anibal Moran CarrilloAún no hay calificaciones
- Evolución de La MamposteríaDocumento3 páginasEvolución de La MamposteríaJeSy QuirogaAún no hay calificaciones
- Expediente Técnico Anexo IDocumento5 páginasExpediente Técnico Anexo IkarenAún no hay calificaciones
- Manual AcerosDocumento1 páginaManual AcerosUlises Corleone BaudelaireAún no hay calificaciones
- Las Sales OxigenadasDocumento7 páginasLas Sales OxigenadasEli Becerra100% (1)
- Practica de SoldaduraDocumento10 páginasPractica de SoldaduraCatalina Ramirez CarreraAún no hay calificaciones
- Serv. Parada Chancado 2.5 24.07.2022Documento7 páginasServ. Parada Chancado 2.5 24.07.2022JHON JAIME PECHO INGAAún no hay calificaciones
- William F. Smith and Javad Hashemi - Fundamentos de La Ciencia e Ingenieria de Materiales-McGraw-Hill (2006) - 384-392Documento9 páginasWilliam F. Smith and Javad Hashemi - Fundamentos de La Ciencia e Ingenieria de Materiales-McGraw-Hill (2006) - 384-392Carlos ClementeAún no hay calificaciones
- Analisis CuantitativoDocumento10 páginasAnalisis CuantitativoJesús Elías Arcaya EscobarAún no hay calificaciones