Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Arcillas
Cargado por
Ana Lucía Aguilar ChávezTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Arcillas
Cargado por
Ana Lucía Aguilar ChávezCopyright:
Formatos disponibles
http://www.eweb.unex.es/eweb/edafo/ECAP/ECAL4FSCMMinPrim.
htm
1. Familia de las caolinitas. Diagramar
2. Familia de las esmectitas. Diagramar
3. Que son los filosilicatos, dar tres ejemplos
4. Como se dan los arreglos cristalinos y las sustituciones en las arcillas
5. Como se denomina el anillo de 6 tetraedros. Diagramar
6. Diagramar una lmina tetradrica
7. Diagramar el caoln y el hexahidroxi de aluminio
8. Diagramar la estructura de cationes intercambiables y agua
intergranular
Siguiendo estas sencillas reglas podemos armar el mecano de
manera que un tetraedro (1T) pueda unirse a otro para
formar un arreglo tipo 2T (dos tetraedros) o bien 3T, ..., etc.
cada uno de estos arreglos es tpico de alguno de los silicatos
minerales ms conocidos.
El mineral circn est compuesto de tetraedros aislados (1T),
que los piroxenos por cadenas simples de un nmero infinito
de miembros (nT).
las redes de tetraedros que se extienden a lo largo y a
lo ancho, formando hojas completas, constituyen el
grupo de FILOSILICATOS, o estructuras laminares, del
que forman parte las arcillas.
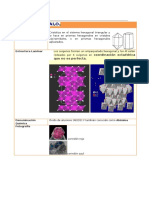
Una propiedad extraordinaria de estas estructuras es su posibilidad
de ser capaces de sustituir al tomo de silicio (Si), situado en
el centro de los tetraedros (Figura 4), por otro de menor carga
como el aluminio (A1
3+
), generando as una deficiencia de carga
positiva, o un exceso de carga negativa en el tetraedro, la cual
necesita atraer a otros cationes para compensarse, por
ejemplo Na, K, Ca, ... , etc.
al unir los vrtices para formar anillos tipo 6T (seis
tetraedros), como se muestra en la figura 5 (b). Las puntas
de los tetraedros se encuentran a la misma altura, formando un
plano, de igual manera ocurre con los tomos de silicio situados
en el centro de los tetraedros y con los de oxgeno situados en las
bases. La articulacin de esos tres planos nos conduce pues a la
formacin de una hoja tetradrica (tipo T).
Figura 5 (b). El anillo de seis tetraedros.
Siguiendo esta secuencia, podemos ahora unir dos hojas para
formar una lmina tetradrica, tal y como se ilustra en la
figura 6. En sta se observa que las dos hojas se
encuentran invertidas, una con respecto a la otra, compartiendo
uno de los vrtices.
Figura 6. Una lmina de tetraedros (T).
Similarmente, existen otros cuerpos poligonales que
podemos unir entre s para formar cadenas, tal y como
ocurre con el octaedro (octa, ocho; edros, cara),
representado en la figura 7, formacin tpica de los
compuestos de aluminio, por ejemplo Al (OH)
6
, o del
magnesio. Este arreglo es una hoja octadrica (tipo O).
Figura 7. Una hoja de octaedros (O).
Ahora bien, la unin de una hoja del tipo T, con otra del
tipo O, genera una lmina T- O,o lmina 1:1, tal y como se
ilustra en la figura 8. La coincidencia, sin embargo, no es
perfecta cuando se trata de hojas T formadas por silicio-
oxgeno y de hojas tipo O formadas por aluminio-oxgeno-
oxhidrilo, lo cual crea un efecto de esfuerzo entre las hojas
que es de gran importancia para algunas de las aplicaciones
de las arcillas que presentan este tipo de lminas (T-O),
por ejemplo el caoln.
Figura 8. Una lmina T-O.
Ahora terminamos la secuencia agregando una tercera hoja
tipo T a la lmina T-O mencionada arriba y el resultado se
ilustra en la figura 9, que muestra la lmina T-O-T, o, como
algunos lectores perspicaces la llaman: la estructura de
sandwich, debido a que dos hojas tipo T se asemejan a los
panes del sandwich, mientras que el jamn correspondera
a la hoja tipo O. Esta lmina tiene pues dos hojas T y una
hoja O, o sea la lmina es del tipo 2:1.
9. Figura 9. Una lmina T-O-T.
Hasta aqu termina el juego del mecano, ya que la
lmina T-O-T es la ms completa y no acepta una nueva
adicin, debido a la saturacin de los enlaces. Una cosa es
clara en este punto: las estructuras de sandwich son nada
menos que la parte esencial de las arcillas! Por si hubiese
alguna duda al respecto, pasaremos ahora a ilustrar la
importancia de las estructuras formadas por las lminas tipo
1:1 y aquellas formadas por las lminas tipo 2:1.
GRUPO 1:1
Los caolines
El nombre caoln proviene de la voz china Kau-Ling, nombre del
cerro de una regin situada al norte de China de donde se extraa
esta arcilla desde el siglo VIII d.C., para la fabricacin de la
porcelana. La unidad fundamental de la estructura del caoln
es la lminaT-O, o sea la lmina 1:1, una hoja de
tetraedros de silicio-oxgeno unida a otra hoja de
octaedros de aluminio-oxgeno-OH. La sustitucin del
silicio por otro elemento, como el aluminio, o bien la
sustitucin del aluminio en la hoja tipo O por otro elemento
de menor carga, por ejemplo el magnesio, causa un cambio
qumico en el material pero mantiene esencialmente la
misma estructura. Estas sustituciones dan origen a la familia de
los caolines (Figura 10).
Figura 10. El rbol de los caolines.
La primera rama comprende a aquellos minerales derivados
de la caolinita que guardan la misma composicin qumica
por cada unidad estructural:
Al
2
Si
2
O
5
(OH)
4
stos son la nacrita, dickita, anauxita, halloisita y el alofano,
los cuales difieren entre si slo por su arreglo laminar.
Imaginemos un paquete de naipes en el que todas las
cartas se encuentran ordenadas perfectamente: sta es la
estructura de la nacrita (Figura 11). En este caso el paquete
de cartas puede llegar a ser muy alto debido a que la
estructura ordenada es ms estable.
Figura 11. La baraja de los caolines.
En cambio, la dickita est dispuesta de tal manera que el
paquete de naipes se abre ms de un lado que del otro,
entre 6 y 7 grados, mientras que la caolinita se abre hasta
15 grados.
Existe un mineral asociado (livesita) que presenta una
abertura a un lado que es siempre regular, mientras que la
carta siguiente se abre de forma irregular hacia el otro lado,
dando origen a una estructura laminar muy desordenada y
poco estable.
El otro grupo de caolines es igualmente importante y
comprende el mismo tipo de estructura laminar, pero con
una sustitucin del aluminio de la hoja tipo O por otro
catin, por ejemplo el hierro (Fe
2+
, Fe
3+
) o el magnesio
(Mg
2+
). Sin embargo, al sustituir el aluminio por el
magnesio se contraen ligeramente las dimensiones de la
hoja tipo O, originando una pequea distorsin en la
lmina T-O, la cual permite acomodar el esfuerzo pero
ocasiona que la forma externa de los cristales de este tipo
sea fibrosa o corrugada, tal es el caso de los asbestos
(crisotilo) y la antigorita, respectivamente.
Una ltima observacin: en las estructuras de estos derivados del
caoln se ve que sus hojas se ensamblan naturalmente unas sobre
otras, como las cartas de una baraja, con las variaciones
mencionadas arriba, de modo que entre una hoja y otra hay un
enlace muy dbil, del tipo Van Der Waals, creando un espacio
interlaminar que guarda propiedades muy interesantes, como
veremos ms adelante.
GRUPO 2:1
1) Las esmectitas
La familia de las esmectitas est formada por todas aquellas
arcillas que presentan una estructura de sandwich!, es decir, que
est constituida por dos hojas de tipo T y por otra intermedia de
tipo O. La frmula estructural tpica de estas arcillas es la
siguiente:
Al
2
Si
4
O
10
(OH)
2
hoja hoja
octadrica tetradrica
Esta estructura es elctricamente neutra debido a que todas las
posiciones en la hoja Tse encuentran ocupadas por tomos de
silicio, mientras, que todas las posiciones de la capa O contienen
aluminio. sta es la frmula tpica de la pirofilita. Sin embargo, tal
y como se muestra en la figura 12, existen numerosas ramas en
el rbol de las arcillas, las cuales presentan la misma estructura
de sandwich, excepto que algunas veces el aluminio sustituye al
silicio parcialmente en la capa T, o bien el magnesio o el hierro
sustituyen al aluminio en la capa O, e inclusive el flor (F)
pudiera sustituir al oxgeno de la capa O. Luego, estas diferencias
de composicin qumica hacen que las propiedades de cada arcilla
mineral sean distintas.
Figura 12. El rbol de las esmectitas.
Entre todas las esmectitas, la rama de las arcillas di-
octadricas presenta propiedades muy interesantes,
derivadas por supuesto de su estructura laminar, de su
espacio interlaminar y de la carga residual. La figura 13
ilustra la composicin de las lminas T-O-T para todas las
arcillas del tipo esmectita, es decir, las lminas tipo 2:1.
Entre ellas destaca la montmorillonita, cuyo nombre se
deriva del francs Montmorillon, lugar de Francia en que se
encontr esta arcilla tpica en 1874. La composicin qumica
de una arcilla esmectita, tipo montmorillonita, es la
siguiente:
Como se observa en esta frmula estructural, la hoja
tetradrica est compuesta slo de silicio y aluminio mientras
que la hoja octadrica contiene aluminio y una variedad de
cationes (B). Esto ilustra perfectamente la gran variedad de
arcillas tipo esmectita que se pueden conseguir simplemente
cambiando el catin de la hoja octadrica y manteniendo
ocupada la hoja T con Si y Al (Figura 13), para cada caso. Por
supuesto, la sustitucin de aluminio (O) y silicio (T) por un
catin de menor carga elctrica, por ejemplo Mg, origina una
deficiencia de carga elctrica que es responsable de algunas de
las propiedades superficiales ms importantes de las arcillas: la
capacidad de intercambio, la absorcin de molculas polares
como el agua, as como de otros compuestos orgnicos, por
ejemplo las aminas, las cuales al introducirse en el espacio
interlaminar causan el hinchamiento de la estructura laminar de
las arcillas.
10.
11. Figura 13. La composicin de la lmina de T-O-T.
12. Debido a su avidez por el agua y las molculas
orgnicas las montmorillonitas encuentran aplicaciones muy
variadas que van desde la extraccin de esencias naturales
hasta la fabricacin de catalizadores para procesar los
hidrocarburos derivados del petrleo. Los mecanismos que
intervienen a escala molecular para llevar a cabo estas
reacciones sern explicados en los captulos siguientes, por
ahora slo mencionaremos que: la estructura de sandwich!
y el grado de sustitucin catinica determinan en gran
medida las propiedades de las arcillas.
13. Ms an, la sustitucin de cationes se lleva a cabo
mediante mecanismos muy sencillos. La figura 14 muestra
la frmula estructural de las arcillas tipo esmectita, en
donde podemos apreciar las sustituciones que se realizan en
las hojas de cada uno de los minerales.
Mineral Carga Composicin
(octa) (tetra) O
10
(OH)
2
Pirofilita ( E = 0 ) Al
2
Si
4
O
10
(OH)
2
Talco " Mg
3
Si
4
O
10
(OH)
2
Minnesotaita " (Fe, Mg)
3
Si
4
O
10
(OH)
2
Saponita
( E
+
=
0.33 )
Mg
3
(Si
3.6
, Al
.33
)
O
10
(OH)
2
nH
2
O
Saponita frrica "
(Fe
2+
, Mg)
3
(Si
3.6
, Al
.33
)
O
10
(OH)
2
nH
2
O
Hectorita "
(Mg
2.6
, Li
.33
)
Si
4
O
10
(OH)
2
nH
2
O
Sauconita "
(Mg, Zn)
3
(Si
3.6
, Al
.33
)
O
10
(OH)
2
nH
2
O
Stevensita
( 2E
+
=
2x )
Mg
3-x
Si
4
O
10
(OH)
2
Montmorillonita
( E
+
=
0.33 )
(Al
1.67
, Mg
.33
)
Si
4
O
10
(OH)
2
nH
2
O
Beidellita "
Al
2
(Si
3.6
, Al
.33
)
O
10
(OH)
2
nH
2
O
Nontronita "
Fe
2
3+
(Si
3.6
, Al
.33
)
O
10
(OH)
2
nH
2
O
Volkonskoita "
(Al, Fe
3+
, Cr)
2
(Si,
Al)
4
O
10
(OH)
2
nH
2
O
Figura 14. Arcillas esmectitas del grupo 2:1.
Frmula qumica.
14. Existe otra familia de arcillas que se asemeja a la de
las montmorillonitas: las vermiculitas, que tienen la misma
estructura de sandwich, pero que pueden presentar un
grado de sustitucin mayor en la hoja octadrica,
originando una carga residual mayor que las
montmorillonitas y, por eso mismo, la atraccin entre las
lminas es mayor tambin, por lo que la estructura no es
tan expansible.
15. 2) Las micas
16. Las micas son los minerales clasificados como arcillas
que tienen la misma estructura que las esmectitas, excepto
que el grado de sustitucin y la naturaleza de los cationes
que se alojan entre lminas, por ejemplo el potasio, hacen
que la carga residual sea muy alta. En estas condiciones,
las lminas se fijan unas a otras haciendo que su estructura
no sea expansible, ni sus cationes interlaminares
intercambiables. La familia de las micas se ilustra en la
figura 15 y la frmula estructural en la figura 16.
17.
Figura 15. El rbol de las micas.
Mineral Carga Frmula
Plogopita ( E
+
= 1 ) KMg
3
(Si
3
Al) O
10
(OH)
2
Biotita "
K (Mg, Fe
2+
, Fe
3+
,
Mn)
3
(Si
3
Al) O
10
(OH)
2
Lepidolita "
K (Al, Li)
3
(Si,
Al)
4
O
10
(OH)
2
Sinnwaldita "
K (Al, Li, Fe
2+
, Fe
3+
)
3
(Si,
Al)
4
O
10
(OH)
2
Muscovita " KAl
2
(Si
3
Al) O
10
(OH)
2
Paragonita " NaAl
2
(Si
3
Al) O
10
(OH)
2
Mica-Al ( E
+
= 1 )
K
x
(Al, Mg)
2
(Si,
Al)
4
O
10
(OH)
2
NH
2
O
Mica-Fe ( E
+
= 1 ) KMgFe
3+
Si
4
O
10
(OH)
2
Celadonita
Mica-Fe
(Glauconita)
K (R
1.3
3+
R
.67
2+
) (Si
3.6
Al
.33
)
O
10
(OH)
2
Figura 16. Micas, frmula qumica y formas
estructurales.
El lector recordar la facilidad con la que la mica comn se parte
a lo largo de las hojas que la componen, pero, qu difcil es
partirla en la direccin perpendicular! no es as? Esto ilustra
perfectamente la constitucin laminar de tales minerales.
Adems, conociendo la estructura podemos explicarnos fcilmente
por qu las micas son buenos alsiantes trmicos, por ejemplo en
las planchas elctricas y en las conexiones: debido al espacio
interlaminar, el cual no es un buen conductor trmico o elctrico
(las hojas se encuentran "desconectadas" unas de otras, lo que
impide el paso del fluido trmico o elctrico).
En contraste con la montmorillonita, la cual tiene una
deficiencia de carga localizada en el centro de los octaedros, la
carga residual de las micas est localizada en la hoja
tetradrica, es decir, en la superficie misma de las hojas,
originando un amarre fuerte de los cationes interlaminares con
las hojas, por lo que la estructura no es fcilmente expansible.
Entre las micas ms conocidas se encuentran la muscovita,
cuyo nombre deriva del "vidrio de Mosc", con el que se
fabricaban antiguamente las ventanas de las casas de esa
ciudad.
En resumen, las arcillas expansibles son las esmectitas, las
vermiculitas y las haloisitas, que derivan esta propiedad de la
concentracin de carga interlaminar, por ejemplo de 0.33
unidades por cada celda unitaria, mientras que sta es igual a
0.86 en las vermiculitas y 1.0 en las muscovitas.
La figura 17 muestra los distintos espesores que se obtienen
con las distintas arcillas al intercalarse una o dos capas de
agua en el espacio interlaminar:
a) Pirofilita cationes octadricos
b) Mica
o cationes
intercambiables
c) Esmectita
w capas de
molculas
d) Vermiculita
e) Clorita OH
f) Caolinita-
serpentina
K ion de potasio
g) Haloisita (10A)
Una cosa queda clara: los edificios moleculares que constituyen a
las arcillas y el grado de sustitucin logrado, permiten obtener
una serie de propiedades de inters en diversos campos de
aplicacin. No slo esto es cierto cuando interviene la mano del
hombre al tratar de modificar el espacio interlaminar (Figura 17),
sino que el proceso de modificacin a travs del intercambio con
otras especies qumicas ocurre naturalmente, lo que conduce a
una variacin constante de la naturaleza de la arcilla que se
traduce en variaciones de la fertilidad del suelo, permeabilidad,
etc. Estas modificaciones del edificio molecular son susceptibles
de estudiarse experimentalmente en el laboratorio y para ello es
necesario introducir, ya sea un catin, ya sea una especie qumica
distinta, en el interior del espacio interlaminar, lo cual ser el
tema que abordaremos enseguida.
Figura 17. El espesor de las arcillas expandidas.
También podría gustarte
- Balance Con ReacciónDocumento5 páginasBalance Con ReacciónAna Lucía Aguilar ChávezAún no hay calificaciones
- Documentos AuditoriaDocumento3 páginasDocumentos AuditoriaAna Lucía Aguilar ChávezAún no hay calificaciones
- EXPO Técnicas Analíticas Determinación de Parámetros F-QDocumento35 páginasEXPO Técnicas Analíticas Determinación de Parámetros F-QAna Lucía Aguilar ChávezAún no hay calificaciones
- Lab BalanceDocumento17 páginasLab BalanceAna Lucía Aguilar Chávez100% (1)
- NTP 898 Ohsas 18001Documento8 páginasNTP 898 Ohsas 18001ares950hotmailcomAún no hay calificaciones
- CerroverdeDocumento20 páginasCerroverdeAna Lucía Aguilar ChávezAún no hay calificaciones
- Diseño ExperimentalDocumento24 páginasDiseño ExperimentalAna Lucía Aguilar ChávezAún no hay calificaciones
- Experimento en La AgriculturaDocumento355 páginasExperimento en La AgriculturaILIANAAún no hay calificaciones
- Corindón AndreaDocumento1 páginaCorindón AndreaAna Lucía Aguilar ChávezAún no hay calificaciones
- Realismo literario: características y representantesDocumento11 páginasRealismo literario: características y representantesAna Lucía Aguilar ChávezAún no hay calificaciones
- Industria Del Petróleo y GasDocumento11 páginasIndustria Del Petróleo y GasAna Lucía Aguilar ChávezAún no hay calificaciones
- Tricloro CentrigugaDocumento17 páginasTricloro CentrigugaAna Lucía Aguilar ChávezAún no hay calificaciones
- Industria Del Petróleo y GasDocumento11 páginasIndustria Del Petróleo y GasAna Lucía Aguilar ChávezAún no hay calificaciones
- TrabajoDocumento22 páginasTrabajoAna Lucía Aguilar ChávezAún no hay calificaciones
- Taller Numero 4 y 5Documento8 páginasTaller Numero 4 y 5Ana Lucía Aguilar ChávezAún no hay calificaciones
- Taller n02Documento5 páginasTaller n02Ana Lucía Aguilar ChávezAún no hay calificaciones
- Manual de Seguridad en Laboratorios Químicos. SIDocumento128 páginasManual de Seguridad en Laboratorios Químicos. SIelenasan80Aún no hay calificaciones
- CerroverdeDocumento20 páginasCerroverdeAna Lucía Aguilar ChávezAún no hay calificaciones
- Auditoría Ambiental Del LaboratorioDocumento18 páginasAuditoría Ambiental Del LaboratorioAna Lucía Aguilar ChávezAún no hay calificaciones
- Capitulo2 - Gerencia 2Documento54 páginasCapitulo2 - Gerencia 2Alejandra VeraAún no hay calificaciones
- Lista de Chequeo Ohsas 18001Documento20 páginasLista de Chequeo Ohsas 18001kelymuoz100% (2)
- ECA y LMPDocumento2 páginasECA y LMPAna Lucía Aguilar ChávezAún no hay calificaciones
- Procesos Lineales y Variables de DesviaciónDocumento4 páginasProcesos Lineales y Variables de DesviaciónAna Lucía Aguilar ChávezAún no hay calificaciones
- Cristalizacion EstructurasDocumento2 páginasCristalizacion EstructurasAna Lucía Aguilar ChávezAún no hay calificaciones
- Receta de La Mermelada de YaconDocumento3 páginasReceta de La Mermelada de YaconAna Lucía Aguilar ChávezAún no hay calificaciones
- Gerencia 2 Unsa-Capitulo 4,5,6Documento43 páginasGerencia 2 Unsa-Capitulo 4,5,6Ana Lucía Aguilar ChávezAún no hay calificaciones
- Dpi Cap 1 y 2Documento49 páginasDpi Cap 1 y 2Ana Lucía Aguilar ChávezAún no hay calificaciones
- Realismo literario enDocumento11 páginasRealismo literario enAna Lucía Aguilar ChávezAún no hay calificaciones
- Unidad #1 y 2 Aspectos Conceptuales de Empresa, Promocvion Empresarial GERENCIA 1Documento61 páginasUnidad #1 y 2 Aspectos Conceptuales de Empresa, Promocvion Empresarial GERENCIA 1Ana Lucía Aguilar ChávezAún no hay calificaciones
- COMPARACIÓN DE SISTEMAS CONSTRUCTIVOSDocumento140 páginasCOMPARACIÓN DE SISTEMAS CONSTRUCTIVOSJavier Alejandro AyalaAún no hay calificaciones
- Plan de Inicio de Gestion Kenneth Lee PDFDocumento58 páginasPlan de Inicio de Gestion Kenneth Lee PDFYumy VelásquezAún no hay calificaciones
- Utencilios de CocinaDocumento4 páginasUtencilios de CocinaCristian DominguezAún no hay calificaciones
- Juntas dinámicas y uniones para procesos asépticosDocumento15 páginasJuntas dinámicas y uniones para procesos asépticosLilia YacomoskyAún no hay calificaciones
- Catalogo IlumedicaDocumento2 páginasCatalogo IlumedicaSebastián Valencia100% (1)
- Cuestionarios Sobre La MadurezDocumento9 páginasCuestionarios Sobre La MadurezCindySantana1103Aún no hay calificaciones
- 101 Mitos de La Biblia - Gary GreenbergDocumento187 páginas101 Mitos de La Biblia - Gary GreenbergSilvio Martin100% (13)
- Auges Del EcuadorDocumento11 páginasAuges Del EcuadorCustodio PaolaAún no hay calificaciones
- Sistema productivo de Nicomar Electronics y su marca PowestDocumento13 páginasSistema productivo de Nicomar Electronics y su marca PowestJENNIFER PAOLA MU�OZ DUQUEAún no hay calificaciones
- Basura y Pelicano Feb 2023Documento7 páginasBasura y Pelicano Feb 2023Jesus MoralesAún no hay calificaciones
- Conductos en C: anatomía, clasificación y tratamientoDocumento94 páginasConductos en C: anatomía, clasificación y tratamientodjcAún no hay calificaciones
- Roca William - Cultivo de Tejidos en La Agricultura (2007)Documento960 páginasRoca William - Cultivo de Tejidos en La Agricultura (2007)Javier Solana CampoyAún no hay calificaciones
- Albeitar198 El Huevo Del FuturoDocumento44 páginasAlbeitar198 El Huevo Del FuturoINCOGNITO AudioboxAún no hay calificaciones
- Diseño caída vertical canalDocumento8 páginasDiseño caída vertical canalJose GuevaraAún no hay calificaciones
- Aplicación de Un Circuito Eléctrico Conectado en Serie Del Tipo RC y RLDocumento38 páginasAplicación de Un Circuito Eléctrico Conectado en Serie Del Tipo RC y RLdiego sebastianAún no hay calificaciones
- Altiplano y ValleDocumento5 páginasAltiplano y ValleJosé Luis PérezAún no hay calificaciones
- 01 Escorrentia SuperficialDocumento22 páginas01 Escorrentia Superficialdavid aguilar gutierrezAún no hay calificaciones
- Preguntero 1er Parcial Grupo y Liderazgo UESIGLO 21 Año 2017Documento13 páginasPreguntero 1er Parcial Grupo y Liderazgo UESIGLO 21 Año 2017ceciliaAún no hay calificaciones
- Arquitectura de La Impresora Láser Evidencia NoDocumento8 páginasArquitectura de La Impresora Láser Evidencia Nojonathan40056Aún no hay calificaciones
- Composición Corporal PediátricaDocumento17 páginasComposición Corporal PediátricaXimena TobarAún no hay calificaciones
- Las Poleas Son Mecanismos Capaces de Transmitir Fuerza y MoDocumento4 páginasLas Poleas Son Mecanismos Capaces de Transmitir Fuerza y MoedutecnoAún no hay calificaciones
- Los Mandamientos Del Abogado Eduardo J CoutureDocumento61 páginasLos Mandamientos Del Abogado Eduardo J CoutureCarla Francisca Fuentes GonzalezAún no hay calificaciones
- Grupo NutresaDocumento2 páginasGrupo NutresaLeidy Maritza MORA SUAREZAún no hay calificaciones
- Taller Evaluativo Áreas de Figuras PlanasDocumento1 páginaTaller Evaluativo Áreas de Figuras PlanasRodrigoAún no hay calificaciones
- Eval Diagn - 4°-DpccDocumento4 páginasEval Diagn - 4°-DpccCELIA ANGELITA HERNANDEZ VASQUEZAún no hay calificaciones
- COCHURADODocumento4 páginasCOCHURADOVaneAún no hay calificaciones
- Manual Del Rio V-Star 650 2001Documento104 páginasManual Del Rio V-Star 650 2001paco_leon_698618100% (2)
- PDF Gaita Zuliana Taller - CompressDocumento20 páginasPDF Gaita Zuliana Taller - CompressAngel Benicio MontielAún no hay calificaciones
- 8 Formas de Utilizar El Agua BenditaDocumento3 páginas8 Formas de Utilizar El Agua BenditaLAURAAún no hay calificaciones
- Palabras en CoreanoDocumento3 páginasPalabras en CoreanoAlex Varon PolyglotAún no hay calificaciones