Documentos de Académico
Documentos de Profesional
Documentos de Cultura
MODULO 005 QUÍMICA Primer Año
Cargado por
PAUL ALEGRETítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
MODULO 005 QUÍMICA Primer Año
Cargado por
PAUL ALEGRECopyright:
Formatos disponibles
I. E. P. D.
SANTA ROSA DE LIMA
Qumica
1 ao
2012
PRF. QUEZADA AMAYA MARILYN
Apellidos y Nombres : Fecha : // 12 Grado : I Seccin :Nivel : Secundaria Bimestre : II Prof. Marilyn Quezada Amaya
I.
INDICADORES DE LOS APRENDIZAJES:
1. Explica los principales postulados de los modelos atmicos de Bohr, Somerfeld y actual. 2. Compara los modelos atmicos de Bohr y Sommerfeld. 3. Emiten juicios acerca de los postulados del modelo mecnico ondulatorio del tomo.
II.
DESARROLLO TEMTICO CAPACIDADES:
EL MODELO DE BOHR Y LA ESTRUCTURA ELECTRNICA. El modelo de Bohr, publicado en 1913, se basa en una hiptesis que desarroll Max Planck. Se resume manifestando que la energa no puede variar en cualquier cantidad. La cantidad de energa se modifica variando su valor en cantidades determinadas, que reciben el nombre de cuantos de energa. La teora de Bohr es vlida para tomos que slo tienen un electrn, como el hidrgeno. El trabajo de Bohr puede considerarse como el inicio de la bsqueda de informacin relacionada con el comportamiento de los electrones en los tomos. El modelo de Bohr no modifica el modelo de Rutherford. Sus principales innovaciones residen en la explicacin de cmo se disponen los electrones y son los siguientes:
Los electrones giran alrededor del ncleo, pero no siguen una rbita fija. Cada una de estas zonas est caracterizada por un valor de energa, llamado nivel de energa. El valor de la energa de cada nivel es caracterstico de cada tomo y no puede tomar cualquier valor. En cada nivel de energa slo puede existir un nmero limitado de electrones. Los electrones pueden absorber energa para saltar a otra capa que tenga espacios disponibles. En este caso, el electrn tiene ms energa y se dice que est excitado. Un electrn excitado puede volver a su lugar inicial emitiendo energa de un nivel superior a un nivel inferior.
2. MODELO ATMICO DE BOHR - SOMMERFELD.- Sommerfeld modific el modelo de Bohr especificando que el electrn se mueve en rbitas elpticas, siendo las rbitas circulares simplemente un caso especial de rbitas elpticas. Introdujo un nuevo concepto: El desdoblamiento de cada nivel de energa en subniveles de energa.
I. E. P. D. SANTA ROSA DE LIMA
Qumica
1 ao
2012
PRF. QUEZADA AMAYA MARILYN
3. MODELO ATMICO ACTUAL. El austriaco Edwin Schrodinger en 1926, sustento el modelo atmico actual. Diseo un modelo matemtico para el tomo, y manifest que no se puede describir con exactitud la posicin del electrn como lo establece el modelo de Borh, si no que matemticamente se puede calcular la regin del espacio donde debe encontrarse el electrn. A esta regin del espacio se le llama Orbital, por lo tanto, el electrn no circula por una orbita, si no que se mueve ondulatoriamente alrededor del ncleo en una regin del espacio atmico denominado orbital produciendo una nube elctrica.
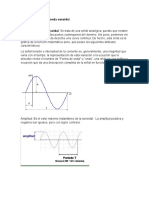
3.1 POSTULADOS DEL MODELO MECANICO ONDULATORIO DEL ATOMO 1. Niveles Estacionarios de Energa (Bohr). 2. Dualidad de la materia de Luis De Broglie (1924). La materia al igual que la energa, presenta un carcter dualstico de onda - corpsculo. Es decir, la luz presenta un comportamiento ondulatorio (en el que se considerar que es una onda con una frecuencia y una longitud de onda caractersticas) o bien un comportamiento corpuscular (en el que se considerar que es un chorro de fotones de energa: E h . f ). Esto significa que toda partcula en movimiento lleva asociada una onda, de modo que la longitud de onda () de la onda asociada est relacionada con la velocidad () de la partcula mediante la siguiente expresin:
I. E. P. D. SANTA ROSA DE LIMA
Qumica
1 ao
2012
PRF. QUEZADA AMAYA MARILYN
3. Principio de Incertidumbre de Heinsemberg (1926). Es imposible conocer con exactitud y al mismo tiempo, la velocidad y posicin del electrn. Slo se puede hablar de una probabilidad de hallar el electrn en cierta regin del espacio atmico. Las zonas de probabilidad ocupadas por el electrn se llama REEMPE (orbital). 4. Pauli establece que cada orbital (REEMPE) puede contener un mximo de dos electrones que debern tener giros opuestos. 5. Ecuacin de Onda de Schrdinger. Formula una ecuacin que describe el comportamiento y la energa de partculas submicroscpicas en general. Esta ecuacin requiere clculos avanzados que escapan al contenido de la asignatura. Pero podemos advertir que la solucin a esta ecuacin, nos proporciona tres variables llamados parmetros cunticos: n, l y m. 6. Ecuacin de onda de Dirac y Jordan complementaron la ecuacin de onda de Schrdinger incorporando la teora general de la relatividad de Einstein a la mecnica cuntica, encontrndose un cuarto parmetro: s ( parmetro cuntico spin). 7. Cuando se aplica un campo magntico al espectro del hidrgeno, las lneas espectrales se desdoblan dando lugar a un espectro muy diferente al que aparece sin presencia del campo. Este fenmeno se denomina efecto Zeeman. Estas nuevas lneas (ms finas), se relacionan con las rbitas elpticas de Sommerfeld y a su vez con la presencia de subniveles.
III. 3.1
EVALUANDO LOS APRENDIZAJES:
REACTIVOS DE CLASE
1. Qu diferencia encuentras entre el modelo atmico de Borh y el modelo atmico actual. 2. En qu modelo atmico los electrones se mueven en rbitas elpticas? 3. Quin introdujo los niveles de energa en su modelo atmico? a) Borh a) rbita b) Sommerfeld b) niveles de energa c) Schrodinger c) subnivel de energa d) Dalton d) orbital e) N.A e) Fotn 4. La regin del espacio donde hay la probabilidad de hallar un electrn se denomina: 5. Cul ser la longitud de onda asociada a un cuerpo de 0,50 kg de masa que se mueve con una velocidad de 20 m/s?. 6. La masa de un electrn es 9,11 x 10 velocidad es 6,12 x 108 cm/s?.
28
g. Cul es la longitud de onda de un electrn si la
I. E. P. D. SANTA ROSA DE LIMA
Qumica
1 ao
2012
PRF. QUEZADA AMAYA MARILYN
7. Cul ser la masa de una partcula si su longitud de onda es de 3,315 x 10 35 m y se mueve con una velocidad de 15 m/s?.
3.3 ACTIVIDAD DE EXTENSIN 1. Segn Bohr, los electrones tienen el siguiente comportamiento: A. Pueden alcanzar niveles de energa ms altos. B. No siguen una rbita fija. C. Es vlida slo para el tomo de Hidrgeno. D. Los electrones caen a niveles ms bajos de energa por la emisin de energa. E. Todas las anteriores 2. De las siguientes proposiciones: - La nube electrnica posee carga elctrica negativa. - Todos los orbitales tienen la misma forma. - Un electrn excitado puede volver a su posicin inicial. - Segn Borh los electrones pueden ganar o perder energa Cuantas son correctas: A) 0 B) 1 C) 2 D) 3 3. Respecto al modelo atmico actual se afirma que: A. Los niveles de energa se desdoblan en subniveles. B. El electrn se mueve ondulatoriamente alrededor del ncleo. C. Los electrones forman campos magnticos iguales. D. Es similar al sistema planetario solar. E. N.A 4. Una esfera de 4 kg de masa se mueve con una velocidad constante de 25 km/h. Calcula la longitud de onda asociada a dicha esfera. 5. Una esfera de 1 kg de masa se mueve con una velocidad constante de 50 km/h. Calcula la longitud de onda asociada a dicha esfera. PARTCULAS ELEMENTALES Cuando se descubri el neutrn, se pens que ya se tenan todos los constituyentes elementales de la materia. stos seran cuatro: el electrn, el neutrn, el protn y el fotn. Con ello era posible construir todos los tomos que forman la materia ordinaria, as como la energa que desprenden o absorben cuando hay cambios de energa. En la dcada de los sesenta, del siglo pasado, surgi la idea de que quizs algunas de las partculas elementales conocidas hasta el momento no eran tales, sino que podan estar formadas de otras ms pequeas y, por tanto, ms elementales. La primera evidencia experimental de ello se logr al hacer chocar electrones contra protones en equipos conocidos como aceleradores de partculas. A partir de entonces, toda una serie de trabajos mostr que la materia est constituida por partculas realmente elementales y absolutamente indivisibles: los quarks.
E) 4
REFLEXIN METACOGNITIVA
Describe detalladamente el momento de la clase, en el que te sentiste mejor aprendiendo
Crees que en el proceso de aprendizaje de hoy hiciste todo lo necesario por aprender ( sustenta tu repuesta)
I. E. P. D. SANTA ROSA DE LIMA
Qumica
1 ao
2012
PRF. QUEZADA AMAYA MARILYN
También podría gustarte
- Composición Porcentual o Determinación de PorcentajesDocumento4 páginasComposición Porcentual o Determinación de PorcentajesPAUL ALEGRE100% (1)
- III BIM - QUIM - 1ER AÑO - GUIA #4 - Modelo Atómico IIDocumento6 páginasIII BIM - QUIM - 1ER AÑO - GUIA #4 - Modelo Atómico IILeonardoctavioAún no hay calificaciones
- Examen 1 Onb 2014 Mundo MejorDocumento16 páginasExamen 1 Onb 2014 Mundo MejorPAUL ALEGREAún no hay calificaciones
- El FrutoDocumento12 páginasEl FrutoPAUL ALEGREAún no hay calificaciones
- Examen 02 de CelulaDocumento4 páginasExamen 02 de CelulaPAUL ALEGREAún no hay calificaciones
- MODULO 001 QUÍMICA Primer Año MARILYNDocumento5 páginasMODULO 001 QUÍMICA Primer Año MARILYNPAUL ALEGREAún no hay calificaciones
- 010 QUÍMICA Primer Año MARILYNDocumento4 páginas010 QUÍMICA Primer Año MARILYNPAUL ALEGREAún no hay calificaciones
- FIX Office 2010Documento1 páginaFIX Office 2010PAUL ALEGREAún no hay calificaciones
- 011 QUÍMICA Primer Año MARILYNDocumento3 páginas011 QUÍMICA Primer Año MARILYNPAUL ALEGREAún no hay calificaciones
- 1º Seminario de Trigonometría preuniversitario-2006-ISaraDocumento20 páginas1º Seminario de Trigonometría preuniversitario-2006-ISaraPAUL ALEGRE100% (1)
- Alquenos SaludDocumento2 páginasAlquenos SaludPAUL ALEGREAún no hay calificaciones
- Solucionario Aptitud Academica y Cultura General - Admision UNI 2011-2 - PamerDocumento45 páginasSolucionario Aptitud Academica y Cultura General - Admision UNI 2011-2 - PamerRubensaiDAún no hay calificaciones
- Informe N°05 - Velocidad Del Sonido - Panduro Marina, SoreyDocumento9 páginasInforme N°05 - Velocidad Del Sonido - Panduro Marina, SoreySOREY SOLANGE PANDURO MARINAAún no hay calificaciones
- 5 Fis Tema 5 Fenómenos OndulatoriosDocumento21 páginas5 Fis Tema 5 Fenómenos OndulatoriosMOISESAún no hay calificaciones
- Clasificasion de Los Modelos Hidrologicos PDFDocumento12 páginasClasificasion de Los Modelos Hidrologicos PDFRigoberot Ruiz SanchezAún no hay calificaciones
- ParónimosDocumento31 páginasParónimosQuique Gonzalez100% (1)
- Acontecimiento SonoraDocumento2 páginasAcontecimiento SonoraOswaldo ChoAún no hay calificaciones
- Area FisicaDocumento7 páginasArea FisicaMayerli MonroyAún no hay calificaciones
- Descarga de Un Colector de Aguas Lluvias A Un Cauce Natural PDFDocumento109 páginasDescarga de Un Colector de Aguas Lluvias A Un Cauce Natural PDFRodrigo PradenaAún no hay calificaciones
- Estandarés Básicos de Competencias - Ciencias NaturalesDocumento32 páginasEstandarés Básicos de Competencias - Ciencias NaturalesGustavo CardonaAún no hay calificaciones
- Características de La Onda SenoidalDocumento3 páginasCaracterísticas de La Onda SenoidalZedei Antonio100% (2)
- Temario Semestral UNI 2024-IDocumento9 páginasTemario Semestral UNI 2024-IIsael Bautista FernándezAún no hay calificaciones
- Espectometria SWIRDocumento26 páginasEspectometria SWIRFernando Velasquez DiazAún no hay calificaciones
- 20111sicf006952 1Documento6 páginas20111sicf006952 1GabyValladolidAún no hay calificaciones
- Secuencia Didactica de OndasDocumento10 páginasSecuencia Didactica de OndasLuis castroAún no hay calificaciones
- Patron de Radiacion en Dos DimencionesDocumento102 páginasPatron de Radiacion en Dos DimencionesClaudio Andrés Matamoros PicadoAún no hay calificaciones
- 4 Física I Fj2022Documento124 páginas4 Física I Fj2022Debanhi Paola Macías TorresAún no hay calificaciones
- Peligro SismicoDocumento33 páginasPeligro SismicoRobert Javier Vilca ValverdeAún no hay calificaciones
- S. Safina, Incorporación de Los Efectos de La Interacción SuDocumento28 páginasS. Safina, Incorporación de Los Efectos de La Interacción SuricardobonillaAún no hay calificaciones
- Tema 2: Estructura Atómica Y Clasificación Periódica de Los ElementosDocumento35 páginasTema 2: Estructura Atómica Y Clasificación Periódica de Los ElementosVíctor Manuel Pérez RomeroAún no hay calificaciones
- El Cerebro HolográficoDocumento2 páginasEl Cerebro Holográficojorge osco100% (1)
- Glosario SismosDocumento5 páginasGlosario SismosMiguel Alexis NuñezAún no hay calificaciones
- Generador de Señal Lab 12 ArduinoDocumento15 páginasGenerador de Señal Lab 12 ArduinoErwin RojasAún no hay calificaciones
- Monitoreo de RuidoDocumento120 páginasMonitoreo de RuidoDarik Hossein Marcatoma0% (1)
- 001 Aislamiento CIP v1Documento88 páginas001 Aislamiento CIP v1Juan Alex Carpio CabreraAún no hay calificaciones
- 30882f - UMSS - Problemas de Olimpiada OBF - OBAA Fase Departamental 1ra Ed PDFDocumento143 páginas30882f - UMSS - Problemas de Olimpiada OBF - OBAA Fase Departamental 1ra Ed PDFHugo FloresAún no hay calificaciones
- 2013 1 235 Sin EnunciadohhDocumento89 páginas2013 1 235 Sin EnunciadohhgorkantolinprraAún no hay calificaciones
- Preguntas Saber SimulacroDocumento9 páginasPreguntas Saber SimulacroTomasERodriguezRomeroAún no hay calificaciones
- Lab N2 - Física 2 PDFDocumento3 páginasLab N2 - Física 2 PDFalexander duque roaAún no hay calificaciones
- Act 13 ElectromagnetismoDocumento5 páginasAct 13 ElectromagnetismoLuisa VergaraAún no hay calificaciones
- Interconexión de Radios de VHF Con Plantas Telefónicas IPDocumento116 páginasInterconexión de Radios de VHF Con Plantas Telefónicas IPFidel Atahuichi TorrezAún no hay calificaciones