Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Derivados de Las Aminas
Cargado por
Jackson Huayta EnriquezDescripción original:
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Derivados de Las Aminas
Cargado por
Jackson Huayta EnriquezCopyright:
Formatos disponibles
DERIVADOS DE LAS AMINAS: AMIDAS
I. INTRODUCCION La acetanilida por si misma es un analgsico, pero no es un frmaco til pues ocasiona daos hepticos cuando se toma durante un periodo de tiempo prolongado. De hecho, otro compuesto que puede obtenerse a partir de la acetanilida, la 4-bromoacetanilida, es a este respecto un analgsico mucho mejor. En este laboratorio prepararemos una amida a partir de una amina y un anhdrido, debemos tener presente que las aminas primarias y secundarias reaccionan con los anhdridos de acido o haluros de cidos formando amidas. Algunas de estas amidas se preparan por deshidratacin de las sales correspondientes. La acilacion de grupos amino se hace frecuentemente para protegerlos en forma adecuada.
1 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
II.
OBJETIVOS Sntesis de la acetalidina Importancia del grupo protector presente en la acetalidina
2 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
III.
PROCEDIMIENTO 1. En un baln adicionar 1 ml de de anilina, luego adicionar 3 ml de anhdrido actico, y calentar por unos minutos a reflujo. 2. Enfriar, adicionar 5 ml de agua y seguir con el calentamiento, enfriar y observar si se forman cristales. (Si no se observan cristales adicionar 5 ml mas de agua helada, y raspar las paredes con al bageta). Recristalizar a partir del agua, secar los cristales.
3 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
IV.
MECANISMO 1. Reaccin Global
2. Mecanismo
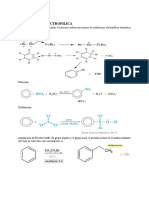
Resonancia del anhdrido actico
El anhdrido actico reacciona con la anilina
*Por transferencia de protones nos de los siguientes productos
4 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
V.
RESULTADOS
93.13 g/mol 1 ml
102,1 g/mol 3 ml
135,17 g/mol
60.05 g/mol
1. Conversin de volumen en masa
*Para la anilina
*Para el anhdrido actico
2. Reactivo limitante reactivo en exceso *Para el anhdrido actico
*Para la anilina
Reactivo exceso
5 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
3. Hallaremos la masa terica
93.13 g/mol
102,1 g/mol 3.24g
135,17 g/mol Xg
60.05 g/mol
4. Rendimiento
6 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
VI.
DISCUSIONES Un grupo amino es un activante fuerte, que orienta a las posiciones orto y para en las reacciones de sustitucin electrofilica aromtica. Esta alta reactividad en ocasiones se puede convertir en una desventaja debido a que con frecuencia dificulta prevenir la polisustitucion, en consecuencia yo no pueda detener la reaccin en cierta etapa. Esto lo puedo observara claramente en la bromacion de anilina la cual me dar una tribromoanilina y no una monobromoanilina. Otra desventaja respecto al uso de los bencenos sustituidos con grupos amino en las reacciones de sustitucin electrofilica aromtica es que las reacciones de acido-base son el catalizador AlCl3 el cual previene que ocurra la reaccin posterior. El tratamiento de una amina con anhdrido actico, produce la acetil amida correspondiente, o acetamida. Aunque los sustituyentes amido (-NHCOR) siguen siendo activantes para y orto orientadores, son activantes menos fuertes y menos bsicos que los grupos amino debido a que el par de electrones no enlazado del nitrgeno esta deslocalizado por el grupo carbonilo vecino.
7 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
VII.
CONCLUSIONES Se sntesis la acetanilida cuidando de que ebullan la anilina con el anhdrido actico en un ambiente SIN AGUA debido a la presencia del anhdrido Observamos la importancia de proteger la amida sintetizada para que al nitrarlo en nuestro siguiente laboratorio no nos de varios productos y nuestro rendimiento sea bajo
8 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
VIII.
CUESTIONARIO 1. Menciona tres reactivos que pueden ser utilizados para la acetilacin de aminas. Las aminas pueden ser aciladas de varios modos. Entre estos, est el uso de anhdrido actico, cloruro de acetilo o cido actico glacial. El procedimiento con cido actico glacial es de inters comercial porque es econmico. Sin embargo, requiere calentar por mucho tiempo. Cloruro de acetilo no es recomendable por varias rezones. Principalmente, reacciona vigorosamente liberando HCl; esto convierte la mitad de la amina a su sal de hidrocloruro tornndola incapaz de participar en la reaccin. Anhdrido actico es el mtodo preferido para sntesis en el laboratorio y es el mtodo que se utiliza en este experimento. Su velocidad de hidrlisis (reaccin con agua) es lo suficientemente bajo como para permitir que la acetilacin de aminas se pueda llevar a cabo en soluciones acuosas. El procedimiento da un producto de gran pureza y de alto rendimiento, pero no es til para desactivar aminas (bases dbiles) tales como las orto y para-nitroanilinas. 2. En la preparacin de p-nitroanilina, por que la anilina se debe convertir en acetanilida antes de al nitracin. La anilina en una amina muy reactivo frente a al ataque electrofilico, que la utilizacin de electrolitos poderosos, como las mezclas de cidos ntrico y sulfrico, halgenos, y reactivos de Friedel-Crafts, conduce a la polisustitucion, o la formacin de mezclas intratables. Sin embargo, la acetanilida, en contraste con la anilina o las anilinas N-alquiladas, puede nitrarse y bromarse, en condiciones suaves y fcilmente controlables, a p-nitro y p-bromoacetanilida.
9 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
IX.
BIBLIOGRAFIA H. D. Durst/ G. W. Gokel, Qumica Orgnica Experimental, 2007, Editorial Reverte, Espaa, Pg. 227, Solano Oria, Practicas De Laboratorio de Qumica Orgnica, 1991, Editorial Sucesores de Nogues, Espaa, Practica n20 Pg. 163, John Mc Murry, Qumica Orgnica, 2008, 7 edicin, Editorial Edamsa, Mxico, pg. 939-940 Harry Alices-Villanueva, Universidad Interamericana de Puerto Rico, Laboratorio de Qumica Orgnica III, Experimento 6: Sntesis de Acetanilida, T.A. Geissman, Principios de Qumica Orgnica, 1974, Editorial Reverte, Segunda Edicin, pg. 630, , Espaa
10 UNFV/Escuela de Qumica/Laboratorio de Orgnica III/Laboratorio N4
También podría gustarte
- Energia solar térmica: Técnicas para su aprovechamientoDe EverandEnergia solar térmica: Técnicas para su aprovechamientoCalificación: 2.5 de 5 estrellas2.5/5 (3)
- Química de macrocomponentes de alimentosDe EverandQuímica de macrocomponentes de alimentosAún no hay calificaciones
- Practica 5 OrganicaDocumento2 páginasPractica 5 OrganicaHilda HMAún no hay calificaciones
- Informe 10Documento8 páginasInforme 10LiziQuimisPonceAún no hay calificaciones
- Trabajo Colaborativo Practica 7Documento6 páginasTrabajo Colaborativo Practica 7GABRIELA VILLACISAún no hay calificaciones
- Síntesis de la acetanilida a partir de la anilina mediante acetilaciónDocumento2 páginasSíntesis de la acetanilida a partir de la anilina mediante acetilaciónaprolabgpAún no hay calificaciones
- Informe de Laboratorio Practica 2Documento6 páginasInforme de Laboratorio Practica 2jeffersonAún no hay calificaciones
- Práctica N10Documento8 páginasPráctica N10Sial Lual50% (2)
- SÍNTESIS DE ÉSTERES POR REACCIÓN DE WILLIAMSONDocumento14 páginasSÍNTESIS DE ÉSTERES POR REACCIÓN DE WILLIAMSONMaría Fernanda Carmona MartínezAún no hay calificaciones
- Grupos FuncionalesDocumento13 páginasGrupos FuncionalesDaniela RomeroAún no hay calificaciones
- Obtención p-nitroanilinaDocumento7 páginasObtención p-nitroanilinaLiLiana Niño100% (1)
- Informe de Práctica Nro 4 Química OrgánicaDocumento9 páginasInforme de Práctica Nro 4 Química OrgánicaKaroline FloriánAún no hay calificaciones
- ACILACIONDocumento6 páginasACILACIONMorocha BellaAún no hay calificaciones
- Quimica Organia LL Practica P NitroanilinaDocumento13 páginasQuimica Organia LL Practica P NitroanilinaCharlie ReyesAún no hay calificaciones
- Practica 6Documento5 páginasPractica 6Carlos CastilloAún no hay calificaciones
- Síntesis de ParacetamolDocumento8 páginasSíntesis de ParacetamolKikin LR0% (1)
- Practica 7 de QuimicaDocumento2 páginasPractica 7 de QuimicaAlex Rey0% (1)
- PRACTICA #10 ChanzapaDocumento9 páginasPRACTICA #10 ChanzapaGABY GAMES YTAún no hay calificaciones
- Practica de Síntesis de La ACETANILlDA MAY 19Documento5 páginasPractica de Síntesis de La ACETANILlDA MAY 19AntonioAún no hay calificaciones
- 200 años de independencia peruanaDocumento7 páginas200 años de independencia peruanabetsy cadena tenorio100% (1)
- Sales de DiazonioDocumento7 páginasSales de DiazonioDeysiCarolinaAún no hay calificaciones
- Síntesis de Williamson y propiedades del fenetolDocumento6 páginasSíntesis de Williamson y propiedades del fenetolJavier BarraganAún no hay calificaciones
- Intr. InformeDocumento2 páginasIntr. InformeGabriela OjedaAún no hay calificaciones
- Sintesis de La Anilina A Partir de La AcetanilidaDocumento16 páginasSintesis de La Anilina A Partir de La AcetanilidaTatiana DelesmaAún no hay calificaciones
- Informe Química Orgánica II Síntesis de AcetanilidaDocumento19 páginasInforme Química Orgánica II Síntesis de AcetanilidaJeannette Capa Villar60% (10)
- 4iv52 - Equipo 2 - Obtención de AnilinaDocumento23 páginas4iv52 - Equipo 2 - Obtención de AnilinaEnrique Flores OlivaresAún no hay calificaciones
- INFORME 7 UMSS Lab Química Orgánica 2Documento14 páginasINFORME 7 UMSS Lab Química Orgánica 2Julio RodrigoAún no hay calificaciones
- Sintesis en Varias EtapasDocumento5 páginasSintesis en Varias EtapasKATHERINE LISET ORTIZ PATERNINA ESTUDIANTE ACTIVOAún no hay calificaciones
- Informe de Aminas 1Documento17 páginasInforme de Aminas 1Alison JhoanaAún no hay calificaciones
- PRACTICA 5-Sintesis de Una Amida-2016-1Documento3 páginasPRACTICA 5-Sintesis de Una Amida-2016-1Orlando David Medinueta De AvilaAún no hay calificaciones
- Obtención de éter metilnaftílicoDocumento8 páginasObtención de éter metilnaftílicoAlfonso PA0% (2)
- Practica 1 Sintesis ParanitroanilinaDocumento5 páginasPractica 1 Sintesis ParanitroanilinaRocio100% (1)
- Practica de Síntesis de La ACETANILlDA MAY 19Documento5 páginasPractica de Síntesis de La ACETANILlDA MAY 19Natalia Anchundia GarayAún no hay calificaciones
- Informe de AminasDocumento12 páginasInforme de AminasDiegokxdAún no hay calificaciones
- Aminas CompletoDocumento27 páginasAminas CompletoSandra Hilario QAún no hay calificaciones
- Condensación AldólicaDocumento7 páginasCondensación AldólicaGianfrancoAún no hay calificaciones
- Preparación de AcetanilidaDocumento6 páginasPreparación de AcetanilidaGonzalo RestrepoAún no hay calificaciones
- Práctica 12. "Síntesis 5,5-Difenilhidantoina"Documento5 páginasPráctica 12. "Síntesis 5,5-Difenilhidantoina"Xanat CortésAún no hay calificaciones
- 5.-Aminas y 6.-Ácidos CarboxílicosDocumento24 páginas5.-Aminas y 6.-Ácidos CarboxílicosAurora Esperanza Rojas HuarotoAún no hay calificaciones
- Determinacion Grupo Amida - Analisis OrganicoDocumento6 páginasDeterminacion Grupo Amida - Analisis OrganicoAndrea HerreraAún no hay calificaciones
- Practica 7 NitroanilinaDocumento4 páginasPractica 7 NitroanilinaRomano100% (1)
- Animación ReductivaDocumento2 páginasAnimación ReductivaAna Maria PinillaAún no hay calificaciones
- Prev 6Documento6 páginasPrev 6Gabriela HernandezAún no hay calificaciones
- AnilinaDocumento3 páginasAnilinaDiego GuayacanAún no hay calificaciones
- Previo HidantoínasDocumento9 páginasPrevio HidantoínasUriel RamosAún no hay calificaciones
- Practica NDocumento5 páginasPractica NEduardo Miranda LopezAún no hay calificaciones
- Sustitucion ElectrofilicaDocumento7 páginasSustitucion Electrofilicaela7cu-614774Aún no hay calificaciones
- Práctica 7 Preguntas PreviasDocumento9 páginasPráctica 7 Preguntas PreviasLaura PintaAún no hay calificaciones
- Semana 11 Quimica OrganicaDocumento13 páginasSemana 11 Quimica OrganicaTatiana DelesmaAún no hay calificaciones
- Aldehídos y cetonas: Ensayos de diferenciaciónDocumento12 páginasAldehídos y cetonas: Ensayos de diferenciaciónAlejandra Linda Gomez MenachoAún no hay calificaciones
- Síntesis y reacciones de alquinosDocumento6 páginasSíntesis y reacciones de alquinosPaolaAguirreAún no hay calificaciones
- AcetliacionDocumento8 páginasAcetliacionAndres AlvarezAún no hay calificaciones
- Informe 4 Quimica Organica IiDocumento8 páginasInforme 4 Quimica Organica IiRobinho Sullca CerronAún no hay calificaciones
- OBTENCIÓN DE ÉTERES A. W. Williamson-Jeisson Quinteros CruzDocumento4 páginasOBTENCIÓN DE ÉTERES A. W. Williamson-Jeisson Quinteros CruzJason Q. Cruz100% (1)
- Aminas y amidas: propiedades y reaccionesDocumento6 páginasAminas y amidas: propiedades y reaccionesRUSSEL ORLANDO CCACHURA CHAYACAÑAAún no hay calificaciones
- Cuestionario Practica 5 NitroDocumento2 páginasCuestionario Practica 5 NitroErnesto RuizAún no hay calificaciones
- Alcohol EsDocumento5 páginasAlcohol EsPeluffoLuisAún no hay calificaciones
- Informe de Azlactona 2017Documento14 páginasInforme de Azlactona 2017yamily888Aún no hay calificaciones
- El universo de las energías renovablesDe EverandEl universo de las energías renovablesCalificación: 4.5 de 5 estrellas4.5/5 (4)
- Síntesis de productos químicos derivados de la biomasa empleando catálisis heterogénea: heterociclos de la biomasaDe EverandSíntesis de productos químicos derivados de la biomasa empleando catálisis heterogénea: heterociclos de la biomasaAún no hay calificaciones
- Informe 1Documento14 páginasInforme 1Jackson Huayta EnriquezAún no hay calificaciones
- Calibracion Multivariante en Muestras de AguaDocumento9 páginasCalibracion Multivariante en Muestras de AguaJackson Huayta EnriquezAún no hay calificaciones
- Informe 6 ElectroquimicaddDocumento23 páginasInforme 6 ElectroquimicaddJackson Huayta EnriquezAún no hay calificaciones
- Informe 5-Instru 2Documento35 páginasInforme 5-Instru 2Jackson Huayta EnriquezAún no hay calificaciones
- Dureza Del AguaDocumento5 páginasDureza Del AguaJackson Huayta EnriquezAún no hay calificaciones
- Bio Digest orDocumento8 páginasBio Digest orJackson Huayta EnriquezAún no hay calificaciones
- Caracterización de Materiales Polímeros Mediante La Utilización de La Microespectroscopia Vibracional (Raman, Ftir y Ft-Raman)Documento44 páginasCaracterización de Materiales Polímeros Mediante La Utilización de La Microespectroscopia Vibracional (Raman, Ftir y Ft-Raman)Ronaldo Alex CyAún no hay calificaciones
- Laboratorio 1 - Potenciometria Acido-Base Jose y ValDocumento19 páginasLaboratorio 1 - Potenciometria Acido-Base Jose y ValJose Carlos M93% (14)
- Ellen Gua JeDocumento6 páginasEllen Gua JeJackson Huayta EnriquezAún no hay calificaciones
- Fisica NuclearDocumento14 páginasFisica NuclearJackson Huayta EnriquezAún no hay calificaciones
- El RomanticismoDocumento20 páginasEl RomanticismoJackson Huayta EnriquezAún no hay calificaciones
- Informe 7 - Fisica IIIDocumento20 páginasInforme 7 - Fisica IIIJackson Huayta EnriquezAún no hay calificaciones
- Informe 7 - Fisica IIIDocumento20 páginasInforme 7 - Fisica IIIJackson Huayta EnriquezAún no hay calificaciones
- Taller 8. Termoquimica - CalorimetriaDocumento1 páginaTaller 8. Termoquimica - CalorimetriaCuenta Cuenta100% (1)
- Examen Final - Control AutomáticoDocumento5 páginasExamen Final - Control AutomáticoAlex AlmeidaAún no hay calificaciones
- Acero Estructural Astm Grados y QuímicaDocumento9 páginasAcero Estructural Astm Grados y QuímicaADGAún no hay calificaciones
- MSDS Milk System Cleaning Agent 567.0000.009 567.0000.005Documento263 páginasMSDS Milk System Cleaning Agent 567.0000.009 567.0000.005Juan RadaAún no hay calificaciones
- EL COQUE TesisDocumento3 páginasEL COQUE TesisJuan Felipe Cortes FernandezAún no hay calificaciones
- Prueba 2 de Resis 1 PDFDocumento7 páginasPrueba 2 de Resis 1 PDFjorge david ordoñez mogrovejoAún no hay calificaciones
- Práctica II EspectroDocumento6 páginasPráctica II EspectrosolutionerAún no hay calificaciones
- Contenido de bicarbonato en Alka-Seltzer mediante cálculos estequiométricosDocumento5 páginasContenido de bicarbonato en Alka-Seltzer mediante cálculos estequiométricosEVCAún no hay calificaciones
- 2.0 Balance Polar ElectromagneticoDocumento9 páginas2.0 Balance Polar ElectromagneticoJavier Garcia ChongAún no hay calificaciones
- Lab - Ii-Variacion de Presion Con La ProfundidaDocumento7 páginasLab - Ii-Variacion de Presion Con La ProfundidaheberAún no hay calificaciones
- La Corona de AdvientoDocumento22 páginasLa Corona de AdvientoMarcos AntonioAún no hay calificaciones
- Leyes de NewtonDocumento4 páginasLeyes de NewtonSofiaAún no hay calificaciones
- Informe 4 QUODocumento10 páginasInforme 4 QUOMARÍA SANTIBÁÑEZAún no hay calificaciones
- Informe de Fluido en ReposoDocumento18 páginasInforme de Fluido en ReposoGeorge MartínezAún no hay calificaciones
- Que Es La Sublimacion y CausasDocumento2 páginasQue Es La Sublimacion y CausascarolinaAún no hay calificaciones
- Tipos de CablesDocumento7 páginasTipos de CablesJuan martin BarcalaAún no hay calificaciones
- Descripción de Procesos PMJ PDFDocumento62 páginasDescripción de Procesos PMJ PDFAaron Josue SalazarAún no hay calificaciones
- Ecuaciones DimensionalesDocumento12 páginasEcuaciones DimensionalesPatriciarosaria50% (2)
- Solubilidad y cristalizaciónDocumento4 páginasSolubilidad y cristalizaciónAbril Sosa100% (1)
- Jp-Semana 03Documento26 páginasJp-Semana 03Alonso JustinianoAún no hay calificaciones
- Etección Óptica Simultánea y Extracción de Cobalto (II) de Baterías de Iones de Litio Utilizando Monolitos de NanocollectorDocumento16 páginasEtección Óptica Simultánea y Extracción de Cobalto (II) de Baterías de Iones de Litio Utilizando Monolitos de NanocollectorBastian EstayAún no hay calificaciones
- 30 Reacciones Químicas de La Vida Cotidiana - LifederDocumento9 páginas30 Reacciones Químicas de La Vida Cotidiana - LifederMarvin Ramírez Alvarez100% (1)
- Trabajo Colaborativo PHDocumento11 páginasTrabajo Colaborativo PHanon_6716891900% (1)
- SICROMETYROQDocumento10 páginasSICROMETYROQS.G.S. S.TAún no hay calificaciones
- Problemas de Recacciones de Orden y Vida Media de CineticaDocumento46 páginasProblemas de Recacciones de Orden y Vida Media de CineticaalbertoAún no hay calificaciones
- Permeabilidad RelativaDocumento4 páginasPermeabilidad RelativatrinoAún no hay calificaciones
- Laboratorio 3Documento11 páginasLaboratorio 3Javier MichaelAún no hay calificaciones
- Raloy Turbinas 46Documento1 páginaRaloy Turbinas 46Luis ReyesAún no hay calificaciones
- Ejercicios de Calculo de Varias VarialblesDocumento5 páginasEjercicios de Calculo de Varias VarialblesDaniel Corona Gonzalez33% (3)
- Ecuacion Hagen-PoiseuilleDocumento7 páginasEcuacion Hagen-PoiseuilleCrosszeriaAún no hay calificaciones