Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Teoria
Cargado por
dinamicoboysTítulo original
Derechos de autor
Formatos disponibles
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
Formatos disponibles
Teoria
Cargado por
dinamicoboysCopyright:
Formatos disponibles
VOLUMETRIA ACIDO BASE
Objetivo: Adquirir el concepto de valoracin como una de las tcnicas ms utilizadas en el laboratorio para el anlisis cuantitativo. Afianzar los conceptos de cido, base, pH, indicador y neutralizacin.
Motivacin:
La titulacin es el procedimiento utilizado para determinar el volumen de una solucin que es necesario para reaccionar con una cierta cantidad de otra sustancia. En este experimento, usted realizar la titulacin de una disolucin de cido clorhdrico, HCl, con una disolucin bsica de hidrxido de sodio, NaOH. La concentracin de la disolucin de NaOH est dada y usted determinar la concentracin desconocida del HCl. Los iones hidrgeno del HCl reaccionan con los iones hidrxido del NaOH en una razn uno a uno produciendo agua, donde la reaccin completa es: H+(ac) + Cl-(ac) + Na+(ac) + OH-(ac) ---> H2O(l) + Cl-(ac) + Na+(ac) La determinacin del pH en una muestra es un proceso muy habitual en el laboratorio de anlisis qumico para determinar el grado de acidez o basicidad de la misma. La medida puede llevarse a cabo aproximadamente mediante indicadores, o de manera exacta mediante el pH-metro. Otro procedimiento de amplio uso en el laboratorio analtico consiste en determinar la concentracin de protones o de iones hidroxilo en una disolucin mediante una valoracin cidobase, basada en las reacciones de neutralizacin entre cidos y bases. cido + Base Sal + Agua Cuando todo el cido o la base inicialmente presente se ha consumido, viene dado por el punto de equivalencia, que se puede detectar mediante el uso de un indicador adecuado o de un pH- metro. En esta prctica vamos a valorar una solucin de cido clorhdrico, cuya concentracin es desconocida, con una solucin de hidrxido sodio estandarizada previamente con un patrn primario. Dado que la proporcin durante la reaccin es de uno a uno, el nmero de moles de cido clorhdrico es igual al nmero de moles de hidrxido de sodio. Es en el punto equivalencia. El pH aumenta muy poco al aadir la base en las etapas iniciales, sin embargo, en la vecindad del punto de equivalencia aumenta drsticamente. Indicadores que se pueden utilizar deben tener una zona de viraje desde pH = 4 hasta pH = 9. (azul de bromotimol, verde bromocresol y fenolftalena)
El procedimiento para llevar a cabo la valoracin consistir en ir aadiendo cantidades sucesivas de la solucin de NaOH a la solucin de HCl y registrar mediante el programa Data Studio, gracias a un pH-metro las variaciones del pH resultante. Al representar grficamente pH frente a volumen aadido se obtiene una curva, denominada curva de valoracin, a partir de la cual se calcula el punto de equivalencia. Dicho punto corresponde a un cierto volumen aadido que nos dar, tras un sencillo clculo, la concentracin del reactivo valorado. PRECAUCIN: Nunca pipetee con la boca. Utilice siempre una bomba para pipetas. Tenga cuidado al manipular los reactivos pueden causar quemaduras
También podría gustarte
- S01 s1 Ingenieria EconomicaDocumento29 páginasS01 s1 Ingenieria EconomicadinamicoboysAún no hay calificaciones
- Kia EX PlusDocumento1 páginaKia EX PlusdinamicoboysAún no hay calificaciones
- Ofertas de autos 2018 modelos entre $53,990 y $60,990Documento3 páginasOfertas de autos 2018 modelos entre $53,990 y $60,990JordyAún no hay calificaciones
- Formato de Afiliacion Al Debito Automatico PDFDocumento2 páginasFormato de Afiliacion Al Debito Automatico PDFGeysson Matta0% (1)
- Tarjetas de crédito LATAM Pass ofrecen bonos de millasDocumento1 páginaTarjetas de crédito LATAM Pass ofrecen bonos de millasdinamicoboysAún no hay calificaciones
- Hyundai Simulador FinanciamientoDocumento1 páginaHyundai Simulador FinanciamientodinamicoboysAún no hay calificaciones
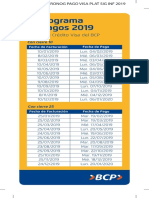
- Cronograma pagos Visa Plat BCP 2019Documento2 páginasCronograma pagos Visa Plat BCP 2019Esmeralda Carmen EcuaAún no hay calificaciones
- Semana 9 - TA4 (Economia para La Gestion) INGDocumento5 páginasSemana 9 - TA4 (Economia para La Gestion) INGdinamicoboysAún no hay calificaciones
- Tareasemana10 AliagaBereche Rodrigo HU316Documento3 páginasTareasemana10 AliagaBereche Rodrigo HU316dinamicoboysAún no hay calificaciones
- Causas Psicológicas Causadas Por La Adicción Al Teléfono CelularDocumento1 páginaCausas Psicológicas Causadas Por La Adicción Al Teléfono CelulardinamicoboysAún no hay calificaciones
- Cotizacin Seguro de Vehculos Nro 5358-CLIENTE - DFSK 2019Documento3 páginasCotizacin Seguro de Vehculos Nro 5358-CLIENTE - DFSK 2019dinamicoboysAún no hay calificaciones
- Matriz de Análisis para Relacionar Textos y RecursosDocumento1 páginaMatriz de Análisis para Relacionar Textos y RecursosdinamicoboysAún no hay calificaciones
- Causas Psicológicas Causadas Por La Adicción Al Teléfono CelularDocumento1 páginaCausas Psicológicas Causadas Por La Adicción Al Teléfono CelulardinamicoboysAún no hay calificaciones
- Economia Par Ala GestionDocumento3 páginasEconomia Par Ala Gestiondinamicoboys0% (1)
- Fernandez y Zambrano - Pag225-255 El Estado de Derecho en La Construccion de La CiudadaniaDocumento16 páginasFernandez y Zambrano - Pag225-255 El Estado de Derecho en La Construccion de La Ciudadaniadinamicoboys0% (1)
- Listado IESDocumento20 páginasListado IESYrhecAún no hay calificaciones
- Ejercicios Energia Del MAS - PPT SOL - 2Documento2 páginasEjercicios Energia Del MAS - PPT SOL - 2dinamicoboysAún no hay calificaciones
- Laboratorio 1 - UPC (Fisica 1)Documento4 páginasLaboratorio 1 - UPC (Fisica 1)dinamicoboys0% (1)
- Guia de Matricula en Línea UTP 2017-1Documento9 páginasGuia de Matricula en Línea UTP 2017-1dinamicoboysAún no hay calificaciones
- FORMATO de EVALUACIONES UTP-Formulacion y Evaluacion de Proyectos-practica-3-N06860Documento2 páginasFORMATO de EVALUACIONES UTP-Formulacion y Evaluacion de Proyectos-practica-3-N06860dinamicoboysAún no hay calificaciones
- Proyectos MecatronicosDocumento11 páginasProyectos MecatronicosdinamicoboysAún no hay calificaciones
- Problemas de MecanicaDocumento2 páginasProblemas de MecanicadinamicoboysAún no hay calificaciones
- Consejos Docente AulaDocumento1 páginaConsejos Docente AuladinamicoboysAún no hay calificaciones
- Informe de MantenimientoDocumento26 páginasInforme de MantenimientodinamicoboysAún no hay calificaciones
- GuiaPostulacionBeca18 PDFDocumento10 páginasGuiaPostulacionBeca18 PDFMiguel GasparAún no hay calificaciones
- P1 PcoDocumento24 páginasP1 PcodinamicoboysAún no hay calificaciones
- Configuración de Correo Dominio Propio - OutlookDocumento8 páginasConfiguración de Correo Dominio Propio - OutlookdinamicoboysAún no hay calificaciones
- A162WFM4 AplicacionesdelGasyMotoresdeCombustionInternaDocumento4 páginasA162WFM4 AplicacionesdelGasyMotoresdeCombustionInternadinamicoboysAún no hay calificaciones
- SKF Energy Efficient Deep Groove Ball Bearings 6692 3 ESDocumento12 páginasSKF Energy Efficient Deep Groove Ball Bearings 6692 3 ESjosee19100% (1)
- 11 Maneras de Matar A Una Persona, Manual Del Asesino en SerieDocumento3 páginas11 Maneras de Matar A Una Persona, Manual Del Asesino en Seriejosejuan0796Aún no hay calificaciones