Documentos de Académico
Documentos de Profesional
Documentos de Cultura
11a 1 081104
Cargado por
jocmjm0 calificaciones0% encontró este documento útil (0 votos)
8 vistas1 páginaTeste FQA 11ºAno
Título original
11a_1_081104
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoTeste FQA 11ºAno
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
8 vistas1 página11a 1 081104
Cargado por
jocmjmTeste FQA 11ºAno
Copyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 1
Escola Secundria de Alccer do Sal
Fsica e Qumica A 11 ano teste 1
08/11/2004
1. Considere os seguintes esquemas qumicos:
(A) (NH4)2CO3 (aq) + CaCl2 (aq) CaCO3 (s) + NH4Cl (aq)
(B) Na2S (s) + ZnCl2 (aq) NaCl (aq) + ZnS (s)
1.1 Acerte os esquemas qumicos de modo a transform-los em equaes qumicas.
1.2 Escreva os esquemas qumicos na forma inica e indique, para cada um deles, os ies espectadores.
2. A frmula qumica da ureia CO(NH2)2. Para 15 g de ureia determine:
2.1 A quantidade de ureia presente.
2.2 O nmero de molculas.
2.3 O nmero de tomos de carbono e hidrognio.
3. Em trs vidros de relgio colocou-se, separadamente, igual quantidade de nitrato de potssio (KNO3),
nitrato de magnsio (Mg(NO3)2) e nitrato de alumnio (Al(NO3)3). Em qual dos vidros de relgio existe
menor nmero de tomos de azoto? Justifique a sua resposta.
4. Atestou-se o depsito de um automvel com 40,0L de combustvel, sabendo que nesse volume de
combustvel existem, aproximadamente, 265 mol de octano (C8H18).
A equao que traduz a combusto do octano a seguinte:
2 C8H18 (l) + 25 O2 (g) 16 CO2 (g) + 18 H2O (g)
Para percorrer determinado percurso consumiram-se 10,0L de combustvel. Com base nestes dados
determine:
4.1 A quantidade de oxignio necessria para queimar completamente os 10,0L de combustvel.
4.2 O volume de dixido de carbono que se liberta, nas condies PTN.
5. O cianeto de sdio (NaCN) obtm-se industrialmente pelo processo de Castner. Tm-se como
reagentes o sdio, o carbono e o amonaco e obtm-se como produtos de reaco o cianeto de sdio e
hidrognio. Para obter 9,00 toneladas de cianeto de sdio a reaco tem de processar-se a uma
temperatura de 750C, durante 8 a 12 horas. A equao qumica que traduz esta reaco :
2 Na (s) + 2 C (s) + 2 NH3 (g) 2 NaCN (s) + 3 H2 (g)
Sabendo que se consumiram 4,80 toneladas de sdio, calcule:
5.1 O rendimento deste processo industrial.
5.2 A quantidade de hidrognio que se libertou.
FIM
También podría gustarte
- Receitas Aula2Documento8 páginasReceitas Aula2jocmjm100% (1)
- 8fqYxHSIROaH1TxUSZxA - 6.2 Mole - Massa - Volume - Molar PDFDocumento1 página8fqYxHSIROaH1TxUSZxA - 6.2 Mole - Massa - Volume - Molar PDFjocmjmAún no hay calificaciones
- Exercicios TermodinamicaDocumento28 páginasExercicios TermodinamicaEudes Santos80% (5)
- Programa Fqa 10 11Documento80 páginasPrograma Fqa 10 11IsabelFreitasAún no hay calificaciones
- Formulário ESPR 2016 2017Documento2 páginasFormulário ESPR 2016 2017jocmjmAún no hay calificaciones
- Perguntas Kahoot - 9ºano GlobalDocumento6 páginasPerguntas Kahoot - 9ºano GlobaljocmjmAún no hay calificaciones
- Medição em QuímicaDocumento16 páginasMedição em Químicajocmjm0% (1)
- 919 Questoes de Fisica Resolvidas LibreDocumento273 páginas919 Questoes de Fisica Resolvidas Librejocmjm0% (1)
- Teste FQ 8ano 2 Som e LuzDocumento3 páginasTeste FQ 8ano 2 Som e LuzjocmjmAún no hay calificaciones
- Saber Estar em SociedadeDocumento2 páginasSaber Estar em Sociedadejocmjm100% (1)
- Teste No 2 Lig QuimicaDocumento6 páginasTeste No 2 Lig QuimicaNarcisa Alexandra FilipeAún no hay calificaciones
- FI Nº7 - LuzDocumento5 páginasFI Nº7 - LuzjocmjmAún no hay calificaciones
- Cap3 4Documento59 páginasCap3 4jocmjmAún no hay calificaciones
- Campo Magnetico e Campo EléctricoDocumento3 páginasCampo Magnetico e Campo EléctricoOlivia GomesAún no hay calificaciones
- 10a 1 031105Documento2 páginas10a 1 031105Santana RamosAún no hay calificaciones
- Equações de Palavras e Escala de PHDocumento3 páginasEquações de Palavras e Escala de PHjocmjmAún no hay calificaciones
- 2015 10 29 Vocacional - Doc.8Documento5 páginas2015 10 29 Vocacional - Doc.8jocmjmAún no hay calificaciones
- Nomenclatura AlcanosDocumento16 páginasNomenclatura AlcanosjocmjmAún no hay calificaciones
- Teste Química 12ºanoDocumento5 páginasTeste Química 12ºanojocmjmAún no hay calificaciones
- 2014 05 06 F6 (SOM) - ExameDocumento5 páginas2014 05 06 F6 (SOM) - Examejocmjm100% (1)
- Aniões e CatiõesDocumento1 páginaAniões e Catiõesjocmjm100% (1)
- BEnzeno e Compostos AromáticosDocumento2 páginasBEnzeno e Compostos AromáticosjocmjmAún no hay calificaciones
- FT12 CompostosOrgânicosDocumento7 páginasFT12 CompostosOrgânicosjocmjm0% (1)
- FI Nº10 - Representação Das Reacções QuímicasDocumento3 páginasFI Nº10 - Representação Das Reacções QuímicasjocmjmAún no hay calificaciones
- Ebook Algas Na AlimentacaoDocumento27 páginasEbook Algas Na AlimentacaojocmjmAún no hay calificaciones
- Cfq8 Exercicios1 Acerto EquacoesDocumento1 páginaCfq8 Exercicios1 Acerto EquacoesHugo CostaAún no hay calificaciones
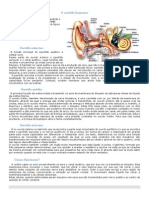
- O Ouvido HumanoDocumento1 páginaO Ouvido HumanojocmjmAún no hay calificaciones
- Ebook AlimentacaoDocumento30 páginasEbook AlimentacaoAnonymous xuph2ZzeAún no hay calificaciones