Documentos de Académico
Documentos de Profesional
Documentos de Cultura
Orto Piro Meta PDF
Orto Piro Meta PDF
Cargado por
cabrojanu0 calificaciones0% encontró este documento útil (0 votos)
30 vistas3 páginasTítulo original
ORTO-PIRO-META.pdf
Derechos de autor
© © All Rights Reserved
Formatos disponibles
PDF, TXT o lea en línea desde Scribd
Compartir este documento
Compartir o incrustar documentos
¿Le pareció útil este documento?
¿Este contenido es inapropiado?
Denunciar este documentoCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
0 calificaciones0% encontró este documento útil (0 votos)
30 vistas3 páginasOrto Piro Meta PDF
Orto Piro Meta PDF
Cargado por
cabrojanuCopyright:
© All Rights Reserved
Formatos disponibles
Descargue como PDF, TXT o lea en línea desde Scribd
Está en la página 1de 3
FORMAS ORTO/PIRO/META
Algunos anhdridos se pueden combinar con ms de una molcula de
agua. Para diferenciarlos se utilizan los prefijos orto/piro/meta.
Se usan los prefijos meta- al aadir una molcula de H2O, piro- cuando
son dos y orto- al aadir tres molculas de H2O para los cidos de los no metales
trivalentes y pentavalentes.
Se usan los prefijos meta- al aadir una molcula de H2O, y orto- al
aadir dos molculas de H2O, para los cidos de los no metales tetravalentes.
A continuacin se presenta una relacin de los diferentes cidos que existen.
1. El fsforo, arsnico y antimonio con valencias +1, +3, +5.
Forma meta: A los xidos correspondientes se les suma una molcula de agua.
P2O3 + H2O HPO2 cido metafosforoso
P2O5 + H2O HPO3 cido metafosfrico
Forma piro: A los xidos se les unen dos molculas de agua.
P2O3 + 2 H2O H4P2O5 cido pirofosforoso
P2O5 + 2 H2O H4P2O7 cido pirofosfrico
Forma orto A los xidos se les suman 3 molculas de agua a los xidos
correspondientes.
P2O3 + 3H2O H6P2O6 H3PO3 cido ortofosforoso o fosforoso
P2O5 +3H2O H6P2O8 H3PO4 cido ortofosfrico o fosfrico
2. El silicio con valencia +4
En el caso del silicio puede formar dos cidos:
Meta A los xidos correspondientes se les suma una molcula de agua.
Orto A los xidos se les unen dos molculas de agua.
SiO2 + H2O H2SiO3 cido metasilcico
SiO2 + 2 H2O H4SiO4 cido silcico (ortosilcico)
3. El Boro con valencia +3.
El boro puede formar los cidos meta y orto al igual que los elementos del grupo
15.
B2O3 + H2O HBO2
B2O3 + 2 H2O H4B2O5
cido metabrico
cido pirobrico
B2O3 + 3 H2O H3BO3 cido brico (ortobrico)
4. Dicidos o pirocidos (S, Se y Te con valencias +4, +6).
El azufre puede formar los dicidos. El prefijo di- hace referencia al grado de
polimerizacin de los cidos respectivos. El cido se forma restando una
molcula de agua a dos molculas del cido:
2 H2SO3 1 H2O H2S2O5 cido disulfuroso
2 H2SO4 1 H2O H2S2O7 cido disulfrico
5. Cromo con valencia +6.
2 CrO3 + 1 H2O H2Cr2O7 cido dicrmico
CUADRO GENERAL FORMAS ORTO PIRO META
ORTO PIRO META
<<<
VALENCIA IMPAR
VALENCIA IMPAR
Meta 1 mol. anhdrido + H2O 1 mol. anhdrido + H2O
Piro 1 mol. anhdrido + 2 H2O 2 mol. anhdrido + H2O
Orto 1 mol. anhdrido + 3H2O 1 mol. anhdrido + 2 H2O
ORTO PIRO META
<<<
VALENCIA IMPAR
VALENCIA PAR
+1 +3 +5 +4 +6
Meta HXO HXO2 HXO3 H2XO3 H2XO4
Piro H4X2O3 H4X2O5 H4X2O7 H2X2O5 H2X2O7
Orto H3XO2 H3XO3 H3XO4 H4XO4 H4XO5
También podría gustarte
- Qué Son Los Números de OxidaciónDocumento4 páginasQué Son Los Números de OxidaciónRoberto MoralesAún no hay calificaciones
- Sales Dobles o MixtasDocumento7 páginasSales Dobles o MixtasGuadalupe VillegasAún no hay calificaciones
- Nomenclatura de Sales Binarias e HidroxidosDocumento3 páginasNomenclatura de Sales Binarias e HidroxidosLuisAún no hay calificaciones
- Primer Examen de Formulación Orgánica 2º BtoDocumento3 páginasPrimer Examen de Formulación Orgánica 2º Btoisabelsu1Aún no hay calificaciones
- Capitulo 2 Alcanos Mzo Resuelto27Documento22 páginasCapitulo 2 Alcanos Mzo Resuelto27Jeremy Jara RosasAún no hay calificaciones
- QUÍMICA-REDOX, Exámenes Resueltos 2023 PDFDocumento23 páginasQUÍMICA-REDOX, Exámenes Resueltos 2023 PDFMarta López OlivaresAún no hay calificaciones
- Dinamica, Cuerpos EnlazadosDocumento3 páginasDinamica, Cuerpos Enlazadosprobe13Aún no hay calificaciones
- Tabla de ValenciasDocumento1 páginaTabla de Valenciasmusicart30008394100% (3)
- Partes Por MillónDocumento2 páginasPartes Por MillónHugo MayorgaAún no hay calificaciones
- Meta, Piro, OrtoDocumento1 páginaMeta, Piro, Ortoeducate10100% (3)
- 3-4 Eso - Formulación ÓxidosDocumento13 páginas3-4 Eso - Formulación Óxidosangela_zamorano_4Aún no hay calificaciones
- U 1 - Sales Básicas y Sales Dobles - Nomenclatura de Sustancias QuímicasDocumento4 páginasU 1 - Sales Básicas y Sales Dobles - Nomenclatura de Sustancias QuímicasGEORGE Xd:v100% (2)
- Oxoacidos Meta Piro Di OrtoDocumento5 páginasOxoacidos Meta Piro Di OrtoGema Gómez0% (2)
- Material Didáctico de Apoyo para La Nomenclatura Química Inorgánica PDFDocumento51 páginasMaterial Didáctico de Apoyo para La Nomenclatura Química Inorgánica PDFbcvbcvbcbv62% (13)
- Nomenclatura de CetonasDocumento9 páginasNomenclatura de CetonasAndrés Brun100% (1)
- Tareas BinariosDocumento17 páginasTareas BinariosBrayan Toapanta QuillupanguiAún no hay calificaciones
- Acidos OxácidosDocumento9 páginasAcidos OxácidosRicardo VillavicencioAún no hay calificaciones
- Actividad 13 Ejercicios de Ley de RichterDocumento1 páginaActividad 13 Ejercicios de Ley de RichterProfe Rafa F.DAún no hay calificaciones
- Tema N°2 Tipos de SalesDocumento5 páginasTema N°2 Tipos de SalesSaterdoAún no hay calificaciones
- 3º-4º Eso - Formulación de HidrurosDocumento18 páginas3º-4º Eso - Formulación de Hidrurosangela_zamorano_4Aún no hay calificaciones
- Tabla de Valencias Profesor10demates PDFDocumento1 páginaTabla de Valencias Profesor10demates PDFCati Lara CazorlaAún no hay calificaciones
- OxácidosDocumento2 páginasOxácidosngbios67% (3)
- Tipos de Disoluciones y Enfoque Molecular Del Proceso de DisoluciónDocumento2 páginasTipos de Disoluciones y Enfoque Molecular Del Proceso de Disolución000yasAún no hay calificaciones
- Ejercicios de Identificacion de Grupos FuncionalesDocumento3 páginasEjercicios de Identificacion de Grupos FuncionalesBryan Hernandez0% (1)
- Examen 4 Eso EnlaceDocumento2 páginasExamen 4 Eso EnlaceSara Maria Bello SalcedoAún no hay calificaciones
- RadicalesDocumento1 páginaRadicalesLuis F. González AñezAún no hay calificaciones
- Ejercicios Sobre El Enlace Químico-EditadoDocumento4 páginasEjercicios Sobre El Enlace Químico-EditadoLoroAún no hay calificaciones
- Laboratorio de Balanceo Metodo Algebraico - Raul ApresaDocumento7 páginasLaboratorio de Balanceo Metodo Algebraico - Raul ApresaAngie JimenezAún no hay calificaciones
- EJE 7-NomenclaturaDocumento5 páginasEJE 7-NomenclaturaalamparonAún no hay calificaciones
- Química I Parte 2Documento8 páginasQuímica I Parte 2Teofilo Donaires FloresAún no hay calificaciones
- Balanceo de Ecuaciones 1 Tanteo AlgebraicoDocumento1 páginaBalanceo de Ecuaciones 1 Tanteo AlgebraicoRosmel Michael Lazo QuispeAún no hay calificaciones
- Inorganica Ejercicios Peroxidos Con SolucionesDocumento2 páginasInorganica Ejercicios Peroxidos Con SolucionesMesías Sebastian100% (1)
- Tabla Comparativa Teorica Acido-BaseDocumento1 páginaTabla Comparativa Teorica Acido-BaseFcoJTorresCAún no hay calificaciones
- Tarea 5 QuimicaDocumento4 páginasTarea 5 QuimicaAnita Morales67% (3)
- Evaluación de QuímicaDocumento2 páginasEvaluación de QuímicaLeidy Yohana ChaconAún no hay calificaciones
- Examen Falso y VerdaderoDocumento1 páginaExamen Falso y VerdaderoJesaja RostovAún no hay calificaciones
- Folleto SexualidadDocumento4 páginasFolleto SexualidadLuis Tadeo Pérez Reyes100% (2)
- Quimica Tercer Periodo (Johnny Bueno) 11 3pDocumento8 páginasQuimica Tercer Periodo (Johnny Bueno) 11 3pjhonny Bueno Romero100% (1)
- 55023Documento3 páginas55023luis chonilloAún no hay calificaciones
- Victor 2Documento14 páginasVictor 2Víctor Manuel MoralesAún no hay calificaciones
- Nomenclatura 23 de OctubreDocumento6 páginasNomenclatura 23 de OctubreEstrella GonzálesAún no hay calificaciones
- Ion Electrón-Medio BásicoDocumento3 páginasIon Electrón-Medio BásicoARIEL SEBASTIAN MARQUEZ GOMEZAún no hay calificaciones
- Ejercicios Imprimir Numeros de OxidaciónDocumento1 páginaEjercicios Imprimir Numeros de OxidaciónfridaylaikaAún no hay calificaciones
- Ejercicios de Oxigenados-NitrogenadosDocumento5 páginasEjercicios de Oxigenados-NitrogenadossaulotejadaAún no hay calificaciones
- Examen Elementos Tabla PeriodicaDocumento2 páginasExamen Elementos Tabla Periodicafennchu100% (2)
- Tema-Tabla Periodica de Los Elementos QuimicosDocumento3 páginasTema-Tabla Periodica de Los Elementos QuimicosAlfredo FernandezAún no hay calificaciones
- Ejercicios Sobre Clasificacin de La MateriaDocumento3 páginasEjercicios Sobre Clasificacin de La Materiamireida morales25% (4)
- Nomenclatura Quimica DecimoDocumento7 páginasNomenclatura Quimica DecimoRamón DíazAún no hay calificaciones
- Taller de Enlace Quimico H H GDocumento11 páginasTaller de Enlace Quimico H H GJULLY MARCELA PACHON HUERTASAún no hay calificaciones
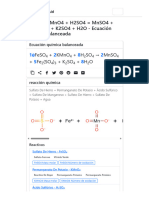
- FeSO4 + KMnO4 + H2SO4 MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O - Ecuación Química BalanceadaDocumento5 páginasFeSO4 + KMnO4 + H2SO4 MnSO4 + Fe2 (SO4) 3 + K2SO4 + H2O - Ecuación Química BalanceadaGontanjimT.JiménezAún no hay calificaciones
- Ejercicios de Doble DesplazamientoDocumento1 páginaEjercicios de Doble DesplazamientomarcoAún no hay calificaciones
- Puntos de Ebullición Hidruros Grupo 16Documento16 páginasPuntos de Ebullición Hidruros Grupo 16hectorhernandoms100% (1)
- Ejercicios de Enlaces de Hidrógeno.Documento1 páginaEjercicios de Enlaces de Hidrógeno.Clases particulares en la Laguna50% (2)
- Composición PorcentualDocumento1 páginaComposición PorcentualLorena Isabel Arancibia CortesAún no hay calificaciones
- Práctica Los Alcanos - Alqueno - AlquinosDocumento10 páginasPráctica Los Alcanos - Alqueno - Alquinoscasa RodriguezAún no hay calificaciones
- Taller de Formulación de Compuestos InorganicosDocumento10 páginasTaller de Formulación de Compuestos InorganicosEstefany CamargoAún no hay calificaciones
- Quimica N3Documento5 páginasQuimica N3Josué ChimarroAún no hay calificaciones
- Ejercicios PHDocumento4 páginasEjercicios PHA01312078Aún no hay calificaciones
- Acidos PolihidratadosDocumento3 páginasAcidos PolihidratadosRafael Sullon Maza73% (15)
- Ácidos PolihidratadosDocumento2 páginasÁcidos PolihidratadosAnonymous 8TK6ziVGFxAún no hay calificaciones